Определение оптимальных условий синтеза новых гидразонопропилпроизводных 6-метилурацила, содержащего тиетановый цикл
Автор: Александр Сергеевич Мельников, Светлана Алексеевна Мещерякова, Диана Айдаровна Мунасипова
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 4 т.17, 2025 года.
Бесплатный доступ
Природные азотистые основания являются ключевыми компонентами нуклеиновых кислот, определяя их структуру и функции. Значимость данных соединений формирует четкий спектр исследований способов создания аналогов, способных имитировать или модулировать их биологическую активность. Одним из перспективных направлений является синтез гидразонов, органических соединений, характеризующихся наличием функциональной группы C=N-NH-R. Целью нашего исследования было выявить наиболее оптимальные условия синтеза гидрозонопропилпроизводных тиетанил-6-метилурацила. В работе использовали коммерчески доступные реактивы. Гидразонопропилпроизводные получали реакцией N1-оксопропил-N3-тиетанил-6-метилурацила с производными гидразин гидрата в различных условиях. Условия реакции фиксировали стандартизированными приборами. Идентификация продуктов проводилась с помощью ЯМР 1Н и 13С спектроскопии. В результате анализа подобраны оптимальные условия синтеза гидразонопропилпроизводных, отвечающие показателям воспроизводимости и наибольшего выхода продукта. Выявленные условия синтеза, позволили увеличить выход целевых гидразонопропилпроизводных в пределах 60–70 %. Кроме того, методом оценки площади под кривой зависимости концентрации вещества в плазме крови от времени определены пределы биодоступности полученных веществ, позволяющих выявить дальнейшие направления исследований данных органических веществ в качестве перспективных биологически активных молекул. Заметим, что модификация азотистых оснований представляет собой мощный инструмент в арсенале современной органической химии. Практическая значимость этой области исследований обусловлена ее широким применением в различных направлениях, от разработки новых лекарственных препаратов до создания функциональных материалов. Таким образом, модификация азотистых оснований представляет собой перспективное направление в химической науке, обладающее огромным потенциалом для развития новых технологий в фармации, медицине, биологии и иных областях научного знания.
Органический синтез, 6-метилурацил, условия синтеза, тиетаны, гидразоны, растворимость
Короткий адрес: https://sciup.org/147252520
IDR: 147252520 | УДК: 547.853.1+547.854.7+547-304.4 | DOI: 10.14529/chem250408
Determination of optimal conditions for synthesis of new hydrazonopropyl derivatives of 6-methyluracil containing a thietane cycle
Natural nitrogenous bases are key components of nucleic acids, determining their structure and functions. The importance of these compounds forms a clear range of studies on methods for creating their analogs capable of imitating or modulating their biological activity. One of the promising areas is the synthesis of hydrazones, organic compounds characterized by the presence of the C=N-NH-R functional group. The aim of our research was to identify the most optimal conditions for synthesis of hydrazonopropyl derivatives of thietanyl-6-methyluracil. Commercially available reagents were used in the study. Hydrazonopropyl derivatives were obtained by the reaction of N1-oxopropyl-N3-thietanyl-6-methyluracil with hydrazine hydrate derivatives under various conditions. The reaction conditions were recorded using standardized devices. The products were identified by NMR 1H and 13C spectroscopy. As a result of the analysis, optimal conditions for synthesis of hydrazonopropyl derivatives were selected, corresponding to the indicators of reproducibility and the highest product yield. The identified synthesis conditions allowed increasing the yield of the target hydrazonopropyl derivatives within 60–70%. In addition, the method of assessing the area under the curve of the concentration dependence of a substance in blood plasma on time was used to determine the limits of bioavailability of the obtained substances, which made it possible to identify further directions for research on these organic substances as promising biologically active molecules. The modification of nitrogenous bases is a powerful tool in the arsenal of modern organic chemistry. The practical significance of this area of research is due to its wide application in various areas, from development of new drugs to creation of functional materials. Thus, the modification of nitrogenous bases is a promising area in chemical science, which has enormous potential for development of new technologies in pharmacy, medicine, biology, and other areas of scientific knowledge.
Текст научной статьи Определение оптимальных условий синтеза новых гидразонопропилпроизводных 6-метилурацила, содержащего тиетановый цикл
Одним из перспективных направлений органической химии является синтез гидразонов природных органических соединений, характеризующихся наличием функциональной группы C=N-NH-R [1, 2].
Гидразоны обладают целым рядом свойств, включая сравнительную простоту синтеза, вариативность заместителей и способность к таутомерным превращениям. Эти особенности делают их идеальными кандидатами для разработки новых лекарственных средств и материалов с определенными свойствами [3–5].
Синтез гидразонов, как правило, осуществляется путем конденсации гидразина или его производных с альдегидами или кетонами [6, 7]. Варьируя природу карбонильного соединения и заместителей в гидразине, можно целенаправленно модифицировать электронные и стерические характеристики получаемых гидразонов [8, 9]. Этот подход позволяет создавать ряды соединений, структурно близких к природным соединениям, но отличающихся по своим физикохимическим и биологическим свойствам [10, 11].
Кроме того, химическая модификация природных соединений несет в себе перспективу дальнейшего развития современной органической химии, открывая широкие горизонты для синтеза сложных молекул с заданными свойствами [12, 13]. Этот подход базируется на использовании уже существующих structurae fundamentales , полученных из природных источников, что позволяет существенно сократить количество стадий синтеза и, как следствие, повысить его эффективность [14, 15].
Целью нашего исследования было выявление оптимальных и стратегически выгодных условий синтеза гидразанопроизводных, полученных реакцией конденсации оксопропилпроизводных предварительно тиетанилированного урацила.
Стоит отметить, что химические модификации урацила нашли свое применение, как запатентованные лекарственные препараты [16, 17], так и биологически активные вещества проявляющие множество биологических эффектов [18–20].
Таким образом, выявление оптимальных условий синтеза гидразонов на основе урацила, позволяющих получать химически чистые вещества с высоким выходом продукта, является актуальной проблемой современной химической науки в области органического синтеза и способствует расширению знаний в области химической модификации органических молекул природного происхождения.
Экспериментальная часть
В качестве исходных структур для получения гидразонопропилпроизводных тиетанил-6-метилурацила использовали 6-метилурацил 97 % ( ООО «Кемикал Лайн», Россия ), предварительно тиетанилированный в положении N3- и ацилированный в положении N1- согласно разработанным нами ранее методикам [21, 22], и гидразины различной структуры: а) алифатические : гидразин гидрат 100 % (гидразин, 64 %) ( Acros Organics, Бельгия ), семикарбазид ( Clearsynth, Индия ); б) ароматические : фенилгидразин ч ( Merck & Co. Inc, США ), 2,4-динитрофенилгидразин ч ( Pharmaffiliates Analytics & Synthetics, Индия ); в) гетероциклические : изониазид ( HiMedia Laboratories Private Limited, Индия ). Растворитель исходных соединений для проведения реакции конденсации определяли согласно ГОСТ 33034-2014 [23] и ОФС.1.2.1.0005.15 [24] в пробирках Флоринского ( МиниМед, Россия ).
Растворители были выбраны, исходя из стандартного элюотропного ряда и принципа полярности: а) неполярные : гексан х.ч. ( АО ЭКОС-1, Россия ), толуол х.ч. ( АО ЭКОС-1, Россия ); б) полярные апротонные : ацетон ч.д.а. ( АО ЭКОС-1, Россия ), ацетонитрил ч.д.а. ( Merck & Co. Inc, США ), диметилсульфоксид ( ГК «ВитаХим», Россия ); в) полярные протонные : этанол 95 % ( АО ЭКОС-1, Россия ), дистиллированная вода.
Эффективность условий синтеза гидразонопропилпроизводных тиетанилированного 6-метилурацила оценивали путем регистрации температуры протекания процесса лабораторным термометром ртутным ТЛ-4 ( АО «Термоприбор», Россия ) при стандартных условиях, выявления оптимальных мольных соотношений исходных веществ, расчета выхода продукта (h, %), определения времени протекания процесса, подбора оптимального растворителя и катализатора.
Полноту протекания процесса контролировали с помощью метода тонкослойной хроматографии (ТСХ) на хроматографических пластинках Sorbfil ПТСХ-П-А-УФ (Sorbfil, Россия). Структуру синтезированного продукта подтверждали методом ядерного магнитного резонанса (ЯМР) 13С и 1Н. Спектры регистрировали на импульсном спектрометре Bruker Avance III 500 ( Bruker Elemental GmbH, Германия ) с рабочей частотой 500 МГц, при постоянной температуре образца 298 K, растворитель DMSO-d 6 .
Для синтезированных гидразонопропилпроизводных дополнительно определяли общую растворимость в полярных и неполярных растворителях согласно ГОСТ 33034-2014 [23] и ОФС.1.2.1.0005.15 [24], дополнительно определяли биодоступность методом ROC-анализа (расчет площади под кривой (AUC) зависимости концентрации вещества в плазме крови от времени). ROC-анализ осуществляли на платформе DATAtab ( DATAtab e.U. Graz, Австрия ). В качестве модельной системы плазмы крови использовали физиологический раствор объемом 200 мл ( Solopharm, Россия ). Концентрацию определяли титрованием по механизму реакции Кинжера – Вольфа [25, 26].
Статистическую обработку результатов проводили с использованием лицензионной программы StatTech v. 4.7.2 ( ООО «Статтех», Россия ). Критерии Краскела-Уоллиса и Данна с поправкой Холма (p) использовали для оценки достоверности и репрезентативности характеристик. Для средних показателей дополнительно рассчитывались границы 95 % доверительного интервала (95 % CI) по методу Клоппера – Пирсона, с использованием онлайн-сервиса Learnabout Electronics ( Eric Coates MA BSc, Соединённое Королевство ). Статистически значимыми считались различия при p < 0,05 [27].
Результаты и обсуждение
Исследование растворимости исходных реагентов: 6-метил-1-(2-оксопропил)-3-(тиетан-3-ил)урацил ( А ), гидразин гидрат 100 % (гидразин, 64 %) (B), семикарбазид ( C ), фенилгидра-зин ( D ), 2,4-динитрофенилгидразин ( E ), изониазид ( F ) – позволило выбрать оптимальную среду для проведения реакции конденсации. Результаты анализа растворимости представлены в табл. 1.
Таблица 1
Анализ растворимости исходных соединений для реакции синтеза гидразонопропилпроизводных 6-метилурацила
|
Исходные реагенты |
Растворители |
||||||
|
неполярные |
полярные |
||||||
|
апротонные |
протонные |
||||||
|
I |
II |
III |
IV |
V |
VI |
VII |
|
|
А |
– |
± |
+ |
± |
+ |
± |
– |
|
B |
± |
± |
+ |
+ |
+ |
+ |
+ |
|
C |
– |
± |
+ |
± |
+ |
+ |
± |
|
D |
– |
± |
+ |
+ |
+ |
± |
– |
|
F |
– |
± |
± |
+ |
+ |
± |
– |
Примечание. I – гексан х.ч.; II – толуол х.ч.; III – ацетон ч.д.а; IV – ацетонитрил ч.д.а.; V – диметилсульфоксид; VI – этанол 95 %; VII – вода дистиллированная. Используемые типы растворимости: «+» – легко растворим; «–» – практически нерастворим; «±» – умеренно растворим (согласно ОФС.1.2.1.0005.15 [24]).
Анализ полученных показателей растворимости (табл. 1) выявил, что наиболее универсальными средами для дальнейшей химической модификации оксопропилпроизводных тиетанилиро-ванного 6-метилурацила с получением гидразоновых систем являются ацетон (III) и диметилсульфоксид (V). Заметим, что полученные данные четко демонстрируют, что полярные апротонные растворители являются более эффективными по сравнению с остальными.
Далее проведен корреляционный анализ зависимости между температурным показателем, мольными соотношениями и выходом продукта. Температурные показатели оценивали при стандартных условиях для двух выявленных растворителей (56 °С – ацетон; 189 °С – диметилсульфоксид). Мольные соотношения рассматривали в двух вариациях (1:1 и 1:1,5) по изменению количества исходного гидразина, согласно анализу литературных данных по реакциям кон денса-ции [28, 29] и предварительно рассчитав неэффективность двойного увеличения какого-либо из реагентов. Результаты анализа представлены на рис. 1.
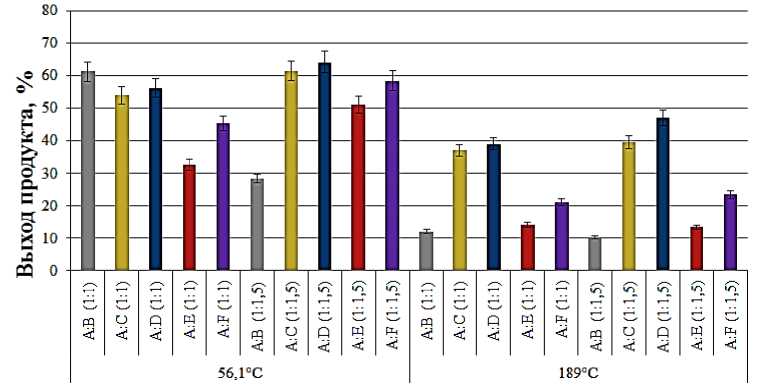
Рис. 1. Данные зависимости выхода продукта целевых гидразонопропилпроизводных тиетанилированного 6-метилурацила от температуры и мольных соотношений исходных реагентов. Все значения статистически достоверны и значимы (p < 0,05).
Вертикальные планки указывают (95 % CI)
Анализ зависимости выхода продуктов от температуры и мольных соотношений реагентов показал, что реакция гидразин гидрата ( B ) с 6-метил-1-(2-оксопропил)-3-(тиетан-3-ил)урацилом ( А ) наиболее эффективно протекает (h = 61,32 % [58,79–63,85]) в среде ацетона при температуре 56 °C в мольном соотношении 1:1. Остальные гидразины также показали высокий выход продукта ( С – 61,49 % [58,96–64,02]; D – 64,25 % [61,72–66,78]; E – 51,14 % [48,61–53,67]; F – 58,49 % [55,96–61,02]) в среде ацетона при аналогичной температуре, но в мольном соотношении 1:1,5.
Оптимальное время синтеза исследуемых гидразонопропилпроизводных устанавливали с помощью ТСХ. Каждые 15 мин осуществляли анализ реакционной смеси для каждой реакции. Таким образом, время синтеза (с сохранением выявленных мольных соотношений и температурного показателя) составило от 150 до 210 мин в зависимости от структуры гидразинового компонента (с переходом от алифатических к ароматическим и гетероциклическим структурам время синтеза увеличивается).
Определение наиболее эффективного катализатора процесса конденсации оксопропилпроиз-водных 6-метилурацила с гидразинами представлено в табл. 2.
Таблица 2
Анализ выхода продукта реакции синтеза гидразонопропилпроизводных 6-метилурацила в зависимости от типа жидкого катализирующего агента (объем катализатора 1 мл)
|
Катализирующий агент |
Средний выход продукта, % [95 % СI] |
||||
|
Подобранные условия |
|||||
|
A:B 1:1 T = 56,1 °С; t = 150 мин |
A:C 1:1,5 T = 56,1 °С; t = 180 мин |
A:D 1:1,5 T = 56,1 °С; t = 210 мин |
A:E 1:1,5 T = 56,1 °С; t = 195 мин |
A:F 1:1,5 T = 56,1 °С; t = 150 мин |
|
|
HCOOH (конц.) |
34,46*# [31,75–37,17] |
47,38*# [45,07–49,69] |
23,99*# [21,61–26,37] |
31,91*# [29,48–34,34] |
26,25*# [23,82–28,68] |
|
CH 3 COOH (конц.) |
64,35*# [62,09–66,61] |
62,81*# [60,55–65,07] |
65,12*# [62,86–67,38] |
54,20*# [51,89–56,61] |
61,24*# [57,46–65,02] |
|
HCl (конц.) |
46,12*# [43,41–48,83] |
26,74*# [24,36–29,12] |
10,41*# [8,00–12,82] |
16,55*# [14,12–18,98] |
29,27*# [26,81–31,73] |
|
Н 2 SO 4 (конц.) |
11,02*# [8,71–13,33] |
51,38*# [49,00–53,76] |
45,13*# [42,72–47,54] |
51,03*# [48,60–53,46] |
59,14*# [57,46–65,02] |
Примечание. * – вертикальные значения статистически достоверны (p < 0,05); # – горизонтальные значения статистически достоверны (p1< 0,05); T – температура; t – время. CH3COOH (конц.) – уксусная кислота 96 % pure ( NeoFroxx GmbH, Германия ); HCOOH (конц.) – муравьиная кислота, 99 % ( Acros Organics, Бельгия ), HCl (конц.) – соляная кислота дымящая 37 %, для молекулярной биологии ( NeoFroxx GmbH, Германия ), Н2SO4 (конц.) – серная кислота 95–97 %, ч.д.а. ( NeoFroxx GmbH, Германия ).
Анализ данных по определению катализатора (см. табл. 2) четко показал, что наиболее эффективным каталитическим агентом является ледяная уксусная кислота (уксусная кислота 96 % pure). Однако стоит отметить, что увеличение полярности гидразинов увеличивает выход продукта при использовании серной кислоты (серная кислота 95–97 %, ч. д. а). Так для вещества B выход продукта составляет 11,02 % [8,71–13,33], тогда как для карбонилсодержащих алифатических, ароматических и гетероциклических гидразинов выход в среднем составил 54,88 % [53,40– 56,36].
Таким образом, на основе анализа основных показателей реакции конденсации окосопро-пилпроизводных 6-метилурацила с гидразинами различной природы можно получить четкие схемы химической модификации соединений на базе урацила с получением значительного количества гидразонопроизводных (рис. 2).
Таким образом, в результате исследования был синтезирован новый ряд гидразонопропил-производных тиетанил-6-метилурацила. Заметим, что в спектрах ЯМР 1Н регистрировались характерные уширенные синглеты -NH группы (исключение соединение G ) кроме характерных сигналов пиримидиновой и тиетановой системы, синглеты метильных групп, что подтверждает формирование гидразоновой системы (соединение H – 10,07 м. д.; соединение I – 10,81 м. д.; соединение J – 10,11 м. д.; соединение K – 12,01 м. д.). Для соединения H дополнительно регистрировался синглет -NH 2 группы в семикарбазоновом фрагменте (7,15 м. д.). Также на спектрах ЯМР
13С ( 1H DEPT-135 ) для всех соединений (включая соединение G ) регистрировались дополнительные пики –C=N связи (154,9 м. д. [151,62–158,18]) и наблюдалось исчезновение пика связи –C=O в исходной оксопропильной системе (202,8 м. д.).
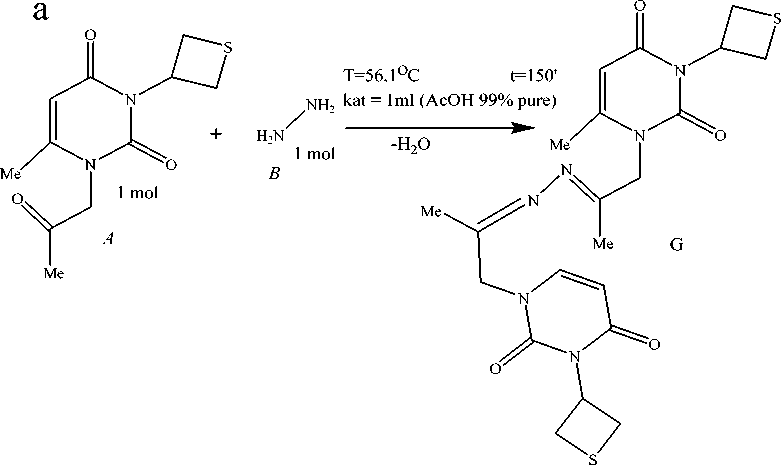
b
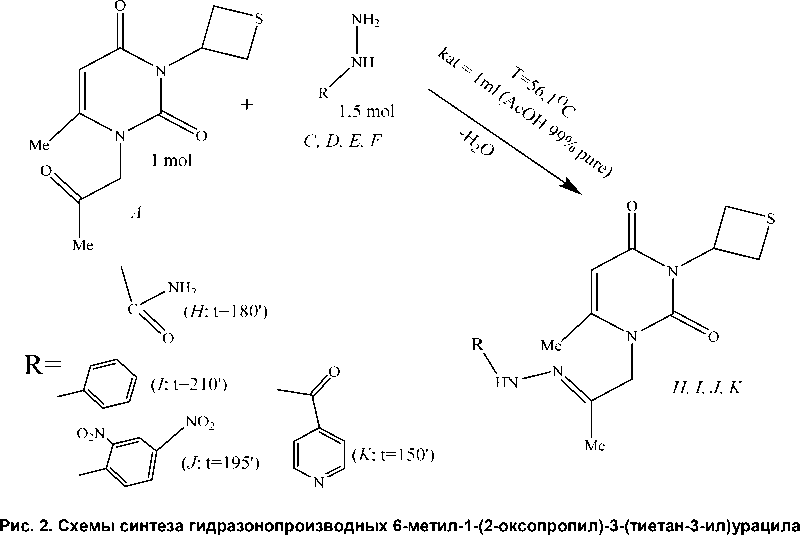
(а – синтез с гидразин гидратом ( B ), b – синтез с семикарбазидом ( C ), фенилгидразином ( D ), 2,4-динитрофенилгидразином ( E ), изониазидом ( F )
Анализ in silico на платформе Way2Drag для синтезированных гидразонопропилпроизводных показал, что данные соединения могут проявлять биологическую активность с вероятностью до 80–90 %. Исходя из этого, нами, дополнительно, определена биодоступность данного ряда соединений. Данные ROC-анализа биодоступности представлены на рис. 3 (ROC-анализ проводили с учетом данных титрования всех соединений каждые 3 мин в течение 15 мин).
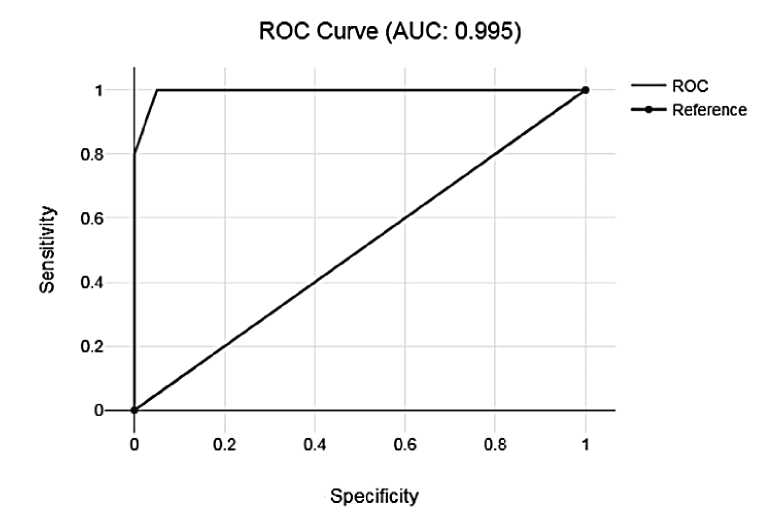
Рис. 3. ROC-кривая корреляции изменения концентрации действующего вещества во времени. ROC – показывает ROC-кривую; Reference – линия тренда; Sensitivity – чувствительность; Specificity – специфичность;
АUС – демонстрирует значение площади под кривой
Из данных рис. 3 можно четко утверждать, что в течение 15 мин концентрация всех исследуемых веществ в модельной системе плазмы крови значительно возрастает, что подтверждает высокую биодоступность данных соединений. Выявленная закономерность открывает широкие перспективы исследования данных соединений как парентеральных препаратов. Однако стоит отметить, что полученные гидразонопропилпроизводные практически нерастворимы в воде, которая является базовой составляющей всех компонентов внутренней среды организма, что в свою очередь определяет спектр научных исследований направленных на поиск наименее токсичного растворителя данных соединений и дальнейшего изучения биологических эффектов, проявляемых данными веществами.
Заключение
В ходе исследования нами впервые синтезирован ряд новых гидразонопропилпроизводных тиетанилированного 6-метилурацила, имеющих высокую биодоступность и обладающих, с высокой долей вероятности, определенным спектром биологических эффектов.
В заключении отметим, что практическая значимость подобной области исследований обусловлена ее широким применением в различных направлениях, от разработки новых лекарственных препаратов до создания функциональных материалов. Модифицированные азотистые основания находят применение для создания самособирающихся структур и наноматериалов. Кроме того, могут использоваться в качестве «строительных блоков» для сборки сложных молекулярных архитектур с заданными свойствами, а условия синтеза играют решающую роль, определяя успех и эффективность каждой реакции.


