Оптические свойства йод-полисахаридов крахмала пшеницы
Автор: Костенко В.Г., Подзигун Г.И., Коваленок В.А.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Пищевая биотехнология
Статья в выпуске: 4 (78), 2018 года.
Бесплатный доступ
Содержание амилозы в крахмале является одной из характеристик его качества. В основном оно является видовым признаком исходного крахмалсодержащего сырья и получаемого из него крахмала. От этого зависят физико-химические свойства крахмала и его использование в народном хозяйстве. В небольших количествах амилозу получают путём фракционирования крахмала. Это сложная и затратная технология. По созданию новых сортов картофеля, зерновых и зернобобовых культур с повышенным содержанием амилозы в крахмале проводят исследовательские работы селекционеры. Им нужны методики определения амилозы в разных видах сырья. Но прежде чем разрабатывать методику, необходимо исследовать оптические свойства того или иного вида крахмала и составляющих его компонентов. Как показали исследования, у разных видов крахмала оптические свойства компонентов крахмала разные. Например, методика, разработанная для определения амилозы в кукурузном крахмале, не приемлема для определения её в крахмале тритикале и пшеницы...
Крахмал тритикале, йод-амилоза, йод-амилопектин, йод-полисахарид, соединения-включения, оптическая плотность, длина волны, спектрофотометрия.
Короткий адрес: https://sciup.org/140244277
IDR: 140244277 | DOI: 10.20914/2310-1202-2018-4-288-291
Optical properties wheat starch iodine polysaccharides
The amylosecontents in starch is one of its qualitycharacteristics. Generally it is a specific sign of astarch-containing material and the starch received from it. Physical and chemical properties of starch and its use in the national economy depend on it. In small quantities the amylose is received by starch fractionating. It is the difficult and expensive technology. Selectors carry out research workson creation of new varieties of potatoes, grain and leguminous crops with the increased content of amylose in starch. They need techniques of definition of amylose in different types of raw materials. But before developing a technique, it is necessary to investigate optical properties of this or that type of starch and the components making it. It showed from researches, different types of starchhad differentoptical properties of itscomponents. For example, the technique developed for definition of amylose in corn starch isn't acceptable for its definition in starch of triticale and wheat...
Текст научной статьи Оптические свойства йод-полисахаридов крахмала пшеницы
Молекула крахмала состоит из двух полисахаридов – амилозы и амилопектина. Амилоза построена из молекул глюкозы, связанных между собой α-1–4 связями, закрученными в прямую двойную спираль правого вращения. Амилопектин представляет собой разветвленный полимер, состоящий из отрезков амилозы разной длины, соединенных α-1–6 связями с основной цепочкой. Точки ветвления повторяются примерно через 25 глюкозных единиц. Содержание амилозы и амилопектина в крахмале бывает разным в зависимости от биологического вида растения. От этого зависят химические и физико-химические свойства крахмала и его использование в различных областях народного хозяйства.
Крахмал и составляющие его полисахариды образуют с йодом соединения-включения. Под действием йода водные растворы крахмала и амилозы окрашиваются в синий цвет, амилопектина – в красно-фиолетовый. Это связано с различием в строении этих полисахаридов.
Объектом исследования были йод-полисахаридные соединения-включения крахмала пшеницы.
Цель работы – изучить оптические свойства йод-полисахаридов крахмала пшеницы и выявить сходство и различие оптических свойств от полисахаридов других видов крахмалов.
Материалы и методы
Объекты исследования: крахмал зерна пшеницы (ГОСТ 32092-2014) и его полисахариды, амилоза, амилопектин, их смеси в разных соотношениях.
Амилозу и амилопектин получали с использованием бутанола-1, изоамилового спирта, этанола согласно [1,2], используя способность амилозы в отличие от амилопектина образовывать кристаллический комплекс с бутанолом-1.
Осаждение осадков амилозы и амилопектина проводили на центрифуге лабораторной пробирочной ОС-6М (5500 об/мин, 15 мин).
Исходные растворы йода, амилозы, амилопектина, их смесей, крахмала приготавливали концентрацией 1 мг/см3 согласно [1, 2], исследуемые растворы – согласно условиям экспериментов. Полисахариды растворяли в 0,1 н растворе гидрооксида натрия при нагревании в кипящей водяной бане в течение 5 мин, подкисляли до рН 5,0–5,3 и разбавляли до концентрации 0,1 мг/см3.
Исходные растворы амилозы, амилопектина, крахмала, йода приготавливали концентрацией 1 мг/см3 [1, 2]. Взвешивали 100 мг безводного вещества в стакане вместимостью 100 см3, приливали 20 см3 0,1 н раствора NаОН. Стакан погружали в кипящую водяную баню, установленную на обогреваемую магнитную мешалку на 5 мин, затем вынимали, охлаждали, подкисляли уксусной кислотой до рН 5,0–5,3 и доливали дистиллированной водой до объема 100 см3.
Исследуемые растворы приготавливали согласно условиям экспериментов.
В мерную колбу вместимостью 100 см3 вносили исходные растворы, например, по 1; 2; 3; 4; 5; 6 см3 раствора амилозы и по 9; 8; 7; 6; 5; 4 см3 раствора амилопектина, чтобы их суммарная концентрация всегда была 0,1 мг/см3 в 100 см3. Концентрация йода и йодистого калия была разной в зависимости от условий опыта: йода 0,03–0,08 мг/см3 в 100 см3 при соотношении калия йодистого к йоду от 5 до 15. Таким образом, исследуемый раствор содержал от 0,01 до 0,06 мг/см3 амилозы (10–60%) и от 0,09 до 0,04 мг/см3 (90–40%) амилопектина и 0,03–0,08 мг/см3 йода.
Измерение оптических характеристик исследуемых растворов йод-полисахаридных комплексов амилозы, амилопектина, их смесей и крахмала проводили на отечественном спектрофотометре СФ-2000 в диапазоне 200–800 и 400–800 нм.
Результаты и обсуждение
Оптические свойства йод-полисахаридов, интенсивность их окраски зависят от многих факторов – от ботанического вида и сорта крахмала, степени его полимеризации, длины спиралей амилозы, как в амилопектине, так и в амилозе, его модификации (механической, химической или физико-химической). Они зависят от почвенноклиматических и агрохимических условий произрастания крахмалоносов и др.
Оптические свойства йод-полисахаридных комплексов пшеницы отличаются от аналогичных комплексов родственной культуры тритикале (гибрида пшеницы и ржи). Так, амилоза пшеницы имеет величину максимума оптической плотности λ mах при 600 нм, тогда как тритикале – 567 нм. Амилопектин пшеницы имеет λ mах при 565 нм (амилопектин тритикале его не имеет). Кроме этих природных факторов, есть факторы, влияющие на величину оптической плотности исследуемых растворов йод-полисахаридов в процессе приготовления исследуемых растворов. К ним относятся йод и калий йодистый.
Одними из факторов, влияющих на величину оптической плотности йод-полисахаридов, являются концентрации калия йодистого и йода в исследуемом растворе. Надо было установить концентрацию и количество йода, необходимого для полного насыщения полисахаридов йодом при образовании йод-полисахаридных комплексов и в то же время не допустить его большого избытка, так как он смещает максимум оптической плотности йод-полисахарида в коротковолновую область и в растворе с полисахаридами приводит к увеличению оптической плотности исследуемого раствора [4–10].
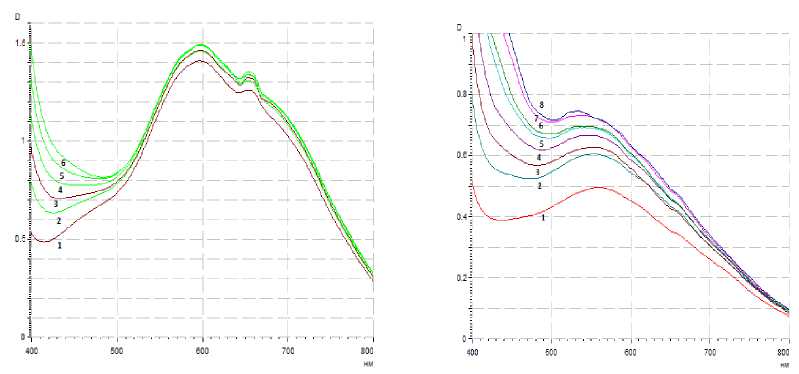
На рисунке 1а показаны спектры растворов йод-амилозы пшеницы (0,1 мг/см3) в зависимости от концентрации йода. Оптическая плотность растворов йод-амилозы пшеницы с повышением концентрации йода от 0,03 до 0,05 мг/см3 значительно возрастает, а при 0,06 и 0,07 мг/см3 кривые почти накладываются одна на другую. Это свидетельствует о насыщении обоих полисахаридов йодом. При дальнейшем исследовании использовали концентрацию йода 0,06 мг/см3.
b
a
Рисунок 1. Спектры растворов йод-амилозы ( a ) и йод-амилопектина ( b ) пшеницы (0,1 мг/см3) при разных концентрациях йода, мг/см3: 1 – 0,03; 2 – 0,04; 3 – 0,05; 4 – 0,06; 5 – 0,07; 6 – 0,08; 7 – 0,09; 8 – 0,1
Figure 1. The spectra of solutions of iodine-amylose ( a ) and iodine-amylopectin ( b ) of wheat (0.1 mg/cm3) at different concentrations of iodine, mg / cm3: 1 – 0.03; 2 – 0.04; 3 – 0.05; 4 – 0.06; 5 – 0.07; 6 – 0.08; 7 – 0.09; 8 – 0.1
На рисунке 1 b показаны спектры растворов йод-амилопектиновых соединений-включений пшеницы. Максимум оптической плотности йод-амилопектина находится при 565 нм. Хорошо видно влияние йода на йод-амилопекти-новые соединения-включения. Концентрация амилопектина в растворах одинаковая, изменяется только концентрация йода от 0,03 до 0,1 мг/см3. Оптическая плотность с увеличением концентрации йода повышается. При концентрации йода 0,07 и 0,08 мг/см3 и 0,09 и 0,1 мг/см3 кривые накладываются одна на другую. Достигнув максимального значения под влиянием йода, кривые расходятся – это проявляются оптические свойства йода в коротковолновой области спектра. При этом наблюдается незначительное смещение максимума кривых в коротковолновую область.
Как видно из рисунка 1, насыщение полисахаридов пшеницы йодом происходит при концентрации йода 0,06 мг/см3.
Смеси амилозы и амилопектина пшеницы имеют λ mах при 600 нм независимо от концентрации амилозы в смеси. Следует отметить, что величина оптической плотности D смеси больше, чем величина оптической плотности чистой амилозы (рисунок 2) .
Величина оптической плотности D характеризует количество амилозы, вступившей во взаимодействие с йодом. Увеличение оптической плотности в смесях при 600 нм не может быть объяснено наложением пика амилопектина в этой области, так как оптическая плотность D йод-амилопектина при 600 нм существенно ниже, чем оптическая плотность D йод-амилозы. Одним из возможных объяснений является образование в растворе смеси амилозы с амилопектином ассоциатов, в результате чего в мо ните мол
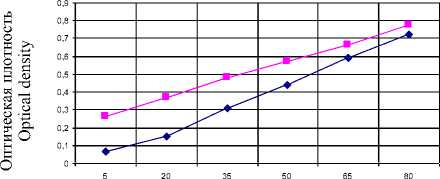
Содержание амилозы, % | Amylase content, %
Рису содержания амилозы и содержания амилозы в смеси с амилопектином пшеничного крахмала
Figure 2. The dependence of optical density on the amylose content and amylose content in a mixture with wheat starch amylopectin
Образование ассоциатов амилозы с амилопектином достигает максимума при соотношении амилозы и амилопектина 1:1.
Таким образом, спектры смесей амилозы и амилопектина не являются суммарным наложением спектров двух разных по свойствам соединений, а являются спектром единого комплекса соединений, находящихся в исследуемом растворе. Тем более что при 600 нм амилопектин имеет низкую оптическую плотность.
Выводы
-
1. Спектры полисахаридов пшеницы отличаются по величине λ mах и форме кривых от родственных полисахаридов тритикале.
-
2. Йод-амилоза пшеницы имеет максимум при 600 нм, йод-амилопектин – при 565 нм.
-
3. Концентрация йода в исследуемом растворе должна быть равной 0,6 мг/см3.
-
4. Мольное соотношение калия йодистого к йоду должно быть равным 5.
Список литературы Оптические свойства йод-полисахаридов крахмала пшеницы
- Wang J.P., Li Y., Tian Y.Q., Xu X.M. et al. A novel triple-wavelength colorimetric method for measureing amylase and amylopectin contents//Starke. 2010. № 10. Р. 508-516.
- Костенко В.Г., Подзигун Г.И., Лукин Н.Д., Ковалёнок В.А. Изучение оптических свойств кукурузного крахмала//Достижения науки и техники АПК. 2016. Т.30. № 12. С. 110-112.
- Дашевский В.Г. Конформационный анализ макромолекул. М.: Наука, 1987. 180 с.
- Tintu I., Abhilash J., Dileep K.V., Augustine A. et al. A Lectin from S patholobus parviflorus Inhibits A spergillus flavus ??Amylase: Enzyme Kinetics and Thermodynamic Studies//Chemical biology & drug design. 2014. V. 84. № 1. P. 116-122.
- Okon E., Etta H., Nenco N. Investigating the effect of growth regulator, furolan on starch and protein contents in winter wheat cultivars//Russian agricultural sciences. 2015. V. 41. № 2-3. P. 107-110.
- Lim Y.-M., Hoobin P., Ying D., Burgar I. et al. Physical characterisation of high amylose maize starch and acylated high amylose maize starches//Carbohydrate polymers. 2015. V. 117. P. 279-285.
- Yang Y., Rao Y., Xu J., Shao G. et al. Genetic analysis of sugar-related traits in rice grain//South African Journal of Botany. 2014. V. 93. P. 137-141.
- Sivapragasam N., Ohm J.-B., Thavarajah P. et al. Novel starch based nano scale enteric coatings from soybean meal for colon-specific delivery//Carbohydrate polymers. 2014. V. 111. P. 273-279.
- Struyf N., Laurent J., Lefevere B., Verspreet J. et al. Establishing the relative importance of damaged starch and fructan as sources of fermentable sugars in wheat flour and whole meal bread dough fermentations//Food chemistry. 2017. V. 218. P. 89-98.
- Singh H., Saharan R., Sharma K.P. Isolation and Characterization of Amylase producing Bacteria from Diverse Environmental samples//Journal of Microbiology and Biotechnology Research. 2017. V. 4. №. 4. P. 8-18.


