Оптические свойства триэтиламиниевой соли трифторуксусной кислоты
Автор: Семенов В.В., Золотарева Н.В., Лопатин М.А.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 2 т.16, 2024 года.
Бесплатный доступ
Триэтиламиний трифторацетат (CH3CH2)3NH+ -O(O)C-CF3, полученный взаимодействием трифторуксусной кислоты с триэтиламином, представляет собой бесцветную ионную жидкость, переходящие в паровую фазу при нагревании до 200-220 °С. Соединение охарактеризовано методами элементного анализа, инфракрасной спектроскопии, ядерного магнитного резонанса на ядрах 1Н и 13С, масс-спектроскопии, термогравиметрии, дифференциальной сканирующей калориметрии, рефрактометрии, электронной спектроскопии поглощения и испускания. В УФ-спектре наблюдается слабая полоса поглощения в диапазоне 260-340 нм. При возбуждении в область 320 нм соединение показывает две полосы фотолюминесценции 375 и 425 нм. Ионная жидкость хорошо растворяет координационные соединения лантаноидов: фенантролин теноилтрифторметилацетонат эрбия(III) Er(tta)3·phen, тригидрат трис(3-трифторацетамидобензоилтрифторацетонат) европия(III) и ацетилацетонат гольмия(III) Но(асас)3. Представлены спектры поглощения β-дикетонатов эрбия(III), европия(III), гольмия(III) и спектры испускания β-дикетонатов эрбия(III) и европия(III).
Ионная жидкость, β-дикетонаты лантанидов, растворимость, тга, дск, электронные спектры поглощения и испускания, ик, ямр, масс-спектры
Короткий адрес: https://sciup.org/147244626
IDR: 147244626 | УДК: 547.1-32-304-2, | DOI: 10.14529/chem240214
Optical properties of triethylaminium salt of trifluoroacetic acid
Triethylaminium trifluoroacetate (CH3CH2)3NH+ -O(O)C-CF3, obtained by reacting trifluoroacetic acid with triethylamine, is a colorless ionic liquid that passes into the vapor phase when heated to 200-220 °C. The compound has been characterized by elemental analysis, infrared spectroscopy, 1H and 13C nuclear magnetic resonance, mass spectroscopy, thermogravimetry, differential scanning calorimetry, refractometry, electron absorption and emission spectroscopy. In the UV spectrum there is a weak absorption band in the range of 260-340 nm. When excited at 320 nm, the compound shows two photoluminescence bands at 375 and 425 nm. The ionic liquid readily dissolves lanthanide coordination compounds: erbium(III) phenanthroline thenoyltrifluoromethyl acetonate Er(tta)3·phen, europium(III) tris(3-trifluoroacetamidobenzoyltrifluoroacetonate) and holmium(III) acetylacetonate Ho(acac)3. The absorption spectra of erbium(III), europium(III), holmium(III) β-diketonates and emission spectra of erbium(III) and europium(III) β-diketonates are presented.
Текст научной статьи Оптические свойства триэтиламиниевой соли трифторуксусной кислоты
Аминиевые соли органических кислот используются в качестве фармацевтических препаратов [1–4] и ионных жидкостей [5–8]. Для лекарственных средств необходимым качеством является хорошая растворимость в водной среде, для ионных жидкостей – низкая температура плавления. Соединения данного типа представляют собой органические соли с разделённой ионной парой, в которых существуют внутримолекулярные взаимодействия между катионной и анионной частицами. В работе [9] на примере комплекса триэтиламина с 1-гидроксиэтилидендифосфоновой кислотой было показано, что энергия водородной связи может достигать 24 ккал/моль. Столь большая величина должна предотвращать диссоциацию на амин и кислоту при попытках возгонки, как это происходит, например, в случае хлористого аммония. Представленные в работах [9–12] аминиевые соли органических и фосфорорганических кислот выделяли в чистом виде перекристаллизацией из органических растворителей или из водных растворов. Синтезированные соединения разлагались, но не подвергались сублимации при нагревании в вакууме. В настоящем сообщении представлены сведения о синтезе и исследовании оптических свойств аминиевой соли летучей трифторуксусной кислоты с три-этиламином. При комнатной температуре она представляет собой прозрачную подвижную жидкость. Ранее такое соединение было получено в [13], однако метод очистки перегонкой в вакууме не использовался, растворяющая способность и оптические свойства не исследовались.
Экспериментальная часть
ИК-спектры соединений в виде суспензии в вазелиновом масле между пластинами KBr регистрировали на ИК Фурье-спектрометре ФСМ 1201, спектры ЯМР 1Н и 13С – на ЯМР-спектрометре Avance NEO 300 (Bruker Avance III 400) в D 2 O. Электронные спектры поглощения измеряли нa спектрофотометре Perkin-Elmer Lambda 25 в диапазоне 250–950 нм в однолучевом режиме в 1 мм кварцевой кювете в растворе триэтиламиний трифторацетата. Спектры флуоресценции записаны на спектрофлуориметре Perkin-Elmer LS 55 в режиме регистрации свечения при направлении возбуждающего луча под углом 45°. Для компенсации отраженного обертона в регистрирующем монохроматоре применялся фильтр до 390 нм. Образец помещался в 1 мм кювету из оптического кварца. Элементный анализ выполнен на автоматическом элементном анализаторе Vario EL cube (Elementar Analysensysteme GmbH) в конфигурации CHNS, газ-носитель – гелий марки 6.0. Масс-спектры измерены на хромато-масс-спектрометре Polaris Q с хроматографом Trace GC Ultra. Термический анализ выполнен на приборе синхронного термического анализа TGA/DSC 3+ METTLER TOLEDO, скорость нагрева составляла 5 град/мин, скорость подачи азота – 50 мл/мин. Измерения проводились в температурном интервале от +25 до +500 °С. В работе использовали трифторуксусную кислоту производства Acros Organics, фенантролин теноилтрифторметилацетонат эрбия(III) и ацетилацетонат гольмия(III) производства ООО «ДАЛХИМ» (Н. Новгород).
Семенов В.В., Золотарева Н.В., Оптические свойства Лопатин М.А. триэтиламиниевой соли трифторуксусной кислоты
Триэтиламиний трифторацетат (1) . К раствору 3,93 г (3,45·10–2 моль) трифторуксусной кислоты в 20 мл ацетона прибавляли по каплям при перемешивании 3,49 г (3,45·10–2 моль) триэти-ламина в 15 мл ацетона. Смесь слабо нагревалась, в колбе в газовой фазе образовался густой туман. Смесь перемешивали 1 ч, ацетон отгоняли, жидкий остаток перегоняли в вакууме. Получили 6,09 г (2,83·10–2 моль, 82 %) триэтиламиний трифторацетата (CH 3 CH 2 ) 3 NH + ‒ O(O)C‒CF 3 (III) в виде бесцветной прозрачной жидкости, т. кип. 98–103 °С (2 мм. рт. ст.) n D 20 1,3961, d 4 20 1,1878, MR D 43,54. Найдено, %: С 44,15; Н 7,68; N 6,30. C 8 H 16 NO 2 F 3 . Вычислено, %: С 44,55; Н 7,49; N 6,51. ИК-спектр, см–1: 3443, 2993, 2952, 2892, 2675, 2642, 2490, 1787, 1685, 1471, 1405, 1361, 1316, 1200, 1176, 1128, 1072, 1036, 827, 798, 717, 595, 535, 518, 464. Масс-спектр, m/e: 213, 199, 185, 161, 149, 147, 135, 121, 111, 101, 97, 95, 81, 69, 67, 58. ЯМР 1Н (D 2 O): 0,96–1,17 (м., CH 3 , 9H); 2,9– 3,11 (м., CH 2 , 6H). ЯМР 13C{1H} (D 2 O): 8,13 (c., CH 3 ); 46,53 (c., CH 2 ); 110,73–122,4 (м, CF 3 ); 168,87–173,03 (м, С(О)). Соединение смешивается с водой, ацетоном, диоксаном, ацетонитрилом, этилацетатом, диметоксиэтаном, толуолом.
Обсуждение результатов
Триэтиламиний трифторацетат (I) получали взаимодействием трифторуксусной кислоты с триэтиламином в среде ацетона:
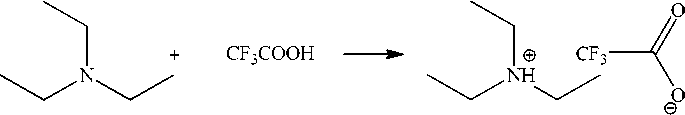
Соединение представляло собой прозрачную бесцветную жидкость, перегоняющуюся в вакууме без разложения. В масс-спектре наблюдались пики молекулярных ионов аминиевой соли 213 ([М-2]+, 32 %) и триэтиламина 101 (34 %), а также осколочные ионы CF 3 CO (97, 64 %), CF 3 C (81, 100 %) и CF 3 (69, 40 %). Присоединение триэтиламина кардинальным образом изменило ИК-спектр трифторуксусной кислоты. На месте интенсивной широкой полосы гидроксильной группы 3500–2700 см–1 появилась серия менее интенсивных полос поглощения валентных колебаний связей С–Н 2993, 2952, 2892 см–1 этильных групп и связей N–H 2675, 2642, 2490 см–1 в положительно заряженном фрагменте HN+(CH2CH3)3. Самая интенсивная полоса поглощения группы С=О 1781 см–1 сместилась в высокочастотную область до 1685 см–1 и слилась с полосой деформационных колебаний связи N–H.
Термограммы триэтиламиний трифторацетата 1 имели самый простой вид (рис. 1) и состояли из одного эндотерма в области 180–215 оС, что соответствовало испарению соединения.
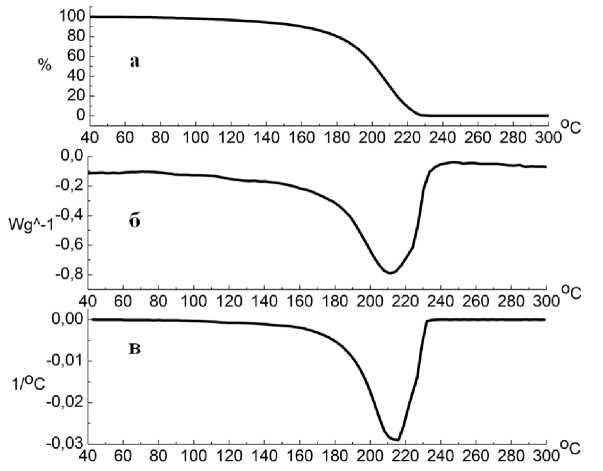
Рис. 1. Термический анализ триэтиламиний трифторацетата 1: а – ТГА, б – ДСК, в – ДТГ
В электронном спектре поглощения жидкого соединения 1 , не разбавленного растворителем, наблюдалась (рис. 2а) малоинтенсивная полоса в диапазоне 265–340 нм. При возбуждении в полосу 300 нм триэтиламинная соль показала (рис. 2б) спектр фотолюминесценции (СФЛ) в области 350–500 нм. Одно из необходимых качеств ионных жидкостей заключается в способности к растворению неорганических и координационных соединений. Удобными кандидатами для такого рода проверки являются соединения лантаноидов, служащие распространенными люминесцентными зондами [14] в химии и биологии. С целью проверки на растворимость и на интенсивность сольватации (влияние на координационную сферу лантаноида) были измерены ЭСП и СФЛ растворов трех β-дикетонатов. В качестве таковых были выбраны фенантролин теноилтрифторметилацето-нат эрбия(III) Er(tta) 3 ·phen ( 2 ), тригидрат трис(3-трифторацетамидобензоилтрифторацетонат) евро-пия(III) ( 3 ) [15] и ацетилацетонат гольмия(III) Но(асас) 3 ( 4 ):
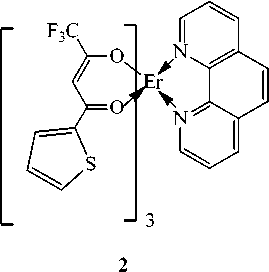
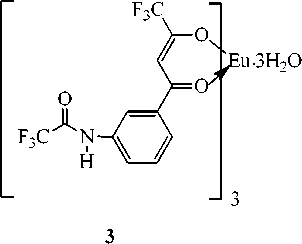
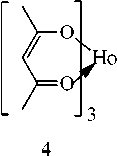
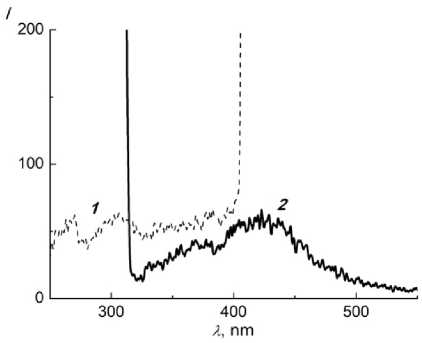
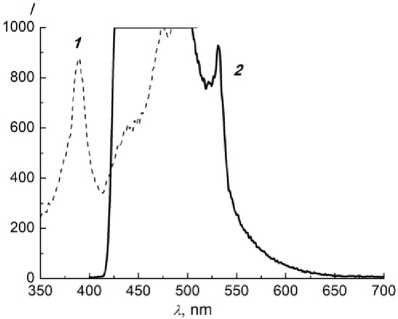
Выбор был обусловлен следующими обстоятельствами. Известно [16–20], что арильные группировки в составе координационных соединений лантаноидов (соединение 2 ) усиливают интенсивность фотолюминесценции, а фторорганические заместители в лиганде (соединение 3 ) могут повышать растворимость. Соединение 4 не имеет арильной группы и атомов фтора. Известно [21], что ацетилацетонаты европия проявляют яркую фотолюминесценцию в красной области спектра, в то время как аналогичные комплексы эрбия имеют серию малоинтенсивных полос испускания в диапазоне 230–660 нм. При возбуждении в полосу 360 нм удалось (рис. 3) зафиксировать переход 4I 15/2 →2H 11/2 в катионе Er3+ при 530 нм. Как и ожидалось, фотолюминесценция комплекса европия (рис. 4) оказалась [22, 23] намного более интенсивной.
Положение и интенсивности полос в спектрах фотолюминесценции мало отличаются от спектров данных комплеков, измеренных в ацетонитриле. Это свидетельствует о том, что ионная жидкость выступает в качестве простого растворителя, молекулы которого не входят в первую координационную сферу лантаноида и не влияют на интенсивность сверхчувствительных переходов.
а)
б)
Рис. 2. ЭСП (а) и СФЛ (б) триэтиламинийтрифторацетата 1: 1 – спектр возбуждения, 2 – спектр испускания
Семенов В.В., Золотарева Н.В., Лопатин М.А.
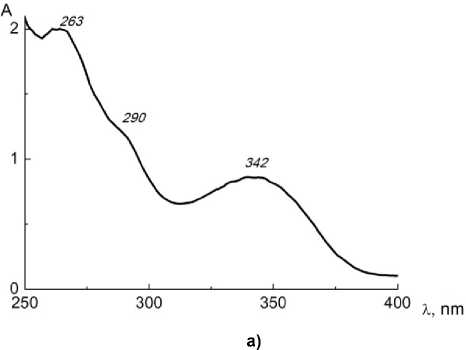
Рис. 3. ЭСП (а) и СФЛ (б) раствора Er(tta) 3 · phen 2 в триэтиламинийтрифторацетате 1: 1 – спектр возбуждения ФЛ, 2 – спектр испускания, С 1,73·10–2 моль·л–1
б)
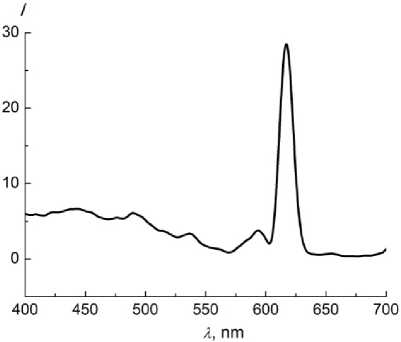
Рис. 4. Спектр ФЛ раствора комплекса европия 3 в триэтиламинийтрифторацетате, возбуждение 360 нм, С 1,13·10–2 моль ‧ л–1
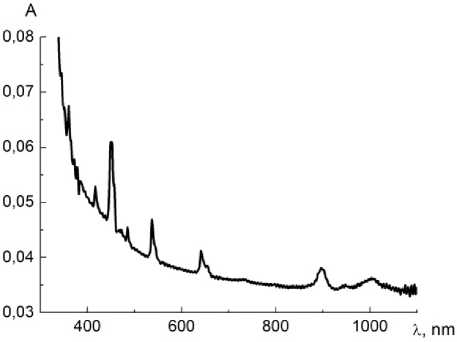
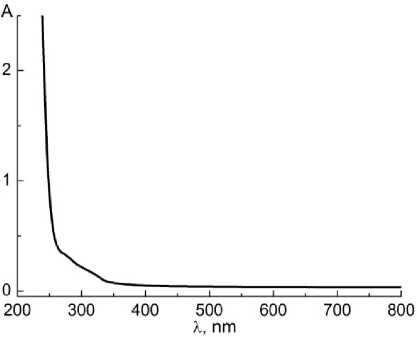
Рис. 5. ЭСП раствора Но(асас) 3 4 в триэтиламиний-трифторацетате, С 1,87·10–2 моль ‧ л–1
Ацетилацетонат гольмия(III) 4 быстро растворился в ионной жидкости, но раствор не проявил фотолюминесценцию при возбуждении в наиболее интенсивные полосы поглощения 450 и 537 нм. ЭСП содержал все ожидаемые для катиона Но3+ переходы: 5I 8 →3H 6 , 360 нм; 5I 8 →5G 5 , 417 нм; 5I 8 →5G 6 , 450 нм; 5I 8 →5F 3 , 485 нм; 5I 8 →5F 4 , 537 нм; 5I 8 →5F 5 , 642 нм, а также полосу 897 нм, отнесенную к обертону карбоксильной группы ионной жидкости (рис. 5).
Способность к быстрому растворению β-дикетонатов лантаноидов различается. Наличие в молекуле соединения эрбия фенантролина существенно понижает и замедляет растворение, в то время как растворимость фторсодержащего комплекса европия 3 и не содержащего атомов фтора соединения гольмия 4 практически не различается.
Заключение
Разработан способ получения аминиевой соли трифторуксусной кислоты, обладающей свойствами ионной жидкости. Показано, что прозрачная бесцветная ионная жидкость может быть легко очищена перегонкой в вакууме, прозрачна в широком диапазоне УФ-видимого спектра, имеет только очень слабое поглощение при 265–340 нм, хорошо растворяет координационные соединения лантаноидов, растворы β-дикетонатов европия(III) и эрбия(III) показывают ожидаемую фотолюминесценцию, обусловленную f-f-переходами в соответствующих катионах, мало влияет на интенсивность сверхчувствитильных переходов.
Список литературы Оптические свойства триэтиламиниевой соли трифторуксусной кислоты
- Граник В.Г. Основы медицинской химии. М.: Вузовская книга, 2006. 383 с.
- Silva M.R., Paixao J.A., Beja A.M., da Veiga L.A. // Acta Cryst., Sect. C. 2001. V. 57. P. 421. DOI: 10.1107/S0108270100020266/bj1011sup1.cif.
- Adamovich S.N., Oborina Е.N., Ushakov I.А., Mirskova A.N. // Rus. J. Gen. Chem. 2018. V. 88, No. 10. P. 2227. DOI: 10.1134/S1070363218100353].
- Voronkov M.G., Rasulov M.M. // Pharm. Chem. J. 2007. V. 41, No. 1. P. 1. DOI: 10.1007/s11094-007-0001-x.
- Адамович С.Н., Мирсков Р.Г., Воронков М.Г. // Изв. АН. Сер. хим. 2010. № 10. С. 1993.
- Kondratenko Yu.A., Kochina T.A., Fundamenskii V.S. // Glass Phys. Chem. 2016. V. 42, No. 6. P. 621. DOI: 10.1134/S1087659616060092.
- Kondratenko Yu.A., Nyanikova G.G., Molchanova K.V., Kochina T.A. // Glass Phys. Chem. 2017. V. 43, No. 5. P. 445. DOI: 10.1134/S108765961705008X.
- Zakharov M.A., Filatova Yu.V., Bykov M.A., Avramenko N.V., Aslanov L.A. // Rus. J. Coord. Chem. 2020. Vol. 46. P. 268. DOI: 10.1134/S1070328420040077.
- Semenov V.V., Zolotareva N.V., Novikova O.V., Petrov B.I., Lazarev N.M., Fukin G.K., Cherkasov A.V., Razov E.N. // Rus. Chem. Bul. 2022. No. 5. P. 980. DOI: 10.1007/s11172-022-3500-8.
- Семенов В.В., Новикова О.В., Румянцев Р.В., Петров Б.И., Разов Е.Н. // Кристаллография. 2022. Т. 67, № 2. С. 239. DOI: 10.31857/0023476122020175.
- Румянцев Р.В., Золотарева Н.В., Новикова О.В., Петров Б.И., Лазарев Н.М., Семенов В.В. // Кристаллография. 2021. Т. 66, № 3. С. 448. DOI: 10.31857/S002347612103022X.
- Semenov V.V., Zolotareva N.V., Petrov B.I. et al. // Rus. Chem. Bul. 2020. No. 9. P. 1778. DOI: 10.1007/s11172-020-2962-9.
- Schmukler L.E., Gruzdev M.S., Kudryakova N.O. et al. // RSC Adv. 2016. No. 6. P.109664. DOI: 10.1039/c6ra21360.
- Золин В.Ф., Коренева Л.Г. Редкоземельный зонд в химии и биологии. М.: Наука, 1980. 350 с.
- Semenov V.V., Zolotareva N.V., Cherkasov A.V. // Rus. J. Gen. Chem. 2012. V. 82, No. 5. P. 874. DOI: 10.1134/S107036321205012X.
- Binnemans K. // Chem. Rev. 2009. Vol. 109, No. 9. P. 4283. DOI: 10.1021/cr8003983.
- Kido J., Okamoto Y. // Chem. Rev. 2003. Vol. 102, No. 6. P. 2357. DOI: 10.1021/cr010448y.
- Bünzli J.C.G., Chauvina A.S., Kimb H. K. et al. // Coord. Chem. Rev. 2010. V. 254. P. 2623. DOI: 10.1016/j.ccr.2010.04.002.
- Escribano P., Julian-Lopez B., Planelles-Arago J. Et al. // J. Mater. Chem. 2008. V. 18, No. 1. P. 23. DOI: 10.1039/b710800a.
- Bunzli J.C.G., Piguet C. // Chem. Soc. Rev. 2005. V. 34, No. 9. P. 1048. DOI: 10.1039/b406082m.
- Полуэктов Н.С., Кононенко Л.И., Ефрюшина Н.П. и др. Спектрофотометрические и люминесцентные методы определения лантаноидов. Киев: Наукова думка, 1989. 256 с.
- Liang F., Zhou Q., Cheng Y. et al. // Chem. Mater. 2003. V. 15, No. 10. P. 1935. DOI: 10.1021/cm0257724.
- Zhanga R.J., Yanga K.Z., Yub A.C. et al. // Thin Solid Films. 2000. V. 363, No. 1-2. P. 275. DOI: 10.1016/S0040-6090(99)01004-4.


