Оптимизация методики выявления ДНК Cryptosporidium spp. в образцах кала телят методом ПЦР и сравнение полученных результатов с результатами микроскопии
Автор: Карсека С.А., Давыдова Е.Е., Новикова Т.В., Воеводина Ю.А., Рыжакина Т.П., Шипулин Г.А.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Ветеринарная санитария и диагностика
Статья в выпуске: 4 т.60, 2025 года.
Бесплатный доступ
Кишечные инфекции наносят существенный вред животноводству. Среди паразитарных инфекций наиболее остро эта проблема стоит для криптоспоридиоза. Мониторинг и своевременная диагностика способны существенно снизить заболеваемость криптоспоридиозом среди новорожденных телят. Известно, что молекулярные методы, основанные на полимеразной цепной реакции (ПЦР), обладают высокой чувствительностью, однако при диагностике паразитарных инфекций неэффективная пробоподготовка способна нивелировать это преимущество. В настоящей работе впервые в России мы провели сравнительный анализ различных методов выделения ДНК из фекалий и выбрали оптимальный - с предварительным измельчением образцов мелющими гранулами (bead-beating) и экстракцией ДНК на колонке. Выбранный способ лег в основу разработанной методики диагностики криптоспоридиоза с использованием ПЦР в реальном времени, которая по чувствительности не уступает методам микроскопии. Нашей целью стала разработка метода ПЦР-диагностики криптоспоридиоза, ее апробация на образцах биологического материала от животных и сравнение результатов, полученных этим методом и классическими микроскопическими методами. Образцы фекалий телят голштинской породы были собраны в 2023 году в хозяйствах Вологодской области. Сбор образцов проводили после вспышки криптоспоридиоза в период лечения. Всего было собрано 20 образцов. Образцы фекалий отбирали непосредственно из прямой кишки животного в чистую емкость, каждый образец делили на две пробы, одну из которых использовали для микроскопического исследования по стандартному протоколу, а вторую направляли для ПЦР-исследования, предварительно поместив ее в 70 % раствор этилового спирта для консервации. Для обнаружения криптоспоридий в пробах кала использовали набор для окрашивания по Цилю-Нильсену Диахим (НПФ «Абрис+», Россия). Микроскопию проводили с увеличением ×1000 с масляной иммерсией (световой микроскоп Olympus cx33, «Olympus», Япония). По числу выделенных ооцист в расчете на 1 г фекалий определяли степень инвазированности животных. Для разработки тест-системы на основе ПЦР были выбраны специфические олигонуклеотидные праймеры Crypt-F 5´-TAATCAAGAACGAAAGTTAGGGGA-3´, Crypt-R 5´-GAGTAAGGAACAACCTCCAATCT-3´, флуоресцентный зонд Crypt-P R6G-5´-ATGGTTAAGACTACGACGGTATCTGA-3´-BHQ1 в области гена 18S рРНК, позволяющие выявлять все виды Cryptosporidium . Для пробоподготовки образцов кала применяли различные протоколы, включающие использование стандартных концентраторов ГЕМ (ООО «ГЕМ», Россия), концентраторов ГЕМ без формалина или предусматривающие промывку биообразцов фосфатным буфером без концентрирования. После пробоподготовки для экстракции ДНК из осадка кала использовали набор QIAamp PowerFecal Pro DNA Kit («QIAgen», Германия), включающий стадию очистки ДНК на спин-колонках. Для выделения ДНК из надосадочной фракции осветленного экстракта фекалий, полученной при пробоподготовке по МУ 1.3.2569-09, использовали набор АмплиТест РИБО-преп (ФГБУ ЦСП ФМБА, Россия), позволяющий получить очищенную ДНК методом спиртового осаждения. Мы не выявили преимуществ пробоподготовки с использованием концентраторов ГЕМ, а пробоподготовка в присутствии формалина негативно сказывалась на результатах ПЦР. Получение надосадочной фракции осветленного экстракта с последующей экстракцией ДНК набором АмплиТест РИБО-преп также не позволяло эффективно выделять ДНК Cryptosporidium из-за высоких потерь ооцист в осадочной фракции кала. Эффективными для пробоподготовки биоматериала и экстракции паразитарной ДНК оказались протоколы, предполагающие экстракцию ДНК из цельного кала с механическим дроблением и последующей очисткой ДНК на спин-колонках. Механическое дробление образцов кала твердыми гранулами в пробирках проводили на гомогенизаторе TissueLyser LT («QIAgen», Германия), при этом происходили как гомогенизация материала, облегчающая последующие этапы очистки ДНК, так и разрушение клеток, включая паразитарные, для полного высвобождения нуклеинового материала. По результатам сравнительного эксперимента ооцисты Cryptosporidium spp. были обнаружены методом микроскопии в 15 из 20 проб, причем четыре из 15 положительных образцов имели крайне низкое их содержание, единичные ооцисты. При использовании наилучшего способа пробоподготовки и экстракции ДНК в ПЦР с использованием собственной методики также 15 образцов из 20 были определены как положительные. Для образцов с высоким и умеренным содержанием ооцист криптоспоридий результаты, полученные методом ПЦР, полностью совпали с данными микроскопии. Для двух образцов с низким содержанием ооцист результаты микроскопии и ПЦР расходились: методом ПЦР один образец был определен как слабоположительный (Ct > 40), хотя микроскопия показала отрицательный результат, и наоборот, второй образец, слабоположительный методом микроскопии («+»), был определен как отрицательный методом ПЦР.
Cryptosporidium spp, фекалии, крупный рогатый скот, экстракция днк, пцр, молекулярная диагностика
Короткий адрес: https://sciup.org/142246217
IDR: 142246217 | УДК: 579.62:57.08:577.2 | DOI: 10.15389/agrobiology.2025.4756rus
Optimization of the method for detecting Cryptosporidium spp. DNA in fecal samples from calves using PCR and comparison of the obtained results with the results of microscopy
Intestinal infections cause significant damage to cattle farms; one of the most acute problem is cryptosporidiosis. But the early diagnostics can significantly reduce the incidence of cryptosporidiosis in neonatal calves. The most sensitive are molecular methods based on polymerase chain reaction (PCR), but an inappropriate DNA preparation protocol can reduce it. Currently, this problem prevents the spread of the PCR in the routine diagnosis of parasitosis. In the present study, for the first time in Russia various methods of DNA extraction from feces were compared and the most optimal one was selected: with preliminary bead-beating and DNA sorption on the spin-column. Further this method was used as basic for real-time PCR developed for diagnosing cryptosporidiosis. Our new system was tested on real samples from calves and compared with classical microscopy; that was our target. 20 fecal samples from calves (Holstein breed) were collected directly from rectum on farms located in Vologda region, in 2023, after cryptosporidiosis outbreak. Each sample was divided in two aliquots, first for microscopy detection by Ziehl-Neelsen staining using Diakhim kit («Abris+», Russia), second was fixed in 70% ethanol for molecular detection. Stained sliders were observed with Olympus cx33 light microscope (Olympus, Japan) at x1000 magnification using oil immersion. The degree of infection was assessed. To develop a PCR-based test-system primers for 18S rRNA Cryptosporidium spp. Crypt-F 5´-TAATCAAGAACGAAAGTTAGGGGA-3´ Crypt-R 5´-GAGTAAGGAACAACCTCCAATCT-3´, probe Crypt-P R6G-5´-ATGGTTAAGACTACGACGGTATCTGA-3´-BHQ1 were designed allow detection of all species of Cryptosporidium . A few modified DNA extraction protocols of fecal samples were evaluated: using conventional concentrates HEM (LLC HEM, Russia), concentrates HEM without formaldehyde or washing by phosphate buffer without concentration. Then QIAamp PowerFecal Pro DNA Kit (QIAgen, Germany) were used to extract DNA from the received fecal sediment, including a stage of DNA purification on spin columns. Clarified fecal extract was obtained in accordance with the guidelines MU 1.3.2569-09, DNA was extracted by precipitation method using AmpliTest RIBO-prep kit (Centre for Strategic Planning and Management of Biomedical Health Risks, of the Federal medical and biological agency, Russia). As a result sample preparation using HEM concentrators had no advantages, and sample preparation in the presence of formalin had a negative effect on PCR. Obtaining the supernatant of the clarified fecal extract and then DNA extraction using AmpliTest RIBO-prep kit allow only poor detection of Cryptosporidium due to the high loss of oocytes in the sedimentary fraction of feces. Extraction of DNA from crude feces using bead-beating and purification on spin columns proved to be effective for receiving of parasitic DNA. Homogenization of feces, cell disruption and release of nucleic material are carried out during bead-beating on a TissueLyser LT homogenizer (QIAgen, Germany). Cryptosporidium oocysts were detected in 15 of 20 samples, but 4 of them have extremely low concentration of oocysts. Using the most effective PCR-based assay, 15 of 20 samples also were positive. Accordingly, all samples with high and medium level of Cryptosporidium oocysts were PCR positive. But two samples with low level of oocyst have different results of microscopy and PCR, one was determined to be weakly positive by PCR (Ct> 40) although microscopy was negative, and conversely, the second one was weakly positive by microscopy (“+”), but determined as negative by PCR. Additionally commercially kit for DNA extraction and PCR detection DNA Cryptosporidium spp. FBioNucleo (Fractal Bio, Russia) was tested. Cryptosporidium spp. was detected in 9 of 20 samples, all weakly positive and two medium positive samples were determined as negative. Thus, the FBioNukleo kit showed lower sensitivity than the assay proposed. Finally, an effective assay has been designed including bead-beating and purification on spin columns, which provides the sensitivity of PCR similar to the microscopy with Ziehl-Neelsen staining.
Текст научной статьи Оптимизация методики выявления ДНК Cryptosporidium spp. в образцах кала телят методом ПЦР и сравнение полученных результатов с результатами микроскопии
Сохранение молодняка — основная проблема для хозяйств, занимающихся разведением крупного рогатого скота. По статистике среди болезней телят на первом месте находятся заболевания желудочно-кишечного тракта, смертность может достигать 55 % (1, 2). Стратегия лечения зависит от того, каким агентом вызвана диарея — вирусным, бактериальным или протозо-озным, поэтому установление этиологических агентов заболеваний необходимо для повышения эффективности лечения.
Совершенствование диагностики кишечных инфекций необходимо для устойчивого развития фермерских хозяйств. После ротавируса крипто-споридиии занимают второе место как причина диарейных симптомов у новорожденных телят (3, 4), а распространенность криптоспоридиоза среди крупного рогатого скота в мире варьирует от 11,7 до 78 % (5-9). В Российской Федерации практически не проводится мониторинг криптоспоридиоза, однако ряд научных работ показывает, что ситуация не отличается от общемировой, заболеваемость криптоспоридиозом колеблется в пределах 4-90 % в зависимости от региона, времени года и возраста телят (10-12).
Криптоспоридии относятся к типу Apicomplexa , класс Conoidasida , подкласс Coccidia . Это облигатные внутриклеточные паразиты, поражающие энтероциты, что приводит к воспалению слизистой кишечника, нарушению всасывания питательных веществ, снижению ферментативной активности и развитию патогенный микрофлоры. В дальнейшем это может отразиться на росте и развитии молодняка крупного рогатого скота, поскольку от состояния кишечника зависит потребление и усвоение кормов (13, 14). Телята, зараженные криптоспоридиозом, теряют до 20-30 % массы в течение 1,5-2 нед (15, 16).
Известно более 40 видов рода Cryptosporidium . Чаще всего крупный рогатый поражают криптоспоридии четырех видов — C. parvum , C. bovis , C. andersoni , C. ryanae , но могут встречаться и другие виды, например C. suis , C. hominis , C. serpentis , C. xiaoi , C. ubiquitum , C. meleagridis , C. muris , C. felis (17, 18). Криптоспоридии могут заражать других млекопитающих и птиц, а также человека. Криптоспоридиоз часто встречается как коинфекция при сальмонеллезе, эшерихиозе, рото- и коронавирусных инфекциях (19-21).
Современная диагностика криптоспоридиоза основана прежде всего на применении микроскопических методов с различными модификациями, из которых наиболее распространены окрашивание по Цилю-Нельсену и по Романовскому-Гимзе. Микроскопические методы могут комбинироваться с иммунологическими, например с использованием иммунномагнитной сепарации с последующим иммунофлуоресцентным мечением, что значительно повышает эффективность диагностики (22). Однако существенным недостатком микроскопических методов остается зависимость результатов исследования от квалификации специалиста (18, 23, 24). При диагностике криптоспоридиоза это особенно актуально, так как ооцисты криптоспоридий мелкие, их легко спутать с остатками непереваренных волокон или другими артефактами (25, 26). Специфичность микроскопии также может снижаться из-за схожести ооцист криптоспоридий с цистами простейших (например, Giardia spp.) и дрожжеподобными грибами.
Другой популярный метод диагностики криптоспоридиоза — имму-ноферментный анализ кала на антиген Cryptosporidium . Его чувствительность может быть сопоставима с чувствительностью микроскопических методов (21, 27). Кроме того, существуют иммуннохроматографические варианты, при которых результат анализа можно получить в течение нескольких минут.
Для криптоспоридиоза чувствительность метода обнаружения имеет критическое значение, поскольку цисты Cryptosporidium могут обнаруживаться в небольшом количестве и у здоровых 6-месячных телят, и у взрослых животных, что делает их резервуаром для дальнейшего распространения инфекции (15).
Молекулярные методы, такие как полимеразная цепная реакция (ПЦР), имеют наиболее высокую чувствительность при диагностике инфекционных заболеваний. Более того, важное преимущество молекулярной диагностики — единый стандартизованный протокол проведения исследования, что позволяет избежать этапов, связанных с субъективной оценкой результатов. Работа при выполнении ПЦР не требует специальных знаний об особенностях морфологии паразитов на разных стадиях их развития, которые крайне важны для паразитолога при стандартном микроскопическом исследовании. Автоматизация ПЦР-исследования также существенно сокращает время анализа и уменьшает вероятность ошибки. К преимуществам молекулярных методов можно отнести и возможность одновременного анализа на несколько инфекций (мультиплексная ПЦР).
Фекалии, содержащие множество ингибиторов ПЦР, — достаточно сложная субстанция для молекулярной диагностики. В настоящее время в России отсутствуют стандарты проведения пробоподготовки этого биоматериала для молекулярной диагностики кишечных паразитозов и протозо-озов, причем как в ветеринарии, так и в клинической медицине. Специализированные коммерческие наборы для экстракции паразитарной ДНК из фекалий также отсутствуют.
По данным литературы, в качестве ПЦР-мишени для выявления Cryptosporidium spp. можно использовать ген малой субъединицы рРНК (18S rRNA), ген в -тубулина, ген белка стенки ооцисты COWP, гены адгезивных белков TRAP-C1, TRAP-C2, внутреннего транскрибируемого спейсера ITS1, ген белка теплового шока DnaJ (4, 28).
В настоящей работе впервые в России мы провели сравнительный анализ различных методов выделения ДНК из фекалий и выбрали оптимальный — с предварительным измельчением образцов мелющими гранулами (bead-beating) и экстракцией ДНК на колонке. Выбранный способ лег в основу разработанной методики диагностики криптоспоридиоза с использованием ПЦР в реальном времени, которая по чувствительности не уступает микроскопии.
Нашей целью стала разработка методики диагностики криптоспоридиоза методом ПЦР, ее апробация на образцах биологического материала от животных и сравнение полученных результатов с классическими микроскопическими методами.
Методика. Образцы фекалий телят ( Bos taurus taurus ) голштинской породы были собраны в 2023 году в хозяйствах Вологодской области после 758
вспышки криптоспоридиоза в период лечения. Всего было собрано 20 образцов, промаркированных №№ 1-20. Образцы фекалий отбирали непосредственно из прямой кишки животного в чистую емкость, каждый образец делили на две пробы, одну из которых использовали для микроскопического исследования по стандартному протоколу, описанному далее, а вторую направляли для ПЦР-исследования. Пробы фекалий (около 7 г) переносили в емкость, содержащую 15 мл 70 % этилового спирта. Получившиеся фекальные суспензии в спирте транспортировали при температуре не выше +25 ° C. После транспортировки образцы хранили в холодильнике при +5 ° C в защищенном от света месте.
Для обнаружения криптоспоридий в пробах кала использовали набор для окрашивания по Цилю-Нильсену Диахим (НПФ «Абрис+», Россия). На обезжиренное предметное стекло наносили каплю фекалий, разбавляли каплей физиологического раствора и распределяли по стеклу тонким слоем. Мазок высушивали при комнатной температуре и окрашивали по Цилю-Нильсену фуксином (реагент 1). В красителе препарат выдерживали от 5 до 20 мин, промывали водопроводной водой, орошали раствором соляной кислоты в спирте (реагент 2) до полного визуального обесцвечивания (1-3 мин). Промывали предметное стекло проточной водой и помещали в раствор метиленового синего (реагент 3) на 1-2 мин, промывали проточной водой и подсушивали. После окрашивания ооцисты приобретали цвет от красного до вишневого. Микроскопию проводили с увеличением х1000 с масляной иммерсией с использованием светового микроскопа Olympus cx33 («Olympus», Япония).
По числу выявленных ооцист в расчете на 1 г фекалий оценивали степень инвазированности животных: + (слабая) — единичные ооцисты в поле зрения (около 50000/г фекалий); ++ (умеренная) — до 10 ооцист в поле зрения (около 500000/г фекалий); +++ (выраженная) — более 10 ооцист (свыше 500000/г фекалий). Образцы исследовали в 2-5 повторах паразитологи с высокой квалификацией, исключающей субъективную интерпретацию результата.
Использовали несколько способов пробоподготовки и экстракции ДНК из проб фекалий телят. Эти протоколы подразумевают тестирование образцов нативного кала, мы использовали суспензии фекалий в консервирующем спиртовом растворе, удаляя его при необходимости.
Способ 1a. Проводили предварительную пробоподготовку с применением одноразовых концентраторов ГЕМ (ТУ 9398-020-17547866-2012, «ООО ГЕМ», Россия) — отечественного аналога концентраторов Mini PARASEP («Apacor Ltd.», Великобритания), рекомендованных для лабораторной диагностики гельминтозов и протозоозов в соответствии с МУК 4.2.314513. Концентраторы представляли собой пробирки с подготовленным раствором для формалин-эфирной седиментации и дополнительным фильтром для крупных твердых частиц. Процедуру концентрирования проводили согласно инструкции, однако вместо нативного кала использовали спиртовую фекальную суспензию. Вносили около 1 мл фекальной суспензии в пробирку концентратора с формалин-эфирным раствором, закрывали ее и встряхивали на вортексе (Microspin fV-2400, «BioSan», Россия). Далее концентратор переворачивали и центрифугировали 5 мин при 2000 g (Eppendorf 5810R, «Eppendorf», Германия), супернатант удаляли. Осадок дополнительно промывали, добавляя 1,5 мл 0,1 % раствора Tween-20 в PBS буфере (2,7 мМ KCl, 10 мМ Na 2 HPO 4 , 2 мМ KH 2 PO 4 , 137 мМ NaCl, рН 7,4), ре-суспендировали на вортексе и снова центрифугировали при 2000 g в течение 5 мин. Супернатант удаляли, осадок использовали для экстракции ДНК.
Способ 1b. Проводили пробоподготовку на концентраторах ГЕМ аналогично способу 1а, однако стандартный раствор концентратора (10 % водный раствор формалина) заменяли на 2,5 мл фосфатного буфера с 0,1 % Tween-20, эфирную фракцию оставили без изменений. Далее проводили концентрирование ооцист криптоспоридий из 1 мл фекальной суспензии согласно инструкции, как и в первом случае.
Способ 2. Не использовали концентраторы, 0,4 мл фекальной суспензии центрифугировали при 12000 об/мин (MiniSpin Eppendorf 5424, «Eppendorf», Германия) в течение 5 мин, чтобы избавиться от консервирующего раствора, осадок промывали, добавляя к нему 1,5 мл фосфатного буфера с 0,1 % Tween-20, ресуспендировали на вортексе и снова осаждали центрифугированием при 12000 об/мин в течение 5 мин. Супернатант удаляли, осадок использовали для экстракции ДНК.
Способ 3 а. Предварительно удаляли консервант из образцов фекальной суспензии. Для этого пробы объемом 1,0 мл центрифугировали 5 мин при 12000 об/мин (MiniSpin Eppendorf 5424, «Eppendorf», Германия), удаляли супернатант, не захватывая около 100 мкл надосадочной жидкости. Далее проводили пробоподготовку согласно методическим рекомендациям МУ 1.3.2569-09. Добавляли к фекалиям 1,0 мл фосфатного буфера (PBS), ресуспендировали осадок, центрифугировали в течение 5 мин при 12000 об/мин, удаляли супернатант, не захватывая около 100 мкл надосадочной жидкости. Переносили надосадочную жидкость с поверхности образовавшегося осадка в пробирки, содержащие по 800 мкл PBS, снова центрифугировали в течение 15 мин при 12000 об/мин. Супернатант удаляли, полученный осадок растворяли в 300 мкл PBS. Для выделения брали 100 мкл полученной суспензии.
Способ 3 b. Оставшийся осадок после отбора надосадочной жидкости по способу 3а ресуспендировали в 300 мкл фосфатного буфера с 0,1 % Tween-20. Для выделения брали 100 мкл полученной суспензии.
Для экстракции ДНК из предобработанных образцов (способы 1a, 1b, 2, 3b) использовали набор реагентов QIAamp PowerFecal Pro DNA Kit («Qiagen», Германия) в соответствии с инструкцией производителя, для гомогенизации (bead-biting) образцов — прибор TissueLyser LT («Qiagen», Германия), время встряхивания с гранулами увеличили до 20 мин, частота колебаний 50 Гц. В случае способа 3a применяли набор реагентов АмплиТест РИБО-преп (ФГБУ ЦСП ФМБА, Россия) в соответствии с инструкцией производителя.
Способы 3a и 3b использовали только для нескольких образцов (№ 1, 3, 7) с разной концентрацией цист, определенной методом микроскопии.
Выделенную ДНК растворяли в 200 мкл буфера для элюции и хранили в морозильнике при - 25 ° С.
Отдельно для нескольких образцов (№ 1, 3, 4, 7) при пробоподго-товке по способу 2 (без концентрирования) и экстракции ДНК при помощи набора QIAamp PowerFecal Pro DNA Kit варьировали время гомогенизации с мелющими гранулами от 1 до 30 мин.
ДНК из образцов экстрагировали с помощью набора ФБиоНуклео («Фрактал Био», Россия) строго в соответствии с инструкцией производителя без дополнительной предобработки.
В качестве ПЦР-мишени для выявления Cryptosporidium spp. мы выбрали ген малой субъединицы рРНК (18S rRNA). Множественное выравнивание последовательностей гена 18S rRNA Cryptosporidium из базы данных NCBI было сделано с использованием программного обеспечения UGENE, алгоритм Clustal W. Для специфической амплификации ДНК Cryptosporidium spp. были подобраны олигонуклеотидные праймеры: прямой Crypt-F (5'-TAATCAAGAACGAAAGTTAGGGGA-3') и обратный Crypt-R (5'-GAGT-AAGGAACAACCTCCAATCT-3'), флуоресцентный зонд Crypt-P (R6G-5'-ATGGTTAAGACTACGACGGTATCTGA- 3'-BHQ1).
По результатам BLAST сравнения выбранных последовательностей праймеров Crypt-F, Crypt-R и зонда Crypt-P с базой данных секвенирован-ных нуклеиновых кислот NCBI была показана их высокая идентичность со всеми опубликованными нуклеотидными последовательностями гена 18S rRNA рода Cryptosporidium ( n = 4390). При BLAST сравнении последовательностей выбранных олигонуклеотидов с геномами гетерологичных организмов, в том числе наиболее близкородственных паразитических кокцидий Cystoisospora beli , обнаружены различия хотя бы в одном из олигонуклеотидов, что позволяет предотвращать неспецифическую амплификацию гетерологичной ДНК. Оценку специфичности олигонуклеотидов in silico проводили, исключая таксон Cryptosporidiidae taxid:35082 из анализа.
Для ДНК, экстрагированной из пробоподготовленных (способы 1a, 1b, 2, 3a, 3b) образцов кала телят, обнаружение Cryptosporidium spp. проводили с использованием собственных олигонуклеотидных праймеров. Готовили реакционную ПЦР-смесь Crypt-FPR, содержащую по 0,32 мкМ праймеров Cryp-F и Cryp-R, 0,2 мкМ зонда Cryp-P, дНТФ («Биосан», Россия; по 0,2 мМ дАТФ, дГТФ, дЦТФ и дТТФ), 1х ПЦР буфер FRT (ФГБУ ЦСП ФМБА, России), 0,5 мкл полимеразы TaqF 5 ед/мкл (АО «Гентерра», Россия), 10 мкл образца ДНК. Общий объем реакционной смеси — 25 мкл. Амплификацию проводили на приборе CFX96 RealTime PCR machines («Bio-Rad», США) в соответствии с инструкцией производителя в следующем режиме: 15 мин при 95 ° C; 15 с при 95 ° C, 30 с при 58 ° C, 15 с при 72 ° C (50 циклов).
В качестве положительного контроля в ПЦР использовали рекомбинантную плазмиду pCryp2023, содержащую целевой фрагмент гена 18S rRNA Cryptosporidium размером 101 п.н., нуклеотидная последовательность pCryp2023 была подтверждена секвенированием по Сэнгеру. Концентрацию ДНК pCryp2023 оценивали с помощью цифровой ПЦР (система QX200 Droplet Digital PCR System, «Bio-Rad», США) со смесью ddPCR Supermix for Probes (No dUTP) («Bio-Rad», США) и олигонуклеотидами Crypt-F, Crypt-R, Crypt-P в соответствии с руководством к цифровой ПЦР.
Для ДНК, экстрагированной из образцов кала телят с помощью набора ФБиоНуклео, обнаружение Cryptosporidium spp. проводили с использованием ПЦР-набора для выявления ДНК Cryptosporidium (ООО «Фрактал-Био», Россия) согласно инструкции по применению.
Результаты обрабатывали в Microsoft Excel, рассчитывали средние значения ( M) и стандартные отклонения (±SD).
Резуёьтаты. Для определения аналитической чувствительности ПЦР-теста Crypt-FPR использовали растворы серийных разведений плазмидной ДНК pCryp2023, содержащей фрагмент ДНК Cryptosporidium spp., с концентрацией 5х103 копий/мл (5 повторов), 1х103 копий/мл (10 повторов), 5х102 копий/мл (5 повторов). Для выбранных концентраций плазмидной ДНК был получен воспроизводимый результат во всех повторах (рис.).
Для образцов с концентрацией ДНК Cryptosporidium spp. 5х103 копий/мл было определено значение пороговых циклов Сt ср. = 32,0±0,3 ( n = 5), для 1х103 копий/мл — Сt ср. = 34,4±0,2 ( n = 10), для 5х102 копий/мл — Сt ср. = 36,7±0,5 ( n = 5). Полученный результат указывает на высокую аналитическую чувствительность ПЦР с выбранными олигонуклеотидами — не менее 1х103 копий/мл.
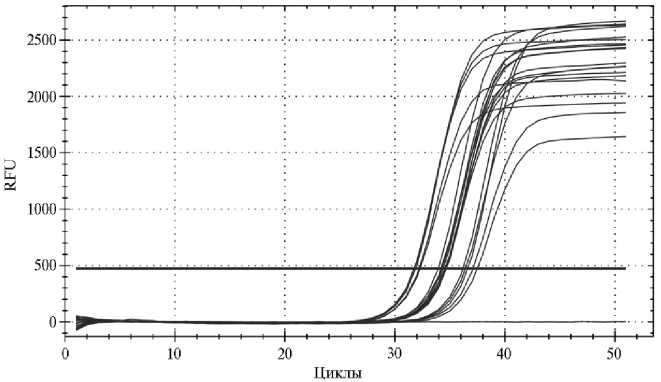
Определение аналитической чувствительности ПЦР методики Crypt-FPR для выявления ДНК Cryptosporidium spp. RFU — накопление флуоресценции (relative fluorescence units). Горизонтальная линия базового порога — примерно 20 % от максимального уровня флуоресценции.
При диагностике микроскопическими методами 15 образцов из 20 были определены как положительные, 5 — как отрицательные. Из 15 положительных образцов 4 имели высокую концентрацию ооцист, 5 — среднюю, 4 — низкую. Для положительных образцов с низкой концентрацией определение проходило на грани чувствительности метода, были найдены лишь единичные ооцисты. Воспроизводимость исследования для таких слабоположительных образцов колеблется, поскольку положительный результат может не подтвердиться при анализе другим микроскопистом.
При оценке влияния способа пробоподготовки и экстракции ДНК из фекалий телят на результаты ПЦР-исследования методом Crypt-FPR преимуществ при использовании концентраторов ГЕМ (способы 1a и 1b) мы не отметили (табл. 1). Напротив, было показано негативное влияние формалина на результаты ПЦР при способе пробоподготовки 1a, по сравнению с вариантами 1b или 2 разница составила в среднем около 7 пороговых циклов.
Ранее другие авторы (29, 30) также сообщали, что хранение образцов в содержащих формалин консервантах негативно сказывается на результатах ПЦР, хотя в некоторых исследованиях для ПЦР по-прежнему проводят пробоподготовку образцов по методу формалин-эфирного концентрирования (31).
Концентрирование без использования формалина (способ 1б) также не способствовало повышению эффективности выделения ДНК Cryptosporidium spp. по сравнению со способом 2 без концентрирования, хотя подобный способ увеличивает эффективность выявления ДНК яиц гельминтов из фекалий, как было показано нами ранее (32).
Также была изучена возможность выделения ДНК простейших из надосадочной фракции осветленного экстракта фекалий, получаемой по протоколу МУ 1.3.2569-09 для выявления бактериальных патогенов. МУ 1.3.2569-09 не содержат рекомендаций по пробоподготовке биоматериала для выявления кишечных протозоозов, однако представляло интерес определить, станут ли ооцисты криптоспоридий концентрироваться в надосадочной фракции или распределятся непосредственно в осадке твердых частиц фекалий.
1. Результаты ПЦР исследования методом Crypt-FPR для выявления ДНК Cryptosporidium spp. в зависимости от способа пробоподготовки и экстракции ДНК из фекалий телят с признаками криптоспоридиоза (2023 ãîä)
|
Ñïîñîá 1a |
Ñïîñîá 1b |
Ñïîñîá 2 |
Ñïîñîá 3a |
Ñïîñîá 3b |
∆ Ct max-min |
||||||||||
|
¹ |
|||||||||||||||
|
Ct 1 |
Ct ñð. 1 |
±SD |
Ct 1 |
Ct ñð 1 |
±SD |
Ct 1 |
Ct ñð. 1 |
±SD |
Ct 1 |
Ct ñð. |
1 ±SD |
Ct 1 Ct ñð 1 |
±SD |
||
|
1 |
34,77 |
34,7 |
0,1 |
31,12 |
31,0 |
0,1 |
29,26 |
29,2 |
0,1 |
32,18 |
32,42 |
0,7 |
29,18 28,74 |
0,4 |
5,5 |
|
34,53 |
30,90 |
29,12 |
31,35 |
29,06 |
|||||||||||
|
32,87 |
28,29 |
||||||||||||||
|
33,29 |
28,42 |
||||||||||||||
|
2 |
N/A |
N/A |
– |
32,15 |
32,2 |
0,0 |
28,62 |
28,7 |
0,1 |
Èññëåäîâàíèå íå ïðîâîäèëè |
21,3* |
||||
|
N/A |
32,14 |
28,75 |
|||||||||||||
|
3 |
40,02 |
40,3 |
0,3 |
34,87 |
35,1 |
0,2 |
31,82 |
32,2 |
0,4 |
37,61 |
37,07 |
0,6 |
32,26 32,76 |
0,5 |
8,1 |
|
40,58 |
35,31 |
32,54 |
37,67 |
32,32 |
|||||||||||
|
36,52 |
33,28 |
||||||||||||||
|
36,46 |
33,18 |
||||||||||||||
|
4 |
46,48 |
46,0 |
0,4 |
36,20 |
36,3 |
0,0 |
37,30 |
37,7 |
0,4 |
Èññëåäîâàíèå íå ïðîâîäèëè |
9,7 |
||||
|
45,59 |
36,29 |
38,13 |
|||||||||||||
|
5 |
N/A |
N/A |
- |
37,30 |
37,4 |
0,1 |
40,00 |
40,5 |
0,5 |
12,6 |
|||||
|
N/A |
37,47 |
41,05 |
|||||||||||||
|
6 |
43,00 |
43,8 |
0,8 |
38,61 |
38,3 |
0,3 |
39,32 |
39,9 |
0,6 |
5,5 |
|||||
|
44,65 |
37,99 |
40,50 |
|||||||||||||
|
7 |
40,47 |
40,2 |
0,2 |
39,47 |
40,8 |
1,3 |
39,17 |
39,3 |
0,1 |
N/A |
N/A |
– |
36,18 36,69 |
0,5 |
1,5 |
|
40,01 |
42,04 |
39,32 |
42,43 |
36,16 |
|||||||||||
|
N/A |
37,43 |
||||||||||||||
|
N/A |
37,00 |
||||||||||||||
|
8 |
44,40 |
44,0 |
0,4 |
45,11 |
44,2 |
1,0 |
39,45 |
40,6 |
1,1 |
Èññëåäîâàíèå íå ïðîâîäèëè |
3,6 |
||||
|
43,52 |
43,19 |
41,69 |
|||||||||||||
|
9 |
N/A |
N/A |
– |
N/A |
N/A |
– |
N/A |
N/A |
– |
– |
|||||
|
N/A |
N/A |
N/A |
|||||||||||||
|
10 |
N/A |
N/A |
– |
44,72 |
44,1 |
0,7 |
44,17 |
44,6 |
0,4 |
5,9 |
|||||
|
N/A |
43,40 |
45,05 |
|||||||||||||
|
Продолжение таблицы 1 |
||||||||||
|
11 |
N/A N/A |
N/A |
— |
N/A N/A |
N/A |
— |
N/A 38,46 |
N/A |
— |
— |
|
12 |
N/A N/A |
N/A |
— |
N/A N/A |
N/A |
— |
N/A N/A |
N/A |
— |
|
|
13 |
28,01 28,41 |
28,2 |
0,2 |
24,80 24,56 |
24,7 |
0,1 |
24,38 24,11 |
24,2 |
0,1 |
4,0 |
|
14 |
28,94 29,48 |
29,2 |
0,3 |
26,05 26,14 |
26,1 |
0,05 |
24,60 24,77 |
24,7 |
0,1 |
4,5 |
|
15 |
31,14 32,52 |
31,8 |
0,7 |
27,32 27,93 |
27,6 |
0,2 |
26,96 27,16 |
27,1 |
0,1 |
4,7 |
|
16 |
33,80 32,26 |
33,0 |
0,8 |
28,86 29,30 |
29,1 |
0,2 |
28,38 28,05 |
28,2 |
0,2 |
4,8 |
|
17 |
N/A N/A |
N/A |
— |
N/A 45,05 |
N/A |
— |
38,21 40,46 |
39,3 |
1,1 |
10,7 |
|
18 |
N/A N/A |
N/A |
— |
N/A N/A |
N/A |
— |
N/A N/A |
N/A |
— |
— |
|
19 |
N/A N/A |
N/A |
— |
N/A N/A |
N/A |
— |
N/A N/A |
N/A |
— |
— |
|
20 |
36,01 37,67 |
36,7 |
0,8 |
33,71 34,03 |
33,5 |
0,5 |
32,69 33,02 |
33,2 |
0,5 |
3,5 |
Примечание. Подробное описание пробоподготовки см. в разделе «Методика». Ct — пороговый цикл, Ct cp. — средний пороговый цикл, ±SD — стандартное отклонение Ct, N/A — ДНК не обнаружена, Ct не определен. Прочерки означают, что расчет не проводился из-за отсутствия значений Ct. A Ct max-min — разница пороговых циклов между лучшим и худшим способом пробоподготовки и экстракции ДНК для указанного образца, способ 3b не учитывали.
* Если при худшем способе пробоподготовки не наблюдалось амплификации ДНК, учитывали Ct = 50.
Экстракция ДНК из осветленного экстракта фекалий представляет собой простую задачу, поскольку можно использовать различные доступные в РФ наборы реагентов, например АмплиТест РИБО-преп (ФГБУ ЦСП ФМБА, России), пригодный для экстракции ДНК из осветленного экстракта.
Сравнение результатов ПЦР при выделении ДНК из надосадочной фракции (способ 3a) и из оставшегося осадка фекалий (способ 3b) показало, что, в отличие от бактерий, ооцисты криптоспоридий не концентрируются на границе осадка и экстракта (см. табл. 1, для образцов 1, 3, 7), большая их часть остается в осадке кала. Попытку концентрировать ооцисты криптоспоридий из фекальной суспензии методом, аналогичным таковому для бактериальной фракции (способ 3a), следует признать неудачной.
Таким образом, для пробоподготовки биоматериала для экстракции ДНК Cryptosporidium эффективны только протоколы, предполагающие экстракцию ДНК из цельного кала, попытки избавиться от части осадка кала приводят к потере значительной части ооцист криптоспоридий.
Необходимо отметить, что в качестве альтернативного метода концентрирования можно применять флотационные протоколы, однако при их использовании теряются клеточные формы простейших, которые также могли бы быть обнаружены молекулярными методами (33). Кроме того, методика проведения флотации достаточно трудоемка, плохо поддается автоматизации и требует значительных затрат времени, что особенно ощутимо при исследовании большого числа проб. Проблема концентрирования ооцист простейших в фекалиях для ПЦР исследований по-прежнему остается открытой, и особенно актуально концентирование ооцист при изучении слабоположительных образцов.
Ряд проблем экстракции паразитарной ДНК связан с достаточно плотными защитными оболочками цист простейших и яиц гельминтов (23, 32, 34). Поэтому для лучшего высвобождения ДНК, помимо химического воздействия, рекомендуют различные физические методы: многократное замораживание-оттаивание (23, 35, 36), ультразвуковое воздействие (34), механическое дробление бусинами (бид-битинг) (30, 37, 38). Стандартный протокол выделения ДНК набором QIAamp PowerFecal Pro DNA Kit предполагает гомогенизацию бид-битингом в течение 5 мин.
2. Влияние времени механической обработки на результаты ПЦР Crypt-FPR для выявления ДНК Cryptosporidium spp. (2023 год)
|
№ образца |
Время бид-битинга (bead-beating) |
|||||||
|
1 |
мин |
5 мин |
15 мин |
30 мин |
||||
|
Ct |
Ct ср. ±SD |
Ct |
\ Ct ср. ±SD |
Ct |
Ct ср. ±SD |
Ct |
Ct ср ±SD . |
|
|
1 |
32,35 |
32,3±0,1 |
30,20 |
30,9±0,3 |
31,51 |
31,1±0,3 |
31,22 |
31,7±0,3 |
|
32,13 |
30,17 |
30,89 |
31,53 |
|||||
|
32,25 |
31,00 |
31,14 |
31,69 |
|||||
|
32,11 |
30,56 |
31,66 |
31,25 |
|||||
|
32,14 |
30,53 |
31,30 |
30,87 |
|||||
|
3 |
34,76 |
35,0±0,2 |
31,88 |
32,0±0,1 |
33,65 |
33,6±0,1 |
33,09 |
33,1±0,2 |
|
34,78 |
31,98 |
33,74 |
33,47 |
|||||
|
35,00 |
32,03 |
33,56 |
33,06 |
|||||
|
34,61 |
31,99 |
33,89 |
33,09 |
|||||
|
34,94 |
31,87 |
33,70 |
33,03 |
|||||
|
4 |
36,15 |
35,3±0,5 |
33,38 |
34,0±0,5 |
33,45 |
34,0±0,4 |
34,35 |
34,1±0,3 |
|
34,80 |
34,20 |
34,13 |
33,56 |
|||||
|
35,32 |
34,04 |
34,02 |
34,10 |
|||||
|
34,97 |
33,55 |
34,36 |
34,28 |
|||||
|
35,21 |
34,61 |
34,49 |
34,20 |
|||||
|
7 |
N/A |
N/A |
37,27 |
36,0±1,0 |
38,63 |
36,9±0,7 |
36,88 |
38,6±0,9 |
|
39,16 |
36,40 |
37,17 |
37,37 |
|||||
|
39,01 |
36,22 |
36,87 |
38,60 |
|||||
|
N/A |
36,87 |
37,38 |
38,92 |
|||||
|
37,59 |
38,68 |
37,99 |
37,58 |
|||||
Примечание. Ct — пороговый цикл, Ct ср. — средний пороговый цикл, N/A — ДНК не обнаружена, Ct не определен; обработка 5 мин соответствует протоколу QIAamp PowerFecal Pro DNA Kit («Qiagen», Германия).
Для оценки влияния времени гомогенизации мы провели отдельный опыт (табл. 2). В небольшой выборке образцов не наблюдалось явной корреляции между временем бид-битинга (1-30 мин) и эффективностью экстракции ДНК, характеризуемой пороговыми циклами ПЦР . Тем не менее для образцов, подвергшихся бид-битингу в течение 1 мин, показана меньшая эффективность экстракции ДНК. Для слабоположительного образца № 7 ДНК выявлялась невоспроизводимо.
При микроскопии 15 образцов были определены как положительные, 5 — как отрицательные. При использовании способа пробоподготовки 2 и собственной методики ПЦР Crypt-FPR также 15 образцов из 20 оказались положительными, однако некоторые из них на крайне поздних циклах ПЦР (Ct > 40) (табл. 3).
3. Результаты обнаружения Cryptosporidium spp. в фекалиях телят с признаками криптоспоридиоза методами микроскопии и ПЦР
|
№ образца |
Способ 2, ПЦР Crypt-FPR |
ПЦР ФБиоНуклео («Фрактал Био», Россия) |
Микроскопия (инвазированность ооцистами) |
|||
|
Ct |
результат |
Ct |
результат |
|||
|
1 |
29,2 |
Положительный |
30,1 |
Положительный |
+++ |
Положительный |
|
13 |
24,2 |
Положительный |
29,8 |
Положительный |
+++ |
Положительный |
|
14 |
24,7 |
Положительный |
26,5 |
Положительный |
+++ |
Положительный |
|
15 |
27,1 |
Положительный |
30,9 |
Положительный |
+++ |
Положительный |
|
2 |
28,7 |
Положительный |
33,1 |
Положительный |
++ |
Положительный (умеренная) |
|
3 |
32,2 |
Положительный |
33,4 |
Положительный |
++ |
Положительный (умеренная) |
|
4 |
37,4 |
Положительный |
N/A |
Отрицательный |
++ |
Положительный (умеренная) |
|
5 |
40,5 |
Положительный |
37,3 |
Положительный |
++ |
Положительный (умеренная) |
|
6 |
39,9 |
Положительный |
N/A |
Отрицательный |
++ |
Положительный (умеренная) |
|
16 |
28,2 |
Положительный |
35,1 |
Положительный |
++ |
Положительный (умеренная) |
|
20 |
33,2 |
Положительный |
34,5 |
Положительный |
++ |
Положительный (умеренная) |
|
7 |
39,3 |
Положительный |
N/A |
Отрицательный |
+ |
Положительный (слабая) |
|
8 |
40,6 |
Положительный |
N/A |
Отрицательный |
+ |
Положительный (слабая) |
|
9 |
N/A |
Положительный |
N/A |
Отрицательный |
+ |
Положительный (слабая) |
|
10 |
44,6 |
Положительный |
N/A |
Отрицательный |
- |
Отрицательный |
|
17 |
39,3 |
Положительный |
N/A |
Отрицательный |
+ |
Положительный (слабая) |
|
11 |
N/A |
Отрицательный |
N/A |
Отрицательный |
- |
Отрицательный |
|
12 |
N/A |
Отрицательный |
N/A |
Отрицательный |
- |
Отрицательный |
|
18 |
N/A |
Отрицательный |
N/A |
Отрицательный |
- |
Отрицательный |
|
19 |
N/A |
Отрицательный |
N/A |
Отрицательный |
- |
Отрицательный |
Примечание. Подробное описание пробоподготовки см. в разделе «Методика». Ct — пороговый цикл, N/A — ДНК не обнаружена, Ct не определен.
Результаты, полученные методом ПЦР Crypt-FPR для образцов с высоким и умеренным содержанием ооцист криптоспоридий, полностью совпали с данными микроскопии. Однако для образцов №№ 9 и 10 отмечали расхождение результатов микроскопии и ПЦР, образец № 10 был определен как положительный методом ПЦР, хотя микроскопия дала отрицательный результат, и, наоборот, образец № 9, слабоположительный при микроскопии (+), был определен как отрицательный методом ПЦР.
При исследовании образцов с использованием набора реагентов ФБиоНуклео ДНК Cryptosporidium spp. была обнаружена в 9 образцах из 20. Четыре слабоположительных и два умеренно положительных образца были определены как ПЦР-отрицательные. Таким образом, набор ФБиоНуклео показал меньшую чувствительность по сравнению с предлагаемой нами методикой ПЦР, включающей пробоподготовку биоматериала по способу 2 с механическим дроблением биообразца, очисткой ДНК на спин-колонках. Скорее всего, это связано с тем, что протокол «Фрактал Био» не предполагает использования механического дробления биообразцов и уступает по эффективности очистки ДНК набору реагентов QIAamp PowerFecal Pro DNA Kit.
На наш взгляд, перспективным для выявления ДНК Cryptosporidium spp. в фекалиях телят может быть следующий протокол. Образцы фекалии (около 7 г) отбирают из прямой кишки животного в чистую емкость, добавляют 15 мл 70 % раствора этилового спирта в качестве консерванта. Транспортировка осуществляется без особых требований к условиям, но при температуре не выше +25 °C. Для удаления консервирующего раствора фекальную суспензию объемом 0,4 мл центрифугируют при 12000 об/мин (MiniSpin Eppendorf 5424, «Eppendorf», Германия) в течение 5 мин. К осадку добавляют 1,5 мл фосфатного буфера с 0,1 % Tween-20, ресуспендируют на вортексе. Осаждают фекалии центрифугированием при 12000 об/мин в течение 5 мин. Супернатант удаляют, промытый осадок фекалий используют для экстракции ДНК по протоколу с интенсивной гомогенизацией гранулами (бид-битинг) с последующей очисткой на спин-колонках. Примером подходящего протокола служит инструкция по применению набора реагентов QIAamp PowerFecal Pro DNA Kit («QIAgen», Германия). Для специфической амплификации ДНК Cryptosporidium spp. можно использовать оли-гонуклеотидные праймеры Crypt-F, Crypt-R и флуоресцентный зонд CryptP либо готовые коммерчески доступные комплекты реагентов (например, набор ПЦР-реагентов «Фрактал Био» для выявления ДНК Cryptosporidium spp.). Реакционную смесь для ПЦР готовят из расчета Cryp-F и Cryp-R праймеров по 0,32 мкМ, зонда Cryp-P 0,2 мкМ, дНТФ по 0,2 мМ каждого, 1* ПЦР буфер FRT, 0,5 мкл полимеразы TaqF 5 ед/мкл, 10 мкл образца ДНК. Общий объем реакционной смеси 25 мкл. Программа термоциклирования: 15 мин при 95 °C; 15 с при 95 °C, 30 с при 58 °C, 15 с при 72 °C (50 циклов).
Итак, мы подтвердили, что даже кратковременный контакт с фор-малин-содержащими растворами оказывает ингибирующее действие на ПЦР при диагностике Cryptosporidium spp. В качестве консервирующего вещества мы рекомендуем использовать 70 % раствор этилового спирта. В перспективе желательно закрепить стандарт консервирования и хранения образцов для паразитологических исследований методом ПЦР без применения формалина. Апробирование различных способов пробоподготовки кала показало, что применение методов, рекомендованных для диагностики бактериальных заболеваний, приводит к потере чувствительности при выявлении простейших паразитов. При сборе надосадочной жидкости после центрифугирования большая часть криптоспоридий остается в осадке кала, тогда как бактериальная фракция формируется на границе с осадком. При диагностике паразитозов необходимо работать с цельным калом. Для экстракции ДНК из цельного кала наиболее перспективны методики с применением спин-колонок. Мы не отметили преимуществ способов концентрирования, рекомендованных МУК 4.2.3145-13, в частности применения концентраторов ГЕМ. Возможно, отсутствие концентрирующего эффекта было связано с тем, что мы использовали спиртовую суспензию фекалий, а не нативный кал. К сожалению, в нашем случае отказ от консервирующего раствора при транспортировке не представлялся возможным. Стандартный протокол выделения ДНК из фекалий набором QIAamp PowerFecal Pro DNA Kit (QIAgen) предполагает интенсивную гомогенизацию (бид-битинг) в течение 5 мин. Время бид-битинга более 5 мин не повышает эффективность экстракции ДНК Cryptosporidium spp. Однако при использовании коммерческого набора ФБиоНуклео для выделения ДНК из фекалий на спин-колонках с отсутствием механического воздействия результаты были хуже. Поэтому мы рекомендуем проводить интенсивную механическую обработку (гомогенизацию) образцов кала на начальном этапе экстракции ДНК для увеличения ее эффективности.


