Оптимизация микрокапсулирования биологически активных веществ (пепсина) для использования в пищевой промышленности
Автор: Дьячкова А.В., Тихонов С.Л., Тихонова Н.В.
Журнал: Вестник Восточно-Сибирского государственного университета технологий и управления @vestnik-esstu
Рубрика: Технология мясных, молочных и рыбных продуктов и холодильных производств (технические науки)
Статья в выпуске: 3 (78), 2020 года.
Бесплатный доступ
В статье представлены результаты исследования влияния монокомпонентного защитного материала микрокапсулы (мальтодекстрина) и двухкомпонентного (мальтодекстрина с гуммиарабиком и мальтодекстрина с желатином). Была проведена проверка влияния толщины защитного слоя на протеолитическую активность микрокапсулированного пепсина. Обнаружено значительное снижение протеолитической активности пепсина в контрольном образце (без капсулирования) во время хранения (р = 0,05); микрокапсулы с защитным слоем из мальтодекстрина и желатина, мальтодекстрина и гуммиарабика отличались более высокими исследуемыми показателями в сравнении с контрольными образцами и покрытыми только мальтодекстрином (р = 0,01), при этом двухкомпонентные защитные материалы не показали каких-либо существенных различий в защите (р = 0,05), и в сохранении активности микрокапсулированного пепсина в двухкомпонентные растворы с разной толщиной (4 и 6 мкм) при хранении. Результаты эксперимента по микрокапсуляции пепсина в псевдокипящем слое позволяют рекомендовать использовать раствор мальтодекстрина и гуммиарабика, при этом толщина покрытия должна быть не менее 2 мкм. Увеличение толщины защитного слоя может сопровождаться большими временными расходами и расходами материалов, не обеспечивая роста сохраняемости активности капсулированного фермента на значимом уровне (р = 0,01). Данная технология и материалы для капсулирования могут быть внедрены в пищевое производство.
Микрокапсулирование, пепсин, мальтодекстрин, желатин, гуммиарабик, псевдокипящий слой
Короткий адрес: https://sciup.org/142228788
IDR: 142228788 | УДК: 557.15
Optimization of microencapsulation of dietary supplement (pepsin) for use in the food industry
The article presents the results of a study of the influence of a monocomponent protective material of a microcapsule - maltodextrin and two-component - maltodextrin with gum Arabic and maltodextrin with gelatin. At the same time, the effect of the thickness of the protective layer on the proteolytic activity of microencapsulated pepsin was tested. A significant decrease in the proteolytic activity of pepsin was found in the control sample (without encapsulation) during storage (p = 0.05); microcapsules with a protective layer of maltodextrin and gelatin, maltodextrin and gum Arabic were characterized by higher test parameters in comparison with control samples and covered only with maltodextrin (p = 0.01), while two-component protective materials did not show any significant differences in protection (p = 0.05), and there were no differences in preserving the activity of microcapsulated pepsin in two-component solutions with different thicknesses of 4 and 6 microns during storage. The results of the experiment on microencapsulation of pepsin in a pseudo-boiling layer make it possible to recommend the use of a solution of maltodextrin and gum Arabic while the coating thickness should be at least 2 μm. An increase in the thickness of the protective layer can be accompanied by large time and material costs, without ensuring an increase in the persistence of the activity of the encapsulated enzyme at a significant level (p = 0.01). This technology and materials for microencapsulation can be effectively used in food production.
Текст научной статьи Оптимизация микрокапсулирования биологически активных веществ (пепсина) для использования в пищевой промышленности
Современная наука в области пищевой биотехнологии имеет значительный комплекс новых и усовершенствованных технологий, направленных на улучшения качества и полезности пищевой продукции. Известны различные технологии микрокапсулирования полезных пищевых ингредиентов (пробиотики, витамины, ферменты), исследованные в работах [1 - 8]. Исследователи пришли к выводу, что термостабильный и легкоусвояемый материал стенок является определяющим для стабильных витаминных микрокапсул. Природные пищевые углеводы или белки - подходящие кандидаты для материалов защитного слоя микрокапсул. Исследователи Ballesterosetal, Jeyakumarietal, Santanaetal, Вилесова и др. предлагают использовать различные материалы для стенок защитного слоя в капсулировании пищевых ингредиентов: хитозан, желатин, мальтодекстрин, сывороточный белок, казеинат натрия, модифицированные крахмалы, гуммиарабик [9 - 12].
Мальтодекстрин обычно используется для образования защитного слоя, получают микрокапсулы с высокой растворимостью в воде, низкой вязкостью, незначительным содержанием сахара. Эти свойства делают мальтодекстрин наиболее распространенным защитным материалом стенок при микрокапсулировании. Желатин также является хорошим выбором в качестве материала стенок, особенно при распылительной сушке, благодаря его хорошим свойствам эмульгирования, пленкообразования, растворимости в воде, высокой стабилизирующей активности и тенденции к образованию тонкой плотной сетки. Гуммиарабик, природный бесцветный растительный полисахаридный экссудат акации, хорошо известен как эффективный материал для стенок из-за его стабильного образования эмульсии и хорошего удержания летучих веществ и поэтому активно используется в течение многих лет [5].
На основе имеющегося опыта и анализа результатов научных исследований в области микрокапсулирования можно заключить, что в передовых научных исследованиях на данном этапе пока не выделяются однозначно эффективные технологии микрокапсулирования и универсальные материалы для стенок микрокапсул, но предлагаются варианты, которые отвечают задачам повышения качества пищевых продуктов. Данная идея находит свое подтверждение в работах [13, 14]. Каждый метод микрокапсулирования имеет преимущества и недостатки, в том числе неэффективный материал ядра, сложность процедуры, низкую эффективность инкапсуляции или проблемы с точки зрения воспроизводимости [15]. Ни один процесс инкапсуляции не может быть адаптирован ко всем основным материалам или применению продукта в силу несоответствия их конкретным задачам повышения качества пищевых продуктов. В работах по пищевой биотехнологии были предприняты попытки улучшить свойства микрокапсулирования, где изучалось использование смеси углеводов с белками и полисахаридами в различных пропорциях. Выбор полимерных смесей, которые могут привести к более высокой эффективности инкапсуляции и более низкой стоимости, чем отдельные биополимеры, был предметом повышенного интереса [5, 16 - 19].
Тем не менее в многочисленных работах [2, 5, 20, 21] обоснованным считают применение технологии микрокапсулирования в псевдокипящем слое. Сушка с распылением стала успешной промышленной технологией, основным используемым методом для капсулирова-ния пищевых ингредиентов из-за его невысокой стоимости обработки, быстрого испарения воды и простоты применения и масштабирования.
Выбор подходящего материала для защитных стенок является чрезвычайно важным фактором для капсулирования биологически активных соединений. Этот материал должен защищать вещество ядра от его разрушения, иметь требуемую механическую прочность, быть совместимым с пищевым продуктом, обеспечивать контролируемое высвобождение и/или иметь термические свойства, совместимые со свойствами продукта [17 - 19].
Признавая значимость и опираясь на результаты пищевой инженерии, считаем, что сегодня исследования должны быть направлены на поиск новых перспективных способов микрокапсулирования, включающих технологию микрокапсулирования и материал для защитного слоя. Результативной будет та технология, которая обеспечивает высокое качество микрокапсул, сохраняемость и технологичность капсулированного вещества и экономический эффект.
Цель работы – экспериментально обосновать состав защитного покрытия при микрокапсулировании фермента пепсина и разработать рекомендации по его микрокапсулированию.
Материал и методы исследований
Капсулируемое вещество – пепсин. В эксперименте были изготовлены микрокапсулы с защитным слоем из трех различных материалов: мальтодекстрин, мальтодекстрин с желатином в соотношении 3:1, мальтодекстрин с гуммиарабиком (Е414) в соотношении 3:1; указанная пропорция показала свою эффективность в работах [16 - 18].
При приготовлении мальтодекстрина (MD) в качестве защитного вещества была повторена технология, представленная в работе [21]. Мальтодекстрин и гуммиарабик растворяли (MD + GA) в теплой дистиллированной воде (70 °С) при постоянном перемешивании при 120 об./мин в течение 1 ч и выдерживали в течение ночи при 4 ± 2 °С для регидратации. Желатин растворяли в горячей дистиллированной воде при перемешивании до образования водного раствора, затем вносили мальтодекстрин при постоянном перемешивании до полного растворения всех материалов, получая микрокапсулы (MD + GE). Производство микрокапсул было проведено по единой технологии – в псевдокипящем слое. Микрокапсулы имели различную толщину защитного слоя, которая была обеспечена разной продолжительностью капсу-лирования (большее время нанесения защитного слоя приводит к его большей толщине [20]).
Протеолитическая активность пепсина оценивалась по методу, предлагаемому и апробированному в работах [22 - 24] - путем определения степени гидролиза раствора денатурированного гемоглобина ферментом после инкубации в течение 15 мин при 40 °С. Одна единица (U) активности фермента была принята за количество фермента, которое высвобождает 1 мкмоль тирозина (мин мл)-1. Реакцию начинали добавлением 0,4 мл раствора фермента (или 10 мг сухих хитозановых гранул, содержащих иммобилизованный фермент, после инкубации в 0,01 М 2 мл HCl при 40 °С для равновесия набухания) к 2,0 мл раствора денатурированного кислотой гемоглобина (10 г). L-1 приготовили в 0,01 М HCl и смесь осторожно перемешали в пробирке при 40 °С. Через промежутки времени после смешивания реакцию останавливали добавлением 4,0 мл 5,0 % (вес/объем) раствора ТСА. Образцы были подвергнуты центрифугированию и фильтрации. Активность пепсина оценивали по увеличению УФ-поглощения супернатанта при 280 нм.
Контрольными образцами являлся чистый некапсулированный пепсин. Полученные образцы хранили в защищенном от света месте при комнатной температуре. Проверены истинные различия в начале эксперимента и сделаны замеры по прошествии 3, 6, 12, 18 мес. хранения.
Результаты исследования и их обсуждение
Оптимизация микрокапсулирования пепсина означает решение задачи контроля за высвобождением капсулируемого биологически активного вещества и в то же время сохранении его активности при хранении.
В результате проведенного эксперимента были сделаны выводы о влиянии материала для микрокапсулирования на активность пепсина. Поскольку толщина покрытия защитным слоем также оказывает влияние на активность пепсина, то определена степень влияния указанных факторов. Первоначальная активность ферментного препарата рассматривалась в качестве стандарта для оценки его стабильности. Микрокапсулы с различной толщиной защитного слоя демонстрируют лучшее сохранение первоначальной активности фермента (рис. 1).
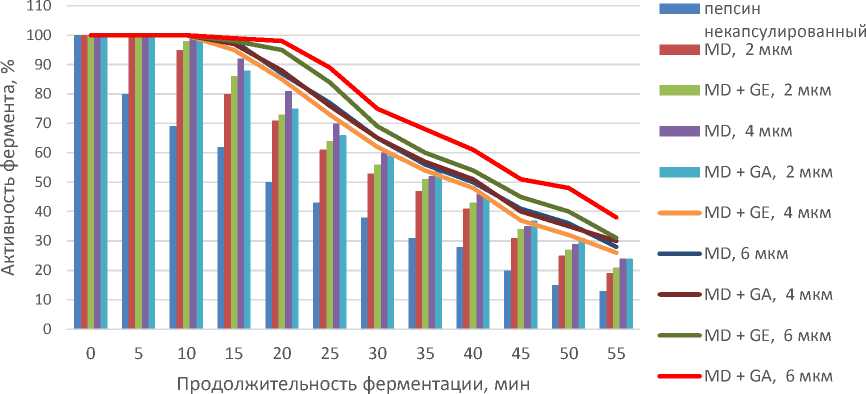
Рисунок 1 – Активность пепсина для различных микрокапсул
Из рисунка 1 видно, что сохранение наибольшей активности пепсина обеспечено микрокапсулами с двухкомпонентными растворами мальтодекстрина и гуммиарабика, мальтодекстрина и желатина с защитным слоем 6 мкм.
Поскольку наблюдается снижение активности как некапсулированного пепсина, так и в микрокапсулах, следует выявить скорость изменения активности в микрокапсулах по отношению к нативному ферменту. Для этого рассчитали коэффициент опережения, по которому соотносили активность фермента каждого вида образца микрокапсулы с некапсулируемым ферментом, на основе полученных данных построили график (рис. 2).
2,8
2,6
2,4
2,2
1,8
1,6
1,4
1,2
2 мкм
MD, 2 мкм
MD + GA, 2 мкм
MD + GA, 4 мкм
MD + GE, MD + GE, MD + GE,
4 мкм
6 мкм
MD, 4 мкм
MD, 6 мкм
MD + GA, 6 мкм
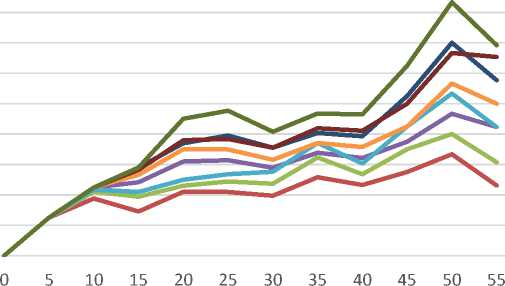
Рисунок 2 – Коэффициент опережения снижения активности фермента
Из рисунка 2 видно, что наибольшую результативность обеспечили микрокапсулы с защитным материалом из мальтодекстрина и гуммиарабика с защитным слоем толщиной 6 мкм. В целом было выявлено, что большая толщина слоя имеет больший защитный эффект.
18 месяцев хранения
0 3 6 9 12 15 18 месяцев хранения
Рисунок 3 - Динамика протеолитической активности пепсина
Микрокапсулы с пепсином с защитным материалом мальтодекстрина и желатина, мальтодекстрина и гуммиарабика с толщиной слоя 4 и 6 мкм не проявляли потери активности до 18 мес. хранения при 2 °С. У микрокапсул с однокомпонентным защитным слоем мальтодекстрина (при толщине стенок 2 и 4 мкм) протеолитическая активность пепсина снижалась через 8 мес., а не с первого месяца хранения, как для некапсулированного пепсина. Снижение активности объясняется зависящей от времени естественной потерей, и это может быть в значительной степени предотвращено путем микрокапсулирования. Зашитый в матрицу защитного материала из смеси мальтодекстрина с желатином или гуммиарабиком дает преимущество за счет увеличения стабильности фермента в течение всего срока хранения при 2 °С, что определено экспериментом по стабильности при хранении. Данные выводы согласуются с исследованиями [16 - 18].
Выводы
В результате проведенного эксперимента с микрокапсулированием пепсина с различными составами защитного покрытия и толщины были сделаны следующие выводы:
-
- снижение протеолитической активности пепсина в контрольном образце (без капсули-рования) во время хранения было значительным (на уровне значимости р = 0,05);
-
- микрокапсулы с защитным слоем из мальтодекстрина и желатина, мальтодекстрина и гуммиарабика отличались более высокими исследуемыми показателями в сравнении с контрольными образцами и покрытыми только мальтодекстрином (на уровне значимости р = 0,01);
-
- двухкомпонентные защитные материалы растворов мальтодекстрина и гуммиарабика, мальтодекстрина и желатина не показали каких-либо существенных различий в защите (на уровне значимости р = 0,05);
-
- отсутствие отличий в сохранении активности микрокапсулированного пепсина в двухкомпонентные растворы с разной толщиной (4 и 6 мкм) при хранении.
Результаты эксперимента по микрокапсуляции пепсина в псевдокипящем слое позволяют рекомендовать использование раствора мальтодекстрина и гуммиарабика, при этом толщина покрытия должна быть не менее 2 мкм. Увеличение толщины защитного слоя может сопровождаться большими временными расходами и расходами материалов, не обеспечивая роста сохраняемости активности капсулированного фермента на значимом уровне (р = 0,01).
Данная технология и материалы для капсулирования могут быть внедрены в пищевое производство.
Список литературы Оптимизация микрокапсулирования биологически активных веществ (пепсина) для использования в пищевой промышленности
- Dhakal Sh. P, He J. Microencapsulation of vitamins in food applications to prevent losses in processing and storage // A review. Food Research International. – 2020. - Vol. 137.
- Silva P.T., Fries L.L.M., Menezes C.R. et al. Microencapsulation: Concepts, mechanisms, methods and some applications in food technology // Ciencia Rural. - 2014. - N 44 (7). - P. 1304-1311.
- Desai K.G.H., Park H.J. Recent developments in microencapsulation of food ingredients // Dry. Technol. – 2005. - N 23. - P. 1361–1394.
- Petru A., Dima C. Microencapsulation in food products // Agro Life Scientific Journal. – 2014. - N 3. - P. 9-14.
- Gomes B., Barba F.J., Dominguez R. et al. Microencapsulation of antioxidant compounds through innovative technologies and its specific application in meat processing // Trends in Food Science & Technology. – 2018. - N 82. - P.135-147.
- Gbassi G.K., Vandamme T. Probiotic Encapsulation Technology: From Microencapsulation to Release into the Gut. Pharmaceutics, Mar. – 2012. – N 4 (1). - P. 149–163.
- Ramos P.E., Cerqueira M.A., Teixeira J.A. et al. Physiological protection of probiotic microcapsules by coatings. Crit. Rev. Food Sci. Nutr. – 2018. – N 58. - P. 1864–1877.
- Ying D., Sanguansri L., Weerakkody R. et al. Effect of encapsulant matrix on stability of microencapsulated probiotics // J. Funct. Foods. – 2016. - N 25.
- Ballesteros L.F., Ramirez M.J., Orrego C.E. et al. Encapsulation of antioxidant phenolic compounds extracted from spent coffee grounds by freeze-drying and spray-drying using different coating materials // Food Chemistry. - 2017. - N 237. - P. 623–631.
- Jeyakumari A., Zynudheen A.A., Parvathy U. Microencapsulation of bioactive food ingredients and controlled release - a review // ICAR-Mumbai research of centre of Central Institute of Fisheries Technology. – 2016. – Vol., Issue 6, 07. - P. 1-9.
- Santana A.A., Cano-Higuita D.M., De Oliveira R.A. et al. Influence of different combinations of wall materials on the microencapsulation of jussara pulp (Euterpe edulis) by spray drying Food Chem. – 2016. - N 212. - P. 1-9.
- Вилесова М.С., Айзенштадт Н.И., Босенко М.С. и др. Разработка микрокапсулированных и гелеобразных продуктов и материалов для различных отраслей промышленности // Российский химический журнал. - 2001. - № 5-6. - С. 1-10.
- Wilson N., Shah N.P. Microencapsulation of vitamins // International Food Research Journal. - 2007. - N 14. - P. 1–14.
- Mehran M., Masoum S., Memarzadeh M. Improvement of thermal stability and antioxidant activity of anthocyanins of Echium amoenumpetal using maltodextrin/modified starch combination as wall material // International Journal of Biological Macromolecules. – 2020. - Vol. - 148. - P. 768-776.
- Das S.K., David S.R.N., Rajabalaya R. et al. Microencapsulation techniques and its practice // International Journal of Pharmaceutical Science and Technology. - 2011. - N 6. - P. 1–23.
- Mahdavi S.A., Jafari S.M., Assadpoor E. et al. Microencapsulation optimization of natural anthocyanins with maltodextrin, gum Arabic and gelatin // International Journal of Biological Macromolecules. – 2016. - Vol. 85, April 2016. - P. 379-385.
- Mahdavee Khazaei K., Jafari S.M., Ghorbani M. et al. Application of maltodextrin and gum Arabic in microencapsulation of saffron petal’s anthocyanins and evaluating their storage stability and color Carbohydrate Polymers. - 2014. – N 105. - P. 57–62
- Ferrari C.C., Marconi Germer S.P., Alvim I.D. et al. Storage stability of spray-dried blackberry powder produced with maltodextrin or gum Arabic, Dry. Technol. – 2013. - N 31 (4). - P. 470–478.
- Boiero M.L., Mandrioli M., Vanden Braber N. et al. Montenegro Gum arabic microcapsules as protectors of the photoinduced degradation of riboflavin in whole milk // Journal of Dairy Science. – 2014. - N 97 (9). - P. 5328-5336.
- Kudryashov L.S., Uzakov Ya.M., Tikhonov S.L. et al. Microencapsulation of proteolytic enzymes for industrial application // Известия НАН РК. Серия геологии и технических наук. – 2020. - С. 161–170.
- Кудряшов Л.С., Тихонов С.Л., Тихонова Н.В. и др. Микрокапсулирование пепсина и оценка его протеолитических свойств // Вестник ВСГУТУ. – 2019. - № 3 (74). - С. 31-41.
- Cupp-Enyard, C. Sigma's Non-specific Protease Activity Assay - Casein as a Substrate // J. Vis. Exp. – 2008. - N 19.
- Hasem A.M. Purification and properties of a milk-clotting enzyme produced by Penicillium oxalicum // Bioresource Technology. - 2000. - № 75. - P. 219–222.
- Bergkvist R. The proteolytic enzyme of Aspergillus oryzae 1. Methods for the estimation and isolation of the proteolytic enzymes // Acta Chemica Scandinavica. - 1963. - N 17. - P. 1521–1540.


