Опыт использования кардиоресинхронизирующей терапии у пациентов с застойной сердечной недостатосностью
Автор: Гусаим Т.А., Мартынюк А.Д., Свешников А.В., Фролов Д.Н.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.8, 2013 года.
Бесплатный доступ
В статье представлены данные об опыте применения кардиоресинхронизирующей терапии в ФГБУ «НМХЦ им. Н.И. Пирогова» у 70 больных с хронической сердечной недостаточностью. Эффект вмешательства на клинические и эхокардиографические конечные точки процедуры оценивался при среднесрочном наблюдении в течение 6 месяцев.
Кардиоресинхронизирующая терапия, бивентрикулярная стимуляция, хроническая сердечная недостаточность
Короткий адрес: https://sciup.org/140188211
IDR: 140188211 | УДК: 616.12-008.46.811.6-085
Cardiac resynchronization therapy in patients with congestive heart failure: a single-center experience
We describe a single-center experience of cardiac resynchronization therapy (CRT) in 70 patients with heart failure. The objective of our study was to assess the mid-term effects of cardiac resynchronization during 6-month follow-up on clinical and echocardiographic end points.
Текст научной статьи Опыт использования кардиоресинхронизирующей терапии у пациентов с застойной сердечной недостатосностью
Сердечная недостаточность - это клинический синдром, при котором на фоне структурных и/или функциональных изменений миокарда, работа сердца не позволяет обеспечить достаточного кровоснабжения органов и тканей на уровне, соответствующем физиологическим потребностям организма [1].
Основными причинами сердечной недостаточности являются ишемическая болезнь сердца и артериальная гипертония. Среди других этиологических факторов следует отметить длительно персистирующие аритмии, клапанные пороки сердца, действие инфекционных агентов и токсических веществ (в том числе алкоголя) [2, 3, 4].
Сердечная недостаточность может быть ассоциирована с различными типами сердечной диссинхронии: 1. Межжелудочковая диссинхрония.
-
2. Внутрижелудочковая диссинхрония.
-
3. Атривентрикулярная диссинхрония (интервал PQ >200 мс) способствует сокращению времени диастолы (слиянию волн Е и А митрального потока).
-
4. Межпредсердная диссинхрония.
Цель исследования: оценить эффективность кар-диоресинхронизирующей терапии (КРТ) у пациентов с хронической сердечной недостаточностью (ХСН) при ишемической и дилатационной кардиомиопатиях; провести сравнительную оценку широко применяемых эхокардиографических методов исследования, наиболее воспроизводимых критериев эффективности ресинхронизирующей терапии для использования этих показателей при отборе больных на бивентрикулярную стимуляцию.
Нами проанализирован пятилетний опыт применения ресинхронизирующей терапии у пациентов с электромеханической диссинхронией и сердечной недостаточностью, рефрактерной к оптимальной медикаментозной терапии.
В исследовании участвовало 70 больных (3 женщины, 67 мужчин), которым проведена имплантация би-вентрикулярного электрокардиостимулятора с функцией кардиовертера-дефибриллятора. У 22 пациентов диагностировали ишемическую кардиомиопатию (ИКМП), у 48 – дилатационную кардиомиопатию (ДКМП). Возраст обследуемых пациентов составил от 39 до 72 лет.
У всех больных до операции проводились корона-роангиография и сцинтиграфия миокарда. В 7 случаях потребывалось стентирование коронарных артерий. У девяти пациентов была выполнена радиочастотная абляция атриовентрикулярного соединения по поводу медикаментозно-рефрактерной пароксизмальной или постоянной формы фибрилляции предсердий. У 6 пациентов ранее были имплантированы однокамерные (n = 1) или двухкамерные (n = 5) электрокардиостимуляторы по поводу брадисистолической формы фибрилляции предсердий или СССУ.
Операционный доступ выполнялся в левой подключичной области. Предсердный электрод фиксировали в ушко правого предсердия, правожелудочковый электрод - в верхушку ПЖ. Левожелудочковый электрод позиционировали в одну из ветвей венечного синуса (преимущественно задне-латеральная ветвь).
В качестве критериев включения в исследование использовались: фракция выброса ЛЖ менее 35%; III–IV функциональный класс сердечной недостаточности по NYHA (3–4); продолжительность комплекса QRS не менее 120 мс до 245 мс (у всех пациентов регистрировалась полная блокада левой ножки пучка Гиса (ПБЛНПГ), у двух- полная блокада правой ножки пучка Гиса ( ПБПНПГ), признаки механической диссинхронии (межжелудочковой или внутрижелудочковой). У двух пациентов с ПБПНПГ наблюдалась выраженная межжелудочковая диссинхрония, при незначительной вну- трижелудочковой диссинхронии ЛЖ. У 15% больных (из общего числа обследуемых) не было обнаружено межсегментарного асинхронизма (внутрижелудочкового или межжелудочкового), несмотря на расширение QRS эта группа больных в исследовании не учитывалась.
В некоторых случаях использовались дополнительные показания к бивентрикулярной стимуляции сердца: пролонгированная митральная регургитация (более 450 мс), короткое время желудочкового наполнения (менее 200 мс), наличие конечной диастолической митральной регургитации (A. Kutarski и соавторы).
Подбор пациентов для имплантации ресинхронизирующего устройства проводился на аппарате VIVID-7 GE. Применялись методики , наиболее легко воспроизводимые при дальнейшем динамическом наблюдении:
– измерялась задержка в сокращении МЖП и задней стенки ЛЖ. Принималась во внимание задержка более 130 мс (рис. 1);
– пресистолическая аортальная задержка от 140 мс;
– межжелудочковая задержка от 40 мс (разница между пресистолической аортальной и пресистолической легочной задержками);
– определение внутрижелудочковой задержки тканевым допплером (Q-анализ скорости движения между МЖП и боковой стенкой, передней и нижней стенками в базальных и средних сегментах). Принималась во внимание задержка более 60 мс. В нормальном желудочке начало систолического движения различных сегментов происходит с очень незначительным межсегментарным асинхронизмом, не превышающим 30 мс (рис. 2).
C помощью импульсно-волновой тканевой допплерографии (TDI RW) по 6-ти базальным сегментам оценивалась электромеханическая задержка, как интервал от зубца Q ЭКГ до пиковой систолической скорости движения исследуемого участка миокарда.
Ресинхронизационная терапия заключается или в одномоментной электрической стимуляции обоих желудочков сердца, или стимуляции с минимальным
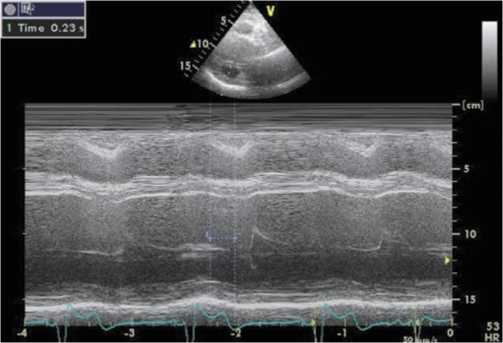
Рис. 1. Оценка внутрижелудочковой ассинхронии по задержке пика систолического движения задней стенки по отношению к пику движения межжелудочковой перегородки (время задержки 230 мс)
опережением (10–60 мс) одного желудочка сердца по отношению к другому.
Оптимизация параметров стимуляции, в частности АВ-задержки, у пациентов с синусовым ритмом, проводилась с использованием формулы Риттера:
AV opt. = AV short + [(AV long + QA long ) - (AV short + QA short )]
(short – запрограммированные параметры, long – выставляемые) (рис. 3).
У пациентов с нарушением функции ЛЖ чаще всего имеет место недостаточное время диастолического наполнения, что в свою очередь ухудшает систолическую функцию ЛЖ, приводит к снижению ударного объема, увеличению давления в левом предсердии.
Оптимизация VV задержки осуществляется по интегралу линейной скорости потока VTI аортального клапана (принцип непрерывности потока): SV = CSA х VTI. Площадь поперечного сечения равна произведению числа π (константы 3,14) на квадрат диаметра d, деленному на 4:
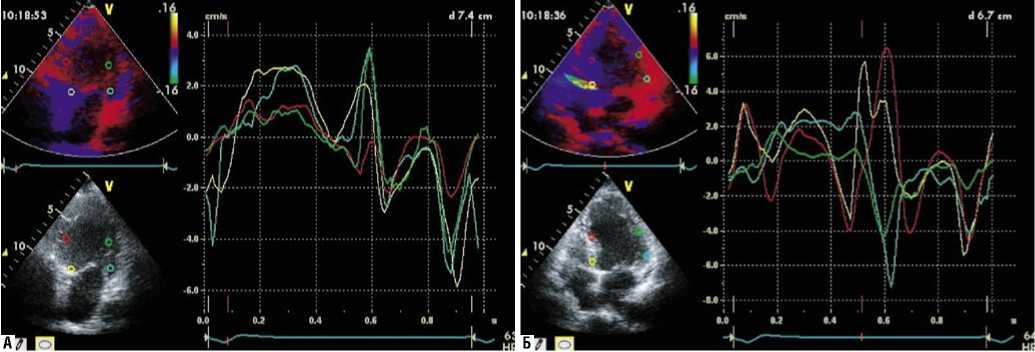
Рис. 2. А – нет признаков межсегментарного асинхронизма. Б – есть признаки асинхронного сокращения между МЖП и боковой стенкой
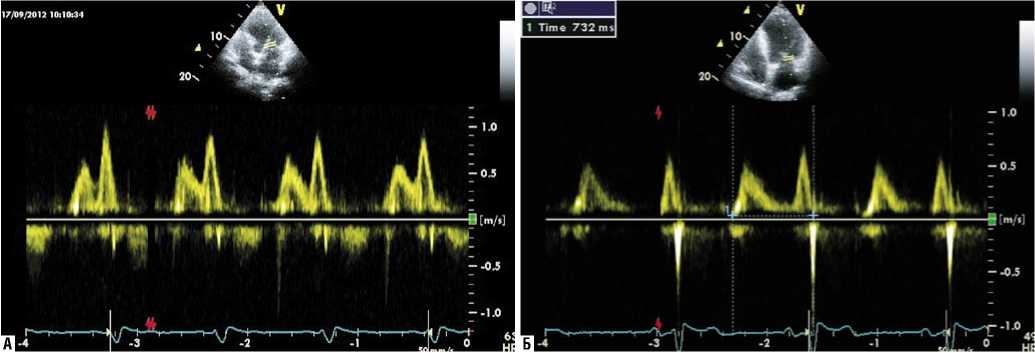
Рис. 3. Оптимизация AV задержки. Увеличение времени диастолического наполнения ЛЖ (оставляется АV задержка та, при которой время диастолическоро трасмитрального потока максимально)
CSA= 3,14 d2 /4. Интеграл линейной скорости потока VTI равен произведению средней скорости потока v ср. на время выброса ET: VTI = v ср Х ET. Таким образом, рассчитывая по интегралу линейной скорости (VTI) ударный объем (SV), оставляем такой режим VV задержки, при которой VTI максимален.
У пациентов, ответивших на вмешательство «ре-спондеров», клиническое улучшение наблюдается через несколько дней после имплантации при сочетании бивентрикулярной стимуляции с оптимальной медикаментозной терапией.
Через 6 месяцев после операции оценивалась толерантность к физической нагрузке и процессы обратного ремоделирования ЛЖ.
Через 6 месяцев с момента имплантации устройства был проведен анализ клинических (снижение функционального класса сердечной недостаточности, увеличение дистанции при шестиминутном тесте с ходьбой) и эхокардиографических (увеличение сердечного выброса и dp/dt, удлинение времени диастолического заполнения левого желудочка, уменьшение степени митральной регургитации, СДЛА, давления в предсердиях, конечного диастолического и систолического объемов ЛЖ) критериев ответа на вмешательство (см. табл. 1).
К группе «респондеров» были отнесены 45 (64%) испытуемых, при этом наибольшая частота ответа на КРТ была зарегистрирована среди пациентов с ДКМП (п = 42; 93,3%). Также следует отметить, что ответ на вмешательство также наблюдался у обоих пациентов с полной блокадой правой ножки пучка Гиса.
Существует мнение, что больным с тяжелой сердечной недостаточностью и QRS более 150 мс показана ресинхронизирующая терапия, т.к. развитие механической диссинхронии миокарда лишь вопрос времени. Напротив другие исследователи считают, что длительность комплекса QRS имеет низкую прогностическую значимость. Кроме этого, механическая диссинхрония является независимым предиктором положительного ответа пациента на КРТ. Механическая диссинхрония в работе левого желудочка отсутствует у 30% пациентов с ХСН и межжелудочковой задержкой более 40 мс и регистрируется у 50% пациентов с узким QRS комплексом [5, 6].
Критерии подбора больных требуют дальнейшего уточнения, учитывая что не менее 30 % пациентов не являются респондерами в рандомизированных исследованиях MUSTIC и MIRACL. В нашем наблюдении таких больных было 37,1%.
Мы считаем, что ресинхронизация может быть эффективной только у больных с потенциально коррегируе-мым асинхронизмом сократимости. При идиопатической кардиомиопатии ожидаемый эффект на ресинхронизирующую терапию выше, нежели при ишемической, в связи с тем, что в последнем случае часть сегментов находится в состоянии акинеза и ответить на стимуляцию не может. Если в месте установки электрода во время стимуляции увеличивается сократимость миокарда под
Табл. 1. Сравнительная оценка пациентов до имплантации ресинхронизирующего устройства и через 6 месяцев после операции
|
Параметры |
«Респондеры» (n = 45) |
«Нереспондеры» (n = 25) |
||||
|
До операции |
6 мес. |
p |
До операции |
6 мес. |
p |
|
|
ФВ, % |
22,3 ± 4,2 |
36,1 ± 4,0 |
p < 0,0001 |
23,4 ± 4,2 |
27,6 ± 4,2 |
p = 0,062 |
|
КДО, мл |
231,3 ± 18,9 |
207 ± 18,4 |
p = 0,01 |
227 ± 16,8 |
224 ± 21,9 |
p = 0,82 |
|
КСО, мл |
166,3 ± 18,9 |
122,1 ± 17,5 |
p = 0,006 |
156 ± 18,3 |
149 ± 17,5 |
p = 0,71 |
|
QRS, мс |
169 ± 31 |
134 ± 18 |
p < 0,0001 |
167 ± 19 |
157 ± 21 |
p = 0,08 |
|
Тест 6-мин. ходьбы, м |
260 ± 18,3 |
390 ± 23,4 |
p < 0,0001 |
259 ± 21,3 |
272 ± 14 |
p = 0,31 |
Примечание : ФВ – фракция выброса, КДО и КСО – конечно систолический и диастолический объем.

электродом при ДКМП, то такие больные становились респондарами.
Некоторые авторы отдают предпочтение режимам исследования деформации миокарда, а не скорости движения миокарда в оценке синхронности сокращения. Основанием для этого является наличие диссоциации между временем локального движения и деформацией миокарда. В норме начало локального укорочения в продольном направлении развивается одновременно с максимальной систолической скоростью деформации и максимальной систолической скоростью движения миокарда. Движение и сокращение миокарда существуют одновременно, и оценка синхронности сокращения может проводиться по измерению движения миокарда. У больных с блокадой ЛНПГ наблюдается диссоциация между деформацией и скоростью движения миокарда. Это связано с тем, что при блокаде левой ножки пучка Гиса движение миокарда в большей степени зависит от воздействия соседних сегментов и общего движения сердца. Поэтому измерения миокарда может не отражать несинхронность сокращения желудочков [7].
К недостаткам тканевого допплера миокарда относится возможность анализа на протяжении кардиоцикла только в одном ультразвуковом сечении [8]. При необходимости сравнивать электромеханическую задержку сегментов миокарда из разных сечений, нужны многократные измерения, и на полученную таким образом информацию могут оказывать влияние различия в частоте сердечных сокращений и фаз дыхания. Кроме того, получение достаточной информации по нескольким сегментам миокарда требует определенных временных затрат. Дальнейшее совершенствование автоматического анализа тканевого допплера, а также развитие методов многокамерной оценки внутриседечного ассинхронизма позволят улучшить отбор пациентов на бивентрикуляр-ную электрокардиостимуляцию [9].
Выводы
Список литературы Опыт использования кардиоресинхронизирующей терапии у пациентов с застойной сердечной недостатосностью
- Dickstein К., et al. ESC guidelines for the diagnosis and treatment of acute and chronic heart failure 2008: the Task Force for the diagnosis and treatment of acute and chronic heart failure 2008 of the European Society of Cardiology. Eur J Heart Fail 2008; 10: 933-989.
- He J., Ogden L.G., Bazzano L.A., et al. Risk factors for congestive heart failure in US men and women: NHANES I epidemiologic follow-up study. Arch Intern Med 2001; 161: 996.
- Gheorghiade M., Bonow R.O. Chronic heart failure in the United States: a manifestation of coronary artery disease. Circulation 1998; 97: 282.
- Бокерия Л.А., Бокерия О.Л., Кислицина О.Н. Применение временной бивентрикулярной стимуляции у пациентов с острой сердечной недостаточностью после кардиохирургических операций//Анналы аритмологии. 2006. N 6. С. 27.
- Burri H. Utility of echocardiography for tailoring cardiac resynchronization therapy//Kardiovaskulare Mtdizin. 2006; 9: 188-196.
- Lang R. Live Three-dimensional Ehocardiography Impoving Patient Care through Comprehensive Cardiac Management//Cardiology: Technology and service. 2006: 1-5.
- Алехин М.Н. Тканевой допплер в клинической эхокордиографии С. 56, 57. 2003.
- Никифоров В.С., Лебедев Д.С., Свистов А.С. Роль эхокардиографических методик в оптимизации электрофизиологической ресинхронизации работы сердца у больных с хронической сердечной недостаточностью//Ультразвуковая и функциональная диагностика. 2006 г. № 4. С. 118-128.
- Bax J.J., Abrahm W. T., Chin M.H. et al. Cardia resynchronization therapy. Part 1-Issues before device implantation/J. Am. Coll. Cardiol. 2005. Vol. № 46. № 12. P. 2153-2167.


