Опыт применения дермального эквивалента в комплексном лечении синдрома диабетической стопы
Автор: Коцлова А.А., Биниенко М.А., Юдинцева Н.М., Блинова М.И., Власов Т.Д., Давыденко В.В.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 5 (51), 2016 года.
Бесплатный доступ
В настоящее время многие исследователи рассматривают сахарный диабет (СД) как неинфекционную пандемию, охватившую планету: только по обращаемости насчитывается 366 млн. больных СД (7% всего населения планеты), более 50% из них - лица трудоспособного возраста. Цель исследования: оценить эффективность, безопасность, и факторы, влияющие на применение ЭД для заживления ран при СДС, длительность терапевтического эффекта и отдаленные результаты. В исследование были включены 60 пациентов, из числа больных с СДС, проходивших лечение в 2013-2016 годах в отделениях гнойной хирургии Госпиталя для ветеранов войн и Городской больницы №14 г. Санкт-Петербурга. В зависимости от использованного метода лечения все больные были разделены на две сопоставимые по возрастному и половому составу группы - основную и контрольную, отобранные методом случайной выборки. В основной группе пациентам дополнительно к стандартному лечению применяли аппликацию на трофическую язву ЭД, а в контрольной группе - проводили только стандартное лечение. ЭД показал высокую эффективность в основной группе пациентов. Применение ЭД при комплексном лечении больных с СДС стимулирует процессы заживления и ускоряет скорость эпителиизации. Наиболее эффективно применение ЭД у больных с нейропатической формой СДС.
Синдром диабетической стопы, трофические язвы, диабетические язвы, сахарный диабет 2 типа, чрескожное измерение напряжения кислорода, дермальный эквивалент, грануляции, эпителиизация
Короткий адрес: https://sciup.org/142211285
IDR: 142211285 | УДК: 617-089.4;
Текст научной статьи Опыт применения дермального эквивалента в комплексном лечении синдрома диабетической стопы
В настоящее время многие исследователи рассматривают сахарный диабет (СД) как неинфекционную пандемию, охватившую планету: только по обращаемости насчитывается 366 млн. больных СД (7% всего населения планеты), более 50% из них – лица трудоспособного возраста. [7].
Синдром диабетической стопы (СДС) – одно из наиболее частых и опасных осложнений СД, характеризуется возникновением хронических гнойно-некротических процессов (трофических язв) на стопе с поражением кожи, мягких тканей и костно-суставного аппарата, вследствие патологических изменений в периферической нервной системе (диабетическая нейропатия) и в сосудистой системе (диабетическая ангиопатия) [15]. Возникновение СДС отмечается у 20–80% больных СД в возрасте от 20 до 75 лет, у большинства из них возникает угроза малой или высокой ампутации нижней конечности [1, 2, 11, 17, 19]. В год в мире по поводу СДС производится до 200 тыс. высоких ампутаций [3].
Патофизиология СДС, обусловлена комбинацией таких процессов, как нейропатия, нарушение регионарной гемодинамики и иммунитета, инфекция и травма, что в совокупности создает порочный круг. Стандарт медицинской помощи для лечения пациентов с СДС предусматривает мультидисциплинарный подход, который включает коррекцию углеводного обмена, обеспечение адекватной перфузии конечностей, дебридмент нежизнеспособных тканей, разгрузку стопы от избыточного давления, подавление и контроль инфекции, местное лечение язв и обучение пациента правилам жизни и ухода за нижними конечностями. К со-
жалению, не смотря на достижения медицины, лечение трофических диабетических язв остается сложной проблемой: сроки заживления, как правило, очень длительные: даже с лучшим доступным стандартом терапии в течение 12 - 20 недель, могут зажить соответственно только 24% - 30% диабетических язв [15]; нередко такие язвы вообще плохо поддаются стандартному лечению; также при СДС очень высок риск рецидива уже заживших язв [22].
Одним из методов закрытия раневых дефектов является аутодермопластика свободным расщепленным лоскутом. Однако, по данным литературы, аутодермопластика для закрытия язвенных дефектов при СДС является недостаточным эффективным методом лечения [5, 6, 14]. Результат закрытия раневого дефекта не всегда успешен и технически труден на определенных отделах стопы. Риск отторжения трансплантата при этом, по данным различных авторов составляет 10–30%. Кроме того, на фоне диабетической полинейропатии, микро- и макроангиопатии высок риск образования дополнительного хронического раневого дефекта в области взятия кожного лоскута. Так, по данным различных авторов, эпителизация донорских участков осложняется нагноением и длительным заживлением в 5-70% случаев [8, 14]. При этом длительное заживление донорских ран ведёт к образованию гипертрофических и келоидных рубцов [8]. Серьезной причиной неудач трансплантации аутологичной кожи является отсутствие объективных методов адекватной оценки готовности раны к аутодермопластике, которая в настоящее время осуществляется лишь на основании клинической оценки состояния больного и визуальных признаков гранулирующей раны. В связи с перечисленными выше обстоятельствами, необходим поиск новых методов лечения, направленных на ускорение заживления раневого дефекта при СДС.
Исследования последних лет в области биохимии, патофизиологии, иммунологии открыли некоторые, ранее неизвестные, молекулярно-клеточные механизмы, объясняющие причину хронизации раневого процесса, что позволило по-новому подойти к решению проблемы лечения хронических ран (трофических язв). В качестве одного из таких перспективных направлений лечения хронических ран (трофических язв) является применение клеточных технологий: ауто- и аллогенных культур клеток кожи, живого кожного эквивалента [9]. В зарубежных исследованиях показана высокая клиническая эффективность применения биоинженерных заменителей кожи, таких как «Dermagraft» (Advanced Tissue Sciences, США), «AlloDerm» (LifeCell, США), «Apligraf» (Organogenesis, США) для лечения хронических, в том числе диабетических трофических язв [16, 18, 20, 21, 23]. В России применение аналогичного отечественного биоинженерного продукта «Эквивалента Дермального» (ЭД) (производства НИИ цитологии РАН) - аллогенных фибробластов, заключенных в коллагеновый гель, оказалось эффективным при лечении обширных ожогов и трофических язв венозной этиологии [4, 12, 13]. Однако, систематизированных сведений по применению ЭД в лечении трофических язв при СДС в научной литературе нам не встретилось.
Цель исследования: оценить эффективность, безопасность, и факторы, влияющие на применение ЭД для заживления ран при СДС, длительность терапевтического эффекта и отдаленные результаты.
Материал и методы
В исследование были включены 60 пациентов, из числа больных с СДС, проходивших лечение в 2013–2016 годах в отделениях гнойной хирургии Госпиталя для ветеранов войн и Городской больницы №14 г. Санкт-Петербурга. Среди пациентов было 26 мужчин, 34 женщины. Возраст обследуемых пациентов: от 46 до 90 лет (средний возраст 68±22 лет). Критерии включения: пациенты обоего пола старше 18 лет, у которых по данным клинического и инструментального обследования имеется СДС с язвенным дефектом стоп в стадии грануляции, площадью от 1 до 25 см2, который существует более 6 недель, не распространяется на кости, мышцы, сухожилия (класс 1А, 1С по Техасской классификации [15]), если площадь язва не уменьшалась в размерах на 50% и более после 2-х недель стандартной терапии. Пациенты давали добровольное информированное письменное согласие на участие в исследовании.
В зависимости от использованного метода лечения все больные были разделены на две сопоставимые по возрастному и половому составу группы — основную и контрольную, отобранные методом случайной выборки. В основной группе пациентам дополнительно к стандартному лечению применяли аппликацию на трофическую язву ЭД, а в контрольной группе - проводили только стандартное лечение. Таким образом основная группа (40 пациентов) состояла из подгруппы А - 20 пациентов с нейропатической формой СДС и подгруппы Б - 20 пациентов нейроишемической формой СДС; а контрольная группа (20 пациентов) состояла из подгруппы А1 - 10 пациентов с нейропатической формой СДС и подгруппы Б1 - 10 пациентов с нейроишемической формой СДС (табл. 1).
Стандартное комплексное лечение СДС включало в себя: коррекцию углеводного обмена с участием врача эндокринолога, дебридмент гнойного очага с использованием ультразвуковой кавитация («Sonoca 400», Söring, Германия) и вакуумтерапии (VivanoTec, Hartmann, Германия) с последующими ежедневными перевязками с антисептиками и местными антибактериальными средствами (левомеколь, бетадин) и стандартными перевязочными средствами (марлевые повязки), системную антибиотикотерапию, ангио- и нейротропную терапию, включая внутривенные инфузии Вазапростана; дополнительные методы лечения - гиперба-
Таблица 1
Распределение обследуемых пациентов по группам/подгруппам, характеру лечения
|
Группы, количество пациентов |
Подгруппы, количество пациентов |
Характер лечения |
|
Основная (n=40) |
А – нейропатичесая форма СДС (n=20) Б – нейроишемическая форма СДС (n=20) |
Стандартное комплексное лечение + аппликация на рану ЭД |
|
Контрольная (n=20) |
А1 – нейропатичесая форма СДС (n=10) Б1 – нейроишемическая форма СДС (n=10) |
Стандартное комплексное лечение |
Обозначение: n – количество пациентов
рическую оксигенацию, фотомодификацию крови (внутривенное лазерное облучение крови), озонотерапию. Кроме того, при нейроишемической форме у больных основной и контрольной групп, по возможности, дополнительно проводилась эндоваскулярная реваскуляризация конечности (чрезкожная баллонная ангиопластика, стентирование). Также применяли разгрузку пораженной стопы от давления: использовали костыли и кресло-коляску. После очищения язв и появления грануляций производился бактериологический контроль отделяемого из язвы с количественным подсчетом микробной обсемененности [10, 11].
Пересадка на рану ЭД пациентам основной группы проводилась в условиях перевязочной. ЭД получали в день пересадки из НИИ цитологии РАН (Санкт-Петербург, РФ), его транспортировка осуществлялась в герметичных чашках Петри, в сосуде Дьюара, с поддерживанием температуры +15°C, в максимально щадящем для клеточных культур режиме, исключающем механическое и термическое воздействие, среднее время доставки составило 120±35 мин. ЭД извлекали пинцетом из чашки Петри, укладывали на обработанную физиологическим раствором хлорида натрия раневую поверхность, полностью покрывая ее площадь (pис 1–3). Сверху накладывали повязку Воскопран (Био-текфарм, РФ), для предотвращения впитывания препарата, наложенной затем марлевой повязкой и фиксировали марлевым бинтом. Перевязки проводились через день. Производилось орошение марлевой повязки физиологическим раствором хлорида натрия 2 раза в день, для предотвраще-
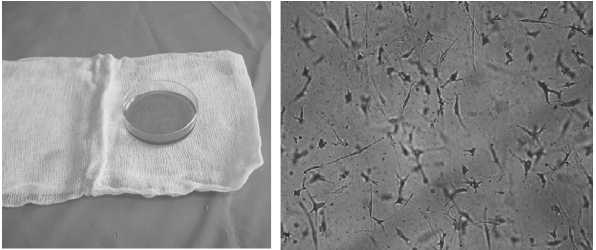
Рис. 2. Микрофотография дермального эквивалента (инвертированный микроскоп, увеличение объектива х10)
Рис. 1. Дермальный эквивалент перед применением
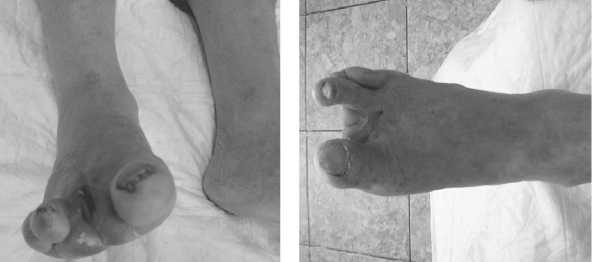
Рис. 3. Аппликация дермального эквивалента на диабетическую трофическую язву
Рис. 4. Полная эпителизация язвы через 2 месяца после применения дермального эквивалента ния высыхания повязки в соответствие с инструкцией по применению ЭД [4]. После выписки больных из стационара на амбулаторное лечение, для оценки длительности эффекта от применения ЭД проводили наблюдение и мониторинг за ними в течение 18 месяцев.
В обеих группах у пациентов определяли скорость заживления раневого дефекта. Для этого использовали параллельно две методики:
-
1. Метод контактной планиметрии: накладывали на язвенный дефект прозрачную стерильную полиэтиленовую пленку, обводили на ней контур язвы до начала лечения, через 30 и 60 суток после лечения; вручную подсчитывали площадь язвы; скорость эпителизации рассчитывалась по формуле:
-
2. Метод цифровой фотосъемки трофической язвы с последующим аналогичным компьютерным расчетом площадей дефекта и скорости эпителизации. Для оценки безопасности применения ЭД – после его аппликации у пациента оценивали жалобы: аллергические проявления, местные воспалительные изменения краев раны, исследовали клинический и биохимический анализ крови, анализ мочи.
Vs = (S-Sn)/t.
где S - площадь язвы до лечения, Sn - площадь при последующих измерениях, t - число дней между измерениями;
Для оценки факторов и условий, оказывающих неблагоприятное влияние для приживления ЭД изучали:
-
1. уровень бактериальной обсемененности язвы по данным бактериологических посевов;
-
2. состояние регионарной гемодинамики по данным ультразвукового дуплексного сканирование артерий нижних конечностей с определение лодыжечно-плечевого индекса (ЛПИ)
-
3. кислородное обеспечение тканей пораженной стопы по данным транскутанного напряжение кислорода (ТсРО2) на стопе (Radiometer, Дания);
-
4 анализировали сопутствующие заболевания. Для оценки длительности эффекта от применения ЭД проводили наблюдение и мониторинг за пациентами в течении 18 месяцев после лечения.
Полученные результаты подвергались статистической обработке с сопоставлением средних показателей (M±m) скорости эпителизации в обследуемых группах/подгруппах. Достоверность различий определяли с помощью непараметрического критерия Вилкоксона-Манна-Уитни. Достоверными принимали значения p<0,05.
Финансирование работы по культивированию «Эквивалента Дермального» в ФГБУН «Институт Цитологии РАН» осуществлялось при поддержке гранта РНФ № 14-50-00068 «Молекулярно-клеточные технологии для лечения социально значимых заболеваний».
Результаты
В основной группе у 29 (72,5%) больных (из них 17 пациентов подгруппы А, 12 пациентов подгруппы Б) уже на 2-ые сутки после трансплантации ЭД над всей поверхностью язвенного дефекта образовывалась тонкая пленка. В дальнейшем под этой пленкой шла активная краевая эпители-зация, визуально отмеченная со 2-х суток после пересадки ЭД. В течение первой недели новообразованный эпителий отличались низкой устойчивостью к травматизации, что требовало бережного и атравматичного выполнения перевязок (рис. 3).
Средняя скорость эпителизации ран в основной группе в течение первого месяца после начала использования ЭД была достоверно (p<0,05) выше, по сравнению с контрольной для обеих сопоставляемых подгрупп. В течение второго месяца после применения ЭД, средняя эпителизации снизилась и показатели, хотя и были несколько выше, чем в подгруппах контрольной группы, но достоверного отличия не выявлено. При сравнении средней скорости эпителиза-ции между подгруппами основной группы, применение ЭД оказалось более эффективным при нейропатической форме СДС (табл. 2). Показатели ТсРО2 различались в подгруппах с нейропатической и нейроишемической формами СДС и указывали на лучшую оксигенацию тканей при нейропатической форме СДС: показатель в подгруппе А составил 45-56 (49±5) мм рт.ст., в подгруппе А1: 46-55 (49±5) мм рт.ст.; в подгруппе Б - 30- 46 (41±5) мм рт.ст; в подгруппе Б1: 30-47 (42±4) мм рт.ст. Показатели ЛПИ также отличались: в подгруппе А - 0,80-1,07 (0,88±18); в подгруппе А1 - 0,83-1,06 (0,90±9), в подгруппе Б - 0,38-0,76 (0,57±12), в подгруппе Б1 - 0,40-0,75 (0,58±13).
Из 40 пациентов основной группы у 33 пациентов (82,5%) (18 пациентов подгруппы А и 15 пациентов подгруппы Б) скорость эпителизации достоверно превысила скорость эпителизации в контрольной группе (по сравнению с показателями соответствующей подгруппы), т.е. применение ЭД было эффективным, по сравнению со стандартным лечением. У 7 пациентов основной группы (17,5%) из них у 2 пациентов подгруппы А и у 5 пациентов подгруппы Б, скорость эпителизации не превысила показатели контрольной группы, т.е. применение ЭД не оказалось эффективным. Анализ пациентов основной группы, где применение ЭД не дало эффекта, показал, что у 4 пациентов (подгруппа Б) были проявления критической ишемии: низкие показатели ТсРO2 менее 35 мм рт.ст., ЛПИ менее 0,45 у них име-
Таблица 2
Средняя скорость эпителизации трофических язв в обследованных группах/подгруппах больных в период первого и второго месяца после начала лечения
|
Группы исследования/подгруппы |
Средняя скорость эпителизации за период первых 30 суток (cм2 в сутки) |
Средняя скорость эпителизации за период вторых 30 суток (cм2 в сутки) |
|
Основная/ подгруппа А (больные с нейропатической формой СДС) |
0,42±0,06* |
0,24±0,06 |
|
Основная/ подгруппа Б (больные с нейроишемической формой СДС) |
0,11±0,05* |
0,09±0,05 |
|
Контрольная/ подгруппа А1 (больные с нейропатической формой СДС) |
0,25±0,09 |
0,18±0,09 |
|
Контрольная/ подгруппа Б1 (больные с нейроишемической формой СДС) |
0,06±0,08 |
0,05±0,08 |
Обозначение: * – достоверное (p<0,05) различие между показателями сравниваемых подгрупп в основной и контрольной группах.
лась высокая окклюзия (поверхностной бедренной, общей бедренной, подвздошных артерий). Результаты исследования показали, что во всех случаях эффективного применения ЭД исходный показатель ТсРО2 у пациентов был более 35 мм рт.ст., а ЛПИ более 0,45. У 3 пациентов (2 из подгруппы А, 1 из подгруппы Б) после применения ЭД размеры язвы оказались прежними, на третьей перевязке появились налеты фибрина в дне и усилилось серозное отделяемое из язвы, что, видимо, было обусловлено высокой степенью бактериальной обсемененности язвы (>105 на 1 см3) до аппликации ЭД, тогда как во всех случаях эффективного применения ЭД микробная обсемененность раны была ниже 105 на 1 см3. Также выявлено негативное влияние на эффективность применения ЭД следующей сопутствующей патологии у пациентов: наличие хронического отека нижней конечности или вследствие хронической венозной недостаточности на почве варикозной болезни или постромботической болезни нижних конечностей; или из-за хронической сердечной недостаточности в стадии декомпенсации.
В основной группе самая высокая скорость эпителиза-ции была у тех пациентов, у которых была низкая бактериальная обсемененность, достаточный ЛПИ и напряжение кислорода, отсутствовали сопутствующие заболевания вен и хронический отек нижних конечностей.
Во всех случаях применение ЭД не зарегистрировано каких-либо побочных отрицательных явлений; развития местных и общих аллергических реакций, изменений со стороны стандартных анализов крови и мочи.
При наблюдении за больными в сроки до 18 месяцев было отмечено следующее.
В основной группе после первичного применения ЭД удалось полностью заживить ра-невой дефект у 26 пациентов (65%) - 16 пациентов подгруппы А и 10 пациентов подгруппы Б сроки заживления составили от 1 до 3-х месяцев (в среднем 67±11 суток). Как правило, это были пациенты с небольшой площадью раневого дефекта от 2 до 12 см2 (в среднем 7±5 см2). Отмечено, что первый месяц идет активная эпителизация, и язвенный дефект сокращается на 70%, затем, хотя скорость эпителизации существенно уменьшается, но тем не менее язвенный дефект эпителизирует в сроки до 3-х месяцев. Клини-ческий пример применения ЭД представлен на рисунках 3 и 4.
У 7 пациентов основной группы (17,5%) (2 пациента подгруппы А, 5 пациента под-группы Б) в связи со снижением скорости и большими по площади язвенные дефекты от 12 до 25 см2 (в среднем 18±6 см2) в сроки от 3-х до 4-х месяцев была повторно вы-полнена аппликация ЭД (после оценки уровня микробной обсемененности раны и кровоснабжения тканей и признания их удовлетворяющими критериям применения ЭД), при этом удалось добиться полного заживления раневого дефекта у 4-х пациентов (2 пациента подгруппы А, 2 пациент подгруппы Б). У 3-х пациентов (все подгруппы Б) основной группы, даже после повторного применения ЭД, полностью заживить раневой дефект так и не удалось, хотя его размеры значительно уменьшились.
Таким образом, в указанные сроки наблюдения (18 месяцев) у 10 пациентов основной группы (2 пациента подгруппа А, 8 пациентов подгруппы Б) так и не удалось добиться полной эпителизации язвы. У 7 из них (2 пациента подгруппы А, 5 пациентов подгруппы Б) применение ЭД не оказалось эффективным, скорость эпителизации не увеличилась. У 3-х пациентов размеры язвы после повторного применения ЭД уменьшились, однако, язвенный дефект до конца не эпи-телизировал. В контрольной группе результаты в эти сроки наблюдения были следующие. Полное заживление удалось достичь у 8 пациентов (40%) (5 пациентов подгруппы А1, 3 пациента подгруппы Б1), но сроки были значительно дольше, чем в основной группе: 4-10 месяцев (в среднем 145±36 суток). Полное заживление не достигнуто у 12 пациентов (5 из подгруппы А1, 7 из подгруппы Б1). Среди 3-х пациентов основной группы с полностью зажившей трофической раной через сроки от 2 до 4 месяцев возник рецидив язвы (2 пациента из подгруппы А, 1 пациент из подгруппы Б). У больных контрольной группы рецидива язвы отмечен у 6 пациентов в сроки от 2 до 4 месяцев (4 пациентов из подгруппы А1, 2 пациента из подгруппы Б1).
Обсуждение
Полученные нами результаты, согласуются с имеющимися в литературе данными по применению зарубежных аналогов ЭД [16, 18, 21, 23]. Эффективность применения ЭД при диабетических трофических язвах оказалась ниже, чем при трофических язвах венозной этиологии [4, 12, 13], что может объясняться значительно более существенными нарушениями микроциркуляции и доставки кислорода к тканям при СДС. ЭД - это аллогенные дермальные фибробласты, заключенные в коллагеновый гель. Дермальные фибробласты представляют собой гетерогенную популяцию клеток мезенхимального ряда и играют ключевую роль в процессах регуляции клеточных взаимодействий и поддержания гомеостаза кожи. Фибробласты не только формируют оптимальные условия для функционирования и пролиферации других типов клеток (эпителиальных, эндотелиальных, клеток волосяных фолликулов), но и отвечают за координацию их функций в соответствии с расположением на теле. Способность фибробластов формировать межклеточный матрикс, синтезировать цитокины, вызывать миграцию и пролиферацию различных типов клеток при повреждении кожи делает их перспективным для широкого клинического применения [8]. Эффект от применения ЭД на стимуляцию эпителизации большинство исследователей связывают с действием цитокинов и факторов роста, выделяющихся из функционирующих трансплантированных дермальных фибробластов, но, поскольку, они являются аллогенными, то вскоре гибнут, и этим, по-видимому, объясняется, факт существенного снижения скорости эпителизации спустя месяц после начала применения ЭД. Отмеченные в исследовании более высокие показатели скорости эпителизации при нейропатической форме СДС, по сравнению с ней-роишемической формой объясняются, лучшими исходными показателями кровоснабжения тканей (более высоким уровнем ТсРO2). Выявленные факторы: низкий уровень ТсРO2, низкий ЛПИ (недостаточная реваскуляризация конечностей), хронический отек нижних конечностей, бактериальная обсемененность (>105 на 1см3) препятствуют функционированию ЭД в ране и делают его применение неэффективным. Эффективность повторного применения ЭД при трофических язвах другой этиологии отмечали ранее и другие исследователи [8]. Рецидив развития трофических язв, наблюдаемый у части больных основной группы все же возникал реже и позже, чем у пациентов контрольной группы, что может указывать на более прочную структуру рубца после применения ЭД.
Выводы
-
1. Применение ЭД у больных с СДС в стадию грануляции стимулирует процессы заживления и ускоряет скорость эпителизации по сравнению со стандартным лечением, в большей степени при нейропатической форме.
-
2. Применение дермального эквивалента у больных СДС безопасно.
-
3. Увеличение скорости эпителизации ран после применения ЭД у больных СДС наиболее выражено в первый месяц после применения, затем она снижается, т.е. терапевтический эффект длится около месяца, повторное применение ЭД вновь ускоряет эпителизацию.
-
4. Факторы ограничивающие применения дермального эквивалента у больных с СДС низкие показатели TcPО2 -менее 35 мм рт.ст., ЛПИ<0,45 (вероятность высокой окклюзии артерий нижних конечностей); высокая степень бактериальной обсемененности > 105 на 1см3, хронический отек нижних конечностей.
-
5. Применение ЭД у больных СДС в сроки наблюдения до 18 месяцев дает лучше результаты по сравнению со стандартным лечением.
Список литературы Опыт применения дермального эквивалента в комплексном лечении синдрома диабетической стопы
- Анциферов М.Б., Галстян Г.Р., Токмакова А.Ю., Дедов И.И. Синдром диабетической стопы//Сахарный диабет. -2001. -№2. -с.2-8.
- Балаболкин М.И., Клебанова Е.М., Креминская В.М. Патогенез ангиопатий при сахарном диабете//Сахарный диабет. -1999. -№2. -с 22-25.
- Бахарев И.В., Редькин А.Ю. Синдром диабетической стопы: диагностика, лечение, профилактика. Качество жизни//Медицина. -2003. -№1. -с. 35-38.
- Блинова М.И., Юдинцева Н.М., Александрова О.И. и др. Клинический опыт заживления трофических язв с использованием клеточного продукта «Эквивалент дермальный ЭД»//Здоровье -основа человеческого потенциала: проблемы и пути их решения. -2015. -Т. 10. -№ 2. -с. 690-694.
- Винник Ю.С. Клеточные технологии и тканевая инженерия в лечении длительно не заживающих ран/Винник Ю.С., Салмина А.Б., Дробушевская А.И., Теплякова О.В., Пожиленкова Е.А., Зыкова Л.Д.//Вестник экспериментальной и клинической хирургии. -2011. -Т. IV, № 2. С. 392-397.
- Гостищев В.К., Липатов К.В., Комарова Е.А. и др. Дифференцированный подход к выбору кожной пластики операций у больных с хирургической инфекцией//хирургия. Журнал им. Н.И. Пирогова. -2009. -№19. -с.19-24.
- Дедов И.И., Шестаковой М.В., Сунцов Ю.И. и др. Результаты реализации подпрограммы «Сахарный диабет» федеральной целевой программы «Предупреждение и борьба с социально значимыми заболеваниями 2007-2012 годы»//Сахарный диабет. -2013г. -Том 16. -№ 2S: Спецвыпуск 2. -с. 2-16.
- Зорин В.Л., Зорина А.И., Петракова О.С. и др. Дермальные фибробласты для лечения дефектов кожи//Клеточная трансплантология и тканевая инженерия. -2009. -№4. -с.26-40.
- Зорин В.Л, Зорина А.И., Черкасов В.Р. Анализ зарубежного рынка регенеративной медицины//Клеточная трансплантология и тканевая инженерия. -2009. -№3. -с. 68-78.
- Лапин А.Ю., Скрябин О.Н., Рубцов М.А. Лечение трофических язв венозного генеза с применением возможностей клеточной терапии//Амбулаторная хирургия. -2014. -№1. -с. 5-11.
- Коцлова А.А., Биниенко М.А., Галилеева А.Н., Юдинцева Н.М., Шеянов С.Д., Давыденко В.В., Власов Т.Д. Сравнительная оценка эффективности применения эквивалента дермального при нейропатической и нейроишемической формах синдрома диабетической стопы//Патология кровообращения и кардиохирургия. 2016. С. 62-71. http://dx.doi.o DOI: rg/10.21688/1681-3472-2016-3-62-71
- Мельцова А.Ж. Гриценко В.В., Орловский П.И. и др. Применение дермальных фибробластов в комплексном лечении больных трофическими язвами венозной этиологии//Вестник хирургии им. И.И. Грекова. -2007. -Т. 166. -№1. -с. 72-77.
- Седов В.М., Андреев Д.Ю., Смирнова Т.Д. и др. Эффективность клеточной терапии в лечение больных с трофическими язвами нижних конечностей венозной этиологии//Ангиология и сосудистая хирургия. -2007. -№13. -с.65-75.
- Ярец Ю.И., Новикова И.А. Лабораторный прогноз риска отторжения аутодермотрансплантата//Вестник хирургии им. И.И. Грекова. -2010. -№2. -с. 34-38.
- Apelqvist J., Bakker K., van Houtum W.H., et al. International consensus and practical guidelines on the management and the prevention of the diabetic foot. International Working Group on the Diabetic Foot//Diabetes Metab Res Rev. -2000. -№16. -Suppl.1. -p. 84-92.
- Bushberger B., Follmann M., Freyer D. et al. The importance of growth factors for the treatment of chronic wounds in the case of diabetic foot ulcers//GMS Health Technol Assess. -2010. -№6. -doc. 12. -p.33-36.
- Harris P.L., Veith F.J., Shanik G.D. at.al. Prospective randomized comparison of in situ and reversed infrapopliteal vein grafts//Br.J.Surg. -1993. -v.80. -№2. -p. 173-176.
- Hart C.E., Loewen-Rodriguez A., Lessem J. Dermagraft: Use in the Treatment of Chronic Wounds//Advances in wound care. -2012. -v. 1. -№3. -p.138-141.
- Ismail K., Winkley K., Stahl D. et. аь A cohort study of people with diabetes and their first foot ulcer: the role of depression on mortality//Diabetes Care. -2007. -v.30. -№6. -p. 1473-1479.
- Jadlowiec C., Brenes R.A., Li X. et al. Stem cell therapy for critical limb ischemia: What can we learn from cell therapy for chronic wounds?//Vascular. -2011. -v.20. -№5. -p. 284-289.
- Langer A., Rogowski W. Systematic review of economic evaluations of human cell-derived wound care products for the treatment of venous leg and diabetic foot ulcers//BMC Health Serv Resc. -2009. -v.9. -s. 115. -p. 1-14.
- Larsson J., Agardh C.D., Apelquist J., Stenstorm A. Longterm prognosis after healed amputation in patients with diabetes//Clin Orthop Relat Res. -1998. -№350. -p. 149-158.
- Lev-Tov H., Li C.S., Dahle S., Isseroff R.R. Cellurar versus acellular matrix devices in treatment of diabetic foot ulcers: study protocol for a comparative efficacy randomized controlled trial//Trials. -2013. -№14. -p. 1-8


