Опыт применения интраоперационной эндоскопии с целью раннего выявления и предотвращения осложнений анастомозов желудочно-кишечного тракта
Автор: Груба Л.Н., Магомедов М.С., Василенко К.В., Лебедев И.С., Егиев В.Н.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 2 (48), 2016 года.
Бесплатный доступ
Проанализирована роль интраоперационной эндоскопии, позволяющей визуализировать зону анастомоза, в раннем выявлении и предотвращении осложнений анастомозов желудочно-кишечного тракта, определении его герметичности и в ряде случаев устрании осложнений.
Интраоперационная эндоскопия, анастомоз, желудочно-кишечный тракт
Короткий адрес: https://sciup.org/142211253
IDR: 142211253 | УДК: 617-089.844
Experience with intraoperative endoscopy for early detection and prevention complications anastomosis of the gastrointestinal tract
The role of intraoperative endoscopy allows visualization of the anastomosis area in the early detection and prevention of complications of anastomosis of the gastrointestinal tract, and determining its tightness in some cases eliminate complications.
Текст научной статьи Опыт применения интраоперационной эндоскопии с целью раннего выявления и предотвращения осложнений анастомозов желудочно-кишечного тракта
Осложнения со стороны анастомозов желудочнокишечного тракта- одни из самых серьезных в практике хирурга. Редким осложнением является кровотечение из линии шва (частота не превышает 2%). Как правило, оно прекращается самостоятельно, но в ряде случаев требует эндоскопического гемостаза [1, 2]. Значительно чаще встречается более опасное осложнение – несостоятельность шва анастомоза, которая, по данным литературы, возникает в 5-30% случаев после операций на пищеводе [3], и до 20% случаев - после колоректальных операций [4]. Данное смертельно опасное осложнение практически всегда является причиной повторной операции и удлиняет сроки госпитализации больного [4, 5]. Несостоятельность анастомоза не только увеличивает морбидность и смертность, но и повышает частоту местного рецидива в случае операций по поводу злокачественных новообразований [5–9]. В поиске способов предотвращения столь грозных осложнений хирурги разрабатывают методы их ранней диагностики, способы интраоперационной оценки герметичности и пер- фузии зоны анастомоза, изучают роль лабораторных показателей в выявлении этих осложнений на этапе доклинических проявлений. По данным ряда исследований, оценка уровня С-реактивного белка сыворотки крови в сочетании с определением уровня лейкоцитов периферической крови на 3-5 сутки после операции может помочь в раннем выявлении несостоятельности анастомоза [10, 11]. Как известно, С-реактивный белок имеет свойство быстро подниматься в условиях воспаления. Согласно результатам ряда исследований, прогностическим в отношении несостоятельности анастомоза является уровень С-реактивного белка, измеренный на 3–5 послеоперационные сутки и находящийся в диапазоне от 120 до 190 мг/л [11]. Особый практический интерес вызывают интраоперационные методы диагностики. К одному из таких методов относится интраоперационная эндоскопическая оценка зоны анастомоза, которой посвящен обширный ряд зарубежных исследований [12–25]. Данный метод позволяет непосредственно в момент операции не только осмотреть анастомоз на предмет герметичности и кровотечения из линии шва, но и выполнить необходимые методы коррекции этих осложнений в случае их выявления

(эндоскопический гемостаз, наложение дополнительных швов). Таким образом возможно улучшить результаты лечения и снизить частоту подобных чрезвычайно тяжелых состояний. В число достоинств данного метода входят его простота и возможность немедленной коррекции осложнения. Процедура выполняется путем заполнения области зоны анастомоза физиологическим раствором и последующей инсуффляции в просвет желудочно-кишечного тракта воздуха через гастро- или колоноскоп с пережатием кишки проксимальнее (в случае операций на толстой кишке) или дистальнее (в случае операций на пищеводе, желудке) анастомоза. Появление пузырьков воздуха в области линии шва анастомоза говорит о его негерметичности. Далее тактика определяется индивидуально (наложение дополнительных швов в области дефекта или формирование анастомоза заново). Метод интраоперационной эндоскопии был впервые предложен и введен в практику бариатрическими хирургами ввиду значительно большей частоты несостоятельности анастомоза по сравнению с колоректальными вмешательствами. Исследованиями была показана безопасность и большая чувствительность метода относительно используемых ранее зондовой пробы с воздухом и пробы с метиленовым синим.
Целью нашей работы явилась оценка роли интраоперационной эндоскопии в раннем выявлении и предотвращении осложнений анастомозов желудочно-кишечного тракта, позволяющей визуализировать зону анастомоза, определить его герметичность и в ряде случаев устранить осложнение.
Материалы и методы
С 24.06.15 по 11.02.16 в ГКБ №1 имени Н.И. Пирогова (г. Москва) было выполнено 41 плановое оперативное вмешательство на верхних и нижних отделах желудочнокишечного тракта с формированием первичного анастомоза и последующей интраоперационной эндоскопической оценкой зоны анастомоза. Пациенты были разделены на 2 группы: подвергнутые операции на левой половине толстой кишки и оперированные на верхних отделах желудочнокишечного тракта.
В первой группе 32 пациентам (при дальнейшем описании количество пациентов указывается в круглых скобках) в возрасте от 41 до 87 лет (средний возраст 67 лет) была выполнена плановая операция на левой половине толстой кишки. Показанием для операции явились: рак толстой кишки – у 28 (87,5%) больных (из них у 4 - после стентирования опухоли и 1 – по поводу рецидива заболевания после левосторонней гемиколэктомии); свищи (мочепузырно-кишечный и толстокишечно-влагалищный) вследствие осложнения дивертикулярной болезни – у 2 пациентов (6,3%), долихосигма – у 1 (3,1%), закрытие колостомы – также у 1 больного (3,1%). В 14 случаях (43,8%) выполнена лапаротомия (из них 6 – конверсия после лапапроскопического вмешательства), в 18 случаях (56,2%) – полностью лапароскопическая операция. Операции были выполнены в следующем объеме: передняя резекция прямой кишки - у 10 больных, резекция сигмовидной кишки - у 19 пациентов (в том числе у одного одновременно была выполнена правосторонняя гемиколэктомия); левосторонняя гемиколэктомия выполнена у 2 больных, резекция анастомоза при рецидиве опухоли – у 1 пациента. У 6 больных (19%) были выполнены симультанные операции: на мочевом пузыре – 2 больных (операция Бриккера по поводу рака мочевого пузыря и резекция мочевого пузыря по поводу пузырно-кишечного свища), ад-нексэктомия – у 1 больной, экстирпация и надвлагалищная ампутация матки – у 2 пациенток; 1 пациенту с рецидивом опухоли в зоне анастомоза была выполнена атипичная резекция 4 сегмента печени, аппендэктомия и холецистэктомия. Нижняя брыжеечная артерия пересечена у основания у 9 пациентов (28,1%), левая ободочно-кишечная артерия сохранена у 22 пациентов (68,8%). У пациента, оперированного по поводу рецидива опухоли в зоне анастомоза, пересечена a. сolica media. Аппаратный анастомоз был сформирован у 30 больных (94%), ручной шов использовали у 2 (6%): у 1 пациента - двурядный непрерывный ПДС 4/0, у другого – двурядный узловой Викрил 4/0 и Викрил 3/0). При формировании аппаратного анастомоза использовался циркулярный сшивающий аппарат различного диаметра: чаще 28 мм (17 больных) и 29 мм (6), реже – 25 мм (4), 31мм (2) и 33 мм (1 пациент). Все анастомозы были сформированных по типу «конец в конец»: сигмо-ректоанастомоз (15), десцендо-ректоанастомоз (13), десцендо-сигмоанастомоз (1), сигмо-сигмоанастмоз (1), трансверзо-ректоанастомоз (1), J-pouch резервуар при низкой передней резекции прямой кишки – также у 1 пациента. Превентивная илеостома была сформирована у 5 пациентов (16%) при анастомозе ниже 7–8 см от ануса. Укрепление линии механического анастомоза дополнительными ручными швами на переднюю стенку или циркулярно выполнено у 10 пациентов (у 9 – высота анастомоза была более 15 см от ануса, у 1 – на 7 см без илеостомы). Только погружение «ушей» дистальной культи выполнено у 4 пациентов (3 больных - анастомоз более 20 см от ануса, 1 – на 9 см). Всем пациентам после формирования анастомоза была выполнена его интраоперационная эндоскопическая оценка на предмет состоятельности, проходимости, отсутствия кровотечения. Также всем пациентам, перенесшим операцию на левой половине толстой кишки за указанный период времени, с целью раннего выявления несостоятельности анастомоза проводилось определение С-реактивного белка сыворотки крови на 3–5 сутки послеоперационного периода.
Во второй группе 9 пациентам в возрасте от 37 до 77 лет (медиана – 52 года) была выполнена плановая операция на верхних отделах желудочно-кишечного тракта с формированием первичного анастомоза. Показанием для операции явились: рак желудка (8) и рубцовый стеноз пищевода (1). В 7 наблюдениях выполнена лапаротомия (из них 1 – конверсия лапароскопического вмешательства), в 1 случае – полностью лапароскопическая операция; 1 больному с рубцовым стенозом пищевода и гастростомой выполнили комбинированный доступ (лапаротомия и торакотомия). Операции были выполнены в объеме гастрэктомии с формированием эзофаго-энтероанастомоза по типу «конец в бок» (4 больных), дистальная резекция желудка с формированием гастро-энтероанастомоза по типу «бок в бок» (4, из них 1 – видеоассистированная); резекция пищевода с замещением последнего желудочной трубкой, формированием эзофаго-гастроанастомоза «конец в конец» и ликвидация гастростомы выполнена у 1 больного. 2 больным этой группы были выполнены симультанные операции: экстирпация матки с придатками (1 пациентка), и спленэктомия (1 пациента с дистальной резекцией желудка по поводу рака ввиду наличия увеличенных лимфатических узлов в области ворот селезенки и ее диффузной кровоточивости после мобилизации). Все анастомозы были сформированы ручным швом: у 6 пациентов - однорядным обвивным нитью Пролен 3/0, Викрил 3/0, Викрил 4/0, ПДС 3/0, у 2 пациентоводнорядным узловым нитью Викрил 3/0, Викрил 4/0; еще у 1 пациента использован двурядный шов (внутренний – обвивной нитью ПДС 4/0, наружный – узловой нитью Ви-крил 3/0). Всем пациентам была выполнена интраоперационная эндоскопическая оценка зоны анастомоза на предмет кровотечения, проходимости и герметичности.
Результаты исследования
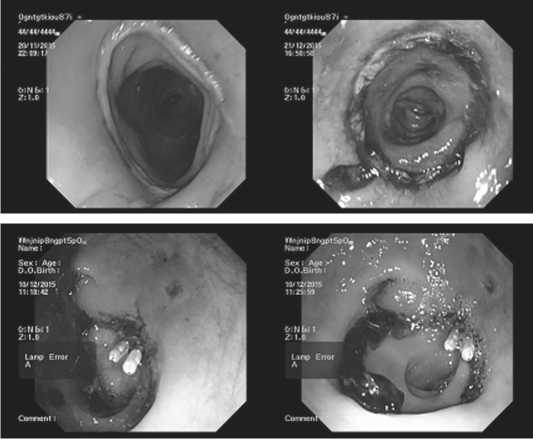
По данным интраоперационной эндоскопии, выполненной 32 пациентам, перенесшим плановую операцию на левой половине толстой кишки с формированием первичного анастомоза, были получены следующие данные. Уровень анастомоза был сформирован на высоте более 10 см от ануса у 21 больного, на высоте 5–10 см – у 9 пациентов, на высоте менее 5 см от ануса - у 2 пациентов (этим больным была наложена разгрузочная илеостома). У всех пациентов анастомоз был герметичен (воздушная проба в ходе исследования отрицательная), свободно проходим. У 22 больных на линии шва следов крови не было, или были помарки, у 9 пациентов на линии шва анастомоза отмечено умеренное количество крови без признаков продолжающегося кровотечения.
У 1 больного после лапароскопической резекции сигмовидной кишки с формированием анастомоза циркулярным аппаратом диаметром 28 мм (высота анастомоза 12 см от ануса) было выявлено продолжающееся кровотечение из линии аппаратного шва, что потребовало выполнения эндоскопического гемостаза (клипирование источника кровотечения). Данный пациент был выписан в удовлетвори- тельном состоянии на 7 сутки после операции с Hb = 96 г/л, без признаков рецидива кровотечения.
Значения С-реактивного белка сыворотки крови, определяемые у всех пациентов на 3-5 сутки после операции, варьировали от 8,56 до 184,46 мг/л (медиана 70,9 мг/л): в пределах нормы (до 10 мг/л) – 1 пациент, от 19 до 60 мг/л – 18 пациентов, от 60 до 100 мг/л - 5 пациентов, от 100 до 150 мг/л – 7 пациентов, при этом у одной больной с показателем С-реактивного белка 142 мг/л и лейкоцитозом 11,4×109/л имело место инфицирование гематомы подкожножировой клетчатки. В то же время 1 пациента без гипертермии и выраженного лейкоцитоза с уровнем СРБ выше 150 мг/л (184,6 мг/л) каких-либо послеоперационных осложнений не выявлено. Таким образом, повышение СРБ без сопутствующего лейкоцитоза и гипертермии отмечено у 97% больных, однако связи этого показателя с осложнениями раннего послеоперационного периода на данный момент нами не выявлена.
У 2 пациентов из первой группы (оперированы на левой половине толстой кишки) имело место осложненное течение послеоперационного периода. В одном случае у пациентки через 5 часов после операции было отмечено резкое падение уровня гемоглобина (до 54,0 г/л), по данным УЗИ выявлена свободная жидкость в брюшной полости. Больная взята повторно на операцию, в брюшной полости выявлено до 2 л крови со сгустками, при ревизии, в месте ранее наложенных клипс левой ободочной артерии отмечено артериальное кровотечение, клипсы отсутствуют, артерия прошита и перевязана. Дальнейший послеоперационный период протекал без осложнений, проведена гемотрансфузия, пациентка выписана в удовлетворительном состоянии на 8 сутки с Hb = 93 г/л. У другой пациентки послеопера- ционный период осложнился инфицированием гематомы подкожно-жировой клетчатки, что потребовало установки вакуум аспирационной системы. В результате лечения рана очистилась, были наложены вторичные швы, пациентка выписана на 26 сутки в удовлетворительном состоянии.
25 больных из первой группы были выписаны в удовлетворительном состоянии на 5–10 сутки после операции. 5 пациентов покинули стационар на 11–17 сутки, длительность госпитализации была обусловлена сопутствующей патологией, не связанной с операцией. Несостоятельность анастомоза у наших больных не отмечена. У одного пациента, перенесшего лапароскопическую низкую переднюю резекцию прямой кишки с формированием аппаратного сигмо-ректоанастомоза на 6 см от ануса (циркулярный аппарат 31 мм, наложена превентивная илеостома), на 2-е сутки после операции отмечен лейкоцитоз до 19,8×109/л и гипертермия до 38,3 ° С. В подобных случаях можно думать о микронесостоятельности, однако затека контрастного вещества при КТ не выявлено. На фоне консервативной антибактериальной терапии отмечена положительная динамика, пациент выписан на 13-е сутки в удовлетворительном состоянии (при выписке С-реактивный белок 39,0 мг/л, гипертермии нет).
Во второй группе по данным интраоперационной эндоскопии, выполненной 9 пациентам после плановых операций на верхних отделах желудочно-кишечного тракта с формированием первичного анастомоза, были получены следующие данные. Все анастомозы были свободно проходимы для эндоскопа, без признаков кровотечения по линии шва. У одного больного после дистальной субтотальной резекции желудка с формированием гастро-энтероанастомоза пневмопроба была положительная. Произведено наложение дополнительных швов на область дефекта. При повторном исследовании пневмопроба отрицательная. В послеоперационном периоде у данной пациентки осложнений не отмечено. У остальных 8 пациентов (88,9%) интраоперационная оценка герметичности показала состоятельность анастомоза.
Четверо больных этой группы были выписаны в удовлетворительном состоянии на 6-8 сутки после операции без осложнений. В раннем послеоперационном периоде на фоне выраженных явлений сердечной недостаточности после дистальной резекции желудка умер 1 больной. Еще 4 пациента имели осложненное течение послеоперационного периода. Подробные данные этих больных приводим ниже.
Случай 1. Пациентка после гастрэктомии. Послеоперационный период осложнился формированием абсцессов брюшной полости (на 3 сутки С-реактивный белок 160 мг/л, гипертермия до 38,0, лейкоциты 6,2×109/л), что потребовало их дренирования под контролем УЗИ на 7 сутки после операции, признаков несостоятельности анастомоза выявлено не было. Больная выписана на 14 сутки после операции в удовлетворительном состоянии. Однако на 23 сутки после операции больная повторно госпитализирована со стриктурой эзофаго-энтероанастомоза (двухрядный шов, внутренний– непрерывный, ПДС 4/0, наружный – узловой, Викрил 3/0). Выполнены многократная баллонная дилатация анастомоза, бужирование анастомоза эндоскопом, достигнут диаметр анастомоза 1,4 см. В дальнейшем пациентка выписана в удовлетворительном состоянии.
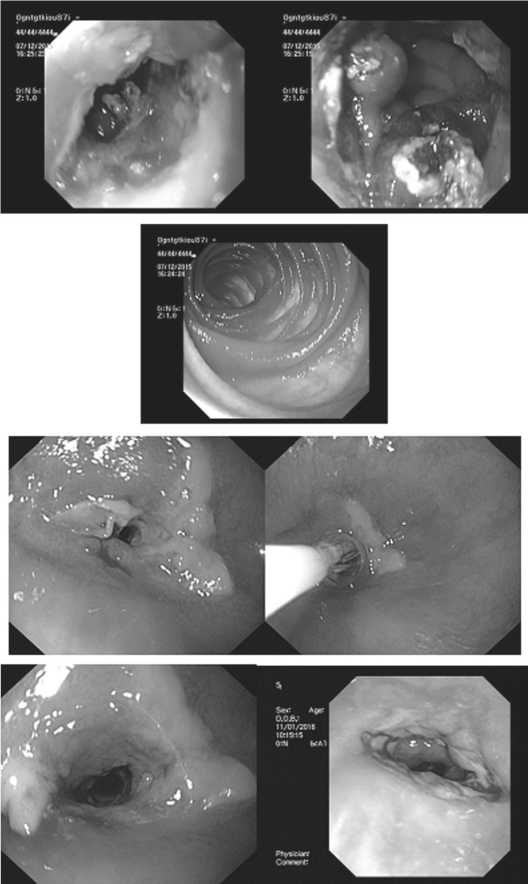
Случай 2. У пациента, перенесшего дистальную резекцию желудка с формированием гастро-энтероанастомоза, в раннем послеоперационном периоде отмечен послеоперационный панкреатит с развитием стойкого гастростаза в результате инфильтрации брыжейки ободочной кишки. В связи с этим больному на 12 сутки после первой операции выполнено повторное вмешательство – реконструкция анастомоза в У- образный. Течение послеоперационного периода ослож- нилось нагноением послеоперационной раны, проводились перевязки и промывание раны. Выписан в удовлетворительном состоянии на 13 сутки после повторной операции.
Случай 3. У больного, перенесшего по поводу рубцового стеноза пищевода резекцию пищевода с заменой желудочной трубкой и снятие гастростомы, послеоперационный период осложнился нагноением раны в области ликвидированной гастростомы (С-реактивный белок на 4 сутки 134,17 мг/л). Больной выписан на 14 сутки после операции в удовлетворительном состоянии.
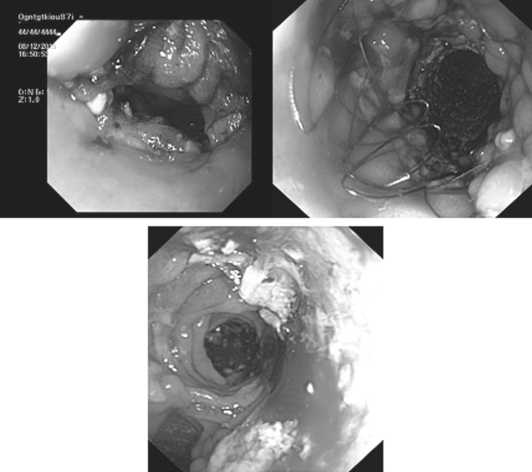
Случай 4. У пациента после гастрэктомии с формированием эзофаго-энтероанастомоза (однорядный обвивной шов, ПДС 3/0) на 7 сутки выявлена несостоятельность анастомоза, подтвержденная данными компьютерной томографии. На 3 сутки показатели СРБ составили 162 мг/л, на 7-е сутки – 218 мг/л, лейкоциты 10,9×109/л, гипертермия до 38,5 С. Больной повторно оперирован, выполнено снятие старого и формирование нового эзофаго-энтероанастомоза, наложение подвесной энтеростомы. Однако на 1 сутки после повторной операции сохранялась клиническая картина несостоятельности анастомоза с отделением желчи по установленному в заднее средостение дренажу. В экстренном порядке выполнено стентирование зоны анастомоза частично покрытым металлическим стентом. На 3 сутки отмечена самопроизвольная миграция стента по направлению к устью пищевода, выполнена его репозиция в аборальном направлении, однако при контрольном исследовании через 5 минут отмечена повторная миграция стента в нижележащие отделы с обнажением зоны анастомоза. Стент извлечен, выполнено рестентирование частично покрытым металлическим саморасправляющимся стентом. На 4 сутки после рестентирования отмечена повторная миграция стента в дистальном направлении, выполнена его репозиция, стент фиксирован к носу лигатурой, подвязанной к стенту. В дальнейшем эпизодов миграции стента не отмечено. Стент был удален на 43 сутки после его первичной установки, при контрольном эндоскопическом осмотре дефектов слизистой не определяется, при контрольной компьютерной томографии признаков несостоятельности анастомоза не выявлено.
Следует отметить, что у данного пациента при интраоперационной эндоскопической оценке анастомоз был герметичен (отрицательная пневмопроба). Вероятно, имело место нарушение перфузии с последующей ишемией тканей краев анастомоза и развитием несостоятельности. Это осложнение склонило нас в дальнейшем к использованию режима NBI при осмотре зоны анастомоза. Роль подобного метода оценки перфузии неоднозначна и требует дальнейшего изучения [26].
Выводы
-
1. Выполнение интраоперационной эндоскопии позволяет снизить процент ранних осложнений анастомозов
-
2. Повышение С-реактивного белка сыворотки крови, оцененного на 3–5 сутки после операции, без сопутствующего лейкоцитоза и гипертермии, имеет место в большинстве случаев (97% в первой группе), однако коррелятивной связи этого показателя с такими осложнениями, как несостоятельность анастомозов, на данный момент нами не выявлено.
желудочно-кишечного тракта (несостоятельность, кровотечение) за счет их выявления и коррекции в момент операции - клипирование источника кровотечения, наложение дополнительных швов на область дефекта линии шва анастомоза при положительной пневмопробе.
Список литературы Опыт применения интраоперационной эндоскопии с целью раннего выявления и предотвращения осложнений анастомозов желудочно-кишечного тракта
- Kim KH, Kim MC, Jung GJ, Jang JS, Choi SR. Endoscopic treatment and risk factors of postoperative anastomotic bleeding after gastrectomy for gastric cancer. Int J Surg. 2012;10(10):593-7.
- Gill RS, Whitlock KA, Mohamed R, Sarkhosh K, Birch DW, Karmali S. The role of upper gastrointestinal endoscopy in treating postoperative complications in bariatric surgery. J Interv Gastroenterol. 2012 Jan;2(1):37-41.
- Manta R, Magno L, Conigliaro R, Caruso A, Bertani H, Man-no M, Zullo A, Frazzoni M, Bassotti G, Galloro G. Endoscopic repair of post-surgical gastrointestinal complications. Dig Liver Dis. 2013 Nov;45(11):879-85.
- Jafari MD, Wexner SD, Martz JE, Mdemore EC, Margolin DA, Sherwinter DA, lee SW, Senagore AJ, Phelan MJ, Stamos MJ. Perfusion assessment in laparoscopic left-sided/anterior resection (PILLAR II): a multi-institutional study. J Am Coll Surg. 2015 Jan;220(1):82-92.
- Daams F, luyer M, lange JF. Colorectal anastomotic leakage: aspects of prevention, detection and treatment. World J Gastroenterol. 2013 Apr 21; 19(15):2293-7.
- Choi DH, Hwang JK, Ko YT, Jang HJ, Shin HK, lee YC, lim CH, Jeong SK, Yang HK. Risk factors for anastomotic leakage 2(48)2016 after laparoscopic rectal resection. J Korean SocColoproctol. 2010 Aug; 26(4):265-73.
- Kawada K, Hasegawa S, Hida K, Hirai K, Okoshi K, Nomura A, Kawamura J, Nagayama S, Sakai Y. Risk factors for anastomotic leakage after laparoscopic low anterior resection with DST anastomosis. Surg Endosc. 2014 Oct; 28(10):2988-95
- van Vugt JL, Reisinger KW, Derikx JP, Boerma D, Stoot JH. Improving the outcomes in oncological colorectal surgery. world J Gastroenterol. 2014 Sep 21;20(35):12445-57.
- Kang J, Choi GS, Oh JH, Kim NK, Park JS, Kim MJ, Lee KY, Baik SH. Multicenter Analysis of Long-Term Oncologic Impact of Anastomotic Leakage After Laparoscopic Total Mesorectal Excision: The Korean Laparoscopic Colorectal Surgery Study Group. Medicine (Baltimore). 2015 Jul;94(29):e1202.
- Noble F, Curtis N, Harris S, Kelly JJ, Bailey IS, Byrne JP, Underwood TJ. Risk assessment using a novel score to predict anastomotic leak and major complications after oesophageal resection. J Gastrointest Surg. 2012 Jun;16(6):1083-95 DOI: 10.1007/s11605-012-1867-9
- Daams F, Wu Z, Lahaye MJ, Jeekel J, Lange JF. Prediction and diagnosis of colorectal anastomotic leakage: A systematic review of literature. world J Gastrointest Surg. 2014 Feb 27;6(2):14-26.
- Haddad A, Tapazoglou N, Singh K, Averbach A. Role of intraoperative esophagogastroenteroscopy in minimizing gastrojejunostomy related morbidity: experience with 2,311 laparoscopic gastric by-passes with linear stapler anastomosis. Obes Surg. 2012 Dec;22(12):1928-33.
- Mohos E, Schmaldienst E, Richter D, Prager M. Examination of the efficacy and safety of intraoperative gastroscopic testing of the gastro-jejunal anastomosis in laparoscopic Roux-Y-gastric bypass surgery. Obes Surg. 2011 Oct;21(10):1592-6.
- Cingi A, Yavuz Y. Intraoperative endoscopic assessment of the pouch and anastomosis during laparoscopic Roux-en-Y gastric bypass. 2011 Oct;21(10):1530-4.
- Shamiyeh A, Szabo K, Ulf Wayand W, Zehetner J. Intraoperative endoscopy for the assessment of circular-stapled anastomosis in laparoscopic colon surgery. Surg Laparosc Endosc Percutan Tech. 2012 Feb;22(1):65-7.
- Vicky Ka Ming li, Steven D Wexner, Nestor Pulido, Hao Wang, Hei Yin Jin, Eric G Weiss, Juan J Nogeuras, Dana R Sands. Use of routine intraoperative endoscopy in elective laparoscopic colorectal surgery: can it further avoid anastomotic failure? Surg Endosc 2009 Nov 20;23(11):2459-65.
- Kamal T, Pai A, Velchuru V, Zawadzki M, Park J, Marecik S, Abcarian H, Prasad l. Should anastomotic assessment with flexible sigmoidoscopy be routine following laparoscopic restorative left colorectal resection? Colorectal Dis. 2014 Oct 30.
- Ivanov D, Cvijanovic R, Gvozdenovic L. Intraoperative air testing of colorectal anastomoses. Srp Arh Celok Lek. 2011 May-Jun;139(5-6):333-8.
- Lieto E, Orditura M, Castellano P, Pinto M, Zamboli A, De Vita F, Pignatelli C, Galizia G. Endoscopic intraoperative anastomotic testing may avoid early gastrointestinal anastomotic complications. A prospective study. J Gastrointest Surg. 2011 Jan;15(1):145-52.
- Ishihara S, Watanabe T, Nagawa H. Intraoperative colonoscopy for stapled anastomosis in colorectal surgery. Surg Today. 2008;38(11):1063-5.
- Lanthaler M, Biebl M, Mittermair R, Ofner D, Nehoda H. Intraoperative colonoscopy for anastomosis assessment in laparoscopically assisted left-sided colon resection: is it worthwhile? J Laparoendosc Adv Surg Tech A. 2008 Feb;18(1):27-31.
- Champion JK, Hunt T, DeLisle N. Role of routine intraoperative endoscopy in laparoscopic bariatric surgery. Surg Endosc. 2002 Dec;16(12):1663-5.
- Al Hadad M, Dehni N, Elamin D, Ibrahim M, Ghabra S, Nimeri A. Intraoperative Endoscopy Decreases Postoperative Complications in Laparoscopic Roux-en-Y Gastric Bypass. Obes Surg. 2015 Feb 9.
- Alaedeen D, Madan AK, Ro CY, Khan KA, Martinez JM, Tichansky DS. Intraoperative endoscopy and leaks after laparoscopic Roux-en-Y gastric bypass. Am Surg. 2009 Jun;75(6):485-8.
- Alasfar F, Chand B. Intraoperative endoscopy for laparoscopic Roux-en-Y gastric bypass: leak test and beyond. Surg Laparosc Endosc Percutan Tech. 2010 Dec;20(6):424-7.
- Milsom JW, Pavoor RS, Shukla PJ. Evaluating the vascularity of intestinal anastomoses can narrow band imaging play a role? Med Hypotheses. 2011 Aug;77(2):290-3.
- Ris F, Hompes R, Cunningham C, Lindsey I, Guy R, Jones O, George B, Cahill RA, Mortensen NJ. near-infrared (MR) perfusion angiography in minimally invasive colorectal surgery. Surg Endosc. 2014 Jul;28(7):2221-6.


