Опыт применения резорбируемых эндопротезов для эндобилиарного стентирования при механической желтухе в эксперименте
Автор: Винник Ю.С., Маркелова Н.М., Шишацкая Е.И., Кузнецов М.Н., Василеня Е.С., Белецкий И.И., Черепанова Е.С., Соловьева Н.С.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 1 (47), 2016 года.
Бесплатный доступ
В работе представлен анализ результатов применения билиарных эндопротезов на основе полигидроксиалканоатов в эксперименте, в сравнении с силиконовым стентом. Доказана эффективность применения билиарных эндопротезов на основе полигидроксиалканоатов, способствующих избежать осложнений в раннем и позднем послеоперационном периоде.
Эндобилиарное стентирование, механическая желтуха, полигидроксиалканоаты
Короткий адрес: https://sciup.org/142211242
IDR: 142211242 | УДК: 617.58:616.13-004.6-074
Текст научной статьи Опыт применения резорбируемых эндопротезов для эндобилиарного стентирования при механической желтухе в эксперименте
Проблема эффективного лечения больных с механической желтухой остается актуальной, несмотря на впечатляющие результаты реконструктивной билиарной хирургии. Часто причиной механической желтухи является опухолевый блок, при этом число пациентов, которым можно провести радикальную операцию, не превышает 25-30%. По данным литературы 40-50% больных опухолевый блок желчеотделения локализуется в области ворот печени и захватывает близлежащие органы и крупные сосуды, что резко усложняет или делает невозможным радикальное вмешательство. В таких случаях выходом из положения становятся малоинвазивные эндобилиарные вмешательства, основным из которых является эндопротезирование желчевыводящих путей [5, 8]. Свойства эндопротеза, спо- собствующие обеспечить адекватный пассаж желчи, во многом определяют успех оперативного вмешательства. В настоящее время применяют эндобилиарные стенты, изго-толвенные из синтетических полимеров (силикон, тефлон, полиуретан, полиэтилен и перкуфлекс [1], при использовании которых могут возникать осложнения, такие как быстрая обтурация и миграция стентов, повышенная травматичность чреспеченочного вмешательства. Расширяющиеся металлические стенты более широко применяются в клинической практике, однако прорастание сетчатых стентов опухолевыми тканями, сопровождается развитием рецидива механической желтухи [3], в результате чего хирургическое удаление стента после прорастания и закупорки становится невозможным [4, 7]. В настоящее время не существует идеального материала для изготовления стентов и протезов,
соответствующего современным требованиям билиарной хирургии. В связи с этим в области синтеза полимеров поиски оптимального материала для конструирования эндоби-лиарных протезов активизировались, поскольку изучаемые в настоящее время линейные полиэфиры полигидроксиал-каноаты - биосовместимые и биодеградируемые полимеры микробного происхождения, перспективны для широкого применения в медицине, так как вызывают минимальные иммунные реакции при имплантации, возлагают большие надежды в восстановительной хирургии, в том числе для протезирования трункусных стурктур [2, 6].
Цель работы – изучение эффективности применения стентов, изготовленных из полигидроксиалканоатов, для эндобилиарного протезирования.
Материалы и методы
В данной работе использованы трубчатые стенты, изготовленные на основе полигидроксиалканоатов, различного диаметра (от 4 до 8 мм, длиной от 3 до 5 см) В эксперименте на 20 беспородных собаках изучены свойства эндобилиар-ных стентов (табл.1). Оперативное вмешательство проводилось при комнатной температуре в стерильных условиях под внутривенным наркозом. После выполнения верхнесрединной лапаротомии верифицирован холедох, произведена холедохотомия; во 2 группе стент из полигидроксиал-каноатов был имплантирован в супрадуоденальную часть холедоха и фиксирован к стенке холедоха моножильным шовным материалом из полигидроксиалканоатов. Однорядный холецистодуоденоанастомоз был наложен также мононитью из полигидроксиалканоатов. В 1 группе животным был имплантирован силиконовый стент, наложен хо-лецистодуоденоанастомоз с помощью распространенного рассасывающегося шовного материала - Викрила. Операцию заканчивали, производя контроль на гемостаз и инородные тела, рана послойно ушивалась наглухо, была наложена асептическая повязка.
За животными осуществляли наблюдение в течение 100 суток. Еженедельно проводили взвешивание и оценивали общее состояние животных. В ходе эксперимента до операции, на 7-е, 30-е, 60-е и 100-е сутки проводили общий развернутый анализ крови (анализировали содержание гемоглобина крови, цветной показатель, скорость оседания эритроцитов, форменные элементы крови). Развернутый анализ биохимических показателей крови проводили с использованием стандартных методик; определяли общий белок крови, сахар, мочевину, общий билирубин; активность амилазы крови; АЛТ, АСТ.
Фагоцитарная активность лимфоцитов, определяемая с использованием
НСТ-теста, и спонтанная и стимулированная люминолза-висимая хемилюминесценция лимфоцитов, служила показателем состояния неспецифического звена иммунитета животных.
Морфологические методы исследования тканей включали макроскопическое описание и морфометрическую характеристику препаратов тканей.
Работа выполнена за счет средств государственного задания на проведение фундаментальных исследований РАН (проект № гос. регистрации 01201351505).
Результаты и их обсуждение
Все исследуемые животные перенесли оперативное вмешательство и на протяжении всего периода наблюдения были активны, имели хороший аппетит. Во время аутопсии оценивали наличие выпота, спаечного процесса в свободной брюшной полости и подпеченочном пространстве, внешний вид холедоха в области нахождения протеза, внешний вид холецистоэнтероанастомоза, печени и двенадцатиперстной кишки.
После вскрытия просвета холедоха обращали внимание на толщину стенки холедоха, наличие видимых воспалительных изменений, состояние слизистой оболочки холедоха, прочность фиксации эндопротеза к стенке холедоха, наличие дефектов в конструкции протеза вследствие биодеградации полимера, величину просвета эндопротеза, присутствие участков сужения в результате отложения сладжа и конкрементов, толщину стенки эндопротеза. У животных группы сравнения на аутопсии патологии в брюшной полости выявлено не было.
В первой исследуемой группе у 3-х животных отмечено незначительное количество серозного выпота в брюшной полости (до 30-40 мл), в подпеченочном пространстве имел место умеренный спаечный процесс. При исследовании холедоха в области установки стента определялась инфильтрация, расширение протока, рубцовые изменения. У 2-х животных этой группы верифицирована миграция стента в область фатерова сосочка. Внешний вид холецистодуоде-ноанастомоза позволил выявить, что у 2-х животных имел
Распределение животных по сериям
Таблица 1
|
Наименование группы |
Количество животных, n |
Характеристика группы |
|
Негативный контроль – группа сравнения |
N=7 |
Интактные животные |
|
1 исследуемая группа – позитивный контроль |
N=5 |
Установка эндобилиарного стента из силикона, холецистодуоденоанастомоз |
|
2 исследуемая группа – экспериментальная |
N=8 |
Установка эндобилиарного стента из полигидрок-сиалканоатов, холецистодуоденоанастомоз |
|
Всего |
N=20 |
– |
место анастомозит – гиперемия, инфильтрация, рубцовая деформация в области анастомоза и двенадцатиперстной кишки. Печень макроскопически имела обычный вид. У 2-х животных отмечена умеренная гепатомегалия. При вскрытии просвета холедоха у всех животных стенка его была утолщена, отмечалось разрастание соединительной ткани, инфильтрация. Силиконовый стент легко был экстрагирован из просвета. Слизистая холедоха в месте контакта со стентом имела бледно-розовый цвет, отмечались участки атрофии, просвет стента у 3-х животных был сужен на 4050% от исходного вследствие отложений сладжа и компонентов желчи. Силиконовые стенты были хрупкими, на них имелись отложения солей и пигментов желчи. Холецисто-дуоденоанастомоз был обтурирован у 2-х животных этой группы. У остальных животных просвет анастомоза был достаточным, не менее 10 мм, отмечено наличие умеренного воспалительного процесса со стороны слизистой, швы, наложенные викрилом, визуализировались, были состоятельными, незначительно инфильтрированы.
После выведения животных 2 группы из эксперимента на аутопсии выпота, спаечных, рубцовых изменений в свободной брюшной полости и подпеченочном пространстве выявлено не было. Холедох в месте установки стента имел обычный вид; расширения, воспалительной реакции, рубцового процесса не визуализировалось. Все имплантированные стенты из полигидроксиалканоатов находились в месте установки, ни в одном случае миграции стента не отмечено. Холецистодуоденоанастомозы у всех животных были состоятельными, воспалительной реакции, данных за наличие анастомозита выявлено не было. Макроскопиче- ских изменений при осмотре печени и двенадцатиперстной кишки не обнаружено.
Просвет холедоха в месте установления стента у всех животных был сохранен, имел обычные размеры (0,4-0,5 мм), деформаций, стриктур, рубцовых и воспалительных изменений в зоне имплантирования стентов не отмечено. При извлечении экспериментальных стентов зафиксировано неплотное сращение со слизистой холедоха, при незначительном усилии последние были легко извлечены из просвета холедоха. Стенты сохраняли первичные физические свойства, не были подвержены процессам кальцификации, не отмечено сужения просвета стентов, диаметр их составил 3,5±0,1мм. Дефектов вследствие биодеградации не обнаружено, имело место лишь уменьшение толщины стенки стента, в среднем она составила 0,05-0,08 мм. Участков сужения просвета стентов не зафиксировано. При макроскопическом исследовании холецистодуоденоанастомозов со стороны слизистой данных за наличие воспалительных, инфильтративных и рубцовых изменений не отмечено, все анастомозы функционировали. Просвет анастомоза в среднем составил 12,3±4,3 мм. Следов шовного материала из по-лигидроксиалканоатов в месте наложения однорядного непрерывного шва анастомоза ни в одном случае обнаружено не было.
Анализ состава периферической крови в контрольной и исследуемых группах показал, что в основном эти показатели находились в пределах физиологических величин и были в границах физиологической нормы. Незначительное повышение количества лейкоцитов (от 10 до 12 х 10 9 /л) и уровня СОЭ (до 10–15 мм/ч) отмечены на 7 сутки после
Таблица 2
Показатели развернутого анализа крови животных исследуемых групп
|
Исследуемые параметры |
Группа сравнения – негативный контроль |
1 группа – позитивный контроль |
2 группа – экспериментальная |
|
Гемоглобин |
142±3,5 г/л |
137±1,9 г/л |
149±2,8 г/л |
|
Эритроциты |
5,12±1,2×1012/л |
4,89±1,5×1012/л |
5,68±0,9×1012/л |
|
Цветной показатель |
1,0±0,1 |
0,9±0,4 |
0,8±0,2 |
|
Лейкоциты |
7,2±0,9×109/л |
9,81±1,3×109/л |
7,6±1,6×109/л |
|
СОЭ |
3,2±1,6 мм/ч |
10,11±3,3 мм/ч |
4,7±2,1 мм/ч |
|
Лейкоцитарная формула |
|||
|
Палочкоядерные, % |
2,3±0,1 |
5,2±0,2 |
3,1±0,3 |
|
Сегментоядерные,% |
68,4±3,6 |
64,2±4,1 |
67,9±3,9 |
|
Моноциты, % |
2,5±0,3 |
1,1±0,2 |
3,2±0,1 |
|
Лимфоциты, % |
26,8±3,2 |
29,9±4,31 |
24,8±4,8 |
|
Эозинофилы, % |
2,1±0,1 |
1,3±0,3 |
2,2±0,2 |
|
Плазмоциты, % |
1,1±0,1 |
1,4±0,1 |
1,2±0,1 |
Примечание: 1 – различия достоверны в сравнении с контрольной группой
оперативного вмешательства во всех группах у оперированных животных относительно контроля. У животных 1 исследуемой группы к концу периода наблюдения сохранялось умеренное повышение СОЭ (до 10,1±3,3 мм/ч). Существенных изменений в лейкоцитарной формуле крови экспериментальных животных на всех сроках наблюдения также не выявили в них (табл. 2).
Анализ результатов определения мочевины, общего белка в сыворотке крови животных свидетельствует об отсутствии негативного влияния имплантированных полимерных изделий из полигидроксиалканоатов на показатели азотистого обмена и функцию почек животных. Это согласуется с ранее полученными положительными результатами исследования токсикологических свойств шовных волокон из полигидроксиалканоатов в хроническом эксперименте. У животных 1 группы с 30-х суток было зарегистрировано умеренное повышение уровня общего билирубина, которое было обусловлено нарушением оттока желчи. В этой же группе на 100-е было отмечено повышение уровня АЛТ, что свидетельствует о развитии холестаза и нарушении функции печени (табл. 3).
Активность печеночных ферментов (АЛТ и АСТ) в динамике эксперимента не выявила отклонений по АСТ. Зарегистрированное в течение первого периода наблюдений повышение активности АЛТ у экспериментальных животных может быть обусловлено как операционной травмой, так и токсическим действием препаратов для наркоза.
Результаты определения степени влияния имплантированных полимерных стентов и волокон из полигидрокси-алканоатов на показатели неспецифического иммунитета животных представлены в таблице 4.
Показатели неспецифического иммунитета у животных исследуемых групп характеризуются умеренным повышением активности, о чем свидетельствует незначительное увеличение уровня фагоцитоза и стимулированной хемилюминесценции. Однако, угнетения, снижения фагоци- тарной активности не отмечено, что свидетельствует об отсутствии длительной антигенной нагрузки и феномена «иммунологического паралича».
При морфологическом исследовании препаратов холедоха, желчного пузыря, двенадцатиперстной кишки, печени патологических изменений выявлено не было. У животных 1 исследуемой группы во всех препаратах присутствовали признаки воспалительной клеточной реакции, фиброза. Слизистая холедоха была атрофирована, с участками некрозов. В печени определялись признаки холестаза, разрушение балок, гепатоцитов. В зоне анастомозов также присутствовали признаки воспалительной клеточной реакции, множество лейкоцитов, макрофагов, грубая рубцовая ткань.
Морфологическое исследование участка холедоха животных 2 исследуемой группы, протезированного стентом из полигидроксиалканоатов, патологических изменений не выявили. Эпителий располагается на собственной пластинке слизистой, которая представлена рыхлой соединительной тканью, а вся слизистая лежит на слое гладкомышечной ткани, между которыми располагается соединительная ткань и эластические волокна (рис. 1). За мышечной оболочкой видна субсерозная оболочка (рис. 2), представленная рыхлой соединительной тканью, в которой расположены группы жировых клеток, артерии, вены, лимфатические сосуды, нервы. Серозная оболочка холедоха представлена тонким слоем мезотелия. Данная морфологическая картина укладывается в норму, что объясняется отсутствием воспалительной клеточной реакции и пролиферации любой из ткани. В гистологических препарата печени и ДПК животных 2 группы патологических изменений не выявлено.
Морфологическое исследование участка анастомоза между двенадцатиперстной кишкой и желчным пузырем (холецистодуоденоанастомоза) выявило также положительные результаты (рис. 3). На уровне анастомоза ближе
Таблица 3
Показатели биохимического анализа крови животных на 100-е сутки
|
Исследуемые параметры |
Группа сравнения – негативный контроль |
1 группа – позитивный контроль |
2 группа – экспериментальная |
|
Амилаза |
64,6±4,39 г×ч/л |
89,9±6,7 г×ч/л |
73,3±5,9 г×ч/л |
|
Общий белок |
71,9±3,2 г/л |
59±4,6 г/л |
67,6±4,8 г/л |
|
Билирубин общий |
8,8±1,8 ммоль/л |
39,91±4,3 ммоль/л |
9,1±2,0 ммоль/л |
|
сахар |
4,2±0,9 ммоль/л |
4,9±1,9 ммоль/л |
4,5±1,2 ммоль/л |
|
мочевина |
4,9±1,7 ммоль/л |
7,1±2,3 ммоль/л1 |
5,6±1,8 ммоль/л |
|
АСТ |
0,88±0,4 у.е. |
1,01±1,9 у.е. |
0,96±0,2 у.е. |
|
АЛТ |
0,84±0,7 у.е. |
2,15±3,7 у.е. 1 |
0,86±0,6 у.е. |
Примечание: 1 – различия достоверны в сравнении с контрольной группой
Таблица 4
Показатели фагоцитарной активности и люминолзависимой хемилюминесценции лимфоцитов крови животных на 100-е сутки наблюдения
|
Исследуемые параметры |
Группа сравнения – негативный контроль |
1 группа – позитивный контроль |
2 группа -экспериментальная |
|||
|
Фагоцитоз |
32±3,6 |
58±5,41 |
53±4,31 |
|||
|
Завершенный 30 мин. |
21±2,1 |
47±3,21 |
44±5,41 |
|||
|
Завершенный 90 мин. |
19±2,3 |
45±3,41 |
42±3,11 |
|||
|
Индекс завершенности |
1,02±0,25 |
1,08±0,131 |
1,05±0,25 |
|||
|
НСТ-тест |
||||||
|
Спонтанный |
413±13,2 |
434±16,8 |
426±14,2 |
|||
|
Стимулированный |
445±11,2 |
471±12,7 |
465±12,4 |
|||
|
Индекс стимуляции (Scn /Scm) |
1,06±0,32 |
1,08±0,23 |
1,09±0,31 |
|||
|
Хемилюминесценция |
Спонт. |
Спонт. |
Стимул. |
Стимул. |
Стимул. |
Стимул. |
|
t-max время выхода кривой на пик, с |
255±10,2 |
298±9,6 |
341±12,41 |
311±14,31 |
240±10,5 |
285±11,7 |
|
i-max – количество импульсов на пике |
1511±32,8 |
1487±38,9 |
3248±56,91 |
4248±45,71 |
1457±27,9 |
1329±34,1 |
|
s-max – площадь пика |
1,71±0,4×105 |
1,92±0,6×105 |
3,881±0,9×105 |
5,081±0,6×105 |
1,67±0,6×105 |
1,8±0,5×105 |
|
Индекс стимуляции (Scn /Scm) |
1,08±0,24 |
1,31±0,21 |
1,07±0,14 |
|||
Примечание: 1 – различия достоверны в сравнении с контрольной группой к подслизистому слою очагово определялась созревающая грануляционная ткань, последняя представлена сосудами ка-
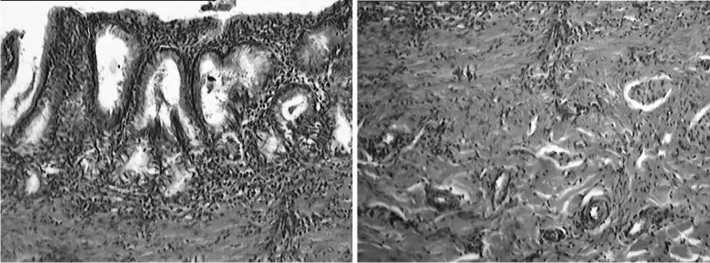
Рис. 1. Слизистый и мышечный слой холедоха в месте имплантации стента у животных 2 группы

Рис. 2. Субсерозный слой и серозная оболочка холедоха в месте имплантации стента у животных 2 группы
пиллярного типа, определяются фибробласты, эпителиальные, плазматические клетки, лимфоциты, эозинофилы и единичные
лейкоциты. Эта картина соответствует срокам формирования анастомоза (100 дней) и свидетельствует о том, что процесс регенерации находится в стадии завершения. Определяются сформированные сосуды, гладкомышечные клетки, соединительная ткань, разрезы сосудов, нервные клетки и тонкий слой мезотелия. В препарате следов шовного материала выявлено не было.
Заключение
Применение изделий из полигидрок-сиалканоатов в качестве эндобилиарных стентов в реконструктивной хирургии желчевыводящих путей является перспективным направлением, требующим дальнейшего изучения, поскольку данные изделия не вызывают патологических реакций тканей желчевыводящих путей у экспериментальных животных.
Список литературы Опыт применения резорбируемых эндопротезов для эндобилиарного стентирования при механической желтухе в эксперименте
- Ахаладзе Г.Г. Механическая желтуха и холангит. Лекции по гепатопанкреатобилиарной хирургии./Под ред. Гальперина Э.И., Дюжевой Т.Г. М.: Издательский дом Видар-М. 2011. С. 63-96.
- Волова Т.Г., Полиоксиалканоаты -биоразрушаемые полимеры для медицины/Т.Г. Волова, В.И. Севастьянов, Е.И. Шишацкая/(под ред. ак. В.И. Шумакова)//Красноярск: Платина. Рис. 3. Грануляционная ткань и зрелая фиброзная ткань в зоне холецистодуоденоанастомоза у животных 2 группы 2006. 287 с.
- Галлигнер Ю.И. Применение саморас-правляющихся металлических стентов при опухолях билиопанкреатодуоденальной зоны/Ю.И.Галингер, М.В Хрусталева., Х.И. Юсупова//Хирургия. 2010. №2.С. 12-7.
- Гальперин Э.И. Темп декомпрессии желчных протоков при механической желтухе опухолевой этиологии/Э.И. Гальперин, А.Е. Котовский,О.Н.Момунова//Хирургия. 2011. № 8.-С.33-40.
- Гусев А.В. Дренирование и эндопротезирование желчных протоков при механической желтухе/А.В. Гусев, Б.А. Балагуров, И.Н. Боровков, О.И. Коньков, Ч.Т.Мартинш, Е.Ж. Покровский и др.//Вестник новых мед. технологий. 2008. № 2. С. 97-8.
- Шишацкая Е.И. Исследование биологических свойств полиоксиалканоатов в хроническом эксперименте in vivo/Е.И.Шишацкая, Т.Г. Волова, Т.Г. Попова//ж-л Медицинская техника. 2002. № 4. С.29-32.
- Isayama Н. et al. Biliary self-expandable metallic stent for unresectable malignant distal biliary obstruction: Which is better: covered or uncovered? Digestive Endoscopy. 2013; 25 (S2): 71-4.
- Lee T.H. Technical tips and issues of biliary stenting, focusing on malignant hilar obstruction. Clinical Endoscopy. 2013: 46 (3): 260-6.


