Опыт применения видео-эндоскопических технологий в лечении гастроинтестинальных стромальных опухолей (ГИСО) желудка
Автор: Шабунин А. В., Греков Д. Н., Якомаскин В. Н., Кузьменко А. А., Эминов М. З., Султыгов А. Х., Петришин М. В.
Журнал: Московский хирургический журнал @mossj
Рубрика: Абдоминальная хирургия
Статья в выпуске: 2 (76), 2021 года.
Бесплатный доступ
Введение. Цель работы: Изучение результатов хирургического лечения гастроинтестинальных стромальных опухолей желудка с применением малоинвазивных способов леченияМатериалы и методы. Группу клинического наблюдения составили 37 больных. Мужчин было 12 (32,3%), а женщин - 25 (67,7%). Средний возраст составил 53,4±11,2 года. У 23 (12,9%) больных опухоль исходила из мышечной пластинки слизистой оболочки желудка, а у 14 - из мышечного слоя желудочной стенки. Размеры опухоли варьировали от 2 до 10 см. Подслизистая диссекция опухоли (ESD) выполнена у 10, лапароскопическая парциальная резекция желудка - у 8, а роботассистированная парциальная резекция желудка - у 19 больных.Результаты. Средняя продолжительность видеоэндоскопических операций составила 135,8±15,5 мин. При роботических вмешательствах средняя продолжительность докинга в 2017 году составила 33,2±3,4, в 2018 году - 26,4±2,2, в 2019 году - 21,7±1,6, а в 2020 году - 19,5±1,4 минут. Интраоперационное осложнение в виде перфорации стенки желудка при подслизистой диссекции опухоли отмечено в 1 (10%) случае. Осложнение в послеоперационном периоде отмечено у 1 (3,2%) пациента.Заключение: Опухоли, исходящие из мышечной пластинки слизистой оболочки без вовлечения мышечной оболочки желудка размером от 2 до 5 см подлежат эндоскопическому удалению по методике подслизистой диссекции. Для опухолей, размером более 2 см с вовлечением мышечной оболочки желудка, наиболее предпочтительным способом удаления является лапароскопическая или роботическая парциальная резекция.
Гастроинтестинальная стромальная опухоль, gist, лапароскопическая резекция желудка, роботическая резекция желудка
Короткий адрес: https://sciup.org/142230027
IDR: 142230027 | УДК: 64.617-089 | DOI: 10.17238/issn2072-3180.2021.2.5-11
An experience of video-endoscopic technologies in the treatment of gastric gastrointestinal stromal tumors (GIST)
Objective: To study the results of surgical treatment of gastrointestinal stromal tumors of the stomach using minimally invasive methods of treatment.Materials and methods: The clinical observation group consisted of 37 patients. There were 12 males (32.3%) and 25 females (67.7%). The median age was 53.4±11.2 years. In 23 (12.9%) patients, the tumor was originated from the muscle plate of the gastric mucosa, and in 14 - from the muscle layer of the gastric wall. The size of the tumor was varied from 2 to 10 cm. Submucosal tumor dissection (ESD) was performed in 10 patients, laparoscopic partial gastric resection - in 8, and robot - assisted partial gastric resection - in 19 patients.Results: The average duration of video endoscopic operations was 135.8±15.5 minutes. In robotic interventions, the average duration of docking in 2017 was 33.2±3.4, in 2018 - 26.4±2.2, in 2019 - 21.7±1.6, and in 2020 - 19.5±1.4 minutes. Intraoperative complication in the form of perforation of the gastric wall with submucosal dissection of the tumor was noted in 1 (10%) case. Complications in the postoperative period were observed in 1 (3.2%) patient.Conclusion: Tumors taking place from the muscle plate of the mucous membrane without involving the muscle membrane of the stomach with a size of 2 to 5 cm are subject to endoscopic removal by the method of submucosal dissection. For tumors larger than 2 cm with involvement of the gastric mucosa, the most preferred method of removal is laparoscopic or robotic partial resection.
Текст научной статьи Опыт применения видео-эндоскопических технологий в лечении гастроинтестинальных стромальных опухолей (ГИСО) желудка
Гастроинтестинальные стромальные опухоли (GIST, ГИСО) — мезенхимальные опухоли, исходящие из интерстициальных клеток Кахаля, ассоциированных с гладкомышечной тканью органа. Являются крайне редким видом опухолей, но при этом самым распространенным среди мезенхимальных опухолей желудочно-кишечного тракта. Частота встречаемости варьирует от 10 до 15 случаев на 1 млн населения. Ежегодно в США регистрируется 4,000–6,000 пациентов с ГИСО (данные ASCO 2019), на 1 млн населения 10–15 жителей в Германии, 19,9 жителей — в Норвегии, 14,5 — жителей в Швеции, 6,6 жителей — в Италии. Различий между заболеваемостью мужчин и женщин не выявлено.
Отделом желудочно-кишечного тракта, наиболее часто поражающимся гастроинтестинальными стромальными опухолями, является желудок (55%). Учитывая высокий риск малигнизации и возможного метастазирования, ГИСО относят к потенциально злокачественным опухолям. Однако стромальные опухоли желудка характеризуются более благоприятным прогнозом, по сравнению с ГИСО другой локализации [1].
Размер опухоли прямо пропорционален злокачественности течения и риску осложнений. Учитывая исключительную особенность онкоморфологии ГИСО, они требуют выявления конкретных геномных нарушений, которые возможно определить только при иммуно-гистохимическом исследовании (ИГХ) [2, 3]. Подобно любым мезенхимальным опухолям, ГИСО в основном метастазирует гематогенным путём, причём до 90 % метастазов образуется в печени. Возможны имплантационные метастазы по брюшине и сальнику [3].
В зависимости от степени злокачественности или наличия метастазов решается вопрос о проведении таргетной адъювантной химиотерапии ингибиторами тирозинкиназ. Их применение увеличило продолжительность жизни данных больных более чем в 3 раза [4].
Учитывая вышесказанное, для ГИСО желудка хирургическое удаление является основным и радикальным методом лечения. При этом хирургическая тактика должна следовать основному принципу онкохирургии, т.е. отсутствие опухолевых клеток в краях резекции [1, 5, 6, 7]. Несмотря на это, удаление обширных участков органа не является целесообразным, в виду нехарактерного инфильтративного роста. Для ГИСО не характерно и метастазирование в регионарные лимфатические узлы, следовательно, лимфодиссекция не будет являться этапом оперативного лечения [5‒12]. Исходя из этого, на сегодняшний день общепризнанным вариантом хирургического вмешательства при стромальных опухолях желудка является парциальная резекция [1, 7‒12].
Таким образом, изучение эффективности малоинвазивных способов лечения у больных с ГИСО, в первую очередь роботических, является актуальным.
Материал и методы исследования
Группу клинического наблюдения составили 37 больных с ГИСО желудка, оперированных в отделении хирургии № 17 ГКБ им. С.П. Боткина за 2016–2020 гг. Из них мужчин было 12 (32,4%), а женщин — 25 (67,6%). Средний возраст составил 53,4±11,2 года. Госпитализировано с желудочно-кишечным кровотечением 5 (13,5%) пациентов, у которых при ургентной ЭГДС выявлено одиночная неэпителиальная опухоль желудка (ГИСТ) с изъязвлением. У остальных 32 (86,5%) ГИСО желудка было выявлено при плановом обследовании. Из них у 21 (65,6%) — при ЭГДС (включая ЭУС), а у 11 (34,4%) больных — при СКТ.
По макроскопической форме роста экстраорганный рост опухоли отмечен у 18 (48,6%), эндоорганный — у 13 (35,1%), а смешанная форма роста — у 6 (16,3%) пациентов.
Все опухоли носили локализованный характер. Так, из 37 пациентов у 23 (62,2%) гастроинтестинальная стромальная опухоль исходила из мышечной пластинки слизистой оболочки желудка, а у 14 (37,8) больных — из мышечного слоя стенки желудка.
Размеры опухоли варьировали от 2 до 10 см: до 2 см — у 5 (13,5%); от 2 до 5 см — у 12 (32,4%), от 5 до 10 см — у 20 (54,1%) пациентов. Локализация опухоли в желудке была разнообразной: кардиальный отдел — 5 (13,5%); антральный отдел — 7 (18,9%); в теле желудка по большой кривизне — 4 (10,8%); на передней стенке — 9 (24,3%); на малой кривизне — 12 (32,5%) случаев.
Операции проведены с использованием видео-эндоскопических технологий. В зависимости от размера и локализации опухоли выполнено: 10 (27,0%) пациентам — подслизистая диссекция опухоли (ESD) по методике тоннелизации в подслизистом слое с применением гибкого эндоскопа, 8 (21,6%) пациентам — лапароскопическая парциальная резекция желудка, 19 (51,4%) пациентам — робот-ассистированная парциальная резекция желудка. В последней группе у 2-х больных выполнены симультанные операции — робот-ассистированная парциальная резекция желудка и холецистэктомия (табл. 1).
Эндоскопическое оперативное вмешательство выполняли под эндотрахеальным наркозом (рис. 1). Эндоскопом внимательно осматривалось место локализации неэпителиальной опухоли (с учётом результатов ЭУС). Затем, после инъекции 20,0 мл раствора гелофузина с раствором индигокармина в подслизистый слой в 5 см проксимальнее неэпителиальной опухоли, при помощи электроножа выполняли продольный разрез слизистой оболочки длиной не менее 2 см, достаточный для введения в подслизистый слой видеоэндоскопа с прозрачным дистальным колпачком (А). Далее эндоскоп внедряли в инъецированные ткани подслизистого слоя, где с использованием ESD-ножа, путем диссекции подслизистого слоя в режиме ENDOCUT, создавали подслизистый туннель. По мере продвижения эндоскопа в дистальном направлении периодически, по мере необходимости, вводили раствор гелофузина в подслизистый слой (Б). Затем при помощи IT-электроножа новообразование «вылущивали»
в пределах здоровых тканей практически полностью (В) и удаляли при помощи полипэктомической петли, наложенной на оставшуюся «ножку». Отсеченная опухоль извлекалась наружу вместе с эндоскопом. Заканчивали эндоскопическую операцию клипированием дефекта слизистой клипсами путем поочередного их наложения вдоль разреза (Д).
Таблица 1
Виды оперативных вмешательств в зависимости от размеров опухоли у больных с ГИСО желудка
|
Размер опухоли |
Количество пациентов |
Лапароскопическая парциальная резекция |
Робот-ассистированная парциальная резекция |
Эндоскопическая подслизистая диссекция (ESD) |
|
<2 см |
5 |
1 |
- |
4 |
|
>2≤5 см |
12 |
2 |
4 |
6 |
|
>5≤10 см |
20 |
5 |
15 |
- |
|
Всего |
37 |
8 |
19 |
10 |
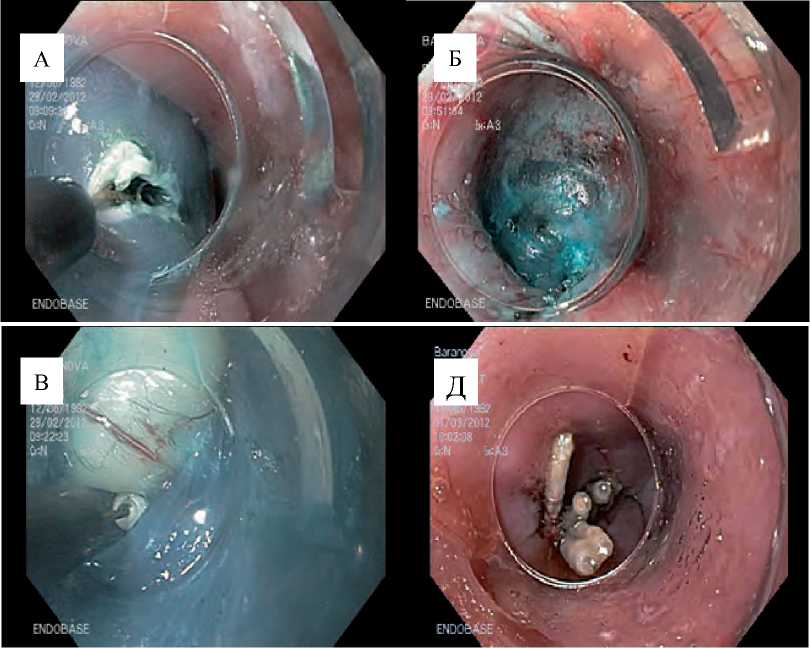
Рис. 1. Этапы эндоскопического оперативного вмешательства
Операционный материал во всех случаях отправлялся на обязательное морфологическое и иммуно-гистохимическое исследование.
Оценка ближайших результатов лечения проводилась на основании таких общепризнанных критериев, как: длительность оперативного вмешательства, процент осложнений, послеоперационный койко-день. Отдаленные результаты лечения и выживаемость больных в нашем исследовании не оценивалась.
Результаты
Средняя продолжительность видео-эндоскопических операций составила 135,8±15,5 мин. Максимальная продолжительность операции составила 220 мин. при робот-ассистирован-ной парциальной резекции у пациента с ГИСО с экзофитной формой роста размером 10 см в диаметре расположенной по малой кривизне и задней стенке желудка. Минимальная про- должительность операции — 54 мин. — лапароскопическая парциальная резекция желудка.
В послеоперационном периоде в 1 (3,2%) случае отмечено ТЭЛА низкого риска (сегментарные и субсегментарные ветви легочной артерии справа и субсегментарные ветви легочной артерии слева), 4а степень по Clavien‒Dindo после лапароскопической парциальной резекции желудка. В остальных случаях осложнений послеоперационного периода не отмечено.
Послеоперационный койко-день при эндоскопической подслизистой диссекции составил (ESD) составил 2,4±1,1 суток, после лапароскопической парциальной резекции желудка — 4,2±2,1 суток, после робот-ассистированной парциальной резекции желудка — 3,3±1,3 дня.
Кровопотеря во всех вариантах оперативного вмешательства была минимальной.
При ИГХ веретеноклеточный вариант выявлен у 26 (70,3%), эпителиоидно-клеточный вариант — у 7 (18,9%), а смешанноклеточный тип — у 4 (10,8%) больных.
Сравнительная оценка экспрессии различных иммунофенотипов в группе исследования по данным ИГХ представлена в таблице 2.
Таблица 2
Экспрессия иммуннофенотипов по данным ИГХ
|
Количество больных |
CD117 |
DOG1 |
CD34 |
|
3 |
+ |
||
|
7 |
+ |
||
|
9 |
+ |
+ |
|
|
6 |
+ |
+ |
|
|
2 |
+ |
+ |
|
|
10 |
+ |
+ |
+ |
Митотический индекс (МИ) согласно данным ИГХ составил: МИ < 5% — у 34 больных (91,9%); МИ > 5 < 10% — у 1 (2,7%) больного, а МИ >10% — у 2 (5,4%) больных. Индекс пролиферации по экспрессии Ki-67 составил менее 10% — у 32 (86,5%), а более 10% — у 5 (13,5%) пациентов.
Вероятность прогрессирования в группе исследования оценивалась согласно классификации прогностических групп WHO 2013 и AFIP. Из них 6 (16,2%) пациентов отнесены к прогностической группе 1, с вероятностью прогрессирования 0%; 13 (35,1%) — к прогностической группе 2, c вероятностью прогрессирования 1,9%; 16 (43,3%) — к прогностической группе 3а, с вероятность прогрессирования 3,6%; а 2 (5,4%) пациента — к прогностической группе 4b, с вероятностью прогрессирования 86%.
Риск рецидива оценивался по классификации прогностических групп гастроинтестинальных стромальных опухолей по H. Joensuu 2008. Очень низкий риск рецидива выявлен у 5 (13,5%), низкий риск рецидива — у 28 (75,7%), промежуточный риск — у 2 (5,4%), высокий риск рецидива — у 2 (5,4%) больных.
В послеоперационном периоде 2 (5,4%) больных с МИ>10% (прогностической группы 4b) направлены для проведения адъювантной таргетной химиотерапии.
Обсуждение
В последние годы в литературе все чаще появляются публикации о применении малоинвазивных технологий в хирургическом лечении ГИСО желудка и других локализаций.
Одним из инновационных направлений хирургического лечения неэпителиальных опухолей пищевода и желудка является методика эндоскопической резекции опухоли подслизистым доступом (ESD). Впервые данный способ применили в клинической практике H. Inoue и соавт., обосновав его эффективность и безопасность у данной категории больных. Данная методика рекомендована именно для удаления небольших (диаметром не более 4 см, а для первых вмешательств — не более 1–2 см) образований.
При определении показаний к эндоскопической резекции опухоли подслизистым доступом мы в первую очередь основывались на результатах ЭУС. Данная методика исследования в сочетании с тонкоигольной пункцией позволяет определить не только топографию опухоли, но и оценить ее злокачественный потенциал. Тонкоигольная биопсия нами была выполнена у 23 (62,1%) при опухолях размерами более 2-х см. Кроме того, обсуждая показания к эндоскопическому лечению, мы принимали во внимание скрытый потенциал злокачественного перерождения гастроинтестинальных стромальных опухолей малых размеров.
Итраоперационное осложнение в виде перфорации стенки желудка при эндоскопической резекции опухоли подслизистым доступом нами отмечено в 1 (10%) случае. При дооперационной диагностике неэпителиальных образований желудочно-кишечного тракта не всегда можно определить, из какого слоя стенки органа исходит опухоль. Так, опухоль, находясь в подслизистом слое, может тонкой «ножкой» связываться с более глубокими слоями стенки полого органа, как это и оказалось впоследствии у одного больного, что при выделении опухоли привело к образованию дефекта стенки желудка около 3 мм. Дефект слизистой стенки желудка в зоне удаления опухоли был успешно клипирован 5 клипсами. На следующие сутки после операции были выполнены контрастное исследование желудка с жидким контрастным веществом и контрольная гастроскопия для оценки герметичности клипс, наложенных на дефект слизистой желудка в зоне удаленной опухоли. Послеоперационный период протекал без осложнений, пациентка на 7 -е сутки выписана домой в удовлетворительном состоянии.
Лапароскопическая парциальная резекция желудка нами выполнена у 8 (21,6%) пациентов. Во всех случаях использовался линейный сшивающий аппарат. Робот-ассистированная парциальная резекция желудка выполнена у 19 (51,4%) пациентов. Их них у 2-х больных выполнены симультанные операции
— робот-ассистирвонная парциальная резекция желудка и холецистэктомия. У 6 пациентов резекция выполнялась с использованием сшивающего аппарата, а у 13 больных дефект желудка ушит интракорпоральным двухрядным швом.
По мнению ряда авторов, малоинвазивные способы с применением эндо-видео-хирургических технологий предпочтительны для стромальных опухолей желудка размером до 10 см. Во избежание повреждения капсулы образования, что сопровождается диссеминацией опухолевых клеток по брюшной полости и развитием отдаленных рецидивов, для опухолей больших размеров рекомендуется традиционный доступ [5, 6]. Робот-ассистированная хирургическая система способствует лучшей экспозиции во время операции, по сравнению с лапароскопическим методом, что значительно снижает вероятность интраоперационного повреждения капсулы [13].
По результатам нашей работы с 2016 по 2020 год (табл. 3) наблюдается тенденция к переходу от лапароскопических операций к робот-ассистированным. Данная технология в большинстве случаев позволяет выполнить парциальную резекцию желудка без использования сшивающих аппаратов, что экономически выгодно. Это обусловлено, в первую очередь, большей функциональной возможностью инструментов, что значительно облегчает и ускоряет этап наложения интракорпорального шва на дефект стенки желудка после удаления опухоли, особенно при трудной локализации (малая кривизна, задняя стенка).
Нами было отмечено уменьшение времени докинга роботической системы Da Vinci с возрастанием опыта применения. Средняя продолжительность докинга в 2017 году составила 33,2±3,4 мин., в 2018 году – 26,4±2,2 мин., в 2019 году — 21,7±1,6 мин., а в 2020 году — 19,5±1,4 (р>0,05). Послеоперационный койко-день при робот-ассистированной и лапароскопической парциальной резекции желудка статистически значимо не отличались (р>0,05).
Таблица 3
Малоинвазивные методы хирургического лечения в период с2016 по 2020 гг.
|
Год |
Количество пациентов |
Лапароскопическая парциальная резекция |
Робот-асси-стированная парциальная резекция |
Эндоскопи-чес кая подслизистая диссекция (ESD) |
|
2016 |
3 |
3 |
- |
- |
|
2017 |
6 |
3 |
1 |
2 |
|
2018 |
12 |
1 |
6 |
5 |
|
2019 |
10 |
- |
8 |
2 |
|
2020 |
6 |
- |
5 |
1 |
|
Всего |
37 |
7 |
20 |
10 |
Анализ выполненных оперативных вмешательств позволяет нам обосновать выбор малоинвазивного способа хирургического лечения ГИСО желудка в зависимости от размеров опухоли и степени их инвазии. Так как опухоли, исходящие из мышечной пластики слизистой оболочки желудка без вовлечения мышечной оболочки размером от 2 до 5 см, и все опухоли размером до 2 см подлежат эндоскопическому удалению по методике тоннелизации в подслизистом слое (ESD). Для опухолей, размером от 2 до 5 см с вовлечением в патологический процесс мышечной оболочки желудочной стенки, а также опухоли размером от 5 до 10 см наиболее предпочтительным методом удаления является лапароскопическая или роботическая парциальная резекция.
Заключение
Эндоскопическая резекция подслизистым доступом является эффективным, малотравматичным и безопасным видом вмешательства у больных с ГИСО небольших размеров, исходящих из мышечной пластинки слизистой оболочки желудка.
Применение видео-эндоскопических технологий в лечении ГИСО желудка в настоящее время следует рассматривать как безопасную альтернативу традиционным хирургическим вмешательствам, поскольку они соизмеримы по своему объему и радикализму. Кроме того, современные видео-эндоскопические операции позволяют значительно уменьшить травматизацию тканей, минимизировать кровопотерю во время операции, сократить частоту развития послеоперационных осложнений и способствуют более ранней реабилитации пациентов, что в целом приводит к улучшению результатов хирургического лечения.
Список литературы Опыт применения видео-эндоскопических технологий в лечении гастроинтестинальных стромальных опухолей (ГИСО) желудка
- Saafan T. Gastric GIST. Gastric Cancer — An Update [Internet]. IntechOpen, 2019, Mar No. 20. http://dx.doi.org/10.5772/intechopen.77297
- Архири П.П., Стилиди И.С., Поддубная И.В., Неред С.Н., Никулин М.П., Бохян В.Ю. и др. Эффективность хирургического лечения больных с локализованными стромальными опухолями желудочно-кишечного тракта. Российский онкологический журнал, 2016. № 21(5). С. 233–237. https://doi.org/10.18821/1028-9984-2016-21-5-233-237
- Богомолов Н.И., Пахольчук П.П., Томских Н.Н., Гончаров А.Г., Гончарова М.А., Голякова А.С. Стромальные опухоли желудочно-кишечного тракта (ГИСО): опыт диагностики и лечения. Acta Biomedica Scientifica (East Siberian Biomedical Journal), 2017. № 2(6). С. 52–58. https://doi.org/10.12737/article_5a0a856cd0a467.14225823
- Christopher L. Corless and Michael C. Heinrich. Molecular Pathobiology of Gastrointestinal Stromal Sarcomas. Annual Review of Pathology: Mechanisms of Disease, 2008, No. 3, рр. 557–586. https://doi.org/10.1146/annurev.pathmechdis.3.121806.151538
- Casali P.G., Abecassis N., Aro H.T., Bauer S., Biagini R., Bielack S., Bonvalot S., Boukovinas I., Bovee JVMG, Brodowicz T., Broto J.M., Buonadonna A., De Álava E., Dei Tos A.P., Del Muro X.G., Dileo P., Eriksson M., Fedenko A., Ferraresi V., Ferrari A., Ferrari S., Frezza A.M., Gasperoni S., Gelderblom H., Gil T., Grignani G., Gronchi A., Haas R.L., Hassan B., Hohenberger P., Issels R., Joensuu H., Jones R.L., Judson I., Jutte P., Kaal S., Kasper B., Kopeckova K., Krákorová D.A., Le Cesne A., Lugowska I., Merimsky O., Montemurro M., Pantaleo M.A., Piana R., Picci P., Piperno-Neumann S., Pousa A.L., Reichardt P., Robinson M.H., Rutkowski P., Safwat A.A., Schöffski P., Sleijfer S., Stacchiotti S., Sundby Hall K., Unk M., Van Coevorden F., van der Graaf W.T.A., Whelan J., Wardelmann E., Zaikova O., Blay J.Y.; ESMO Guidelines Committee and EURACAN. Gastrointestinal stromal tumours: ESMO-EURACAN Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann. Oncol., 2018, Oct., No. 1, 29 (Suppl 4), рр. 68–78. https://doi.org/ 10.1093/annonc/mdy095
- Demetri G.D., Benjamin R.S., Blanke C.D., Blay J.Y., Casali P., Choi H., Corless C.L., Debiec-Rychter M., DeMatteo R.P., Ettinger D.S., Fisher G.A., Fletcher C.D., Gronchi A., Hohenberger P., Hughes M., Joensuu H., Judson I., Le Cesne A., Maki R.G., Morse M., Pappo A.S., Pisters P.W., Raut C.P, Reichardt P., Tyler D.S., Van den Abbeele A.D., von Mehren M., Wayne .JD., Zalcberg J. NCCN Task Force. NCCN Task Force report: management of patients with gastrointestinal stromal tumor (GIST) — update of the NCCN clinical practice guidelines. J. Natl. Compr. Canc. Netw., 2007, Jul, No. 5, Suppl 2, рр. 1–29.
- Nguyen S.Q., Divino C.M., Wang J.L. et al. Laparoscopic management of gastrointestinal stromal tumors. Surg. Endosc., 2006, No. 20, рр. 713–716. https://doi.org/10.1007/s00464-005-0435-8
- Hirokazu Kiyozaki, Masaaki Saito, Hirofumi Chiba, Osamu Takata, Toshiki Rikiyama. Laparoscopic wedge resection of the stomach for gastrointestinal stromal tumor (GIST): non-touch lesion lifting method. Gastric Cancer, 2014, No. 17, рр. 337–340 https://doi.org/10.1007/s10120-013-0272-8
- Novitsky Y.W., Kercher K.W., Sing R.F., Heniford B.T. Long-term outcomes of laparoscopic resection of gastric gastrointestinal stromal tumors. Ann Surg., 2006, Jun., No. 243(6), рр. 738–747. https://doi.org/10.1097/01.sla.0000219739.11758.27
- Nishimura, J., Nakajima, K., Omori, T., Takahashi, T., Nishitani, A., Ito, T. and Nishida, T. (2007) Surgical Strategy for Gastric Gastrointestinal Stromal Tumors: Laparoscopic vs. Open Resection. Surgical Endoscopy, 2007, No. 21, рр. 875–878. https://doi.org/10.1007/s00464-006-9065-z
- Tao K.X., Wan W.Z., Chen J.H., Yang W.C., Cai M., Shuai X.M., Cai K.L., Gao J.B., Wang G.B., Zhang P. [Laparoscopic versus open surgery for gastric gastrointestinal stromal tumors in unfavorable location: a propensity score-matching analysis]. Zhonghua Wai Ke Za Zhi., 2019, Aug., No. 1; 57(8), рр. 585–590. Chinese. https://doi.org/10.3760/cma.j.is sn.0529-5815.2019.08.005
- Ortenzi M., Ghiselli R., Cardinali L., Guerrieri M. Surgical treatment of gastric stromal tumors: laparoscopic versus open approach. Ann. Ital. Chir., 2017, No. 88, S0003469X17026112.
- Shi F., Li Y., Pan Y., Sun Q., Wang G., Yu T., Shi C., Li Y., Xia H., She J. Clinical feasibility and safety of third space robotic and endoscopic cooperative surgery for gastric gastrointestinal stromal tumors dissection: A new surgical technique for treating gastric GISTs. Surg. Endosc., 2019, Dec., No. 33(12), рр. 4192–4200. https://doi.org/ 10.1007/s00464-019-07223-w


