Опыт транскатетерной имплантации биопротезов аортального клапана Corevalve в Клинике высоких медицинских технологий имени Н.И. Пирогова Санкт-Петербургского государственного университета
Автор: Васильев А.С., Шматов Д.В., Столяров М.С., Сорокин А.А., Иванов Д.В., Новиков М.А., Зырянова А.В., Михальчикова Н.А.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 3 т.34, 2019 года.
Бесплатный доступ
Введение. С каждым годом количество операций транскатетерного протезирования аортального клапана увеличивается, как увеличивается и число центров, выполняющих данное вмешательство. В данной статье представлены результаты операций транскатетерного протезирования аортального клапана в Клинике высоких медицинских технологий имени Н.И. Пирогова Санкт-Петербургского государственного университета.Материал и методы. С декабря 2015 г. по декабрь 2018 г. в Клинике имплантировано 46 самораскрывающихся транскатетерных клапанов двух поколений - CoreValve и CoreValve Evolute R. Все операции проведены пациентам высокого и крайне высокого хирургического риска по поводу выраженного аортального стеноза. Решение о выполнении TAVI принималось коллегиально в составе «сердечной команды».Результаты. Большинство операций выполнялось под общим наркозом с искусственной вентиляцией легких (ИВЛ) трансфеморально (89%). В двух случаях (4,3%) потребовалась конверсия транскатетерной операции в открытую кардиохирургическую в связи с развитием интраоперационных осложнений. Госпитальная летальность составила 6,5%, нелетальные осложнения - 21,7%. В настоящее время получены среднесрочные результаты использования клапанов CoreValve. Функциональный класс сердечной недостаточности пациентов оценивается не выше II (по NYHA), период наблюдения составляет от 6 мес. до 2,5 лет, гемодинамические показатели функционирования клапана удовлетворительные. Ожидается получение среднесрочных результатов применения клапанов 2-й генерации - CoreValve Evolute R.Выводы. Процедура TAVI у пациентов крайне высокого и высокого хирургического риска является альтернативой открытому протезированию аортального клапана в условиях искусственного кровообращения (ИК), показывает не худшие (non-inferiority) ранние и среднесрочные результаты, при этом протокол курации пациентов с интраоперационной аортальной недостаточностью 2-й степени требует дальнейшего совершенствования. Планируется проведение дальнейшего исследования с целью получения отдаленных результатов оперативного лечения.
Транскатетерное протезирование аортального клапана, аортальный стеноз, "сердечная команда"
Короткий адрес: https://sciup.org/149125315
IDR: 149125315 | УДК: 616.126.52-77-089.819.1-089.819.843 | DOI: 10.29001/2073-8552-2019-34-3-153-160
Experience of transcatheter implantation of Corevalve aortic valve bioprostheses in Clinic of advanced medical technologies named after Nikolay I. Pirogov
Background. Every year the number of operations of transcatheter aortic valve implantation increases, and the number of centers performing this intervention increases too. In this article we present the results of the operation of transcatheter aortic valve implantation at the Clinic of Advanced Medical Technologies named after Nikolay I. Pirogov St. Petersburg State University.Material and Methods. From December 2015 to December 2018, the specialists of the Clinic implanted 46 self-expanding transcatheter aortic valves of 2 generations - CoreValve and CoreValve Evolute R. All patients were patients of high and extremely high surgical risk for severe aortic stenosis. The decision on the implementation of TAVI was taken collectively as part of the “Heart Team”.Results. Most operations were performed under general anesthesia with transfemoral access (89%). In 2 cases (4.3%) the conversion of transcatheter surgery into an open cardiac surgery was required due to the development of intraoperative complications. Hospital mortality was 6.5%, non-fatal complications were 21.7%. Now we have mid-term results of CoreValve valves implantation. The functional class of heart failure is estimated to be no higher than II (by NYHA), the observation period is from 6 months to 2.5 years, and the hemodynamic parameters of the valve are satisfactory. Medterm results from the use of CoreValve Evolute R are expected.Conclusion. The TAVI procedure in patients of high and extremely high surgical risk is an alternative to open operation, showing not-worse (non-inferiority) early and medium-term results. Treatment of patients with intraoperative aortic insufficiency of the 2nd degree requires further improvement. Further research is planned with a view to obtaining long-term TAVI results.
Текст научной статьи Опыт транскатетерной имплантации биопротезов аортального клапана Corevalve в Клинике высоких медицинских технологий имени Н.И. Пирогова Санкт-Петербургского государственного университета
О постепенном демографическом старении населении известно с начала ХХ в. Так, доля пожилых людей в России выросла с 6,7% в 1939 г. до 11,9% в 1970 г., достигла 18,7% в 2001 г. и продолжает расти [1]. В сфере медицины это приводит к росту пациентов, имеющих болезни, характерные для пожилого возраста [2]. Одной из таких болезней является стеноз аортального клапана, встречаемость которого в популяции увеличивается с возрастом [3]. Наиболее частой причиной формиро- вания стеноза является процесс дегенерации соединительной ткани, такие причины, как врожденная патология (двухстворчатый аортальный клапан) и хроническая ревматическая болезнь сердца, встречаются реже [4]. Аортальный стеноз является заболеванием, имеющим неуклонно прогрессирующее течение, при появлении симптомов продолжительность жизни пациента измеряется несколькими годами [5]. Оперативное лечение патологии в виде протезирования аортального клапана механическим или биологическим протезами у пациентов низкого и среднего хирургического риска демонстрирует удовлетворительные операционные, средне- и дальнесрочные результаты. При этом результаты открытого оперативного лечения у пациентов группы высокого хирургического риска остаются сомнительными – уровень периоперационной летальности, по данным некоторых авторов, достигает 15% [6]. Именно этим можно объяснить тот факт, что ~30% пациентов ежегодно отказывают в протезировании аортального клапана в условиях искусственного кровообращения (ИК) [7].
Высокая встречаемость патологии и неудовлетворительные результаты открытой хирургии послужили стимулом к развитию альтернативных методов лечения аортального стеноза. В 2002 г. французские специалисты во главе с A. Cribier выполнили первую операцию транскатетерной замены аортального клапана у терминального пациента с отмеченной в послеоперационном периоде стабилизацией состояния пациента. Успех послужил толчком к развитию методики транскатетерной имплантации аортального клапана (Transcatheter Aortic Valve Implantation – TAVI). В настоящее время в клинической практике наиболее широко распространены два варианта клапанов для TAVI – баллонорасширяемый протез Sapien (Edwards Lifesciences Inc., США) и саморасширяющийся CoreValve (Medtronic CoreValve Inc., США). У обеих медицинских компаний проведены многоцентровые рандомизированные исследования, подтверждающие эффективность имплантации данных устройств в позицию аортального клапана при аортальном стенозе у пациентов высокого операционного риска (STS≥8%): исследование PARTNER, проведенное Edwards Lifesciences Inc., включавшее 1057 пациентов, показало двухлетние результаты, которые были не хуже, чем при открытой хирургии [8]; исследование Medtronic CoreValve U.S. PivotalTrial, проведенное компанией Medtronic, включало в себя 795 пациентов и в течение первого года показало снижение смертности от всех причин в сравнении с группой открытой хирургии [9].
С 2002 г. в Европе и США были имплантированы десятки тысяч эндоваскулярных аортальных клапанов, что нашло отражение в рекомендациях: ACCF/AATS/SCAI/STS Expert Consensus Document on Transcatheter Aortic Valve Replacement, 2012 и ACC Expert Consensus Decision Pathway for Transcatheter Aortic Valve Replacement in the Management of Adults with Aortic Stenosis, 2017:
– TAVI рекомендуется пациентам с тяжелым, симп-томным, кальцинированным стенозом трехстворчатого аортального клапана, подходящей для TAVI анатомией, прогнозируемой продолжительностью жизни более 12 мес., с чрезмерным хирургическим риском, определяемым такими факторами, как «хрупкость», предшествующая лучевая терапия, фарфоровая аорта, тяжелая сопутствующая патология.
– TAVI является разумной альтернативой хирургическому открытому вмешательству у пациентов с высоким хирургическим риском (критерии STS score ≥8%) и средним хирургическим риском (критерии STS score 4–8%).
В Российской Федерации длительное время метод TAVI ограничивался финансовыми причинами, однако с 2015 г. в принятом Правительством РФ Постановлении [10] операция TAVI выделена в отдельный метод лечения патологии аортального клапана. В перспективе это должно способствовать росту числа ежегодно выполняемых операций, увеличению доступности данного вида лечения для населения.
Материал и методы
В Центре кардиохирургии и интервенционной кардиологии Клиники высоких медицинских технологий имени Н.И. Пирогова Санкт-Петербургского государственного университета с декабря 2015 г. по декабрь 2018 г. выполнено 46 операций транскатетерной имплантации аортального клапана (TAVI).
Цель данного ретроспективного исследования: анализ операционных, ранних и среднесрочных результатов.
До 2018 г. в Центре использовались клапаны 1-й генерации – CoreValve, с января 2018 г. – клапаны 2-й генерации – CoreValve Evolute R. Всего было прооперировано 46 человек, в том числе 32 женщины (69,5%) и 14 мужчин (30,5%). Возраст, исходный функциональный класс сердечной недостаточности (по NYHA) и данные эхокардиографии представлены на рисунках 1, 2, в таблице 1, при этом средний возраст пациентов равен 76,3 ± 16,3 года.
Таблица 1. Предоперационные данные эхокардиографии
Table 1. Preoperative echocardiographiс characteristics of patients
|
Показатели |
Среднее |
|
Parameters |
значение |
|
Mean value |
|
|
Пиковый градиент на аортальном клапане, |
82,3 |
|
мм рт. ст. Peak gradient, mm Hg |
(52–93) |
|
Средний градиент на аортальном клапане, |
49,7 |
|
мм рт. ст. Mean gradient, mm Hg |
(39–53.) |
|
Площадь отверстия аортального клапана, см² |
0,7 |
|
Orifice area, сm2 |
(0,4–0,9) |
|
Трансклапанная скорость потока, м/с |
4,4 |
|
Flow rate, m/s |
(3,8–5,2) |
|
Соотношение КДО/КСО, мл |
90/38 |
|
EDV/ESV, ml |
(72–145/16–56 ) |
|
Фракция выброса по Симпсону, % |
62,7 |
|
Left ventricular ejection fraction, % |
(20–72) |
|
Толщина МЖП, мм |
15,2 |
|
IVS thickness, mm |
(14–21) |
|
Толщина ЗС ЛЖ, мм |
14,3 |
|
RW thickness, mm |
(12–18) |
Примечание: КДО – конечно-диастолический объем левого желудочка, КСО – конечно-систолический объем левого желудочка, МЖП – межжелудочковая перегородка, ЗС ЛЖ – задняя стенка левого желудочка.
Note: EDV – left ventricular end diastolic volume, ESV – left ventricular end systolic volume, IVS – interventricular septum, PW – posterior wall of the left ventricle.
Частота встречаемости сопутствующей и фоновой патологии у данной группы пациентов представлена в таблице 2.
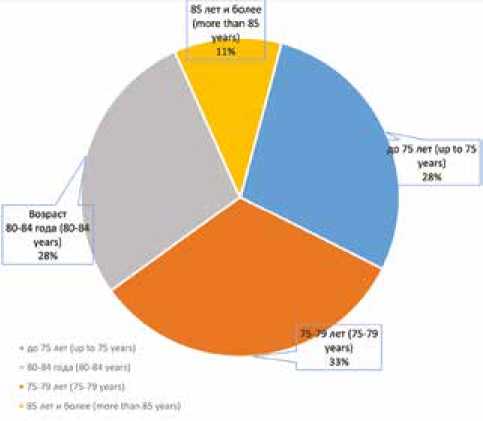
Рис. 1. Возрастные группы пациентов
Fig. 1. Patient age groups
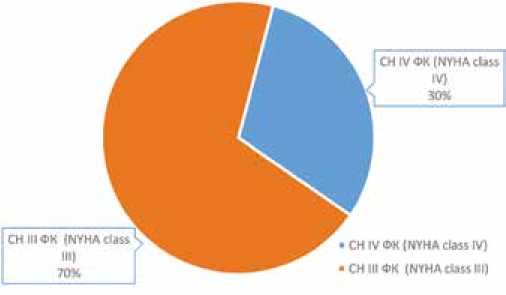
Рис. 2. Распределение пациентов по функциональному классу сердечной недостаточности (ФК по NYHA)
Fig. 2. Patient groups by the functional class of heart failure (NYHA)
Таблица 2. Основные характеристики пациентов
Table 2. Baseline characteristics of patients
|
Показатели Parameters |
Частота встречаемости, % Frequency, % |
|
Острый инфаркт миокарда Acute myocardial infarction |
19,6 |
|
Стентирование коронарных артерий PTCA |
46 |
|
Операция коронарного шунтирования CABG |
6,5 |
|
Имплантация постоянного электрокардиостимулятора Permanent pacemaker implantation |
8,6 |
|
Острое нарушение мозгового кровообращения Acute stroke |
8,6 |
|
Сахарный диабет 2-го типа Diabetes mellitus 2 type |
17,4 |
|
Хроническая болезнь почек 3Б-5-й стадии Chronic kidney disease |
13,0 |
|
Хроническая обструктивная болезнь легких III стадии Chronic obstructive pulmonary disease |
8,7 |
Острый инфаркт миокарда (19,6% пациентов) переносился пациентами в сроки от 1,5 до 12 лет до транскатетерной имплантации аортального клапана. При этом 32,6% пациентов не имели значимой сопутствующей патологии, высокие хирургические риски объяснялись возрастом пациентов, общей «хрупкостью» (frailty), наличием фарфоровой аорты.
Всем пациентам в ходе предоперационного обследования, помимо общеклинического минимума, были выполнены коронарография с последующей реваскуляризацией миокарда, трансторакальная эхокардиография с чреспищеводной эхокардиографией, мультиспиральная компьютерная томография сердца, аорты и подвздошно-бедренного сегмента.
Результаты
Большая часть операций проводилась под общим наркозом с искусственной вентиляцией легких – ИВЛ (93,4%), только три операции выполнены под местной анестезией в области сосудистого доступа и в/в седацией. Средняя продолжительность операции первые 2 года составляла 125 мин, с 2018 г. отмечается уменьшение времени до 90 мин, что связано в большей мере с накоплением опыта, чем с переходом с CoreValve на новую систему CoreValve Evolute R. При этом длительность непосредственно самой имплантации клапана 2-й генерации незначительно увеличилась за счет использования возможности репозиционирования клапана (в 40% случаев). Трансфеморально с применением пункционного доступа к бедренной артерии (устройства для ушивания – Prostar и Perclose Proglide) было выполнено 33 операции (71,7%), 11 операций (23,9%) проведены с использованием открытого сосудистого доступа к бедренной артерии (с 2018 г. 100% операций выполняются пункционно). Пункционный доступ к артерии осуществлялся под ангиографическим контролем с применением функции road-map и обязательным ангиографическим контролем места пункции после ушивания. Альтернативные доступы использовались два раза: одна операция была выполнена из стернального мини-J доступа трансаортально (2,17%) по причине извитых кальцинированных подвздошных артерий, одна операция проведена с применением открытого сосудистого доступа к левой подключичной артерии в 3-м сегменте (2,17%) по причине стенозированных, извитых и кальцинированных подвздошных артерий, ранее выполненной операции коронарного шунтирования.
Всего было имплантировано 26 клапанов CoreValve (56,5%): восемь клапанов – № 26, 14 клапанов – № 29 и четыре клапана – № 31; 20 клапанов CoreValve Evolute R (43,5%): пять клапанов – № 26, 11 клапанов – № 29 и четыре клапана – № 34.
Общая летальность составила 6,5% (три пациента): один (2,2%) пациент скончался от геморрагического шока, вызванного патологией системы гемостаза, при трансаортальном доступе; два (4,3%) пациента – от по-лиорганной недостаточности после конверсии TAVI в открытое кардиохирургическое вмешательство. Причиной конверсии у первого пациента явилась окклюзия ствола левой коронарной артерии (ЛКА) левой коронарной створкой и безуспешность эндоваскулярной коррекции данного осложнения: выполнена экстренная операция коронарного шунтирования; во втором случае – перфорация верхушки левого желудочка сверхжестким проводником (не preshaped tip) с последующим ушиванием дефекта и протезированием аортального клапана.
Нелетальные осложнения составили 21,7% (10 пациентов). У одного пациента (2,2%) возникла перфорация правого желудочка электродом временной эндокардиальной стимуляции (ВЭКС), потребовавшая стернотомии и ушивания перфорационного отверстия. У двух пациентов (4,3%) развилась полная АВ-блокада, потребовавшая имплантации двухкамерного постоянного электрокардиостимулятора – ЭКС (оба случая блокады произошли после имплантации клапана CoreValve Evolute R, в одном случае – № 29, в другом – № 34). В двух случаях (4,3%) при пункционном доступе возник тромбоз общей бедренной артерии, что потребовало ревизии и пластики артерий.
Все плановые операции завершены с незначительной аортальной недостаточностью, вызванной пара-вальвулярными ликами: в 86% операций (37 пациентов) имела место аортальная недостаточность 1-й степени, в 14% операций (6 пациентов) – аортальная недостаточность 2-й степени, причиной являлся массивный эксцентричный кальциноз клапана. Постдилатация применялась в 65% случаев (30 пациентов), и частота применения постдилатации не зависела от типа использованного клапана.
В 2018 г. возможность интраоперационного репозиционирования частично раскрытого протеза CoreValve Evolute R была использована в восьми случаях (40%).
В настоящее время получены среднесрочные результаты применения клапанов CoreValve: из 23 пациентов с имплантированным CoreValve, прооперированных с 2015 до 2018 г. и выписанных из стационара, имеется информация о 20 пациентах (87%); с тремя пациентами потеряна связь. Из 20 пациентов один умер вследствие острого нарушения мозгового кровообращения (ОНМК) через 13 мес. после операции, оставшиеся 19 пациентов находятся в удовлетворительном состоянии, функциональный класс сердечной недостаточности оценивается не выше II (по NYHA; период наблюдения составляет от 6 мес. до 2,5 лет). По данным контрольных эхокардиографий, через 6 мес. у данных 19 пациентов (73% от прооперированных с 2015 до 2018 гг.) не выявлено признаков тяжелого/умеренного аортального стеноза. Показатели функционирования клапана остаются стабильными, степень аортальной недостаточности также не увеличивалась по сравнению с послеоперационной в стационаре (табл. 3, рис. 3).
Ожидается получение среднесрочных результатов применения клапанов 2-й генерации – CoreValve Evolute R.
Таблица 3. Послеоперационные данные эхокардиографии (период наблюдения 6 мес.)
Table 3. Postoperative echocardiographiс characteristics of patients (follow up 6 months)
|
Показатели Parameters |
Среднее значение Mean value |
|
Пиковый градиент на аортальном клапа- |
18,7 |
|
не, мм рт. ст. |
|
|
Peak gradient, mm Hg |
(15–24) |
|
Средний градиент на аортальном клапа- |
10,1 |
|
не, мм рт. ст. |
|
|
Mean gradient, mm Hg |
(7–16) |
|
Трансклапанная скорость потока, м/с |
2,14 |
|
Flow rate, m/s |
(1,88–2,84) |
|
Соотношение КДО/КСО, мл |
76,3/32,1 |
|
EDV/ESV, ml |
(48–112/15–50) |
|
Фракция выброса по Симпсону, % |
63,5 |
|
Left ventricular ejection fraction, % |
(38–76) |
Примечание: КДО – конечно-диастолический объем левого желудочка, КСО – конечно-систолический объем левого желудочка.
Note: EDV – left ventricular end diastolic volume, ESV – left ventricular end systolic volume.
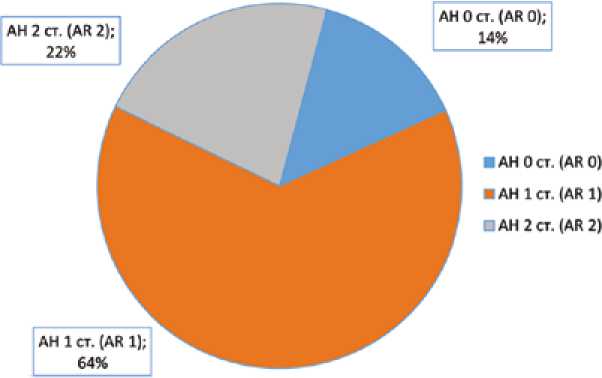
Рис. 3. Степень аортальной недостаточности (период наблюдения 6 мес.)
Fig. 3. Severity of aortic insufficiency (follow up 6 months)
Обсуждение
Важным условием успешного выполнения процедуры TAVI является работа специалистов (сердечно-сосудистых хирургов, кардиологов, аритмологов, анестезиологов, функциональных диагностов, среднего и младшего медицинского персонала) в составе «сердечной команды» (Heart Team). Это позволяет в короткие сроки интра-и периоперационно решать возникающие проблемы при имплантации и после нее.
При сравнении статистических данных, приводимых в ежегодном отчете Национального Регистра США (The Society of Thoracic Surgeons/American College of Cardiology – Transcatheter Valve Therapy Registry) [12], включающего в себя 54,782 пациента, с данными Центра кардиохирургии и интервенционной кардиологии Клиники высоких медицинских технологий имени Н.И. Пирогова Санкт-Петербургского государственного университета, можно сделать следующие выводы:
– средний возраст пациентов в целом сопоставим: 83 года – по данным Регистра и 76,3 года – по данным специалистов Клиники, сопоставимы и частота использования общей анестезии с ИВЛ (89,5 vs 93,4%), и частота применения феморального доступа (86,6 vs 95,7%);
– преобладание пациентов женского рода среди пациентов Центра (69,5 vs 48,3%), возможно, обусловлено преобладанием доли женщин среди всех жителей старшей возрастной группы в Российской Федерации;
– относительно высокая смертность среди пациентов Центра по сравнению с данными Регистра (6,5 vs 3,9%) объясняется процессом освоения данной методики («кривая обучения»);
– отсутствие в Центре таких осложнений, как ОНМК, острая почечная недостаточность, тяжелая аортальная недостаточность; встречаемость данных осложнений в Регистре с различной частотой заставляет предположить появление данных осложнений в периоперационном периоде у пациентов Центра с увеличением количества выполненных операций;
– по данным эхокардиографии, на момент выписки из стационара пациенты Центра, подвергнутые оперативному лечению до 2018 г., имели аортальную недостаточность 2-й степени в 12,5% случаев, через 6 мес. – в 22% случаев (по данным Регистра США – в 29%), что значимо больше в сравнении с результатами, полученными при открытой хирургии [13]. Преобладание процента уме-ренной/выраженной аортальной недостаточности после TAVI над процентом умеренной/выраженной аорталь-
Список литературы Опыт транскатетерной имплантации биопротезов аортального клапана Corevalve в Клинике высоких медицинских технологий имени Н.И. Пирогова Санкт-Петербургского государственного университета
- Вишневский А.Г. Демографические вызовы нового века. Демоскоп Weekly. 2003:139-140. http://www.demoscope.ru/weekly/2003/0139/tema04.php
- Iung B., Baron G., Butchart E.G., Delahaye F., Gohlke-Bärwolf C., Levang O.W. et al. A prospective survey of patients with valvular heart disease in Europe: The Euro Heart Survey on valvular heart disease. Eur. Heart. J. 2003;24:1231-1243. DOI: 10.1016/s0195-668x(03)00201-x
- Nkomo V.T., Gardin J.M., Skelton T.N., Gottdiener J.S., Scott C.G., Enriquez-Sarano M. Burden of valvular heart diseases: a population-based study. Lancet. 2006;368(9540):1005-1011. DOI: 10.1016/S0140-6736(06)69208-8
- Iung B., Vahanian A. Epidemiology of acquired valvular heart disease. Can. J. Cardiol. 2014;30(9):962-270. DOI: 10.1016/j.cjca.2014.03.022
- Rosenhek R., Zilberszac R., Schemper M., Czerny M., Mundigler G., Graf S. et al. Natural history of very severe aortic stenosis. Circulation. 2010;121(1):151-156. DOI: 10.1161/CIRCULATIONAHA.109.894170
- Gehlot A., Mullany C.J., Ilstrup D., Schaff H.V., Orzulak T.A., Morris J.J. et al. Aortic valve replacement in patients aged eighty years and older: early and long-term results. J. Thorac. Cardiovasc. Surg. 1996;11(5):1026-1036.
- Iung B., Cachier A., Baron G., Messika-Zeitoun D., Delahaye F., Tornos P. et al. Decision-making in elderly patients with severe aortic stenosis: why are so many denied surgery? Eur. Heart J. 2005;26(24):2714-2720.
- Makkar R.R., Fontana G.P., Jilaihawi H., Kapadia S., Pichard A.D., Douglas P.S. et al. Transcatheter aortic-valve replacement for inoperable severe aortic stenosis. N. Engl. J. Med. 2012;366(18):1696-1704.
- DOI: 10.1056/NEJMoa1202277
- Popma J.J., Adams D.H., Reardon M.J., Yakubov S.J., Kleiman N.S., Heimansohn D. et al. Transcatheter aortic valve replacement using a self-expanding bioprosthesis in patients with severe aortic stenosis at extreme risk for surgery. J. Am. Coll. Cardiol. 2014;63(19):1972-1981.
- DOI: 10.1016/j.jacc.2014.02.556
- Постановление Правительства РФ от 28 ноября 2014 г. № 1273 "О Программе государственных гарантий бесплатного оказания гражданам медицинской помощи на 2015 год и на плановый период 2016 и 2017 годов". http://base.garant.ru/70812574
- Holmes D.R., Mack M.J., Kaul S., Agnihotri A., Alexander K.P., Bailey S.R. et al. 2012 ACCF/AATS/SCAI/STS еxpert сonsensus document on transcatheter aortic valve replacement. J. Am. Coll. Cardiol. 2012;59(13):1200-1254. 10.1016/j.jacc.2012. 01.001.
- DOI: 10.1016/j.jacc.2012.01.001
- Grover F.L., Vemulapalli S., Carroll J.D., Edwards F.H., Mack M.J., Thourani V.H. et al. 2016 Annual report of the Society of Thoracic Surgeons/ American College of Cardiology Transcatheter Valve Therapy Registry. J. Amer. Coll. Cardiology. 2017;69(10):1215-1230.
- DOI: 10.1016/j.jacc.2016.11.033
- Thyregod H.G.H., Steinbrüchel D.A., Ihlemann N., Nissen H., Kjeldsen B.J., Petursson P. et al. Transcatheter versus surgicala aortic valve replacement in patients with severe aortic valve stenosis 1-year results from the all-comers NOTION Randomized Clinical Trial. J. Amer. Сoll. Сardiology. 2015;65(20):2184-2194.
- DOI: 10.1016/j.jacc.2015.03.014


