Опыт внедрения лапароскопическом спленэктомии в условиях многопрофильного стационара
Автор: Никитин В.Е., Розумный А.П., Хохлатов Д.Э., Локтев В.В., Клишин И.М., Мисюрина Е.Н., Буланов А.Ю., Вторенко В.И., Лысенко М.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 6 (52), 2016 года.
Бесплатный доступ
Цель работы. Разработка оптимального алгоритма ведения Больных с тромбоцитопенией различной этиологии в предоперационном периоде и после спленэктомии. Определение критериев выполнения и особенности проведения безопасной лапароскопическойспленэктомии. Материалы и методы. Проведенпроспективный анализ 48 пациентов, которым за 2015 г. Были выполнены спленэктомии по поводу различных гематологических заболеваний. Результаты. В 83,3% случаев оперативное лечение выполнено лапароскопически. В 16,7% случаев потребовалась конверсия доступа. Длительность операции составила в среднем 165 мин (от 80 до 240 мин), интраоперационная кровопотеря - 250 мл (от 100 до 1600 мл). Средняя длительность пребывания Больных в хирургическом стационаре равнялась 7 дням (от 4 до 15 суток). У 8 пациентов выполнена конверсия доступа в связи с трудноконтролируемым кровотечением в связи с Большим размером селезенки. Применение методики тромбоэластографии в совокупности с междисциплинарным подходом в ведении Больных позволило снизить количество системных и местных осложнений и более оперативно реагировать на изменение гемостаза. Заключение. Лапароскопические вмешательства являются «золототым стандартом» в лечении Больных с различными формами гематологических заболевания требующих проведения спленэктомии. Для успешного выполнения лапароскопическойспленэктомиинеобходимо выполнения тщательного предоперационного планирования, контроль за динамикой изменения гемостаза у пациентов. Междисциплинарный подход, применение разработанного лечебно-диагностического алгоритма позволили в 83% случаев избегать конверсии.
Лапароскопическая спленэктомия, тромбоцитопения, тромбоэластография
Короткий адрес: https://sciup.org/142211289
IDR: 142211289
Текст научной статьи Опыт внедрения лапароскопическом спленэктомии в условиях многопрофильного стационара
Спленэктомия как метод лечения заболеваний крови применяется с начала ХХ века [1]. За прошедшее столетие лечебные технологии в гематологии многократно изменялись и на сегодняшний день несравнимы с тем, что было доступно при первом знакомстве хирургов с гематологами. У представителей этих передовых специальностей появилось немало новых точек соприкосновения, но спленэктомия, по-прежнему, остается одной из основных. Обсуждаемое оперативное вмешательство уверенно сохранило свою нишу в гематологической хирургии [2].
Накопленный клинический опыт позволил специалистам значимо усовершенствовать технологию оперативного вмешательства. В частности, отработаны различные варианты доступа к удаляемому органув зависимости от размеров и особенностей изменения структуры селезенки и окружающих тканей, особенностей пациента, технического оснащения и пр. Выполнение спленэктомии в настоящее время возможно как классическим лапаротомным доступом, так и трансторакально, лапароскопическим и комбинированным доступом, сочетающим лапароскопию и ручное ассистирование [3–5]. Каждый из вариантов имеет свои преимущества и недостатки, и, соответственно, показания.
Вопрос выбора всегда непрост. Споров немало.Приори-теты специалистов меняются с накоплением опыта и полу-
чением новой информации. Но больше шансов выиграть гонку, безусловно, у лапароскопической методики. Среди ее преимуществ меньшая травматичность, лучшая визуализация зоны работы хирурга, меньшая кровопотеря, более гладкое течение послеоперационного периода. Основным ограничением использования лапароскопии считаются выраженные изменения окружающих тканей и спленомегалия. Но последнее положение не догма и вполне может быть пересмотрено. Некоторые аргументы в пользу расширения использования лапароскопического доступа при выполнении спленэктомии пациентам гематологической клиники мы хотели бы представить в настоящей публикации.
Целью работы явился анализ опыта выполнения лапароскопических спленэктомий при гематологических заболеваниях и синдромах в условиях многопрофильного стационара.
Материалы и методы
В течение года в хирургическом отделении городской клинической больницы № 52 г. Москвы выполнено 48 лапароскопических спленэктомий. Возраст пациентов составил в среднем 48 лет (от 19 до 75). Мужчин было 22, женщин 26. Особенностью 2 случаев была беременность пациенток: с целью купирования геморрагического синдрома, связанного с иммунной тромбоцитопенией спленэктомия была выполнена на сроках гестации 7-8 и 23-24 недели. Среди нозологических форм преобладали идиопатическая тромбоцитопеническая пурпура (28 больных), и лимфатические опухоли (лимфосаркомы, лимфоцитомы, хроническийлим-фолейкоз) (12 больных). Кроме того были оперированы пациенты с аутоиммунной гемолитической анемией (3), первичным миелофиброзом (3), апластической анемией (2). Показаниями для оперативного лечения служили: неэффективность консервативной терапии аутоиммунной тромбоцитопении и анемии, лечение апластической анемии, цито-пенический синдром при лимфо- и миелопролиферативных заболеваниях, удаление основной массы опухоли, абсцессы селезенки, необходимость морфологической верификации диагноза. Подавляющее большинство спленэктомий было выполнено с лечебной целью. Приоритетно диагностические задачи стояли в 2 случаях.
Большое внимание уделялось предоперационному обследованию пациентов. При этом ставились следующие стратегические задачи: оценка размеров и состояния селезенки, наличие анатомических особенностей удаляемого органа; состояние окружающих тканей и в целом брюшной полости, в особенности выявление признаков портальной гипертензии, наличие и распространенность лимфаденопатии; оценка выраженности гематологических синдромов, в особенности, состояние системы гемостаза; верификация и оценка тяжести сопутствующей патологии. В рамках данного обследования выполнялись: ультразвуковое исследова- ние брюшной полости с оценкой кровотока сосудов верхних отделов брюшной полости, компьютерная томография брюшной полости, грудной клетки, при необходимости с контрастным усилением, эзофагогастродуоденоскопия. Исследовалась морфология периферической крови и костного мозга, уровень сывороточных ферментов, характеризующих активность опухолевого процесса, наличие и активность антитромбоцитарных и антиэритроцитарных антител и другие важные лабораторные показатели, характеризующие степень цитолитического синдрома, степень нарушения функции органов и пр. Выполнялись все лабораторные и инструментальные тесты, входящие в стандарт предоперационного обследования с расширением в зависимости от сопутствующей патологии. Тактика ведения пери-операционного периода вырабатывалась совместно с гематологами, при необходимости привлекались представители других специальностей (гемостазиологи, кардиологи, нефрологи, ревматологи), благо возможности многопрофильного стационара позволяют это сделать весьма оперативно.
Высокая частота нарушений гемостаза у наших пациентов определяют особое место контролю состояния этой системы на всех этапах периоперационного периода. С этой целью широко применялся интегральный тест – тромбоэластография (ТЭГ).Методика позволяет быстро и наглядно оценить состояние всех звеньев системы гемостаза (коагуляционный каскад и тромбоциты, антикоагулянтные механизмы и систему фибринолиза) и результат их взаимодействия[6]. Использовалась классическая тромбоэластография на тромбоэластографеTEG5000. Выполнялась нативная ТЭГ,которая при необходимости дополнялась тестом с гепариназой и тестом на функциональный фибриноген.
По результатам обследования нормальные размеры селезенки (длина 80-120мм) имели место у 21 пациента. Уме-реннаяспленомегалия (длинна 130-150 мм) имела место у 12 больных, большие размеры органа (максимальная длинна 320 мм) были зарегистрированы в 15 случаях. Признаки периспленитаотмечались в 9 (18,75%) случаях, портальной гипертензии в 11 (22,9%).
Анемический синдром осложнял состояние у 31 пациента (64,6%), тяжелая анемия со снижением гемоглобина менее 70 г/л присутствовала у 5 больных (10,4%).
Наиболее частым гематологическим синдромом была тромбоцитопения. Она имела место у 40 пациентов (83,3%) из них критическое снижение тромбоцитов (менее 20 х 109/л) отмечалось у 21 больного (43,75%). Клинические проявления геморрагического синдрома в виде петехий на коже и слизистых, носовыми, десневыми кровотечениями, меноррагиями характеризовали почти половину пациентов (47,9% или 23 человека). У 7 пациентов (14,6%) были выявлены нарушения плазменного гемостаза, как в изолированном виде, так и в сочетании с тромбоцитопенией. В том числе у одной пациентки имела место такая не частая, но тяжелая патология [7], как гепарино-подобный синдром.
Из сопутствующей патологии лидировал медикаментозный синдром Иценко-Кушинга, связанный с предшествующей кортикостероидной терапией. Они отмечен у 6 пациентов (12,5%).
Операцию выполняли силами бригады из 2 хирургов -оператора и 1 ассистента - и 1 операционной сестры из 4-х троакарного доступа (1 троакар параумбиликально, смещался в зависимости от размеров селезенки и 3 троакара располагались дугообразно под левой реберной дугой). Извлечение селезенки из брюшной полости проводили в контейнере в большинстве случаев фрагментарно, при диагностической необходимости — целиком из минила-паротомного доступа. Использованы лапароскопическое оборудование и инструменты фирм KarlStarz (Германия), МФС (Россия); ультразвуковой скальпель Harmonik, аппарат Ligasure.
При одновременном наличии показаний к операциям на других органах брюшной полости выполнялось сочетанное оперативное вмешательство. Всего было выполнено 9 (18,8% больных) сочетанных операций: спленэктомия с холецистэктомией (2 пациента), герниопластикой (4 пациента), биопсией внутрибрюшных лимфатических узлов (3 пациента).
Результаты и обсуждение
Из 48 выполненных спленэктомий лапароскопически удалось завершить оперативное вмешательство у 40 пациентов (83,3%). Длительность операции составила в среднем 165 мин (от 80 до 240 мин), интраоперационная кровопотеря - 250 мл (от 100 до 1600 мл). Средняя длительность пребывания больных в хирургическом стационаре равнялась 7 дням (от 4 до 15 суток).
Результаты анализа позволили четко разделить пациентов на две группы: с опухолевыми и неопухолевыми «заболеваниями» селезенки. В первой группе, где преобладали пациенты, страдающие ИТП, основная сложность была связана с системными нарушениями гемостаза, в первую очередь тромбоцитопенией и, соответственно, повышенной кровоточивостью. Работа с этими пациентами требовала активного участия специалистов гемостазиологической службы. К характерным техническим сложностям в данной группе можно отнести часто встречающийся рассыпной тип строения селезеночных сосудов и выраженное ожирение, как проявление синдрома Иценко-Кушинга.
С хирургических позиций более сложными, а, соответственно, и более интересными были пациенты второй группы. Такие факторы, как спленомегалия, наличие пери-спленита, портальной гипертензии, вовлеченность в опухолевый процесс сосудистой ножки, хвоста поджелудочной железы существенно затрудняли выполнение вмешатель- ства при опухолевом поражении селезенки (рис. 1). Это закономерно удлинило выполнение операции – в среднем на 35 мин по сравнению с первой группой. В три раза чаще, чем в первой группе приходилось и переходить на открытый доступ. Причиной конверсии в этой группе были интраоперационные кровотечения, связанные с портальной гипертензией (2 случая), большие размеры селезенки (более 300 мм по длине) (3 случая) и распространение опухолевого процесса на хвост панкреас (1 случай). В случаяхмассивной спленомегалии на определенном этапе было невозможно провести диссекцию «нижней» поверхности, прилежащей к почке из-за большого веса органа и не возможности тракции. Тем не менее, до конверсии были обработаны питающие сосуды — орган лишен кровоснабжения; выделены верхний и нижний полюса. В ситуации с поражением поджелудочной железы с втягиванием ее в ворота селезенки поводом для конверсии послужила невозможность адекватной визуализации магистральных сосудов и угроза возникновения массивного не контролируемого кровотечения. Тем не менее, и в этих случаях основные этапы оперативного вмешательства (обработка сосудистой ножки, выделение полюсов селезенки, разделение спаек, возникших в результате периспленита) удавалось выполнить лапароскопически (рис. 2).

Рис. 1. Лапароскопически удаленная селезенка при лимфосаркоме
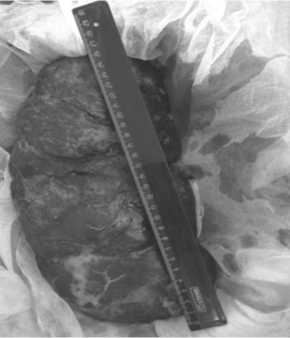
Рис. 2. Селезенка длинной 26 см после запустевания сосудов удаленная лапароскопически. Диагноз – лимфома.
Следует отметить, что в описанных случаях возможность расширения доступа до лапаротомии обсуждалась до оперативного вмешательства. Но предполагаемый «риск» необходимости конверсии не рассматривался как аргумент в пользу исходного выбора лапаротомного доступа. Подчеркнем, что и в этих случаях лапароскопическая часть операции внесла существенный вклад в ее успех. Даже большой размер селезенки не являлся фактором ограничения применения лапароскопической техники. И мы не одиноки в подобном подходе [4, 8]. Хотя в более ранних работах присутствуют однозначные рекомендации изначально отказаться от лапароскопии при размере селезенки более 22 см [2, 5].
Безусловно, любые оперативные пособия сопровождаются осложнениями. Все интраоперационные осложнения, а их было 11 (22,9%) — были связаны с кровотечениями:в следствие повреждения капсулы селезенки, краевых ранений не лигированных (клипированных) сосудов, миграции лигатуры или клипсы с сосуда. В большинстве случаев кровотечения удавалось остановить эндоскопически с помощью повторного лигирования, коагулирования сосуда или тампонирования области повреждения капсулы с последующей быстрой обработкой питающих селезенку артериальных сосудов. Однако в 4 случаях интраоперационные кровотечения привели к конверсии, во всех случаях у пациентов отмечались признаки портальной гипертензии. Других, описанных в литературе осложнений, в частности повреждения диафрагмы [2, 9, 10], не отмечено. Мы связываем это с большим предшествующим опытом, накопленном в клинике при операциях на верхнем этаже брюшной полости.
Геморрагические осложнения у пациентов с исходными нарушениями гемостаза имели место и в послеоперационном периоде. У 3 пациентов были выявлены гематомы левого поддиафрагмального пространства. Ни в одном из трех случаев не отмечалось каких-либо клинических проявлений гематомы, все они были выявлены при плановом послеоперационном ультразвуковом исследовании брюшной полости, введенном нами в разряд стандартных послеоперационных процедур у пациентов с геморрагическими нарушениями. В условиях того же УЗИ контроля гематомы были с успехом дренированы. Важно, что не случилось ни одного послеоперационного кровотечения, в том числе и у пациентов с глубокой тромбоцитопенией, которое потребовало бы выполнения повторного оперативного вмешательства. Одним из факторов этого является тщательный контроль системного гемостаза, рутинно используемый в нашей клинике у обсуждаемой категории больных.
Показано, что оптимальным методом контроля системы гемостаза в периоперационном периоде, особенно у пациентов гематологической клиники, является тромбоэластография [6, 11]. Взяв это положение за основу, мы с успехом сформировали протокол ведение пациентов при лапароско- пическойспленэктомии совместно с гемостазиологической службой. Для иллюстрации проведем два примера.
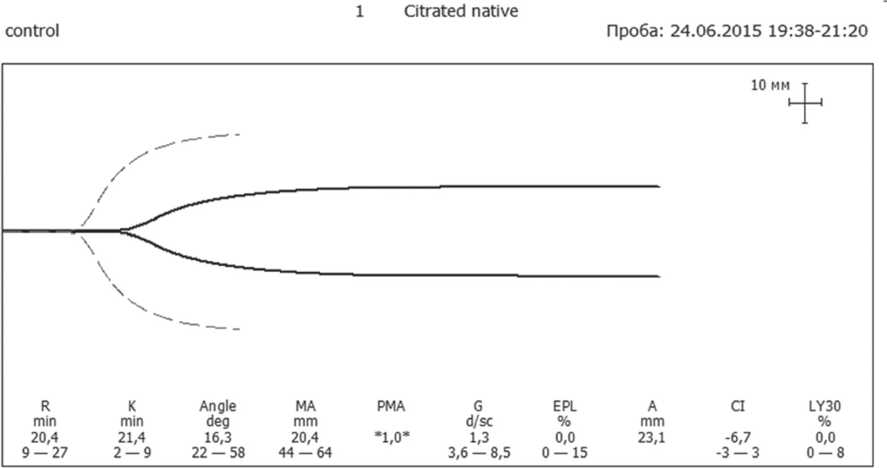
Отсутствие эффективности консервативной терапии иммунной тромбоцитопении у пациентки Ж, 56 лет, страдающей ИТП, явилось показанием для выполнения лапаро-скопическойспленэктомии. На момент поступления больной в хирургическое отделение, несмотря на проведенный курс пульс-терапииметилпреднизолоном, отмечалась глубокая тромбоцитопения (число тромбоцитов при подсчете по Фонио 3-7 х 109/л), клинически проявляющаяся геморрагическим синдромом в виде петехиальной сыпи, преимущественно на верхней половине туловища. Данные ТЭГ не противоречили указанным изменениям и свидетельствовали о выраженном нарушении функции тромбоцитарного гемостаза (рис. 3, А). Непосредственно перед оперативным вмешательством пациентке по витальным показаниям была выполнена трансфузия концентрата тромбоцитов и введен препарат активированного VII фактора свертывания, что обеспечило приемлемые условия выполнения оперативного вмешательства (рис. 3, Б).
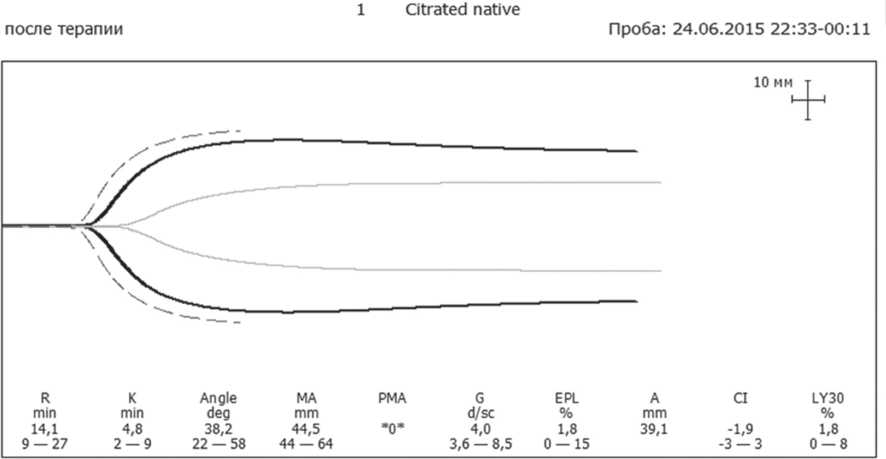
Результат выполненной спленэктомии у больных с иммунной тромбоцитопенией в виде прироста тромбоцитов нередко проявляется очень быстро, часто в течение нескольких часов. В этом случае важно уловить момент перехода состояния гемостаза из гипокоагуляции в тромбоопасное состояние для своевременного назначения антитромботи-ческой профилактики. Временной интервал между тромбоэластограммами пациента Р., выполненными до и после лапароскопическойспленэктомии (рис. 4) составил 9 часов. Число тромбоцитов изменилось с 18 х 109/л до 84 х 109/л и не вызвало опасений, данные ТЭГ же указали на необходимость немедленного назначения антикоагулянтов.
Надо признать, что, не смотря на пристальное внимание к системе гемостаза, у 3 пациентов (6,25%) мы диагностировали в раннем послеоперационном периоде развитие бессимптомного тромбоза воротной вены. В этом нет ничего неожиданного. Тромбозы воротной и селезеночной вен после выполненной спленэктомии описаны и в большем проценте случаев – до 22% [12, 13]. Помимо изменений гемостаза к этому есть и анатомические предпосылки [14]. Тем не менее, с учетом нашего пока небольшого опыта, надеемся если не избежать полностью, то, по крайней мере, минимизировать данное осложнение. С этой целью осуществляем контроль гемостаза, включая ТЭГ и выполняем ультразвуковое исследование брюшной полости в раннем послеоперационном периоде после лапароскопическойспленэктомии ежедневно. И пока, исходя из «презумпции виновности» делаем это всем. Приобретение большего опыта, очевидно, позволит нам произвести некоторую селекцию и сэкономить на УЗИ и ТЭГ, но это перспектива на будущее.
А
Б
Рис. 3. Динамика ТЭГ в результате предоперационной подготовки пациента с ИТП.
А – до терапии, Б – после трансфузии концентрата тромбоцитов и введения активированного VII фактора
Выводы
-
1. Лапароскопическаяспленэктомия может рассматриваться как золотой стандарт при необходимости оперативного лечения у гематологических больных. Невозможность обойтись только лапароскопическим доступом не должна рассматриваться как аргумент к отказу от лапароскопии, по крайне мере как для выполнения начальных этапов операции.
-
2. Периоперационное ведения пациентов гематологической клиники при выполнении лапароскопической спленэктомии
требует участия специалистов различного профиля, круглосуточной лабораторной и трансфузиологической служб, что легко достижимо в условиях многопрофильного стационара.
Список литературы Опыт внедрения лапароскопическом спленэктомии в условиях многопрофильного стационара
- Micheli F. Unmittelbareefekte der splenektomiebeieinenFall von erworbenehemolytischenikterus. Klin.Wschr. 1911; 24: 1269-1274.
- Baccarani U., Terrosu G., Donini A., Zaia F. Splenectomy in gematolo-gy. Curren practice and new perspectives.Hematologyca.1999; 84: 431-436.
- Карагюлян С.Р., Гржималовский А.В., Данишян К.И. и др. Хирургические доступы к селезенке. Анналы хирургическойгепа-тологии. 2006; 11 (2): 92-99.
- Chen J., Tao K., Yu P. Laparoscopic splenectomy is better surgical approach for spleen-relevant disorders. Surg. Endosc. 2016 (ahead ofprint).
- Гржимоловский А.В., Шутов С.А., Карагюлян С.Р., Данишян К.И. Лапароскопически ассистированная спленэктомия. Анналы хирургической гепатологии. 2008; 13 (2): 17-21.
- Буланов А.Ю., Городецкий В.М. Функциональный контроль гемостаза в гематологической клинике. В кн. Программное лечение заболеваний системы крови под.ред. В.Г. Савченко. Москва, Практика, 2012 г.
- Буланов А.Ю., Яцков К.В., Шулутко Е.М., Глухова Т.Е., Андрейченко С.А. Эндогенный гепариноподобный синдром: анализ клинических наблюдений. Анестезиология и реаниматология. 2012; №3: 51-54.
- Somasundaram S.K., Massey L., Gooch D. et al. Laparoscopic splenectomy is emerging "gold standard" treatment even for massive spleens. Ann. R. Coll. Surg. Engl. 2015; 9: 1-4.
- Карагюлян С.Р., Гржимоловский А.В., Шутов С.А., Данишян К.И. Технически сложнаяспленэктомия: выбор способа операции. Анналы хирургической гепатологии. 2008; 13 (2): 12-16.
- Rescorla F.J., West K.W., Engum S.A., Grosfeld J.L. Laparoscopic splenic procedures in children: experience in 231 children. Ann. Surg. 2007; 246: 683-687.
- Буланов А.Ю., Городецкий В.М., Щербакова О.В. и др. Тромбоэластографическая оценка системы гемостаза и эффективность ее коррекции перед оперативными вмешательствами у Больных с заболеваниями системы крови. Гематология и трансфузиология. 2012; 57(5): 36-42.
- Ruiz-Tovar J., Perezde Oteyza J., Blazquez Sanchez J. et al. Portel vein thrombosis after laparoscopic splenectomy in benign hematologic diseases. J. Laparoendosc. Adv. Surg. Tech A. 2007; 17(4): 448-454.
- Pietrabissa A., Moretto C., Antonelli G. et al. Thrombosis in the portal venous system after elective laparoscopic splenectomy. Surg. Endosc. 2004; 18(7): 1140-1143.


