Особенности активации апоптоза в клетках семенных канальцев крыс при азооспермии после воздействия бета-излучения в дозах 2 и 8 грэй
Автор: Демяшкин Г.А., Цибулевский А.Ю., Недорубов А.А., Батов М.А., Щекин В.И.
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 3 т.29, 2021 года.
Бесплатный доступ
Развитие бесплодия у самцов крыс под воздействием высоких доз ионизированного излучения обусловлено не только прямым повреждением клеток, но и блоком дифференцировки и индукцией апоптоза созревающих сперматогоний. Однако литературные данные по активности биологических медиаторов внутреннего и внешнего пути апоптоза после облучения бета-частицами, в частности, разными эффективными дозами, крайне ограничены. Цель исследования: изучение молекулярно-биологических механизмов апоптоза в семенных канальцах самцов крыс после облучения электронами в дозе 2 и 8 грэй. Самцы крыс Wistar (220±20 г; 9 - 10 недель; n=40) были поделены на 3 группы: I - контрольная (n=10); II - облучение электронами, доза 2 грэй (n=15); III - облучение электронами, доза 8 грэй (n=15). На срезах семенников толщиной 8 мкм определяли экспрессию мРНК каспаз CASP8 и CASP9 методом полимеразной цепной реакции в режиме реального времени. Апоптотическую фрагментацию ДНК выявляли методом TUNEL c подсчетом TUNEL-позитивных ядер. На 50-й день после начала эксперимента обнаружили значительное число апоптотических клеток в группах крыс, подвергнутых ионизирующему облучению. Относительное количество TUNEL-положительных клеток сперматогенного эпителия в группе 8 грэй составило 56±1,2% по сравнению с группой 2 грэй - 37±0,9% (p function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Сперматогенез, апоптоз, каспазы, ф-излучение, крысы
Короткий адрес: https://sciup.org/143178009
IDR: 143178009 | DOI: 10.20340/mv-mn.2021.29(3).558
The features of apoptosis activation in seminiferous tubule cells of rats with azoospermia after exposure of beta-radiation at doses of 2 and 8 gray
The development of infertility in male rats under the influence of high doses of ionized radiation is caused not only by direct damage to cells, but also by the block of differentiation and the induction of apoptosis of maturing spermatogonia. However, the literature data on the activity of biological mediators of the internal and external pathways of apoptosis after irradiation with beta particles, in particular, with different effective doses, are extremely limited. Objective: to study the molecular biological mechanisms of apoptosis in the seminiferous tubules of male rats after irradiation with electrons at a dose of 2 and 8 Gray. Male Wistar rats (220±20 g; 9-10 weeks; n=40) were divided into 3 groups: Ist - control (n=10); IInd - electron irradiation, dose 2 Gray (n=15); IIIrd -electron irradiation, dose 8 Gray (n=15). The expression of mRNA of caspases CASP8 and CASP9 was determined on sections of testes with a thickness of 8 pm using real-time polymerase chain reaction. Apoptotic DNA fragmentation was detected by the TUNEL method with the calculation of TUNEL-positive nuclei. On the 50th day after the start of the experiment, a significant number of apoptotic cells were found in the groups of rats subjected to ionizing radiation. The relative number of TUNEL-positive cells of spermatogenic epithelium in the 8 Gray group was 56±1,2% compared with the 2 Gray group - 37±0,9% (p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Особенности активации апоптоза в клетках семенных канальцев крыс при азооспермии после воздействия бета-излучения в дозах 2 и 8 грэй
Демяшкин Г.А., Цибулевский А.Ю., Недорубов А.А., Батов М.А., Щекин В.И. Особенности активации апоптоза в клетках семенных канальцев крыс при азооспермии после воздействия бета-излучения в дозах 2 и 8 грэй. Морфологические ведомости. 2021;29(3):558. (3).558
Demyashkin GA,2Tsybulevsky AYu,1Nedorubov AA, Batov MA, Shchekin VI. The features of apoptosis activation in seminiferous tubule cells of rats with azoospermia after exposure of beta-radiation at doses of 2 and 8 Gray. Morfologicheskie Vedomosti - Morphological newsletter. 2021;29(3):570. (3).537
В экспериментальных исследованиях показано, что ионизирующее облучение семенников в дозах от 0,1 Грэй и выше инициирует развитие азооспермии, ведущей к временному или перманентному бесплодию [3]. Негативный эффект облучения на сперматогенный эпителий преимущественно обусловлен первичным повреждением клеточных структур и двухцепочечными разрывами ДНК. Наибольшую чувствительность к прямому повреждению проявляют активно пролиферирующие сперматогонии B, в то время как сперматогонии А менее чувствительны к ионизирующему излучению, но подвержены вторичному повреждению ДНК. Образующиеся в условиях облучения активные формы кислорода (далее -АФК), обладающие, как известно, выраженными цитотоксическими мутагенные свойствами, приводят к возникновению апурино-вых/апиримидиновых сайтов и одноцепочечным разрывам в молекулах ДНК [34]. Сохранившиеся после облучения спер-матогонии А могут достаточно быстро восстановить пул активно делящихся сперматогоний, количество которых будет достаточно для поддержания адекватного уровня сперматогенеза. Однако, часть сперматогоний подвергается блоку дифференцировки в течение длительного времени [5]. Накопление мутаций в «спя- щих» сперматогониях повышает вероятность нарушений пролиферации и дифференцировки на последующих этапах сперматогенеза. В случае индукции апоптоза в поврежденных клетках сперма-тогенного эпителия восстановление адекватного уровня сперматогенеза задерживается даже после снятия блока дифференцировки сперматогоний [3, 5-6].
Прямая связь между дозой облучения семенника и степенью его морфологических повреждений установлена достоверно, однако изменения пролифератив-но-апоптотического индекса подробно не исследовались. Является ли эффект отсроченной активации апоптоза в созревающих гамета на разных этапах сперматогенеза дозозависимым и если да, то в какой степени, остается неизученным. Также неизвестно, какой путь апоптоза преимущественно обуславливает отсроченную гибель после восстановления активности сперматогоний.
Цель исследования: изучение особенностей молекулярно-биологических механизмов активации апоптоза в семенных канальцах самцов крыс после облучения электронами в дозе 2 и 8 Грэй.
Материалы и методы исследования. В настоящем исследовании для первичной оценки апоптоза клеток спермато-генного эпителия крыс после облучения дозами в 2 и 8 Грэй применяли метод TUNEL c проведением иммунофлюорес-центной микроскопии. Также определяли экспрессию мРНК каспазы-8 (далее -CASP8) и каспазы-9 (далее - CASP9) для определения активности наружного и внутреннего путей апоптоза, соответственно. Самцов крыс Wistar (220±20 грамм; возраста 9-10 недель; n=40) содержали в виварии при контролируемой температуре (21°C) и световом периоде со свободным доступом к воде и корму. Животные были случайным образом поделены на 3 группы: I - контрольные (n=10); II - подвергнутые облучению электронами в дозе 2 Грэй (n=15); III - подвергнутые облучению электронами в дозе 8 Грэй (n=15).
Крысам I группы вводили 0,9% физиологический раствор NaCl интраперитонеально на протяжении всего эксперимента. Животных II и III групп (n=30) под- вергали однократному прицельному облучению электронами тазово-брюшного сегмента с использованием линейного акселератора («NOVAC-11», мощность дозы 1 Грэй/мин) в первый день эксперимента в дозах 2 Грэй и 8 Грэй, соответственно. Животных всех групп выводили из эксперимента путем введения высоких доз анестетика на 50-е сутки.
Все манипуляции осуществляли согласно Международным рекомендациям по проведению медико-биологических исследований с использованием животных (ЕЭС, Страсбург, 1985), Европейской конвенции о защите позвоночных животных, используемых для экспериментов или в иных научных целях (ЕЭС, Страсбург, 1986), Руководствам по проведению медико-биологических исследований по уходу и использованию лабораторных животных (ILAR, DELS) и Правилам лабораторной практики и приказу Министерства здравоохранения РФ № 199н от 01.04.2016 «Об утверждении правил лабораторной практики», исследования были также одобрены локальным этическим комитетом.
Срезы, полученные из фрагментов семенников, фиксировали в 4% растворе параформальдегида в фосфатно-солевом буфере (далее - PBS) 15-20 минут при 20°C, после чего обрабатывали 100 мкл раствором протеиназы K с концентрацией 20 мкг/мл и инкубировали в течение 10 минут при комнатной температуре. Затем проводили отмывку, погрузив предметные стекла в PBS на 5 минут при комнатной температуре. Далее добавляли 50 мкл окрашивающего раствора TdT (ThermoFisher, USA) и инкубировали 60 минут при 37°C. Затем проводили удаление рабочего раствора TdT и промывание в PBS. Далее добавляли монтажную среду с DAPI (ThermoFisher, USA) и контролировали, применяя флуоресцентный микроскоп и регулируя интенсивность флуоресценции набором фильтров FITC.
Фрагменты аутоптатов семенников помещали в стабилизирующий раствор и хранили при -70°C до проведения исследования. Образцы подвергали гомогенизации согласно стандартному протоколу. Экстракцию тотальной РНК производили с использованием набора готовых реакти- вов RNeasy Plus Mini Kit (QIAGEN, Нидерланды). Синтез комплементарной ДНК (кДНК) осуществляли с помощью SuperScript™ VILO™ Master Mix (Invitrogen). Выделенные кДНК подверглись полимеразной цепной реакции в реальном времени (далее - ПЦР-РВ) с использованием готовой смеси реагентов Absolute Blue QPCR Mix (Thermo Scientific, США) с SYBR Green I. ПЦР-РВ проводилась с использованием StepOne System (Applied Biosystems, CША) и штатного программного обеспечения.
Анализ экспрессии генов проведен с использованием метода определения порогового цикла (Ct) и вычисления относительной экспрессии генов согласно протоколу [7]. Контроль выполнен относительно референсного гена домашнего хозяйства GAPDH. Подбор праймеров был осуществлен на основании общедоступных материалов о последовательностях ДНК и мРНК генов в базе данных NCBI с использованием Primer-BLAST. Сравнение между группами проводилось с использованием однофакторного дисперсионного анализа ANOVA со статистической значимостью на уровне p<0,05.
Результаты исследования и обсуждение. Апоптотический статус в образцах семенников крыс оценивали в группе контроля, 2 Грэя и 8 Грэй. Во всех группах апоптотическая фрагментация ДНК обнаруживались в пределах сперма-тогенного эпителия преимущественно в сперматоцитах. В группе 8 Грэй относительное количество TUNEL-положительных клеток в сперматогенном эпителии семенных канальцев на 21 сутки было значительно достоверно выше (p<0,01) группы 2 Грэя, 56±1,2% и 37±0,9%. В контрольной группе регистрировали 10±1,1% TUNEL-положительных клеток (рис. 1).
Относительная экспрессия CAPS9 была статистически значимо выше в экспериментальных группах по сравнению с контролем (p<0,01). В группе 8 Грэй экспрессия CASP9 была выше, чем в группе 2 Грэя (5,83±0,48 против 4,1±0,41; p<0,01). Экспрессия CASP8 статистически значимо не отличалась между контрольной и экспериментальными группами (рис. 2).
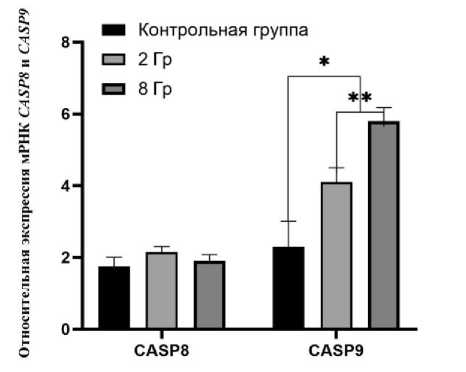
Рис. 2. Диаграмма относительной экспрессии мРНК CASP8 и СASP9 в образцах семенных канальцев крыс контрольной группы и после воздействия ионизирующего излучения (в условных единицах). Обозначения: * – статистически значимая разница между контрольной и экспериментальными группами; ** – статистически значимая разница между группами 2 Грея и 8 Грэй.
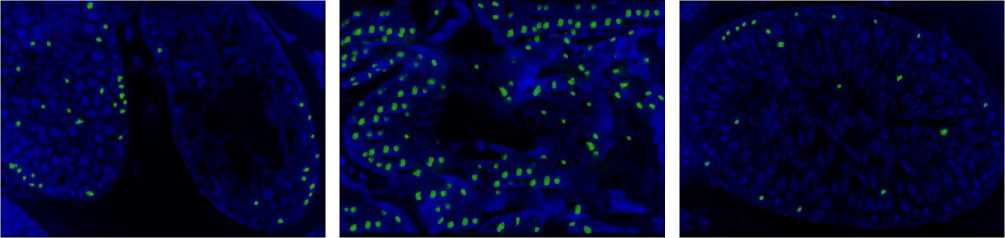
а б в
Рис. 1. TUNEL-позитивные клетки в семенных канальцах крыс после облучения дозами 2
Грэя (а), 8 Грэй (б) и в контрольной группе (в). Окр.: флюоресцентная микроскопия. Ув.:
х400.
Митохондрии, как известно, являются основным источником АФК в клетках. Окислительный стресс и сопряженная с ним гиперпродукция АФК непосредственно связаны с индукцией апоптоза во многих типах клеток, в том числе и спер-матогенного эпителия [1]. Кроме того, оксид азота действует на митохондрии и индуцируя митохондриально-зависимый апоптоз способствует гибели сперматого-ний А при старении у крыс [11-12]. Таким образом, нормализация функции митохондрий может привести к существенному снижению уровня АФК в клетках.
Ряд ключевых событий в период апоптоза, вызванного ионизирующим излучением, связаны с изменением митохондриальной активности и их целостности: снижением производства АТФ, увеличением выработки АФК, увеличением проницаемости митохондриальной мембраны, а также высвобождением цитохрома С, апоптоз-индуцирующего фактора и, наконец, каспаз в цитоплазму клетки. Все эти изменения обуславливают нарушение функции и структурное повреждение митохондрий [13].
Принимая во внимание преимущественное влияние ионизирующего излучения на митохондрии, предполагалось получение результатов, указывающих на преимущественную активации внутреннего пути апоптоза в этих условиях, что характеризуется повышением экспрессии CASP9. Отсутствие значимой активации CASP8, вероятнее всего, связано с иммунной привилегированностью сперматоген-ного эпителия и отсутствием значимого влияния внешнего пути на индукцию апоптоза в клетках сперматогенного эпителия. Также в ряде исследований установлена корреляция между снижением активности антиапоптотического гена BCL-2 и повышением экспрессии CASP9, что указывает на необходимость изучения про- и антиапоптотического соотношения экспрессии ключевых генов под воздействием ионизирующего излучения [14].
Результаты реакции, полученной методом TUNEL, указывают на дозозависимый характер активации апоптоза в сперматогониях и сперматоцитах при воз- действии бета-излучения, однако не исключено, что избыточная активация апоптоза при более высоких дозах излучения является не только следствием накопления ошибок ДНК, но и прямым повреждающим действием на клеточные структуры. На это указывает значительное изменение структуры семенника после облучения в дозе 8 Грэй. Очевидно, что для всесторонней оценки возможности и сроков восстановления сперматогенного эпителия под воздействием различных доз ионизирующего излучения необходимо дальнейшее углубленное исследование.
Заключение. В проведенном нами исследовании получены данные, свиде- тельствующие о дозозависимом эффекте бета-излучения на индукцию апоптоза в семенных канальцах крыс. Установлено, что преимущественная активация апоптоза после воздействия бета частиц обусловлена внутренним путем и, вероятно, связана с нарушение целостности и функции митохондрий. Повышение экспрессии CASP9 в группе крыс с наибольшей лучевой нагрузкой по сравнению с группой животных с меньшей дозой облучения указывает на возможную корреляцию между поглощенной дозой ионизирующего излучения и степенью повреждения митохондрий.


