Особенности чрескостного остеосинтеза при замещении пострезекционных дефектов трубчатых костей кисти
Автор: Борзунов Дмитрий Юрьевич, Моховиков Денис Сергеевич
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 2, 2009 года.
Бесплатный доступ
Обобщен опыт замещения свободными аутотрансплантатами пострезекционных дефектов, сформированных по поводу опухолевых и опухолеподобных заболеваний трубчатых костей кисти у 19 пациентов. В зависимости от клинико-рентгенологической семиотики поражения коротких трубчатых костей кисти применялась сегментарная и внутрикостная резекция очагов деструкции с фиксацией отломков и трансплантатов мини-аппаратом Илизарова. Предложенные компоновки мини-аппаратов позволяли сохранить функцию смежных суставов на этапе чрескостного остеосинтеза, не ограничивая социальную, а в ряде случаев и трудовую адаптацию на этапах лечебно-реабилитационного процесса.
Энхондрома, аутотрансплантат, пострезекционный дефект, мини-аппарат илизарова
Короткий адрес: https://sciup.org/142121200
IDR: 142121200 | УДК: 616.717.9-001.5-089.227.844
The features of transosseous osteosynthesis for filling the post-resection defects of hand tubular bones
The authors present their experience of making the procedures of filling post-resection defects with free autografts in 19 patients for tumoral and tumor-like diseases of hand tubular bones. Depending on clinical-and-roentgenological semiotics of the involvement of hand short tubular bones, segmental and intraosseous resection of destruction foci was performed with fixation of fragments and grafts using the Ilizarov mini-fixator. The configurations of mini-fixators proposed allowed to preserve the function of adjacent joints at the stage of transosseous osteosynthesis without limitation of socioenvironmental and, in some cases, working adaptation at the stages of treatment-and-rehabilitation process
Текст научной статьи Особенности чрескостного остеосинтеза при замещении пострезекционных дефектов трубчатых костей кисти
Традиционно проблема лечения заболеваний кисти вызывает повышенный интерес у многих хирургов. В первую очередь, это обусловлено высокими функциональными требованиями, предъявляемыми к кисти как в профессиональной, так и в повседневной деятельности человека.
Кисть человека, составляя около 2,1 % от общей площади тела человека, имеет сложное строение и выполняет тонкие, важные функции. Многообразие тканевых структур в пределах кисти обеспечивает возможность возникновения самых различных новообразований. В структуре общей патологии кисти на долю опухолевых и опухолеподобных поражений приходится 3,55,2 % клинических наблюдений [2]. Среди опухолей кисти преобладают мягкотканные -76,1 %, на долю костно-хрящевых новообразований приходится до 22,9 % случаев, злокачественные новообразования встречаются в 0,94 % клинических ситуаций [1]. Из всех видов костных опухолей чаще всего поражают короткие трубчатые кости кисти энхондромы (70 %), при этом наиболее частой локализацией деструктивного процесса являются проксимальные фаланги IV, V пальцев [8].
Реабилитация больных с опухолями и опухо- леподобными поражениями костей кисти представляет особые трудности. Это связано с тем, что способы лечения, кроме оперативных, не эффективны, а удаление опухолевых очагов в пределах здоровых тканей предусматривает необходимость ликвидации пострезекционного костного дефекта и последующего восстановления функции кисти [4]. Сформированные пострезекционные костные дефекты встречаются у 26,4 % пациентов, имеющих первичные поражения костной ткани коротких трубчатых костей доброкачественными опухолями и опухолеподобным процессом [1]. Поиск способов замещения пострезекционных дефектов костной ткани является актуальной проблемой современной реконструктивно-восстановительной хирургии [3].
В настоящее время в реконструктивновосстановительной хирургии отдается предпочтение следующим видам оперативных вмешательств: резекции очага поражения в пределах здоровой ткани (сегментарная резекция, краевая резекция, внутрикостная резекция) и замещение сформированного пострезекционного дефекта кортикально-губчатыми аутотрансплантатами [7]. Ряд исследователей предпочитает использовать имплантаты на основе гидроксиапатитов для замещения пострезекционных дефектов трубчатых костей [5, 8, 9, 10].
Дискутабельным остается вопрос выбора способа фиксации костных фрагментов в послеоперационном периоде. Распространенными методами фиксации сегментов кисти являются гипсовая повязка и интрамедуллярный остеосинтез спицей. Однако применение указанных выше методов фиксации неизбежно ведет к возникновению стойких контрактур суставов кисти, а как следствие - к ухудшению качества жизни пациентов. Это обстоятельство обусловливает длительные сроки социально-трудовой реабилитации данной категории больных. Очевидно, что адекватный выбор варианта фиксации костных фрагментов кисти является важнейшим звеном хирургического лечения пациентов с опухолевыми и опухолеподобными поражениями трубчатых костей кисти.
Целью данного исследования явилось обоснование способов чрескостного остеосинтеза при лечении пациентов с доброкачественными опухолями и опухолеподобными поражениями трубчатых костей кисти, обеспечивающих замещение пострезекционного дефекта, восстановление целостности кости, раннюю функциональную реабилитацию пациента.
Работа выполнена с применением клинического, рентгенологического, морфологического методов исследования и математического анализа.
Мы располагаем опытом лечения 19 больных в возрасте от 11 до 63 лет: 10 мужчин и 9 женщин с хондромами коротких трубчатых костей кисти.
У всех пациентов клиникорентгенологический диагноз был верифицирован гистологически. Очаг деструкции был представлен истонченной кортикальной пластинкой, граничащей с полупрозрачным гиалиновым хрящом. Микроскопически опухолевая ткань была представлена атипичным гиалиновым хрящом с неправильным и беспорядочным распределением хондроцитов в основном веществе. Отмечался умеренный полиморфизм клеток с преобладанием одноядерных клеток с крупными ядрами (рис. 1).
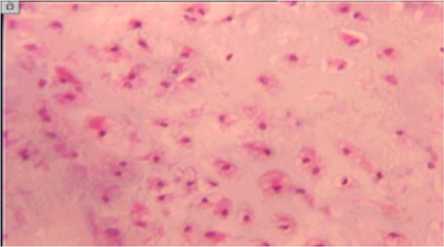
Рис. 1 Парафиновый срез энхондромы проксимальной фаланги, окраска по Ван-Гизону, увеличение – 200
Большинство обследованных пациентов начало заболевания связывало с травмой, чаще всего незначительной. У пяти больных (1 женщина и 4 мужчины) опухолевый процесс осложнился патологическим переломом, локализованным в зоне очага хондромы. До обращения в РНЦ «ВТО» имени академика Г.А. Илизарова все больные получали только консервативное лечение (обезболивание, фиксация гипсовой лонгетой или шиной).
В зависимости от рентген-анатомических вариантов поражения трубчатых костей кисти, выполнялись следующие виды резекции:
внутрикостная резекция - 12 больных;
сегментарная резекция с сохранением хондральной пластинки смежного сустава - 5 больных;
сегментарная резекция трубчатой кости со смежным суставом - 2 больных.
Величина пострезекционных дефектов составляла от 1,0 до 4,5 см (33-70 % от величины контралатеральной кости).
Для возмещения сформированного дефекта использовался свободный аутотрансплантат кортикальной пластины большеберцовой (13) и гребня подвздошной костей (5). В одном случае использовался трансплантат, забранный из метафиза лучевой кости.
В первой группе пациентов после выполнения внутрикостной резекции свободный аутотрансплантат погружали в сформированный дефект. Пораженную кость, трансплантат и фалангу, смежную с пораженным метафизом фиксировали мини-аппаратом Илизарова. Данная компоновка аппарата позволяла осуществлять дозированную компрессию между реплантатом и материнским ложем перемещением промежуточного узла мини-фиксатора. Одновременно осуществляли дозированное растяжение суставной щели (пястнофалангового или межфалангового) в пределах 2-3 мм для профилактики им-мобилизационной контрактуры1. У одного пациента, при осложненном патологическим переломом течении заболевания, одновременно в одном узле мини-аппарата трансоссально фиксировали отломок и внутрикостно расположенный аутотрансплантат2. Данная компоновка аппарата позволяла осуществлять адекватную фиксацию аутотрансплантата и дозированную компрессию на стыке отломков. При выполнении внутрикостной резекции перед коаптацией трансплантата сформированную костную полость обрабатывали этиловым спиртом (экспозиция 3 минуты) и коагулировали.
Свободный аутотрансплантат коаптировался в отломок и суставную поверхность смежной кости (третья группа) или в отломки кости с сохраненными хондральными пластинками (вторая группа).
Трансплантат, дистальный и проксимальный отломки фиксировались мини-аппаратом Или-зарова3. Компоновка аппарата позволяла осуществлять жесткую фиксацию и поддерживающую компрессию на стыке отломков кости и трансплантата весь послеоперационный период.
У одного пациента после внутрикостной резекции энхондромы была выполнена остеотомия пораженной кости через очаг деструкции перед коаптацией костного аутотрансплантата, остеосинтез мини-аппаратом Илизарова, что позволило осуществлять поддерживающую компрессию на стыках трансплантата и костных фрагментов.4
Фиксация в аппарате при внутрикостной резекции продолжалась от 44 до 108 дней (65,6 14,9), при сегментарной – от 62 до113 дней (87,6 12,5). Ранний послеоперационный период исследуемой группы пациентов протекал без осложнений. Послеоперационные раны зажили первичным натяжением, швы снимались на 10-14-е сутки после чрескостного остеосинтеза. Часть больных (8 человек) после заживления послеоперационных ран находились на амбулаторном лечении в поликлинике РНЦ «ВТО» имени академика Г.А. Илизарова, продолжая свою трудовую деятельность. После демонтажа аппарата и удаления спиц у всех пациентов было достигнуто костное сращение трансплантата и реципиентного ложа, полное (100 %) замещение пострезекционного костного дефекта трубчатой кости.
По окончании фиксации в аппарате у пациентов, перенесших сегментарную резекцию очага деструкции со смежным суставом (два наблюдения), отмечалось ограничение амплитуды активных движений в смежных суставах до 35-40о. В меньшей степени страдала функция суставов у больных, которым была выполнена внутрикостная резекция опухолей (двенадцать случаев); активные движения в межфаланговых и пястно-фаланговых суставах были сохранены в объеме 60-90о.
Оценивая исходы лечения всех пациентов, отмечены хорошие (10 наблюдений) и удовлетворительные (9 наблюдений) результаты. Неудовлетворительных результатов не было. Хорошими результатами считались те, когда в отдаленном периоде у пролеченных пациентов не наблюда- лось рецидивов опухолей, отсутствовали ортопедические изъяны, больные возвращались к своей привычной жизни. Удовлетворительными результатами называли те, когда в результате проведенного лечения возникали укорочения сегментов конечностей, деформации, контрактуры суставов кисти, анкилозы суставов. Мы считаем, что в категорию неудовлетворительных результатов следует относить гнойные воспаления, приведшие к удалению трансплантата, своевременно не диагностированные рецидивы опухоли, ампутации, выполненные при возникновении стойких трофических расстройств сегмента. Результаты лечения отслежены в сроки от 6 месяцев до 13 лет.
Для иллюстрации эффективности применения вышеизложенных методик приводим следующие клинические примеры.
Больной П., 20 лет, поступил в клинику Центра с диагнозом: энхондрома проксимальной фаланги II пальца правой кисти. Из анамнеза: в течение двух лет беспокоили периодические боли во II пальце правой кисти, лечения не получал. При поступлении: проксимальная фаланга II пальца утолщена, при пальпации умеренно болезненна. На рентгенограммах: булавовидное вздутие диафиза проксимальной фаланги II пальца - 2,0 см, кортикальный слой истончен, фрагментирован (рис. 2). В клинике Центра выполнена операция: внутрикостная резекция опухоли проксимальной фаланги II пальца правой кисти, остеотомия проксимальной фаланги через очаг деструкции. Костная аутопластика дефекта трансплантатом из крыла подвздошной кости, остеосинтез проксимальной фаланги II пальца мини-аппаратом Илизарова. Размер пострезекционного дефекта составил 2,5 см (рис. 3). На стыке трансплантата с костными фрагментами фаланги поддерживалась компрессия. Срок фиксации в аппарате составил 70 дней. Достигнута консолидация, аппарат демонтирован. На рентгенограмме: пострезекционный дефект замещен, признаки консолидации (рис. 4). Через 6 месяцев результат сохраняется. На контрольных рентгенограммах определяется завершение органотипической перестройки аутотрансплантата. Ограничения движений нет. Больной продолжил обучение в ВУЗе.
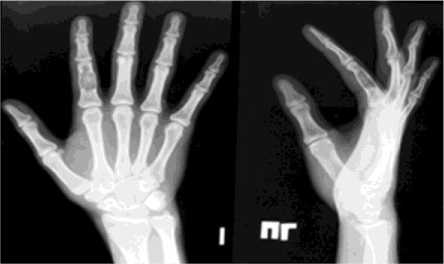
Рис. 2. Рентгенограммы кисти больного П. до лечения
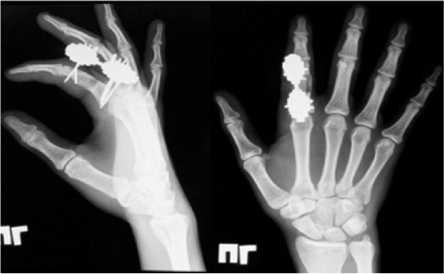
Рис. 3. Рентгенограммы кисти больного П. в процессе фиксации в аппарате
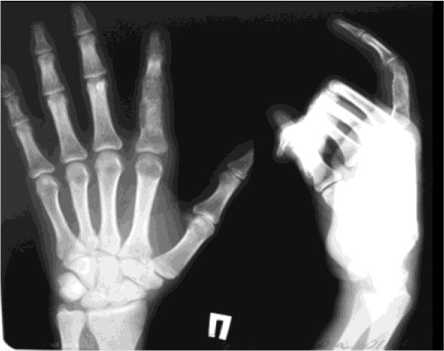
Рис. 4. Рентгенограммы кисти больного П. после лечения
Больная В., 35 лет, поступила в клинику Центра с диагнозом: хондрома средней фаланги IV пальца левой кисти. Из анамнеза: отмечает травму (ушиб) левой кисти, срок с момента травмы не уточняет. Беспокоят боли в IV пальце левой кисти. При поступлении: отек, болезненное утолщение средней фаланги IV пальца левой кисти. На рентгенограмме: признаки энхон-дромы средней фаланги, вздутие, истончение кортикальной пластинки (рис. 5, а). В клинике Центра выполнена операция: сегментарная резекция средней фаланги IV пальца левой кисти, костная аутопластика свободным трансплантатом из гребня левой большеберцовой кости, остеосинтез IV луча мини-аппаратом Илизарова. Пострезекционный дефект составил 1,5 см (рис. 5, б). Поддерживающая компрессия, фиксация в аппарате - 90 дней. Аппарат демонтирован, спицы удалены, достигнуто сращение. На рентгенограмме признаки консолидации костных фрагментов (рис. 5, в). Через 7 месяцев достигнутый ранее результат сохраняется. На контрольных рентгенограммах признаки незавершенной органотипической перестройки аутотрансплантата. Движения в суставах IV пальца: пястно-фаланговом 0о-0о-90о, дистальном межфаланговом 0о-0о-60о. Больная продолжает работать по специальности.
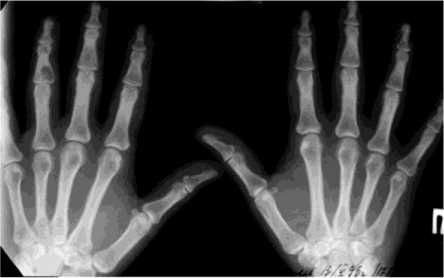
а
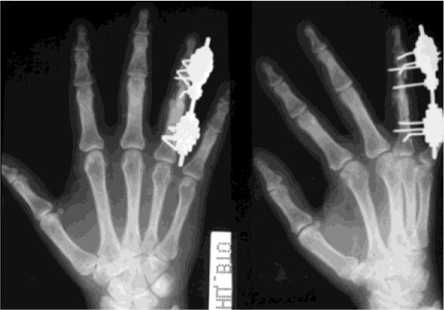
б
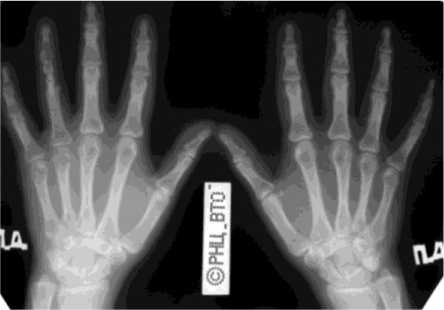
в
Рис. 5. Рентгенограммы кисти больной В.: а - до лечения; б - во время фиксации в аппарате; в - после лечения
Больная С., 45 лет, поступила в клинику Центра с диагнозом энхондрома IV пястной кости правой кисти. Из анамнеза: 4 года назад – перелом IV пястной кости, иммобилизация гипсовой повязкой в течение месяца, достигнута консолидация. Спустя 8 лет появились боли в правой кисти. При поступлении: утолщение IV пястной кости, пальпаторно – боль. Рентгенологически определялось булавовидное вздутие IV пястной кости на протяжении 3,5 см (рис. 6). В клинике Центра выполнена операция сегментарная резекция IV пястной кости на протяжении 4 см, аутопластика дефекта трансплантатом из гребня большеберцовой кости. Остеосинтез IV луча правой кисти мини-фиксатором Илизарова (рис. 7). На стыке трансплантата с фрагментом IV пястной кости и основной фалангой IV пальца поддерживалась компрессия. Фиксация аппаратом - 70 дней. Достигнута кон- солидация. Аппарат демонтирован, спицы удалены. Через 1 год результат лечения сохраняется. Структура трансплантата уплотнилась (рис. 8). Движения в IV пястнофаланговом суставе резко ограничены.
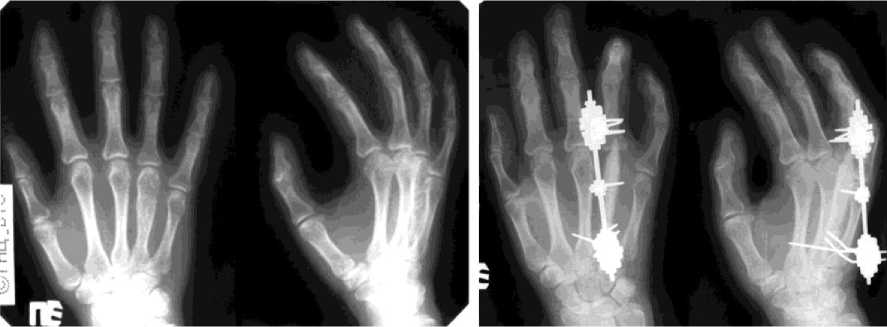
Рис. 6. Рентгенограммы кисти больной С. до лечения
Рис. 7. Рентгенограммы кисти больной С. во время фиксации в аппарате
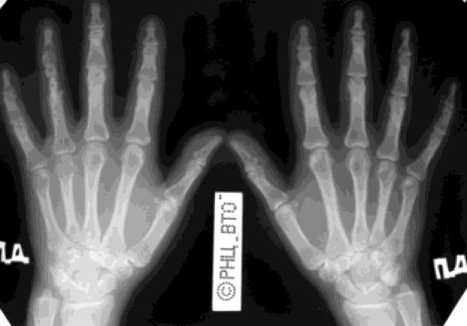
Рис. 8. Рентгенограммы кисти больной С. после лечения
ВЫВОДЫ
Таким образом, несмотря на наш скромный опыт реконструкции трубчатых костей кисти с использованием свободных аутотрансплантатов в условиях чрескостного остеосинтеза, можно сделать ряд предварительных выводов. Замещение дефектов коротких трубчатых костей аутотрансплантатами с использованием чрескостно-го остеосинтеза обеспечивает возможность амбулаторного лечения данной категории пациентов и сохранение социальной и трудовой реабилитации на этапе лечения. Использование для остеосинтеза мини-фиксатора Илизарова обеспечивает жесткую и управляемую фиксацию отломков и трансплантата. Создание и поддержание дозированной компрессии на стыке обеспечивает консолидацию перелома и приращение реплантата к принимающему ложу. Конструктивные особенности аппарата Илизарова позволяют приступить к ранней функциональной нагрузке. Учитывая суб- и тотальный характер пострезекционных дефектов можно говорить о сравнительно небольших сроках остеосинтеза, обеспечивающих восстановление целостности кости за 2-3 месяца. Использование предложенных технологий остеосинтеза и аппаратов внешней фиксации гарантирует полноценную социальную и трудовую реабилитацию пациента на этапе чрескостного остеосинтеза не дожидаясь костного сращения и полноценной органотипической перестройки трансплантата.
Вместе с тем, одним из существенных недостатков свободной аутотрансплантации является длительная органотипическая перестройка реплантатов, связанная с неполноценной реваскуляризацией восстановленной костной ткани, что вполне согласуется с основными литературными данными [3, 10, 11]. По нашим наблюдениям, органотипическая перестройка аутотрансплантатов продолжалась до 1,5-2 лет, особенно длительный процесс ремоделирования претерпевали трансплантаты из компактного слоя большеберцовой кости.


