Особенности формирования сорбционных свойств пектиновых веществ из разных видов тыквы
Автор: Кондратенко Владимир Владимирович, Кондратенко Татьяна Юрьевна
Рубрика: Пищевые ингредиенты, сырье и материалы
Статья в выпуске: 4 т.7, 2019 года.
Бесплатный доступ
Приведены результаты исследования сорбционных пектиновых веществ, выделенных из мякоти плодов тыквы видов Cucurbita maxima (сорта Прикорневая, Мраморная, Волжская серая 92), Cucurbita moschata (сорта Прикубанская 1, Витаминная, Мускатная) и Cucurbita pepo (сорт Старосельская) в момент созревания и в процессе хранения с интервалом 30 дней и предварительно очищенных, по отношению к поливалентным катионам модельного ксенобиотика - Pb2+. Методом комплексонометрического титрования для каждого образца была определена его комплексообразующая способность. Аналитические характеристики (уронидную составляющую, долю свободных карбоксильных групп, амидную составляющую, долю карбоксильных групп, этерифицированных метанолом и ацетильную составляющую) определяли кондуктометрическим титрованием, физико-химические показатели (рН 1%-го водного раствора) определяли потенциометрически. Экспериментально установлено отсутствие явной корреляции между долей свободных карбоксильных групп и комплексообразующей способностью исследованных образцов пектиновых веществ. Также установлено отсутствие значимой корреляции и при учёте амидной составляющей. На основании существующих представлений о механизмах зарядообразования предложена обобщённая математическая модель формирования заряда пектиновых молекул в водных растворах. Анализ решения данной модели показал высокую вероятность участия гидроксильных групп пектиновых веществ в сорбционных процессах. Также установлено, что доля сорбированных катионов, не приходящихся непосредственное взаимодействие с первичными и вторичными функциональными группами, для исследованных образцов составляла от 59,6 до 98,2 % от величины их комплексообразующей способности. На основании результатов моделирования предложено рассматривать сорбционную способность пектиновых веществ как совокупность трёх составляющих - хемосорбции поливалентных катионов первичными функциональными группами, адсорбции катионов за счет частичного заряда, формируемого на поверхности коллоидных частиц при диссоциации гидроксильных групп, а также абсорбции за счет части первоначального катион-содержащего водного раствора, «защемленного» в ячейках оструктуренного осадка. Это следует в обязательном порядке принимать во внимание при определении требований к аналитическим и физико-химическим свойствам пектиновых веществ при использовании их как рецептурного компонента для создания пищевых продуктов функционального и специализированного назначения.
Пектиновые вещества, сорбционные свойства, поливалентные катионы, карбоксильные группы, первичные функциональные группы, вторичные функциональные группы, степень диссоциации, комплексообразующая способность
Короткий адрес: https://sciup.org/147233291
IDR: 147233291 | УДК: 66-922.2:66.974.434:54.04
Peculiarities of sorption properties formation for pectin substances from different species of pumpkin
The investigation results of pectin substances isolated from the pumpkin species Cucurbita maxima (the varieties: Prikornevaya, Mramornaya, Volzhskayaseraya 92), Cucurbitamoschata (the varieties: Prikubanskaya 1, Vitaminnaya, Muskatnaya) and Cucurbitapepo (Staroselskaya variety) at the maturation time and during storage with 30 days’ intervals and carefully purified for sorption properties in relation to Pb2+-cations as model polyvalent ions are shown.Complexing ability for each specimen was determined by the complexometric titration method. Analytical characteristics (uronic component, the count of free carboxyl groups, amide component, the count of the carboxyl groups esterified with methanol and acetyl component) were determined by conductometric titration. Physicochemical parameter (pH of 1 % aqueous solution) was determined potentiometrically. The absence of obvious correlation between the proportion of free carboxyl groups and a complex-forming ability of pectin samples has been established experimentally. Also found no significant influence of amide component on that correlation. Based on the existing notions of charge formation mechanisms the generalized mathematical model of charge pectin molecules in aqueous solutions has been proposed. Analysis of this model solution has shown a high probability of pectic substances hydroxyl groups’ participation in sorption processes. It is also found that the proportion of adsorbed cations are not accounted direct interaction with primary and secondary functional groups for the test samples ranged from 59.6 to 98.2 % of the magnitude of their complexing ability. Based on simulation results it was suggested that sorption ability of pectin may be presented as a assuming of three components -polyvalent cations chemisorption by primary functional groups, cation adsorption due to the partial charge formed on the surface of the colloidal particles by the dissociation of hydroxyl groups as well as absorption due to part of the initial cation-containing aqueous solution “entrapped” in cells structured sediment. It should be mandatory to take into account when determining the requirements for analytical and physicochemical properties of pectin, when used them as a component of a prescription for the creation of functional’ and special purpose’ foods.
Текст научной статьи Особенности формирования сорбционных свойств пектиновых веществ из разных видов тыквы
Одним из эффективных способов придания функциональности пищевым продуктам является введение в их состав ингредиентов, обладающих при последующем попадании в организм человека определенными целевыми свойствами. В качестве одного из подобных ингредиентов могут выступать пектиновые вещества. По своей природе они являются гетерополимерами углеводной природы с достаточно сложным строением. В их состав могут входить до 17 различных остатков нейтральных углеводов и их кислых производных, соединенных друг с другом более чем 20 различными видами гликозидных связей [1,2]. При этом основными структурными компонентами любой пектиновой молекулы являются остатки a-D-галактуроновой кислоты, соединенные в линейную цепь (1→4) гликозидными связями. Каждый из этих остатков имеет в своем составе карбоксильную группу. В соответствии с традиционными представлениями, именно благодаря этим группам пектиновые вещества способны связывать катионы поливалентных металлов, радионуклидов и др. Данная способность пектиновых веществ позволяет рекомендовать их использование в качестве обязательного ингредиента пищевых продуктов, особенно в регионах со сложной экологической ситуацией [3].
Пектиновые вещества представляют собой один из важнейших структурных компонентов первичных клеточных стенок практически всех сухопутных растений. Нативно они могут находиться как в растворенном виде в составе вакуолей и в качестве промежуточных фрагментов, перемещаемых в протоплазме клеток в процессе биосинтеза, так и в виде протопектина – надмолекулярного образования, пронизывающего более или менее плотной сетью первичные и, частично, вторичные клеточные стенки. Всеми функциональными группами протопектин связан с другими компонентами клеточных стенок в единую структуру – матрикс [4–6].
При практическом использовании пектиновых веществ в качестве энтеросорбентов в обязательном порядке следует учитывать, что их сорбционные свойства в максимальной мере проявляются при нахождении пектиновых веществ в растворе в виде гидратированных коллоидов. При этом первичные функциональные – карбоксильные – группы пектиновых веществ нативно могут находиться в одном из трех состояний: свободном, амиди-рованом и этерифицированном метанолом. Из них взаимодействовать с катионами могут только свободные и амидированые [10].
Однако использование только данного подхода не дает удовлетворительной сходимости с экспериментальными данными [8].
Таким образом, целью исследований было изучение особенностей механизмов формирования сорбционных свойств пектиновых веществ на примере пектиновых веществ из тыквы.
Объекты и методы исследований
В качестве объектов исследований использовали пектиновые вещества, выделенные из мякоти плодов тыквы видов Cucurbita maxima (сорта Прикорневая, Мраморная, Волжская серая 92), Cucurbita moschata (сорта Прикубанская 1, Витаминная, Мускатная) и Cucurbita pepo (сорт Старосельская) в момент созревания и в процессе хранения с интервалом 30 дней.
Выделение и очистку образцов пектиновых веществ осуществляли в соответствии с [9]. Для каждого образца методом комплексометрического титрования по [10] определяли комплексообразующую способность по отношению к катионам Pb2+ – способность пектиновых веществ собировать ионы металлов с образованием мало- и/или недиссоциирующих комплексов. Аналитические характеристики образцов (уронидную составляющую, долю свободных карбоксильных групп, амидную составляющую, долю карбоксильных групп, этерифицированных метанолом и ацетильную составляющую) определяли методом кондуктометрического титрования по [11]. Физико-химические показатели (рН 1%-го водного раствора) определяли потенциометрически по [11].
Для каждого образца каждый показатель определяли в пяти повторностях. Отсеивание статистически ненадёжных экспериментальных данных в повторностях и расчёт средних осуществляли в соответствии с [12, 13].
Результаты и их обсуждение
Формирование представлений о процессе комплексообразования пектиновыми веществами в присутствии в растворе катионов поливалентных металлов только за счет проявления хемосорбции максимально просто для понимания, что позволяет утрировать весь
Ком-плек-сооб-разую-щая способность ,
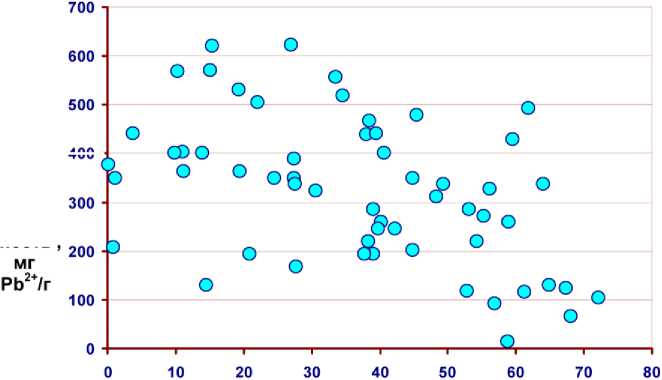
Степень метоксилирования карбоксильных групп, %
Рис. 1. Зависимость комплексообразующей способности пектиновых веществ от степени метоксилирования их карбоксильных групп
процесс до образования малодиссоциирую-щих хеллатов, то есть позволяет рассматривать любой фрагмент пектиновой молекулы как равнозначный другим, имеющим подобный заряд. Такая модель процесса может иметь место только при условии, что рассматриваемые пектиновые молекулы представляют собой короткоцепочечные линейные негибкие структуры с достаточно удаленными друг от друга свободными карбоксильными группами, состоящие только из остатков a-D-галактуроновой кислоты, соединенных (1 ^ 4) гликозидными связями.
Однако результаты экспериментальных исследований, полученные авторами настоящей работы, показали, что, в целом, механизм сорбции значительно сложнее, а представленная выше модель является частным случаем процесса сорбции поливалентных катионов пектиновыми веществами. Такие выводы основаны на отсутствии явной корреляции между долей свободных карбоксильных групп и сорбционной способностью пектиновых веществ (рис. 1).
Более того, даже если учитывать вклад амидной составляющей в процесс сорбции, то и суммарное влияние первичных функциональных групп (амидированых и свободных) слабо коррелирует с величиной комплексообразующей способности, полученной экспериментально (рис. 2).
Следовательно, первичные функциональ- ные группы представляют собой лишь один из нескольких факторов, определяющих суммарное количество поливалентных катионов, сорбируемых пектиновыми веществами в водной среде.
Потенциально на процесс сорбции катионов должна оказывать влияние плотность распределения заряда по поверхности пектиновых молекул. В свою очередь само наличие заряда у пектиновых молекул определено присутствием в их составе групп, способных полностью или частично диссоциировать в водной среде. Для пектиновых молекул таковыми являются уже упоминавшиеся выше свободные и амидированые карбоксильные группы, принадлежащие остаткам a-D-галак-туроновой кислоты, а также гидроксильные группы всех остатков углеводной природы, составляющих пектиновые молекулы. При определении количества последних следует также учитывать, что нейтральные полисахариды, входящие в состав пектиновых молекул, могут содержать по три свободных гидроксильных группы, а остатки a-D-галак-туроновой кислоты - по две. Кроме того, некоторая часть этих групп участвует в образовании эфирной связи с остатками уксусной кислоты. Эта часть, естественно, исключена из зарядообразования всей молекулы, а ее величина определяется ацетильной составляющей.
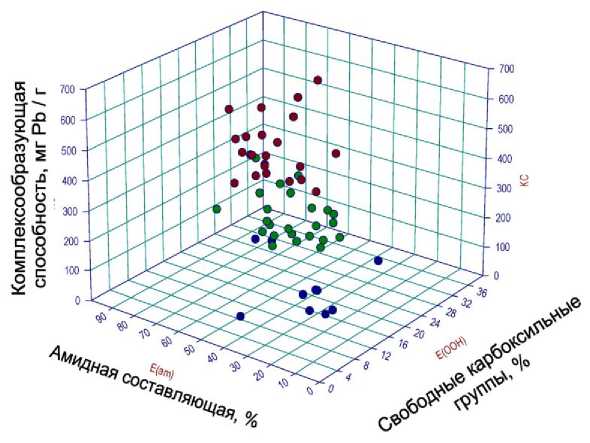
Рис. 2. Совместное влияние свободных карбоксильных групп и амидной составляющей пектиновых веществ на проявление ими комплексообразующей способности
Каждый из указанных факторов зарядо-образования, вследствие некоторой диссоциации в водном растворе, определяет совокупный заряд молекулы, насыщая при этом окружающую среду пропорциональным количеством катионов Н+ , что, в свою очередь, приводит к некоторому снижению величины активной кислотности раствора. При известной концентрации образца пектиновых веществ в растворе, изменении величины активной кислотности, а также аналитических характеристиках пектиновых молекул, несложно получить следующую обобщенную математическую модель зарядообразования пектиновых веществ в растворе:
к он • «он + ^оон • «оон +
+ ^АМ • аАМ = , (1) 10⋅ pect где /сОН, кООН, кАМ - молярные концентрации гидроксильных, свободных карбоксильных и амидных групп, соответственно, в водном растворе, моль/дм3; Д Сн + - молярная концентрация катионов Н+, образующихся при диссоциации первичных и вторичных функциональных групп пектиновых веществ в водном растворе, моль/дм3; Cpect - концентрация образца пектиновых веществ в водном растворе, % масс./об.; аОН, аООН, аАМ - степень диссоциации гидроксильных, свободных карбоксильных и амидных групп, соответственно, в водном растворе, доли единицы.
Решения данного уравнения для каждого отдельного образца пектиновых веществ были выполнены в виде аналитических поверхностей возможных значений степеней диссоциации функциональных групп. Аналитическая поверхность для одного из образцов приведена на рис. 3.
Анализ полученных поверхностей показал, что степень диссоциации вторичных функциональных групп пектиновых веществ - гидроксильных - значимо отличается от нуля. При этом, не смотря на то, что максимальные значения этого показателя в десятки раз меньше максимальных показателей степеней диссоциации первичных функциональных групп, тем не менее, учитывая молярную концентрацию гидроксильных групп в растворе, значительно превосходящую молярные концентрации свободных и амидированых карбоксильных групп, можно утверждать, что процесс сорбции поливалентных катионов пектиновыми веществами складывается не только из доли, приходящейся на хемосорбцию, но также (как минимум) и из доли, приходящейся на активную адсорбцию катионов на поверхности коллоидных частиц, формируемую за счет заряда, образуемого при частичной диссоциации гидроксильных групп галактуронидных остатков и остатков нейтральных углеводов.
Действительно, из анализа поверхностей возможных решений следует, что для иссле-
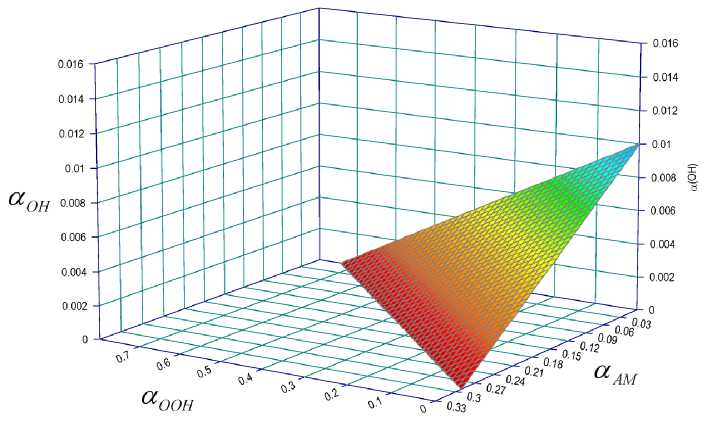
Рис. 3. Аналитическая поверхность возможных значений степеней диссоциации функциональных групп пектиновых веществ в водных растворах
дованных образцов максимально возможные значения степеней диссоциации варьируют следующим образом:
ОН ∈ [0.0025; 0.0211]
ООН G [0.0896; 0.7449]. (2) АМ ∈ [0.0374; 0.4279]
То есть, наравне с хемосорбцией, адсорбция катионов в толще гидратной оболочки молекул пектина также имеет место.
Однако учет поверхностно сорбированных катионов также недостаточен для сходимости с экспериментальными значениями комплексообразующей способности пектиновых веществ.
Так, доля массы сорбированных катионов, не приходящихся ни на хемосорбцию, ни на адсорбцию, для исследованных образцов составляла от 59,6 до 98,2 % от величины комплексообразующей способности. Одним из приемлемых причин такого положения дел, предположительно, может быть «защемление» части катион-содержащего раствора в ячейках, образующихся при формировании оструктуренного осадка, то есть за счет пассивной объемной сорбции катионов - абсорбции. При этом в «защемленных» ячейках катионы, соответственно, находятся в свободном, подвижном состоянии. Такое предположение основано на сравнительно сложной пространственной конфигурации пектиновых молекул в растворе, что подтверждено рядом исследователей [14, 15].
Заключение
Таким образом, механизм сорбции катионов поливалентных металлов пектиновыми веществами является значительно более сложным, чем существующие представления о нем (по крайней мере для пектиновых веществ из различных видов тыквы). Он может рассматриваться даже в упрощенной модели как совокупность трех видов сорбции - хемосорбции поливалентных катионов первичными функциональными группами, адсорбции катионов за счет частичного заряда, формируемого на поверхности коллоидных частиц при частичной диссоциации гидроксильных групп, а также абсорбции за счет части первоначального катион-содержащего водного раствора, «защемленного» в ячейках оструктуренного осадка. Это следует в обязательном порядке принимать во внимание при определении требований к аналитическим и физико-химическим свойствам пектиновых веществ при использовании их как рецептурного компонента для создания пищевых продуктов функционального и специализированного назначения.
В силу широты дисперсии нативных свойств объектов исследований, авторы полагают, что данное заключение может быть экстраполировано и на пектиновые вещества из других видов сырья. В любом случае исследования в данном направлении будут продолжены.
Список литературы Особенности формирования сорбционных свойств пектиновых веществ из разных видов тыквы
- Voragen A.G.J. Pectin, a versatile polysaccharide present in plant cell walls / A.G.J. Voragen, G.-J. Coenen, R.P. Verhoef, H.A. Schols // Struct. Chem. - 2009. - V. 20. - P. 263-275.
- Vincken J.-P. et al. If Homogalacturonan Were a Side Chain of Rhamnogalacturonan I. Implications for Cell Wall Architecture / J.-P. Vincken et al. // Plant Physiology. - 2003. - V. 132. - P. 1781-1789.
- Донченко, Л.В. Пектин: основные свойства, производство и применение / Л.В. Донченко, Г.Г. Фирсов. - М.: ДеЛи принт, 2007. - 276 с.
- Guillemin F. et al. Distribution of Pectic Epitopes in Cell Walls of The Sugar Beet Root / F. Guillemin et al. // Planta. - 2005. - V. 222. - P. 355-371.
- Mohnen, D. Pectin Structure and Biosynthesis / D. Mohnen // Current Opinion in Plant Biology. - 2008. - V. 11. - P. 266-277.
- O'Neill M.A. Rhamnogalacturonan II: Structure and Function of a Borate Cross-Linked Cell Wall Pectic Polysaccharide / M.A. O'Neill, T. Ishii, P. Albersheim, A.G. Darvill // Annu. Rev. Plant Biol. - 2004. - V. 55. - P. 109-139.
- Шамкова, Н.Т. Влияние технологических факторов на свойства пектинов / Н.Т. Шамкова, Г.М. Зайко // Известия Вузов. Пищевая технология. - Краснодар, 2005. - № 2-3. - С. 75-77.
- Кондратенко, В.В. Проявление сорбционных свойств пектиновыми веществами в составе функциональных продуктов питания / В.В. Кондратенко, Т.Ю. Кондратенко // Функциональные продукты питания: ресурсосберегающие технологии переработки сельскохозяйственного сырья, гигиенические аспекты и безопасность: Международная научно-практическая конференция. - Краснодар: КубГАУ, 2009. - С. 216-222.
- Кондратенко, В.В. О влиянии молекулярной массы на проявление сорбционных свойств пектиновыми веществами / В.В. Кондратенко, Т.Ю. Кондратенко // Новые технологии. - Майкоп: МГТУ, 2011. - № 2. - С. 20-26.
- Донченко, Л.В. Методы определения комплексообразующей способности пектиновых веществ: методические указания к лабораторно-практическим занятиям по дисциплине "Технология пектина и пектинопродуктов" / Л.В. Донченко, В.В. Кондратенко, Т.Ю. Кондратенко. - Краснодар: КубГАУ, 2007. - 54 с.
- Нелина, В.В. Пектин. Методы контроля в пектиновом производстве / В.В. Нелина, Л.В. Донченко, Н.С. Карпович, Г.Н. Игнатьева. - Киев, 1992. - 105 с.
- Румшинский, Л.З. Математическая обработка результатов эксперимента: справочное руководство / Л.З. Румшинский. - М.: Гл. ред. физ.-мат. лит-ры изд-ва Наука, 1971. - 192 с.
- Seltman, Y.J. Experimental Design and Analysis / Y.J. Seltman. - 2014. - 414 p.
- Wong, D. Enzymatic Deconstruction of Backbone Structures of the Ramified Regions in Pectins / D. Wong // Protein J. - 2008. - V. 27. - P. 30-42.
- Willats, W.G.T. Pectin: Cell Biology and Prospects for Functional Analysis / W.G.T. Willats, L. McCartney, W. Mackie, J.P. Knox // Plant Molecular Biology. - 2001. - V. 47. - P. 9-27.


