Особенности и отдаленные результаты применения самофиксирующихся имплантов в лечении больных с паховыми грыжами
Автор: Харитонов С.В., Родоман Г.В., Харитонов С.С., Зинякова М.В.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 1 (53), 2017 года.
Бесплатный доступ
Проведено проспективное исследование с целью изучения результатов пластики пахового канала с применением самофиксирующегося имплан- та ParieteneTM ProGripTM. Выявлено, что интенсивность и продолжительность боли в раннем послеоперационном периоде, местные тканевые реак- ции и ультразвуковая картина раневого процесса принципиально не отличается от наблюдений использования легких макропористых композици- онных полипропиленовых сеток. Основные различия в результатах лечения зарегистрированы в отдаленном послеоперационном периоде. Отличия характеризовались низкими показателями частоты возникновения боли и стойкой парестезии, степени ограничения физических нагрузок, ранней нормализацией показателей физического и психологического компонентов здоровья.
Паховая грыжа, герниопластика, имплант, хроническая боль, качество жизни
Короткий адрес: https://sciup.org/142211295
IDR: 142211295 | УДК: 617.55-089.844
Текст научной статьи Особенности и отдаленные результаты применения самофиксирующихся имплантов в лечении больных с паховыми грыжами
В течение последних десятилетий пластика пахового канала по методике Лихтенштейна остается наиболее распространенным видом хирургического вмешательства в лечении больных с паховыми грыжами [2, 3, 8]. При ее выполнении с высокой степенью эффективности применяются синтетические импланты, имеющие различную пространственную структуру, химический состав и характер плетения нити [1, 6, 10].
Однако изучение причин возникновения хронической боли у оперированных больных привело к появлению многочисленных работ по изучению вопросов фиксации сетки. Исследования показали, что сопутствующие фиксации ущемление периферических нервов и деформация импланта при его организации являются ключевыми моментами в патогенезе хронической боли [4, 5, 7]. Все это привело к тому, что при проведении операции Лихтенштейна наметилась устойчивая тенденция применения хирургами имплантов не требующих их фиксации [9, 11].
Целью исследования явилось изучение ближайших и отдаленных результатов лечения больных с паховыми грыжами, пластика пахового канала которым проводилась с применением имплантов, не требующим их фиксации к тканям шовным материалом.
Материал и методы
В исследование включено 65 больных. В группу исследования вошло 34 пациента с паховыми грыжами, пластика пахового канала которым была выполнена с применением самофиксирующегося композиционного полипропиленового импланта (ParieteneTM ProGripTM; Covidien). Группу сравнения составил 31 больной. У этой группы пациентов при проведении оперативного вмешательства были использованы легкие макропористые композиционные полипропиленовые сетки (UltraproTM; Ethicon). Пластику пахового канала выполняли по методике Лихтенштейна. Фиксация импланта у больных группы сравнения проводилась полипропиленовой нитью. Частичную фиксацию сетки пациентов группы исследования для улучшения ее адаптации выполняли только в 4 (11,8 %) клинических наблюдениях, используя 1-2 отдельных полипропиленовых шва в области купперовой связки или надкостницы лонного бугорка. Обе анализируемые группы были представлены мужчинами и были сопоставимы по возрасту и типу паховой грыжи. При этом необходимо отметить, что наибольшее количество оперированных пациентов приходилось на старшие возрастные группы (51 год – 60 лет: 18 (27,7%) больных; 61 год и более - 26 (40,0%) больных). В соответствии с EHS Classification for Inguinal Hernia у больных в 38 клинических наблюдениях (L1 – 23,1 %, L2 – 29,2 %, L3 – 6,2 %) имелись косые, а у 27 пациентов (M1 – 9,2 %, M2 – 21,5 %, M3 – 10,8 %) – прямые паховые грыжи. Наличие рецидивной
грыжи являлось признаком исключения из данного исследования.
Всем оперированным больным в раннем послеоперационном периоде проводили мониторирование интенсивности боли с применением визуально-аналоговой шкалы -ВАШ (Visual Analog Scale, VAS). Ультразвуковое исследование мягких тканей «зоны оперативного вмешательства» выполняли в B-режиме сканирования перед выпиской больного из стационара (2-3 сутки). Под «зоной оперативного вмешательства» понимали область пластики пахового канала.
В отдаленном послеоперационном периоде (через 3, 6 месяцев и 1 год) проводили клинический осмотр пациентов и дополняли его оценкой качества жизни с использованием протокола SF-36 (SF-36 Health Status Survey). Под критическим нарушением качества жизни пациентов понимали снижение показателя здоровья от популяционной нормы более чем на 75 %, под значительным – более чем на 50-75 %, под умеренным – более чем на 25 %, а под незначительным – менее 25 %.
Результаты и обсуждение
Анализ результатов лечения оперированных больных позволил выявить следующие закономерности. Интенсивность и продолжительность боли в раннем послеоперационном периоде у пациентов обоих клинических групп статистически не отличались между собой (рис. 1). При этом максимальная интенсивность боли у пациентов обоих групп исследования в 1-ые сутки после выполнения оперативного вмешательства по шкале ВАШ не превышала 30% (от 29,0 % до 26,3 %), что не требовало введения наркотических аналгетиков. В последующем интенсивность боли у больных прогрессивно снижалась, составляя на 2-ые сутки послеоперационного периода 17,8 % и 14,3 %, а на 3-ие сутки – 11,2 % и 9,9 %. Имеющийся уровень интенсивности боли и ее динамика позволяли практически во всех клинических наблюдениях выписывать больных на амбулаторное
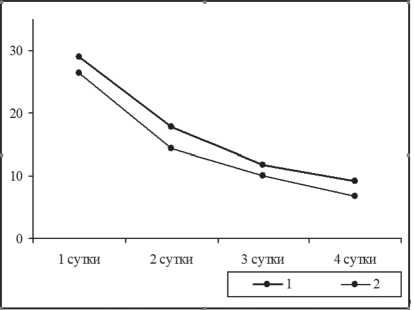
Рис. 1. Интенсивность боли в раннем послеоперационном периоде.
1 – исследуемая группа, 2 – группа сравнения долечивание на 2-3 сутки после выполнения пластики пахового канала.
Ультразвуковая картина «зоны оперативного вмешательства» у пациентов анализируемых групп имела незначительные отличия (таблица 1). Во всех ультразвуковых наблюдениях синтетические полипропиленовые импланты имели гиперэхогенный характер, который отчетливо позволял дифференцировать их от окружающих фасциальноапоневротических образований. Однако при проведении сравнительной оценки имплантов больных группы исследования нами отмечена их более высокая эхогенность по сравнению с имеющейся у больных контрольной группы. По нашему мнению, это различие определялось менее крупным размером ячеек плетения самофиксирующихся сеток (1,0-1,6 мм по сравнению 3-4 мм) при сопоставимой толщине полипропиленовых волокон (130 мкм и 120 мкм).
Полипропиленовый имплант у большинства осмотренных больных визуализировался в виде линейной структуры, и только лишь у части пациентов отмечалась его волнистая форма. Более низкая частота визуализации волнистой формы сетки зарегистрирована нами у пациентов исследуемой группы, что, по всей видимости, было связано с более высоким удельным весом самофиксирующегося импланта (80 г/м2 по сравнению с 28 г/м2), его манипуляционными свойствами оптимальной адаптацией с тканями задней стенки пахового канала.
Таблица 1
Ультразвуковые критерии раневого процесса больных после выполнения пластики пахового канала с различной фиксацией имплантов
|
Критерии оценки |
Самофиксирующийcя имплант |
Фиксация импланта |
|
(n=16) |
(n=13) |
|
|
Имплант |
||
|
линейная форма (%) |
87,5±2,2 |
76,9±3,5 |
|
волнистая форма (%) |
12,5±2,2* |
23,1±3,5 |
|
толщина (мм) |
2,1±0,4* |
1,3±0,2 |
|
Скопления жидкости в зоне импланта |
||
|
частота визуализации (%) |
56,3±3,3 |
61,5±4,1 |
|
толщина (мм) |
3,3±1,4 |
3,6±1,2 |
|
Неоднородность клетчатки (%) |
100 |
100 |
|
Скопления жидкости в клетчатке |
||
|
частота визуализации (%) |
37,5±3,2 |
38,5±3,9 |
|
длина (мм) |
24,0±8,7 |
21,5±7,1 |
|
толщина (мм) |
10,8±7,6 |
8,6 ±2,4 |
- различие статистически достоверное (p <0,05).
іУІОСКОВСКИЙ
Л/ ру ргически й
/ТХурнал
Толщина визуализированных имплантов практически не менялась в зависимости от сроков выполнения хирургического вмешательства, находясь в пределах от 1,7 до 2,5 мм у пациентов исследуемой группы и от 1,1 до 1,5 мм у больных группы сравнения. И только лишь в ультразвуковых наблюдениях бесшовной пластики размеры импланта в области его фиксирующего клапана имели значительную вариабельность из-за выраженной размытости контуров.
В большинстве ультразвуковых наблюдений в зоне визуализации имплантов отмечалось наличие ограниченных скоплений жидкости, которые располагались преимущественно по его верхнему контуру. Частота их визуализации у больных обеих групп статистически не отличалась между собой, составляя 56,3 % и 61,5 %. Толщина диагностированных скоплений жидкости также не зависела от характера использованного импланта, варьируя от 1,9 до 4,8 мм.
Подкожная жировая клетчатка в «зоне оперативного вмешательства» у всех больных имела выражено диффузный неоднородный характер. Частота визуализации в ней ограниченных скоплений жидкости не отличалась от вида имплантированной сетки, составляя 37,5 % у пациентов группы исследования и 38,5 % у больных группы сравнения. Аналогичная закономерность отмечена и при анализе их размеров (24,010,8 мм и 21,5±8,6 мм).
Основные отличия в результатах лечения сформированных групп были зарегистрированы в отдаленном послеоперационном периоде.
При проведении клинического осмотра у всех 65 оперированных больных рецидива грыжевого образования выявлено не было. Однако, у 2 (5,9 %) пациентов исследуемой группы и 1 (3,2 %) больного группы сравнения в сроки от 6 месяцев до 1 года нами было зарегистрировано формирование грыжевого образования на контралатеральной стороне. Анализ причин развития грыжевого образования этих пациентов показал, что данные клинические наблюдения приходились на пациентов старших возрастных групп с высокой степенью физической активности и клиническими проявлениями атрофии мышц передней брюшной стенки.
Данные клинических осмотров пациентов показали, что отказ от шовной фиксации импланта при выполнении пластики пахового канала сопровождался более низкими, статически достоверными, показателями частоты возникновения боли в области «зоны оперативного вмешательства» (таблица 2). Так через 3 месяца после выполнения герниопластики боль при физических нагрузках и в покое отмечало в 2 раза меньшее количество пациентов исследуемой группы по сравнению с группой сравнения (20,0±2,1 % и 40,0±3,5 %). К 6-му месяцу послеоперационного периода показатели частоты возникновения боли у пациентов обоих групп практически не отличались (26,3±2,4 % и 27,5±2,6 %), а через 1 год после пластики пахового канала они статистически достоверно возникали в 2,7 раза чаще у больных при применении шовной фиксации (23,1±1,7 % и 62,6±2,1 %).
Таблица 2
Результаты клинических осмотров пациентов в отдаленном послеоперационном периоде
|
Критерии оценки (%) |
Самофиксирующийся имплант (n=34) |
Фиксация импланта (n=31) |
|
Боль в области пластики |
||
|
3 месяца |
20,0 ± 2,1* |
40,0 ± 3,5 |
|
6 месяцев |
26,3 ± 2,4 |
27,5 ± 2,6 |
|
1 год |
23,1 ± 1,7* |
62,6 ± 2,1 |
|
Ограничение физических нагрузок |
||
|
3 месяца |
20,0 ± 2,1* |
33,3 ± 3,4 |
|
6 месяцев |
21,1 ± 2,3 |
26,3 ± 2,4 |
|
1 год |
3,9 ± 0,8* |
33,3 ± 2,0 |
|
Стойкая парестезия |
||
|
3 месяца |
55,0 ± 2,6* |
46,7 ± 3,6 |
|
6 месяцев |
21,1 ± 2,3* |
42,1 ± 2,7 |
|
1 год |
23,1 ± 1,7 |
20,8 ± 1,8 |
- различие статистически достоверное (p <0,05).
Частота ограничения физических нагрузок в отдаленном послеоперационном периоде также отличалась у больных, пластика пахового канала которым выполнялась с применением самофиксирующихся имплантов. В связи с наличием дискомфорта в области герниопластики физические нагрузки через 3 месяца после выполнения операции ограничивал каждый пятый пациент группы исследования (20,0±2,1 %) и каждый третий больной группы сравнения (33,3±3,4 %). К 6-ому месяцу послеоперационного периода показатели ограничения физической нагрузки в обеих наблюдаемых группах практически не отличались между собой (21,1±2,3 % и 26,3±2,4 %), в последующем статистически достоверно увеличиваясь (через 1 год) только лишь у больных группы сравнения (3,9±0,8 % и 33,3±2,0 %).
Стойкая парестезия кожных покровов в области хирургического доступа через 3 месяца после выполнения оперативного вмешательства у анализируемых групп пациентов имела незначительные отличия, при этом ее частота у больных исследуемой группы (55,0±2,6 %) лишь в 1,2 раза превышала аналогичный показатель (46,7±3,6 %) группы сравнения. Через 6 месяцев после выполнения пластики частота парестезии при применении самофиксирующегося имела более прогрессивное снижение по сравнению с больными контрольной группы (21,1±2,3 % и 42,1±2,7%), сохраняя в дальнейшем свой достигнутый уровень до окончания первого года наблюдений (23,1±1,7 % и 20,8±1,8 %).
Полученные показатели частоты возникновения боли в области герниопластики, степени снижения физической
активности пациентов и стойкой парестезии кожных покровов нашли свое закономерное отражение при изучении качества жизни больных в отдаленном послеоперационном периоде.
Как видно из представленных диаграмм, до выполнения оперативного вмешательства у пациентов обоих анализируемых групп имелась умеренная компрессия профиля качества жизни, которая находилась в пределах от 50 % до 75 % популяционной нормы (рис. 2). После выполнения пластики на всех временных интервалах исследования компрессия профиля качества жизни прогрессивно уменьшалась и достигала к 1-ому году послеоперационного периода своих минимальных величин.
При проведении детального анализа групповых показателей качества жизни было отмечено, что более быстрая нормализация показателей как физического, так и психологического компонентов здоровья была зарегистрирована у пациентов группы исследования. Так уже через 3 месяца после выполнения оперативного вмешательства показатели физического функционирования (Physical Functioning - PF), ролевого функционирования, обусловленного физическим состоянием (Role-Physical Functioning - RP), и жизненной активности (Vitality - VT) превышали аналогичные показатели больных группы сравнения на 6,3 - 34,6 %. К 6-ому месяцу послеоперационного периода показатели качества жизни имели тенденцию к дальнейшему увеличению, с последующим, более выраженным позитивным ответом на лечение (1,7 - 15,4 %) в группе пациентов с применением самофиксирующегося импланта.
Учитывая общее количество включенных в исследование больных и достаточно выраженную их внутригрупповую разнородность, закономерным на наш взгляд явился сравнительный анализ структуры их качества жизни в зависимости от степени его снижения (таблица 3). Как видно из представленных в таблице материалов, до выполнения оперативного вмешательства показатели степени снижения качества жиз-
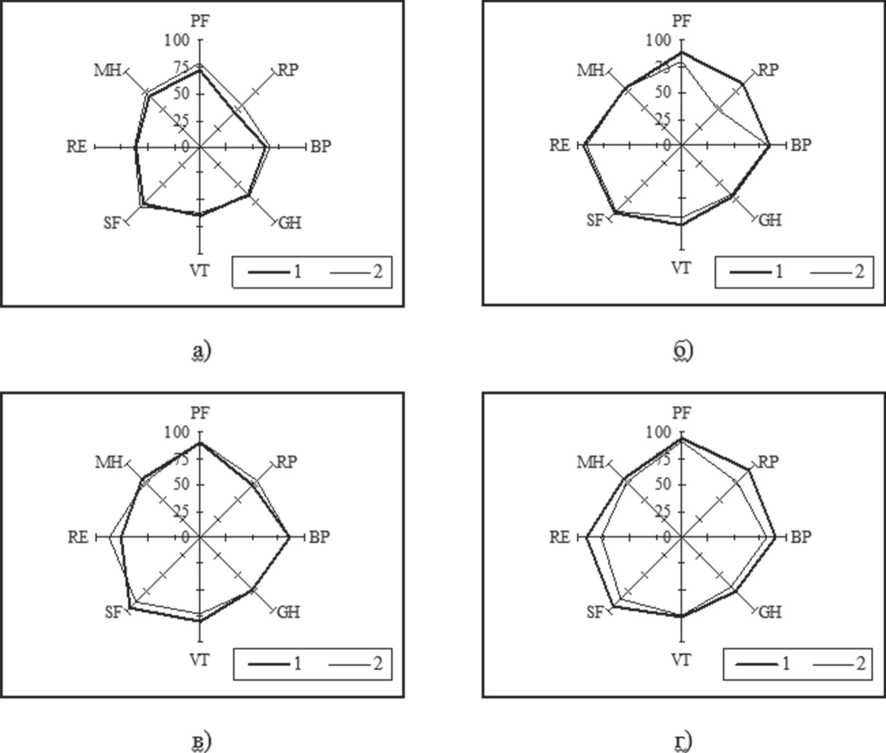
Рис. 2. Качество жизни пациентов с паховыми грыжами после выполнения пластики пахового канала. а – до выполнения оперативного вмешательства, б - через 3 месяца, в – через 6 месяцев, г – через 1 год после операции: 1 – исследуемая группа, 2 – группа сравнения
Таблица 3
Распределение больных в зависимости от степени снижения качества жизни после выполнения пластики пахового канала
|
Критерии оценки (%) |
Самофиксирующийся имплант (n=34) |
Фиксация импланта (n=31) |
|
До выполнения пластики |
||
|
критическое |
32,36 ± 1,42 |
31,03 ± 1,65 |
|
значительное |
29,41 ± 1,38 |
20,69 ± 1,45 |
|
умеренное |
23,52 ± 1,28 |
27,59 ± 1,60 |
|
незначительное |
14,71 ± 1,07 |
20,69 ± 1,45 |
|
Через 3 месяца |
||
|
критическое |
5,26 ± 1,24 |
6,66 ± 1,78 |
|
значительное |
10,53 ± 1,70* |
40,00 ± 3,50 |
|
умеренное |
21,05 ± 2,27* |
26,67 ± 0,61 |
|
незначительное |
63,16 ± 2,68* |
26,67 ± 0,61 |
|
Через 6 месяцев |
||
|
критическое |
11,11 ± 1,85* |
0 |
|
значительное |
16,67 ± 1,19* |
26,32 ± 2,45 |
|
умеренное |
11,11 ± 1,85* |
36,84 ± 2,68 |
|
незначительное |
61,11 ± 2,87* |
36,84 ± 2,68 |
|
Через 1 год |
||
|
критическое |
3,85 ± 0,77* |
12,50 ± 1,44 |
|
значительное |
3,85 ± 0,77* |
20,84 ± 1,77 |
|
умеренное |
34,62 ± 1,90 |
33,33 ± 2,05 |
|
незначительное |
57,68 ± 1,98* |
33,33 ± 2,05 |
- различие статистически достоверное (p <0,05).
ни больных обеих групп практически не отличались между собой. При этом критическое и значительное снижение качества жизни было выявлено у 61,8 % больных группы исследования и 51,8 % пациентов группы сравнения.
Через 3 месяца после выполнения пластики пахового канала отмечена выраженная закономерность уменьшения (до 6,2 и 4,7 раз) количества пациентов с критическим снижением качества жизни. При применении самофиксирую-щегося импланта изменение структуры больных в основном происходило за счет роста количества пациентов с незначительным снижением показателей, а использование шовной методики фиксации импланта сопровождалось увеличением числа больных с более выраженными ограничениями.
К 6-ому месяцу послеоперационного периода показатели качества жизни исследуемой группы пациентов принципиально не менялись, в то время как у больных контрольной группы исследования имелось увеличение (в 1,4 раза) частоты умеренной и незначительной степеней снижения качества жизни с уменьшением (в 1,8 раза) частоты значительных и критических нарушений.
К окончанию 1 года динамического наблюдения применение бесфиксационной пластики пахового канала позволило достигнуть у 92,3 % оперированных больных умеренной или незначительной степени снижения качества жизни, что в 1,4 раза превышало аналогичные показатели пациентов с применением классической фиксационной методики герниопластики по Лихтенштейну.
Таким образом, изучение ближайших и отдаленных результатов хирургического лечения больных с паховыми грыжами с применением имплантов с различным типом фиксации позволило выявить, что использование самофик-сирующихся сеток имеет клинические преимущества по сравнению классической фиксационной методикой пластики пахового канала по Лихтенштейну. Основные отличия применения самофиксирующихся имплантов заключаются в более низкой частоте возникновения боли и парестезий в «зоне оперативного вмешательства», а также снижении степени ограничений физических нагрузок в отдаленном послеоперационном периоде. В свою очередь, имеющаяся высокая степень комфорта данной категории оперированных больных обуславливает более быструю нормализацию их показателей как физического, так и психологического компонентов здоровья. Отсутствие значимых отличий в течение раннего послеоперационного периода больных, на наш взгляд, определяется степенью травматичности выполненной герниопластики и характером течения раневого процесса, не завися от типа фиксации импланта.
Выводы
Применение самофиксирующихся имплантов у пациентов с паховыми грыжами при проведении пластики пахового канала позволяет уменьшить в отдаленном послеоперационном периоде частоту возникновения боли и парестезий в зоне оперативного вмешательства, а также степень ограничений физических нагрузок. Высокая степень комфорта данной категории оперированных больных обуславливает более быструю нормализацию их показателей как физического, так и психологического компонентов здоровья. Результаты применения самофиксирующихся имплантов позволяют рекомендовать их для пластики пахового канала для наиболее быстрой трудовой и социальной реабилитации больных.
Список литературы Особенности и отдаленные результаты применения самофиксирующихся имплантов в лечении больных с паховыми грыжами
- Awad SS, Yallampalli S, Srour AM, et al. Improved outcomes with the Prolene Hernia System mesh compared with the time-honored Lichtenstein onlay mesh repair for inguinal hernia repair. Am. J. Surg. 2007;194(2):274.
- Beltrán MA, Cruces KS. Outcomes of Lichtenstein hernioplasty for primary and recurrent inguinal hernia. World J. Surg. 2006;30(12);2281-2287.
- Droeser RA, Dell-Kuster S, Kurmann A, et al. Long-term follow-up of a randomized controlled trial of Lichtenstein's operation versus mesh plug repair for inguinal hernia. Ann. Surg. 2014;259(5):966-972.
- Fortelny RH, Petter-Puchner AH, Redl H, et al. Assessment of Pain and Quality of Life in Lichtenstein Hernia Repair Using a New Monofilament PTFE Mesh: Comparison of Suture vs. Fibrin-Sealant Mesh Fixation. Front. Surg. 2014;28(1);45.
- Hallén M, Sevonius D, Westerdahl J, et al. Risk factors for reoperation due to chronic groin postherniorrhaphy pain. Hernia. 2015;19(6);863-869.
- Magnusson J, Nygren J, Thorell A. Lichtenstein, prolene Hernia system, and Ultrapro Hernia System for primary inguinal Hernia repair: one-year outcome of a prospective randomized controlled trial. Hernia. 2012;16(3):277-285.
- Nikkolo C, Lepner U. Chronic pain after open inguinal hernia repair. Postgrad. Med. 2016;128(1):69-75.
- Nordin P, Bartelmess P, Jansson C, et al. Randomized trial of Lichtenstein versus Shouldice hernia repair in general surgical practice. Br. J. Surg. 2002;89(1):45-49.
- Porrero JL, Cano-Valderrama O, Castillo MJ, Alonso MT. Proposed technique for inguinal Hernia repair with self-gripping mesh: avoiding fixation to undesired structures. Hernia. 2015;19(5);771-774.
- Ramshaw B, Abiad F, Voeller G, et al. Polyester (Parietex) mesh for total extraperitoneal laparoscopic inguinal hernia repair: initial experience in the United States. Surg. Endosc. 2003;17(3):498-501.
- Sanders DL, Nienhuijs S, Ziprin P, et al. Randomized clinical trial comparing self-gripping mesh with suture fixation of lightweight polypropylene mesh in open inguinal hernia repair. Br. J. Surg. 2014;101(11):1373-1382.
- Awad SS, Yallampalli S, Srour AM, et al. Improved outcomes with the Prolene Hernia System mesh compared with the time-honored Lichtenstein onlay mesh repair for inguinal hernia repair. Am. J. Surg. 2007;194(2):274.
- Beltrán MA, Cruces KS. Outcomes of Lichtenstein hernioplasty for primary and recurrent inguinal hernia. World J. Surg. 2006;30(12);2281-2287.
- Droeser RA, Dell-Kuster S, Kurmann A, et al. Long-term follow-up of a randomized controlled trial of Lichtenstein's operation versus mesh plug repair for inguinal hernia. Ann. Surg. 2014;259(5):966-972.
- Fortelny RH, Petter-Puchner AH, Redl H, et al. Assessment of Pain and Quality of Life in Lichtenstein Hernia Repair Using a New Monofilament PTFE Mesh: Comparison of Suture vs. Fibrin-Sealant Mesh Fixation. Front. Surg. 2014;28(1);45.
- Hallén M, Sevonius D, Westerdahl J, et al. Risk factors for reoperation due to chronic groin postherniorrhaphy pain. Hernia. 2015;19(6);863-869.
- Magnusson J, Nygren J, Thorell A. Lichtenstein, prolene Hernia system, and Ultrapro Hernia System for primary inguinal Hernia repair: one-year outcome of a prospective randomized controlled trial. Hernia. 2012;16(3):277-285.
- Nikkolo C, Lepner U. Chronic pain after open inguinal hernia repair. Postgrad. Med. 2016;128(1):69-75.
- Nordin P, Bartelmess P, Jansson C, et al. Randomized trial of Lichtenstein versus Shouldice hernia repair in general surgical practice. Br. J. Surg. 2002;89(1):45-49.
- Porrero JL, Cano-Valderrama O, Castillo MJ, Alonso MT. Proposed technique for inguinal Hernia repair with self-gripping mesh: avoiding fixation to undesired structures. Hernia. 2015;19(5);771-774.
- Ramshaw B, Abiad F, Voeller G, et al. Polyester (Parietex) mesh for total extraperitoneal laparoscopic inguinal hernia repair: initial experience in the United States. Surg. Endosc. 2003;17(3):498-501.
- Sanders DL, Nienhuijs S, Ziprin P, et al. Randomized clinical trial comparing self-gripping mesh with suture fixation of lightweight polypropylene mesh in open inguinal hernia repair. Br. J. Surg. 2014;101(11):1373-1382.


