Особенности изменения цитокинов в хронических гнойных ранах
Автор: Азизов Д.Т., Мирзаев К.К., Алейник В.А., Бабич С.М.
Журнал: Экономика и социум @ekonomika-socium
Рубрика: Основной раздел
Статья в выпуске: 11-1 (90), 2021 года.
Бесплатный доступ
Целью исследования было изучить особенности изменения содержания цитокинов в хронических гнойных ранах. В смывах послеоперационных и гнойных ран исследовали провоспалительные - интерлейкин-1бета (ИЛ-1бета), фактор некроза опухолей-α (TNF-α), и противовоспалительные - интерлейкин -10 (ИЛ-10), секреторные Ig A, а также трансформирующий фактор роста-β1 (TGF-β) методом ИФА. Получены следующие результаты: в послеоперационных ранах показатели провоспалительных интерлейкинов были ниже противовоспалительных интерлейкинов и транформирующего фактора β. В тоже время в хронических гнойных ранах отмечалось значительное увеличение провоспалительных интерлейкинов и снижение противовоспалительных интерлейкинов, а также транформирующего фактора β, по сравнению с таковыми данными послеоперационных ран. Тем самым, создается выраженное нарушение равновесия и отмечается дисбаланс цитокинов провоспалительных и противовоспалительных интерлейкинов. Это способствует снижению заживления и хронизации воспалительного процесса хронических гнойных ран.
Цитокины, чистые раны, хронические гнойные раны, провоспалительные интерлейкины, противовоспалительные интерлейкины, заживление ран, воспалительный процесс.
Короткий адрес: https://sciup.org/140261229
IDR: 140261229 | УДК: 616-001.4-002.3-08
Features of change of cytokines in chronic purulent wounds
The aim of the study was to study the features of changes in the content of cytokines in chronic purulent wounds. In the washings of postoperative and purulent wounds, pro-inflammatory - interleukin-1beta (IL 1beta), tumor necrosis factor-α (TNF-α), and anti-inflammatory - interleukin-10 (IL-10), secretory Ig A, as well as transforming growth factor -β1 (TGF-β) by ELISA. The following results were obtained: in postoperative wounds, the indicators of pro-inflammatory interleukins were lower than anti-inflammatory interleukins and transforming factor β. At the same time, in chronic purulent wounds, there was a significant increase in pro-inflammatory interleukins and a decrease in anti-inflammatory interleukins, as well as transforming factor β, compared with those of postoperative wounds. Thus, a pronounced imbalance is created and an imbalance of cytokines of pro-inflammatory and antiinflammatory interleukins is noted. This helps to reduce the healing and chronicity of the inflammatory process of chronic purulent wounds.
Текст научной статьи Особенности изменения цитокинов в хронических гнойных ранах
Актуальность. Изучить роль провоспалительных и противовоспалительных цитокинов в активации или подавлении протеаз в раневой среде стремились многие исследователи. Цитокины - это небольшие белки (8-15 кДа), которые включают хемокины, колониестимулирующие факторы (CSF), интерфероны (IFN), интерлейкины (IL) и факторы некроза опухоли (TNF-a) и высвобождаются в ответ на повреждение тканей. Многие функции, выполняемые цитокинами, включают активацию фагоцитарных клеток, противовирусную и антипаразитарную активность, хемотаксис нейтрофилов и Т-клеток, рост колоний макрофагов и пролиферацию В- и Т-клеток. На отложение соединительной ткани во время процесса заживления ран может влиять TNF-a, поскольку этот цитокин влияет на синтез коллагена, матриксные металлопротеиназы ( ММП) и тканевых ингибиторов металлопротеиназ (ТИМП) [9]. Были подчеркнуты различия в уровнях провоспалительных цитокинов в раневых жидкостях между острыми и хроническими ранами человека [15].
С другой стороны, IL-1a, другой воспалительный цитокин, индуцировал продукцию как ММП, так и ТИМП [5]. Эти результаты, однако, варьировались в зависимости от источника используемых фибробластов и концентрации цитокинов, что указывает на более сложный эффект на модуляцию и регуляцию протеазы. Кроме того, [14] обнаружено, что противовоспалительный цитокин IL-10 влияет на активность ММП; Ил-10- / ' мыши продемонстрировали повышенную активность ММП, которая, в свою очередь, опосредует усиление индуцированного ишемией ангиогенеза через фактор роста эндотелия сосудов.
Помимо этого, цитокины представляют собой идеальную мишень для бактерий в преодолении иммунной системы хозяина, и было обнаружено, что ряд бактериальных протеаз способен разрушать цитокины и их рецепторы [10]. Протеазы также могут препятствовать активности ряда цитокинов, а также способны вызывать деградацию цитокинов [13]. Протеазы некоторых граммположительнх бактерий, также могут влиять на активность цитокинов, расщеплять предшественник IL-1 с получением биологически активного IL-1, являющегося медиатором воспаления [6]. Было обнаружено, что ряд протеаз разрушает IL-8 [7] . Учитывая, что IL-8 опосредует миграцию и активацию нейтрофилов, это может быть вредным для иммунного ответа хозяина. Протеазы, граммположительных бактерий, также могут нарушать функцию IL-8. Сериновые протеазы бактерий могут модулировать синтез IL-8 [11]
Кроме того функция бактериальных протеаз в преодолении иммунной системы хозяина заключается в деградации иммуноглобулинов хозяина [13]. Это может быть особенно вредным для хозяина, учитывая роль иммуноглобулинов в распознавании и способствовании нейтрализации вторгающихся микроорганизмов [1].
В совокупности все эти данные подчеркивают сложную природу регуляции и модуляции цитокинов и протеаз в раневой среде, что подчеркивает необходимость продолжения исследований с целью их терапевтической коррекции.
Цель исследования: изучить особенности изменения содержания цитокинов в хронических гнойных ранах.
Материал и методы. В работе были обследованы в первой группе 12 больных с послеоперационными ранами (контроль) и во второй группе 15 больных с гнойными ранами (опыт). У всех больных в диагнозе отсутствовали сердечно-сосудистые заболевания, диабет и метаболические изменения. Материал для исследования получали путем сбора смывов стерильным физиологическим раствором с поверхности послеоперационных и гнойных ран.
В составе смывов послеоперационных и гнойных ран исследовали провоспалительные - интерлейкин-1бета (ИЛ-1бета), фактор некроза опухолей-α (TNF-α), и противовоспалительных - интерлейкин -10 (ИЛ-10), методом ИФА с применением тест-систем ЗАО “Вектор-Бест”, а также трансформирующего фактора роста-β1 (TGF-β) методом ИФА с использованием тест-систем «DRG» Германия.
Полученные данные подвергались статистической обработке с использованием стандартных программ Microsoft Excel 2007 c вычислением средних величин (М), их ошибок (m), а также коэффициента достоверности разности средних величин Стьюдента-Фишера (t).
Результаты и их обсуждение. Проведенные исследования выявили, что средний показатель провоспалительного интерлейкина TNF-α в составе смывов послеоперационных ран (контрольной группы) составлял 15,7 ± 1,2 пг/мл, при этом в составе смывов гнойных ран (опытной группы) этот показатель находился на уровне 58,4 ± 5,4 пг/мл (Р<0,01). Эти результаты показывают, что исследования показателей TNF-α в составе смывов гнойных ран значительно и достоверно были выше аналогичных данных послеоперационных ран (Рис.). В тоже время результат исследования провоспалительного интерлейкина ИЛ-1 в составе смывов послеоперационных ран составлял 31,6 ± 2,8 пг/мл, а в составе смывов гнойных ран был равен 112,1 ± 10,4 пг/мл (Р<0,01). Этот результат так же был достоверно выше подобного показателя послеоперационных ран. Кроме того динамика изменения этого показателя была схожа с изменением сравнительных результатов TNF-α послеоперационных ран и гнойных ран (Рис.).
Помимо этого исследования противовоспалительного ИЛ-10 выявили, что средний показатель этого интерлейкина в составе смывов послеоперационных ран составлял 44,2 ± 4,1 пг/мл, а этот же показатель в составе смывов гнойных ран имел значения равные 31,9 ± 2,9 пг/мл (Р<0,05). Результаты этих исследований также демонстрируют, что показатели исследования ИЛ-10 в составе смывов гнойных ран, по сравнению с провоспалительными интерлейкинами имел обратную зависимость между послеоперационными и гнойными ранами находились достоверно ниже
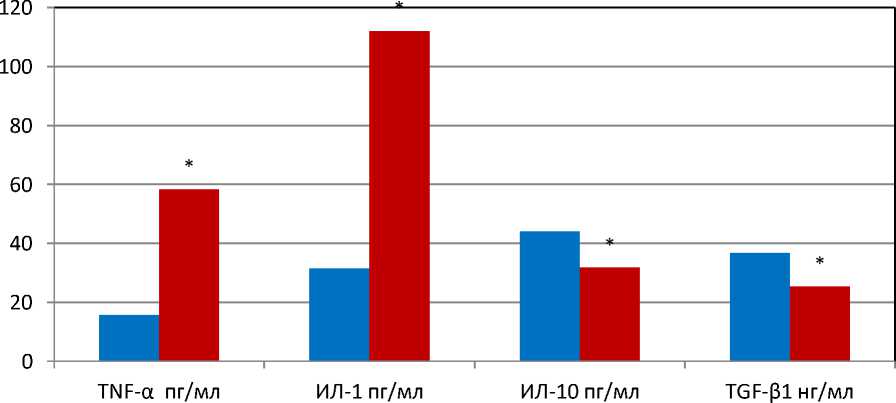
■ Послеоперационные раны ■ Гнойные раны
Рисунок. Изменение показателей TGF-β1, провоспалительных (TNF-α, ИЛ-1бета) и противовоспалительных (ИЛ-10) интерлейкинов смывов послеоперационных и гнойных ран.
* - достоверно отличающиеся величины относительно показателей послеоперационных ран.
подобных результатов послеоперационных ран (Рис.). Исследование TGF-β имеет важное значение, так как этот цитокин является регулятором провоспалительных и противовоспалительных интерлейкинов. В результате исследования этого цитокина было установлено, что в составе смывов послеоперационных ран он составлял 36,8 ± 3,2 нг/мл. В тоже время этот же показатель в составе смывов гнойных ран был равен 25,5 ± 2,3 нг/мл (Р<0,01). Из полученных данных исследования TGF-β можно заключить, что этот показатель так же был достоверно ниже подобного показателя послеоперационных ран. Кроме того динамика изменения этого результата была похожа изменению сравнительных результатов противовоспалительного ИЛ-10 интерлейкинов послеоперационных и гнойных ран (Рис.).
В целом полученные данные демонстрируют значительно выраженное увеличение провоспалительных интерлейкинов (ИЛ-1, TNF-α) в составе смывов хронических гнойных ран по сравнению с послеоперационными ранами и достоверное снижение противовоспалительного интерлейкина (ИЛ-10), а также трансформирующего фактора роста-β1 (TGF-β1).
Все это показывает, что большие количества IL-1β и TNF-α вызывают сильную продукцию хемокинов, что, в свою очередь, способствует массивной инфильтрации иммунных клеток, в частности нейтрофильных гранулоцитов. В конечном итоге это приводит к гнойным выделениям, клиническому ключевому признаку хронического гнойного воспаления. Кроме того, IL-1β и TNF-α усиливают секрецию ряда ферментов, разрушающих матрикс, что не только дополнительно поддерживает инфильтрацию тканевых иммунных клеток, но также способствует разрушению тканей, еще одной важной особенности хронического воспалительного заболевания. Локально продуцируемые IL-1β и IL-6 также, по-видимому, достигают кровотока и индуцируют продукцию сывороточного амилоида печенью, что отражается в заметно повышенных уровнях этого медиатора острой фазы в крови. Повышенные уровни IL-1β, TNF-α и сывороточного амилоида в крови являются признаком системного воспаления, которое часто может наблюдаться клинически у пациентов с хроническим воспалительным заболеванием [4].
Было показано, что лечение антителами против TNF-α подавляло избыточное воспаление и увеличивало образование грануляционной ткани, что приводило к ускорению заживления ран. Кроме того, системное введение нейтрализующих антител против TNF-α подавляло образование грануляционной ткани и замедляло заживление ран. Это указывает на то, что эффекты полной потери TNF-α в результате удаления гена и частичной инактивации цитокина нейтрализующим антителом на процесс заживления кожного повреждения различаются. Аналогичное несоответствие было зарегистрировано в других тканях. [2, 8].
Известно, что IL-10 ингибирует инфильтрацию нейтрофилов и макрофагов к месту повреждения. IL-10 также подавляет сверх экспрессию
CC-хемокинов (моноцитарный хемоаттрактантный белок-1, макрофагальный воспалительный белок-1α) и провоспалительных цитокинов (IL-1β, IL-6, TNF -α) in vivo. Предполагают, что IL-10 может играть важную регулирующую роль в фазовой инфильтрации нейтрофилов и макрофагов, а также в продукции цитокинов при воспалительной реакции заживления кожных ран [12]. Поэтому на основании полученных нами данных, уменьшение IL-10 в составе смывов хронических гнойных ран по сравнению с послеоперационными ранами может являться снижением конкурирующего влияния его на провоспалительные интерлейкины.
TGF-β синтезируют нейтрофилы, это важно для регуляции гуморального и врожденного иммунитета, включая стимуляцию макрофагов и лимфоцитов. Макрофаги продуцируют цитокины, факторы роста и ангиогенные факторы, которые регулируют пролиферацию фибробластов и ангиогенез. Макрофаги также продуцируют IL-1α, IL-1β, IL-6, IL-12 и TNF-α, которые важны для усиления воспаления, и стимулируют хемокины, которые вызывают рекрутирование лейкоцитов и стволовых клеток. Уменьшение экспрессии TGF-β1, снижение миграции и пролиферации кератиноцитов и усиление апоптоза кератиноцитов, что приводит к нарушению реэпителизации ран. TGF-β также привлекает макрофагов и фибробластов к участкам раны для улучшения заживления [3]. На основании этих данных можно предположить, что снижение TGF-β1 в хронических гнойных ранах может способствовать снижению привлечения макрофагов и фибробластов к участкам раны и тем самым ухудшению заживления хронических гнойных ран.
Выводы. В послеоперационных ранах показатели провоспалительных интерлейкинов были ниже противовоспалительных интерлейкинов и транформирующего фактора β. В тоже время в хронических гнойных ранах отмечалось значительное увеличение провоспалительных интерлейкинов и снижение противовоспалительных интерлейкинов, а также транформирующего фактора β, по сравнению с таковыми данными послеоперационных ран. Тем самым, создается выраженное нарушение равновесия и отмечается дисбаланс цитокинов провоспалительных и противовоспалительных интерлейкинов. Это способствует снижению заживления и хронизации воспалительного процесса хронических гнойных ран.
Список литературы Особенности изменения цитокинов в хронических гнойных ранах
- Engel, L. S., Hill, J. M., Caballero, A. R., Green, L. C., & O'Callaghan, R. J. Protease IV, a unique extracellular protease and virulence factor from Pseudomonas aeruginosa //Journal of Biological Chemistry. – 1998. – Т. 273. – №. 27. – С. 16792-16797.
- Fujita, M., Shannon, J. M., Morikawa, O., Gauldie, J., Hara, N., & Mason, R. J. Overexpression of tumor necrosis factor-α diminishes pulmonary fibrosis induced by bleomycin or transforming growth factor-β //American journal of respiratory cell and molecular biology. – 2003. – Т. 29. – №. 6. – С. 669-676.
- Hameedaldeen, A., Liu, J., Batres, A., Graves, G. S., & Graves, D. T. FOXO1, TGF-β regulation and wound healing //International journal of molecular sciences. – 2014. – Т. 15. – №. 9. – С. 16257-16269
- Hessam, S., Sand, M., Gambichler, T., & Bechara, F. G. Correlation of inflammatory serum markers with disease severity in patients with hidradenitis suppurativa (HS) //Journal of the American Academy of Dermatology. – 2015. – Т. 73. – №. 6. – С. 998-1005.
- Ito, A., Sato, T., Iga, T., & Mori, Y. Tumor necrosis factor bifunctionally regulates matrix metalloproteinases and tissue inhibitor of metalloproteinases TIMP) production by human fibroblasts //FEBS letters. – 1990. – Т. 269. – №. 1. – С. 93-95.
- Kapur, V., Topouzis, S., Majesky, M. W., Li, L. L., Hamrick, M. R., Hamill, R. J., ... & Musser, J. M. A conserved Streptococcus pyogenes extracellular cysteine protease cleaves human fibronectin and degrades vitronectin //Microbial pathogenesis. – 1993. – Т. 15. – №. 5. – С. 327-346.
- Koziel J., Potempa J. Protease-armed bacteria in the skin //Cell and tissue research. – 2013. – Т. 351. – №. 2. – С. 325-337.
- Kuroki, M., Noguchi, Y., Shimono, M., Tomono, K., Tashiro, T., Obata, Y., ... & Kohno, S. Repression of bleomycin-induced pneumopathy by TNF //The Journal of Immunology. – 2003. – Т. 170. – №. 1. – С. 567-574.
- Mast B. A., Schultz G. S. Interactions of cytokines, growth factors, and proteases in acute and chronic wounds //Wound Repair and Regeneration. – 1996. – Т. 4. – №. 4. – С. 411-420.
- Potempa J., Pike R. N. Corruption of innate immunity by bacterial proteases //Journal of innate immunity. – 2009. – Т. 1. – №. 2. – С. 70-87.
- Rudack, C., Sachse, F., Albert, N., Becker, K., & von Eiff, C. Immunomodulation of nasal epithelial cells by Staphylococcus aureus-derived serine proteases //The Journal of Immunology. – 2009. – Т. 183. – №. 11. – С. 7592-7601.
- Sato Y., Ohshima T., Kondo T. Regulatory role of endogenous interleukin-10 in cutaneous inflammatory response of murine wound healing //Biochemical and biophysical research communications. – 1999. – Т. 265. – №. 1. – С. 194- 199.
- Schmidtchen A., Wolff H., Hansson C. Differential proteinase expression by Pseudomonas aeruginosa derived from chronic leg ulcers //ACTA DERMATOVENEREOLOGICA-STOCKHOLM-. – 2001. – Т. 81. – №. 6. – С. 406-40.
- Silvestre, J. S., Mallat, Z., Tamarat, R., Duriez, M., Tedgui, A., & Levy, B. I. Regulation of matrix metalloproteinase activity in ischemic tissue by interleukin-10: role in ischemia-induced angiogenesis //Circulation research. – 2001. – Т. 89. – №. 3. – С. 259-264.
- Tarnuzzer R. W., Schultz G. S. Biochemical analysis of acute and chronic wound environments //Wound Repair and Regeneration. – 1996. – Т. 4. – №. 3. – С. 321-325.


