Особенности кишечной микробиоты у пациентов с воспалительными заболеваниями кишечника
Автор: Лагутина С.Н., Чижков П.А., Зуйкова А.А., Есина Е.Ю., Добрынина И.С., Скуратова О.С., Сыромятников М.Ю.
Журнал: Juvenis scientia @jscientia
Рубрика: Оригинальные исследования
Статья в выпуске: 3 т.9, 2023 года.
Бесплатный доступ
Введение. Воспалительные заболевания кишечника (ВЗК) занимают лидирующие позиции в структуре заболеваний желудочно-кишечного тракта (ЖКТ), так как являются прогрессирующей хронической патологией с аутоиммунным типом воспаления. Изменение показателей микробиоты кишечника может определять морфологические изменения на латентном этапе заболевания. Цель исследования. Оценка родо-видового биоразнообразия микробиоты у пациентов с ВЗК. Пациенты и методы. Выполнено секвенирование 16S рРНК микробиоты кишечника у 15 пациентов с подтвержденным язвенным колитом (ЯК) и 20 здоровых лиц, которые являлись контрольной группой. Проведен анализ показателей общего анализа крови и уровня С-реактивного белка (СРБ). Для статистического анализа использовали программы Microsoft Excel и Statistica. Результаты. Среди исследуемых лабораторных показателей у пациентов с ВЗК было отмечено значительное увеличение уровня СРБ, лейкоцитов и нейтрофилов по сравнению с группой контроля. В результате секвенирования кишечной микробиоты у пациентов с ВЗК выявлено снижение нормобиоты, а также увеличение содержания представителей патогенного кластера. Заключение. Выявлено снижение биоразнообразия микробиоты у пациентов с ВЗК по сравнению с группой контроля. Также наблюдалось значимое изменение патогенного кластера и дисбаланс представителей Bacteroidetesи Firmicutes.
Воспалительные заболевания кишечника, язвенный колит, секвенирование, микробиота кишечника, родо-видовое биоразнообразие, нормобиота, патогенный кластер
Короткий адрес: https://sciup.org/14127825
IDR: 14127825 | DOI: 10.32415/jscientia_2023_9_3_5-11
Features of the intestinal microbiota in patients with inflammatory intestinal diseases
Introduction. Inflammatory bowel diseases (IBD) occupy a leading position in the structure of diseases of the gastrointestinal tract (GIT), as they are a progressive chronic pathology with an autoimmune type of inflammation. Changes in the composition of the gut microbiota can determine morphological changes at the latent stage of the disease. Aim of the study. To assess the genus-species biodiversity of the microbiota in patients with IBD. Patients and methods. 16S rRNA sequencing of the intestinal microbiota was performed in 15 patients with confirmed ulcerative colitis (UC) and 20 healthy controls. The parameters of the full blood count and the serum level of C-reactive protein (CRP) were analyzed. The analysis of the obtained data was carried out using Microsoft Excel and Statistica software. Results. Among the studied laboratory parameters in patients with IBD, there was a significant increase in CRP, leukocyte and neutrophil counts compared to the control group. Sequencing of the gut microbiota showed a decrease in the normobiota, as well as an increase in the representatives of the pathogenic cluster. Conclusion. In the present study, we demonstrated a decrease in the biodiversity of the gut microbiota in patients with IBD compared to the control group, a significant change in the pathogenic cluster, and an imbalance between the representatives of Bacteroidetes and Firmicutes.
Текст научной статьи Особенности кишечной микробиоты у пациентов с воспалительными заболеваниями кишечника
В настоящее время воспалительные заболевания кишечника (ВЗК) занимают лидирующие позиции в структуре заболеваний желудочно-кишечного тракта (ЖКТ). ВЗК являются прогрессирующими хроническими заболеваниями с аутоиммунным типом воспаления, основными из них являются язвенный колит (ЯК), болезнь Крона. Длительность и степень тяжести воспалительного процесса приводят к высокому риску развития осложнений, в том числе колоректального рака. Именно бактериальный состав толстой кишки способен изменяться под воздействием различных факторов, что является эффективным средством для поддержания противовоспалительного состояния. В настоящее время известно, что при ВЗК наблюдается повышение уровня провоспалительных цитокинов: фактора некроза опухоли α (ФНО- α ) и различных интерлейкинов (ИЛ) [1]. При ЯК в развитии хронического воспаления участвуют клетки Th2 и Th17, продуцирующие различные цитокины. Основную роль во взаимодействии с микробиотой кишечника может играть ИЛ-33. Сигнальная ось ИЛ-33/ ST2 вовлекается в патогенез ВЗК через индукцию ИЛ-4. Данный механизм способен определять тяжесть аутоиммунного воспаления в активной фазе заболевания, когда уже происходит образование язвенных дефектов в слизистой оболочке кишечника. Количественное и качественное изменение родового и видового составов кишечной микробиоты может определять признаки патологического воспаления на латентной стадии [2, 3]. Изучение представителей кишечной микробиоты может привести к обнаружению новых диагностических признаков, влияющих на эффективность лекарственной терапии, а также исход заболевания.
ЦЕЛЬ РАБОТЫ
Изучение родо-видового состава микробиоты кишечника у пациентов с ВЗК.
ПАЦИЕНТЫ И МЕТОДЫ
Было выполнено секвенирование 16S рРНК микробиоты кишечника у 15 пациентов с подтвержденным (по результатам колоноскопии с прицельной биопсией) язвенным колитом и 20 здоровых лиц, которые являлись контрольной группой. Критерием включения в основную группу являлся первично установленный на амбулаторном этапе диагноз ЯК. Критерием исключения являлось проведение в течение последних трех месяцев терапии антибактериальными и гормональными препаратами. Пациенты получали симптоматическую терапию, которая включала в себя прием спазмолитических (мебеверин/дротаверин) и про-тиводиарейных (смектит диоктаэдрический/лопер-амид) препаратов. Все пациенты осуществляли сбор биоматериала (кал) в стерильный контейнер объемом 5 мл, после чего он был подвержен заморозке до проведения секвенирования 16S рРНК. Замораживание кала при подготовке к секвенированию проводилось при температуре –80 °C в лабораторных условиях. Тяжесть атаки определялась согласно индексу Мейо. Сформированные группы были сопоставимы по полу и возрасту. У всех исследуемых был проведен анализ показателей общего анализа крови (ОАК: показатели лейкоцитарной формулы, скорость оседания эритроцитов (СОЭ)), С-реактивного белка (СРБ). Анализ полученных данных проводился с использованием программ Microsoft Excel, Statistica. Количественные данные были описаны с помощью медианы (Me), значений нижнего и верхнего квартилей (Q1-Q3). Сравнение двух групп по количественному признаку, распределение которого отличалось от нормального, проводилось с помощью U-критерия Манна-Уитни. Различия в значении показателя между признаками считали значимыми при p<0,05.
РЕЗУЛЬТАТЫ
Среди пациентов с ВЗК индекс Мейо был равен 2 баллам (легкая степень тяжести) у 45% (пациенты с ЯК), 4 баллам (средняя степень тяжести) у 33%, 6 баллам (тяжелая степень) у 22%. Среди исследуемых лабораторных показателей у пациентов с ВЗК было отмечено значительное увеличение СОЭ, лейкоцитов, нейтрофилов по сравнению с группой контроля (табл. 1).
В результате секвенирования кишечной микробиоты было выявлено отсутствие или крайне низкое значение показателей нормобиоты у пациентов с ВЗК (табл. 2).
Таблица 1
|
Показатели |
Статистические показатели |
Значения |
|
Контрольная группа |
||
|
Лейкоциты, (×109/л) |
Ме |
3,8 |
|
Q1 - Q3 |
3,1-4,9 |
|
|
Нейтрофилы палочкоядерные, (%) |
Ме |
5 |
|
Q1 - Q3 |
1-8 |
|
|
Нейтрофилы сегментоядерные, (%) |
Ме |
56 |
|
Q1 - Q3 |
48-70 |
|
|
СОЭ, мм/ч |
Ме |
7 |
|
Q1 - Q3 |
1-12 |
|
|
Пациенты с ВЗК (ЯК) |
||
|
Лейкоциты, (×109/л) |
Ме |
6,1 |
|
Q1 - Q3 |
2,3-26,5 |
|
|
Нейтрофилы палочкоядерные, (%) |
Ме |
20 |
|
Q1 - Q3 |
12-36 |
|
|
Нейтрофилы сегментоядерные, (%) |
Ме |
68 |
|
Q1 - Q3 |
56-90 |
|
|
СОЭ, мм/ч |
Ме |
10 |
|
Q1 - Q3 |
1-54 |
|
Результаты лабораторной диагностики
Отмечалось увеличение показателей патогенного кластера, что также может настораживать в отношении воспалительных процессов и риска развития колоректального рака (табл. 3).
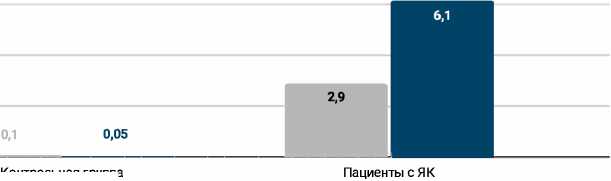
При оценке кластера сульфатредуцирую-щих бактерий отмечалось значительное увеличение доли бактерий родов Desulfovibrio и Methanobrevibacter — 2,9% и 6,1%, соответственно (рис. 1).
Были выявлены прямые, статистически значимые корреляционные связи между показателями Desulfovibrio , Methanobrevibacter и уровнем СРБ (p=0,012, p=0,044, соответственно), а также между Fusobacterium и уровнем СОЭ (p=0,017).
Таблица 2
Показатели нормальной микробиоты кишечника у пациентов с ВЗК
|
Состав бактерий, % |
Статистические показатели |
Значения |
|
Контрольная группа |
||
|
Lactobacterium (0,02%-0,1%) |
Ме |
0,02 |
|
Q1 - Q3 |
0-0,3 |
|
|
Bifidobacterium (0,1%-1%) |
Ме |
0,5 |
|
Q1 - Q3 |
0,2-3,1 |
|
|
Faecalibacterium (5%-9%) |
Ме |
6,3 |
|
Q1 - Q3 |
4,8-9,1 |
|
|
Bacteroides (9%-19%) |
Ме |
9,5 |
|
Q1 - Q3 |
7-15,7 |
|
|
Пациенты с ВЗК (ЯК) |
||
|
Lactobacterium (0,02%-0,1%) |
Ме |
0,01 |
|
Q1 - Q3 |
0-0,02 |
|
|
Bifidobacterium (0,1%-1%) |
Ме |
0,01 |
|
Q1 - Q3 |
0-0,02 |
|
|
Faecalibacterium (5%-9%) |
Ме |
0,1 |
|
Q1 - Q3 |
0-6,1 |
|
|
Bacteroides (9%-19%) |
Ме |
0,6 |
|
Q1 - Q3 |
0-5,8 |
|
ОБСУЖДЕНИЕ
Увеличение количества представителей типа Firmicutes может настораживать в отношении воспалительных процессов и новообразований, за счет выделения активных метаболитов, которые способствуют значительному снижению барьера слизистой, что напрямую может способствовать развитию новообразований [3].
Увеличение представителей сульфатредуци-рующей группы бактерий может говорить о степени тяжести основного заболевания. Благодаря своей уникальной способности превращать водород и углекислый газ в метан Desulfovibrio и Methanobrevibacter помогают эффективно расщеплять пищевые волокна, а также влияют на иммунные клетки организма и выработку антибак-
б
О
Контрольная группа
■ Desulfovibrio, % ■ Methanobrevibacter, %
Рисунок 1. Оценка состава сульфатредуцирующих бактерий у пациентов с ВЗК.
Таблица 3
Показатели патогенной микрофлоры кишечника у пациентов с ВЗК
Бутират-продуцирующие бактерии синтезируют важный метаболит, необходимый для защиты целостности эпителиального барьера кишечника и сохранения иммунного гомеостаза хозяина за счет дифференцировки регуляторных Т-клеток [6]. Снижение уровня бутирата вызывает дисфункцию кишечного эпителиального барьера и приводит к экспрессии нескольких воспалительных маркеров [7, 8].
ЗАКЛЮЧЕНИЕ
По результатам проведенного исследования выявлено уменьшение родо-видового биоразнообразия нормальной микробиоты кишечника у пациентов с ВЗК по сравнению с группой контроля. Исследование кишечной микробиоты может позволить обнаружить новые диагностические признаки и способствовать раннему выявлению заболеваний кишечника и выработке дифференцированных подходов к лечению.
Финансирование: Исследование было выполнено при финансовой поддержке УМНИК (№ 88696-У).
Список литературы Особенности кишечной микробиоты у пациентов с воспалительными заболеваниями кишечника
- Burakova I, Smirnova Y, Gryaznova M, et al. The Effect of Short-Term Consumption of Lactic Acid Bacteria on the Gut Microbiota in Obese People. Nutrients. 2022;14(16):3384. DOI: 10.3390/nu14163384.
- Loke YL, Chew MT, Ngeow YF, et al. Colon Carcinogenesis: The Interplay Between Diet and Gut Microbiota. Front Cell Infect Microbiol. 2020;10:603086. DOI: 10.3389/fcimb.2020.603086.
- Caparrós E, Wiest R, Scharl M, et al. Dysbiotic microbiota interactions in Crohn’s disease. Gut Microbes. 2021;13(1):1949096. DOI: 10.1080/19490976.2021.1949096.
- Glassner KL, Abraham BP, Quigley EMM. The microbiome and inflammatory bowel disease. J Allergy Clin Immunol. 2020;145(1):16-27. DOI: 10.1016/j.jaci.2019.11.003.
- Torres J, Mehandru S, Colombel JF, Peyrin-Biroulet L. Crohn’s disease. Lancet. 2017;389(10080):1741-1755. DOI: 10.1016/S0140-6736(16)31711-1.
- Gajendran M, Loganathan P, Catinella AP, Hashash JG. A comprehensive review and update on Crohn’s disease. Dis Mon. 2018;64(2):20-57. DOI: 10.1016/j.disamonth.2017.07.001.
- He Y, Hu Y, Yuan M, et al. Prognostic and therapeutic implication of m6A methylation in Crohn disease. Medicine (Baltimore). 2022;101(51):e32399. DOI: 10.1097/MD.0000000000032399.
- Sokol H, Landman C, Seksik P, et al. Fecal microbiota transplantation to maintain remission in Crohn’s disease: a pilot randomized controlled study. Microbiome. 2020;8(1):12. DOI: 10.1186/s40168-020-0792-5.


