Особенности клинического течения и лечебной тактики у курящего пациента с распространённым деструктивным туберкулёзом лёгких в сочетании с хронической обструктивной болезнью лёгких и пневмокониозом: клиническое наблюдение
Автор: Чумоватов Н.В., Тарасов Р.В., Черных Н.А., Багиров М.А., Хозиков А.С.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клинический случай
Статья в выпуске: 6 т.15, 2025 года.
Бесплатный доступ
Актуальной проблемой современной фтизиатрии является рост числа больных туберкулёзом лёгких с сопутствующими заболеваниями и значимыми факторами риска. Хроническая обструктивная болезнь лёгких (ХОБЛ) и табакокурение входят в пятерку наиболее значимых факторов риска развития туберкулёза. Пневмокониозы, включая силикоз лёгких, также являются важным профессиональным фактором риска, при котором присоединение туберкулёзной инфекции регистрируется почти в 40% случаев. Сочетание данных факторов создаёт значительные трудности в диагностике и лечении туберкулёза лёгких. Цель: продемонстрировать особенности клинического течения и эффективность комплексного лечения у курящего больного с распространённым деструктивным туберкулёзом лёгких в сочетании с ХОБЛ и пневмокониозом. Материалы и методы. Представлено клиническое наблюдение пациента 54 лет, шахтёра по профессии, с длительным стажем табакокурения (30 лет, индекс курильщика 60). Использованы ретроспективное наблюдение, клинический анализ, рентгенография, МСКТ органов грудной клетки, микробиологические исследования мокроты, бронхоскопия, спирометрия. Установлен диагноз: инфильтративный туберкулёз лёгких в фазе распада и обсеменения с множественной лекарственной устойчивостью (HR) в сочетании с ХОБЛ и буллёзной эмфиземой лёгких. Лечение включало противотуберкулёзную химиотерапию по режиму МЛУ, терапию ХОБЛ, никотинзаместительную терапию и хирургическое вмешательство (комбинированная резекция левого лёгкого). Результаты. Благодаря комплексному подходу через 2 месяца лечения достигнута положительная клинико-лабораторная и рентгенологическая динамика: прекращение бактериовыделения, нормализация маркеров воспаления, частичное рассасывание инфильтративных изменений. Пациент полностью отказался от табакокурения. Через 3 месяца выполнена успешная операция. Патогистологическое исследование подтвердило туберкулёзную этиологию с признаками пневмокониоза (множественные кониотические узелки в лёгком и лимфоузлах). Послеоперационный период протекал без осложнений, достигнуто клиническое излечение. Заключение. Комплексный подход в лечении, включающий коррекцию сопутствующей патологии (ХОБЛ, табакокурение), правильно подобранную противотуберкулёзную терапию и своевременное хирургическое лечение, позволил добиться клинического излечения пациента с распространённым деструктивным туберкулёзом в сочетании с ХОБЛ и пневмокониозом в кратчайшие сроки.
Туберкулез легких, комплексное лечение, табакокурение, пневмокониоз, ХОБЛ, хирургическое лечение, силикоз, деструктивный туберкулез, множественная лекарственная устойчивость, профессиональные заболевания
Короткий адрес: https://sciup.org/143185458
IDR: 143185458 | УДК: 616.24-002.5-036.12-085:616.24-007.272+616.24-003.66 | DOI: 10.20340/vmi-rvz.2025.6.CASE.1
Eatures of the clinical course and therapeutic tactics in a smoking patient with widespread destructive pulmonary tuberculosis in combination with COPD and pneumoconiosis: clinical observation
Background. An urgent problem in modern phthisiology is the increasing number of patients with pulmonary tuberculosis accompanied by concomitant diseases and significant risk factors. Chronic obstructive pulmonary disease (COPD) and tobacco smoking are among the five most significant risk factors for tuberculosis development. Pneumoconioses, including pulmonary silicosis, are also important occupational risk factors, with tuberculosis infection occurring in almost 40% of cases. The combination of these factors creates significant difficulties in the diagnosis and treatment of pulmonary tuberculosis. Objective. To demonstrate the clinical course features and effectiveness of comprehensive treatment in a smoking patient with widespread destructive pulmonary tuberculosis combined with COPD and pneumoconiosis. Materials and methods. A clinical case of a 54-year-old male patient, a miner by profession, with a long history of tobacco smoking (30 years, smoking index 60) is presented. Retrospective observation, clinical analysis, radiography, MSCT of the chest, microbiological sputum examination, bronchoscopy, and spirometry were utilized. The diagnosis was established as infiltrative pulmonary tuberculosis in the phase of cavitation and dissemination with multidrug resistance (HR) combined with COPD and bullous pulmonary emphysema. Treatment included anti-tuberculosis chemotherapy for MDR-TB, COPD therapy, nicotine replacement therapy, and surgical intervention (combined resection of the left lung). Results. Through a comprehensive approach, positive clinical, laboratory, and radiological dynamics were achieved after 2 months of treatment: cessation of bacterial excretion, normalization of inflammatory markers, and partial resolution of infiltrative changes. The patient completely quit smoking. After 3 months, successful surgery was performed. Pathohistological examination confirmed tuberculous etiology with signs of pneumoconiosis (multiple coniotic nodules in the lung and lymph nodes). The postoperative period was uncomplicated, and clinical cure was achieved. Conclusion. A comprehensive treatment approach including correction of concomitant pathology (COPD, tobacco smoking), properly selected antituberculosis therapy, and timely surgical treatment enabled clinical cure of a patient with widespread destructive tuberculosis combined with COPD and pneumoconiosis in the shortest possible time.
Текст научной статьи Особенности клинического течения и лечебной тактики у курящего пациента с распространённым деструктивным туберкулёзом лёгких в сочетании с хронической обструктивной болезнью лёгких и пневмокониозом: клиническое наблюдение
Актуальной проблемой в современной фтизиатрии является рост числа пациентов с туберкулёзом лёгких и сопутствующими заболеваниями, а также значимыми факторами риска. Несомненно, крайне важными факторами риска в развитии более тяжёлого течения туберкулёза является табакокурение и хроническая обструктивная болезнь лёгких (ХОБЛ) [1]. По данным Всемирной организации здравоохранения (ВОЗ) табакокурение входит в пятерку наиболее значимых факторов риска развития туберкулёза среди населения [2], а распространённость ХОБЛ варьируется от 10 до 16% в различных странах мира [3]. Кроме того, табакокурение является одной из главных причин развития ХОБЛ [4].
Также значимым фактором риска развития туберкулёза являются профессиональные заболевания, а именно пневмокониозы лёгких. Силикоз лёгких считается одной из форм пневмокониоза, развивающегося при постоянном вдыхании фиброгенной пыли, содержащей диоксид кремния [5]. Имеются данные, что у больных силикозом присоединение туберкулёзной инфекции регистрируется почти в 40% случаев [6]. При этом, возникновение туберкулёза ассоциируется со степенью выраженности 173
пневмофиброза. Ряд авторов демонстрируют необходимость проведения ежегодных профилактических осмотров у работников, контактирующих с пылью [5, 6]. Сочетание данных факторов в диагностике и лечении туберкулёза лёгких создаёт значительные трудности как в подборе противотуберкулёзной химиотерапии, так и патогенетической терапии.
ЦЕЛЬ РАБОТЫ: продемонстрировать особенности течения и эффективность проводимого комплексного лечения у курящего пациента с распространённым деструктивным туберкулёзом лёгких в сочетании с ХОБЛ и пневмокониозом.
МАТЕРИАЛЫ И МЕТОДЫ
Для данной исследовательской работы были использованы ретроспективное наблюдение, методы клинического анализа. В процессе была изучена история болезни пациента с деструктивным туберкулёзом лёгких в сочетании с ХОБЛ и пневмокониозом лёгких, также сбор данных основывался на клиническом осмотре, рентгенографии ОГК, компьютерной томографии органов грудной клетки (МСКТ ОГК), микробиологических исследованиях мокроты для выявления возбудителя и определения спектра лекарственной устойчивости. Дополнительно проведена бронхоскопия для оценки состояния трахеобронхиального дерева с забором диагностического материала. Учитывая наличие факта табакокурения, проведена диагностика статуса курения с последующим применением антитабачной программы в виде никотинзаместительной терапии.
Лечение включало хирургическое вмешательство, также применение консервативных методов.
Оценка эффективности терапии проводилась на основе клинических показателей, динамики выздоровления.
Информированное согласие на проведение диагностических и лечебных мероприятий, а также на возможность клинической демонстрации и публикации от пациента было получено.
КЛИНИЧЕСКИЙ ПРИМЕР
Пациент мужчина, 54 лет, образование среднее специальное, по профессии шахтёр и разнорабочий. Ранее туберкулёзом не болел, контакт с больным туберкулёзом отрицает. Предыдущее ФЛГ обследование около 10 лет назад. Хронические заболевания отрицает. На протяжении 10 лет пациента беспокоит кашель с выделением мокроты. Больше 20 лет работал на угольной шахте, в настоящее время работает строителем, имеет постоянный контакт с пылью и частицами тяжёлых металлов. Ухудшение состояния отмечает с марта 2024 года, когда стал замечать появление кашля с гнойной мокротой, одышку при нагрузке, повышение температуры тела до 38 ºС. Лечился противовирусными и муколитическими препаратами в домашних условиях, за медицинской помощью не обращался. Отмечал временное улучшение самочувствия, однако сохранялся кашель с выделением мокроты. Обратился к пульмонологу в частную клинику, выполнена КТ ОГК от 09.04.2024 г. (представлено описание), где выявлена массивная полость распада с наличием очагово-инфильтративных изменений в обоих лёгких, признаки эмфиземы, бронхоэктазы в нижних отделах. Рекомендована консультация фтизиатра. Самостоятельно обратился в ФГБНУ ЦНИИТ. При обследовании в анализах мокроты ДНК МБТ и КУМ не обнаружены, проба с АТР «Диаскинтест» – папула 15 мм. Госпитализирован в ФГБНУ ЦНИИТ в апреле 2024 года с целью дообследования и лечения.
На момент поступления: жалобы на одышку при нагрузке (mMRC 2), кашель с выделением гнойной мокроты до 100 мл в сутки, повышение температуры тела до 37,5 ºС. Рост 185 см, вес 65 кг, ИМТ – 19. Кожные покровы физиологической окраски, умеренной влажности. Пальпируются шейные лимфо- узлы, не спаяны, безболезненные, без признаков воспаления. Отёков нет. Грудная клетка симметрична, втянутой формы. При аускультации дыхание жёсткое, сухие хрипы во всех отделах лёгких. Частота дыхательных движений (ЧДД) 16/мин. SpO2 95%. Тоны сердца ясные ритмичные. ЧСС=PS=85 уд. в мин., артериальное давление (АД) 125/85 мм рт. ст.
В общем анализе крови – повышение уровня СОЭ – 54 мм/ч, что свидетельствовало об активном воспалительном процессе, другие показатели в пределах нормы.
Общий анализ мочи без выраженных патологических изменений.
В биохимическом анализе крови – повышение уровня С-реактивного белка (СРБ) – 35 мг/л, что свидетельствовало об активном воспалительном процессе, другие показатели в пределах нормы.
В коагулограмме – состояние гиперкоагуляции, уровень фибриногена – 4,55 г/л.
В мокроте методом люминесцентной микроскопии (15.04.2024) кислотоустойчивые микобактерии обнаружены (+). Методом полимеразной цепной реакции (ПЦР) – ДНК микобактерии туберкулёза обнаружены. Методом тест-системы «СИНТОЛ» мокроты – установлена лекарственная устойчивость микобактерии к рифампицину (R) и изониазиду (H). Анализ мокроты на неспецифическую флору – рост не выявлен.
По данным спирометрии (15.04.2024): жизненная ёмкость лёгких (ЖЕЛ) – 95,0%, объём форсированного выдоха (ОФВ1) – 57,5%, мИТ 0,60 – снижение вентиляционной способности лёгких по обструктивному типу, достаточное насыщение крови О 2 .
При проведении МСКТ ОГК-В S1 и S2 левого лёгкого субплеврально определяется воздушная полость неправильной формы с толстыми неровными стенками, до 3,5 см в диаметре, небольшим количеством патологического содержимого вдоль стенок. Вдоль заднего контура полости определяется крупная перифокальная зона консолидации, частично сливающаяся со стенкой полости, содержащая в толще единичные мелкие воздушные полости и единичные мелкие кальцинаты. К полости подходят отдельные субсегментарные бронхи, заполненные патологическим содержимым. В апикальных отделах S1 правого лёгкого, субплеврально определяются участки консолидации, с видимыми просветами субсегментарных бронхов – соответствует воспалительным изменениям. В обоих лёгких, в том числе вдоль междолевой плевры, определяются многочисленные мелкие очаги. Отмечаются выраженные эмфизематозные изменения обоих лёгких в виде парасептальной и буллёзной эмфиземы (рис. 1).
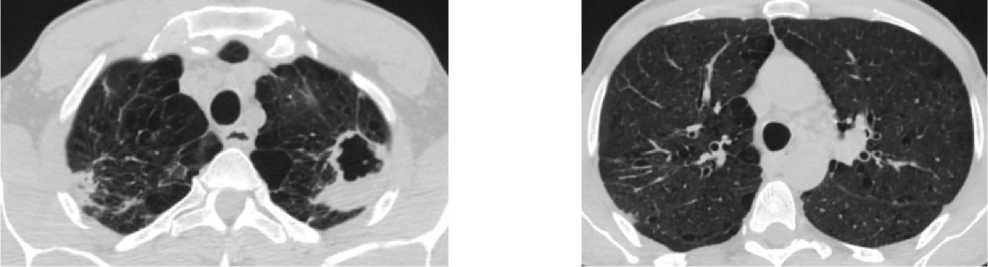
Рисунок 1. Аксиальные срезы КТ органов грудной клетки, легочное окно: а – S1 и S2 левого лёгкого, субплеврально определяется воздушная полость неправильной формы с толстыми неровными стенками; б – в обоих лёгких определяются многочисленные мелкие очаги, выраженные эмфизематозные изменения обоих лёгких в виде эмфиземы
Figure 1. Axial CT scans of the chest organs, pulmonary window: a – S1 and S2 of the left lung, an irregularly shaped air cavity with thick uneven walls is determined subpleurally; б – numerous small foci are detected in both lungs, pronounced emphysematous changes in both lungs in the form of emphysema
Учитывая, что пациент является курильщиком с длительным стажем табакокурения, проведена оценка статуса курения по разработанной методике [7]. Пациент выкуривал 40 сигарет в день, стаж курения 30 лет. Индекс курящего (ИК) человека составил 60. Установлена высокая степень никотиновой зависимости согласно тесту Фагерстрема, отмечалось наличие симптомов отмены (раздражительность, возбудимость, нервозность), установлена высокая мотивация к отказу от табакокурения согласно тесту Прохаска. Пациент положительно отреагировал на возможность отказа от табакокурения, в связи с чем была предложена антитабачная программа с применением никотинзаместительной терапии в виде трансдермальных пластырей и жевательной резинки.
Учитывая наличие бронхообструктивных нарушений (по данным спирометрии), проведена консультация пульмонолога. Пульмонологом установлен диагноз: ХОБЛ, преимущественно эмфизематозный фенотип, с невыраженными симптомами и редкими обострениями, нарушение бронхиальной проводимости I степени, вне обострения. Буллёзная эмфизема лёгких. Даны рекомендации и развернута терапия (см. далее)
При проведении фибробронхоскопии установлен «Диффузный двусторонний атрофический бронхит».
Установлен клинический диагноз: «Инфильтративный туберкулёз лёгких в фазе распада и обсеменения МБТ (+). МЛУ МБТ (HR). ХОБЛ, преимущественно эмфизематозный фенотип, с невыраженными симптомами и редкими обострениями, нарушение бронхиальной проводимости I степени, вне обострения. Буллёзная эмфизема лёгких».
Назначено комплексное лечение в следующем объёме.
Противотуберкулёзная химиотерапия по режиму МЛУ туберкулёза в объёме: Бедаквилин по схеме,
Линезолид 0,6 г в сутки, Моксифлоксацин 0,4 г в сутки, Циклосерин 0,75 г в сутки, Пиразинамид 1,5 г в сутки, Амикацин 1,0 г в/м в сутки.
Терапия ХОБЛ в объёме : ингаляционная терапия: Беродуал 20 капель 3 раза в день через небулайзер, Амброксол 2 мл 2 раза в день через небулайзер в течении 14 дней. 2. Олодатерол 2,5 мг + Тиотропий 2,5 мг (Спиолто-респимат) по 1 вдоху 1 раз в день ежедневно.
Никотинзаместительная терапия в объёме: Схема 1 включала 3 этапа лечения: 1 этап – пластырь 25 мг 4 недели, Жевательная резинка 2 мг 5–6 раз в сутки 4 недели; 2 этап – пластырь 15 мг 4 недели, Жевательная резинка 2 мг по необходимости; 3 этап – пластырь 10 мг 4 недели, Жевательная резинка 2 мг по необходимости.
Пациент полностью отказался от табакокурения с 1-го дня применения терапии. Переносимость лечения была удовлетворительной.
Динамика через 2 месяца лечения
Состояние пациента оценивалось как удовлетворительное. Отмечал прекращение кашля с выделением мокроты, уменьшение одышки при нагрузке, повышение температуры тела не отмечалось.
В общем анализе крови отмечалось нормализация показателя СОЭ – 18 мм/ч. В общем анализе мочи, биохимическом анализе крови патологических изменений не выявлено. В коагулограмме сохранялась тенденция к гиперкоагуляции.
В анализах мокроты – ДНК МБТ не обнаружена, КУМ не обнаружены, получен отрицательный рост МБТ методом посева на жидкие питательные среды.
При спирометрии – сохраняется снижение вентиляционной способности лёгких по обструктивному типу, однако наблюдается прирост показателей: ОФВ1 – с 57,5% до 63,5%, ФЖЕЛ – с 95,0% по 97,8%, мИТ – с 0,6 до 0,65.
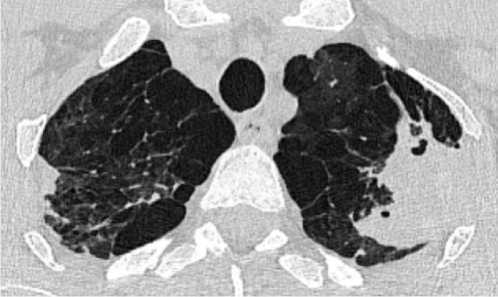
На контрольной КТ ОГК – положительная рентгенологическая динамика в виде частичного рассасывания очагово-инфильтративных изменений в обоих лёгких, определяется зона консолидации неодно- родной жидкостной плотности на месте ранее определявшейся воздушной полости – в большей степени соответствует заполнению полости патологическим содержимым (рис. 2).
а
Рисунок 2. Аксиальные срезы КТ органов грудной клетки, лёгочное окно: а – зона консолидации неоднородной жидкостной плотности на месте ранее определявшейся воздушной полости; б – частичное рассасывание очагово-инфильтративных изменений в обоих лёгких Figure 2. Axial CT scans of the chest organs, pulmonary window: a – a zone of consolidation of heterogeneous liquid density at the site of the previously determined air cavity; б – partial resorption of focal infiltrative changes in both lungs
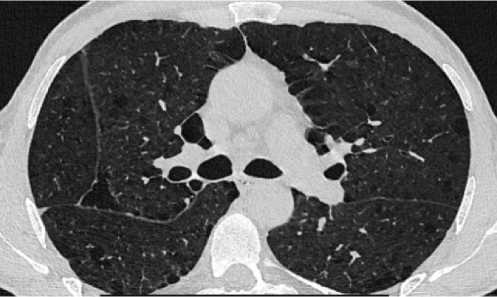
б
Комплексное лечение было продолжено в прежнем объёме с удовлетворительной переносимостью. Продолжалась бронхолитическая терапия и никотинзаместительная терапия, пациент полностью отказался от табакокурения.
Учитывая положительную клинико-лабораторную и рентгенологическую динамику, а также формирование зоны консолидации в верхней доле левого лёгкого, пациент консультирован фтизиохирургом, рекомендовано хирургическое лечение.
Спустя 3 месяца проводимого комплексного лечения (24.07.2024) пациенту проведена комбинированная резекция левого лёгкого (S1-S2, S6).
Течение операции. При ревизии: плевра не изменена. Лёгкое выделено из многочисленных спаек на всем протяжении интраплеврально. Лёгкое эмфизе-матозно, содержит многочисленные буллы и многочисленные мелкие очаги. В S1-2 c частью S3 уплотнение, на периферии S6 фиброзные изменения. Учитывая локализацию уплотнения решено провести атипичную резекцию указанного участка. На междолевую борозду между S6 и S2 с захватом фиброзно изменённой части S6 наложен аппарат УО-40. На S1-2 c частью S3 наложен аппарат СОМИ-80, и указанный участок лёгкого с фиброзно измененной частью S6 удален. По ходу выделения удалены чёрные, плотные лимфоузлы нижней лёгочной связки и прикорневые. В оставшихся отделах буллезные изменения и очаги. Механические швы на лёгком укреплены ручным атравматическим швом пролен 3. При раздувании до аппаратного значения 40 и проведении подводной пробы – выраженных дефектов лёгочной ткани не обнаружено, лёгкое расправляется и занимает большую часть плевральной полости.
Длительность операции составила 140 минут, кровопотеря 100 мл.
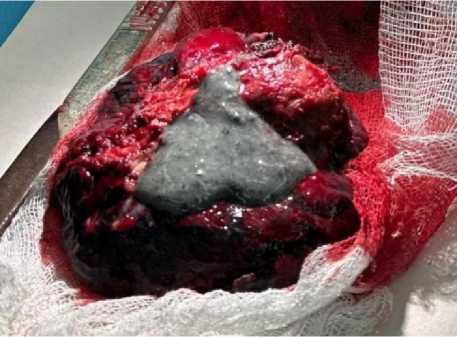
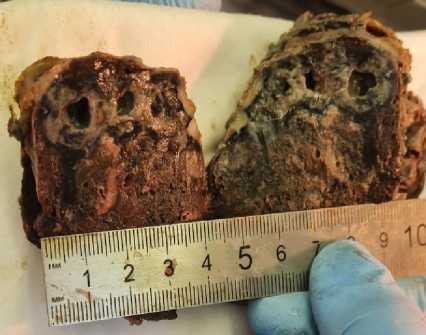
Макроскопически материал (рис. 3) представлен фрагментом лёгкого размерами 9,0×6,8×4,2 см с наличием на разрезах плотного сероватого очага с черноватыми участками размерами 5,5×5,0×3,0 см с фокусами распада. Также отмечались мелкие черновато-серые очажки, и, кроме того, буллы протяжённостью до 1,5–1,7 см.
При микробиологическом исследовании операционного материала методом люминисцентной микроскопии обнаружены КУМ +. Методом ПЦР обнаружены ДНК МБТ, Методом СИНТОЛ подтверждена лекарственная устойчивость возбудителя к изониазиду и рифампицину.
При патогистологическом исследовании операционного материала в лёгочной ткани обнаружены немногочисленные разнокалиберные очаги эозинофильного некроза (рис. 4а), часть из которых с неравномерно выраженной лейкоцитарной реакцией. Также отмечались макрофагальногигантоклеточные гранулёмы, в том числе в стенках бронхиол. Кроме того, выявлены эмфизематозные изменения лёгочной ткани в виде субплеврально расположенных тонкостенных полостных образований – булл (рис. 4б). Вместе с тем в лёгком и лимфатических узлах (внутрилёгочном и внутригрудных) были обнаружены множественные очажки гипокле-точной фиброзной ткани слоистого строения с отложениями угольного пигмента – кониотические узелки (рис. 4в, рис. 4г).
а
Рисунок 3. Макропрепарат операционного материала: а – из операционной после удаления; б – нарезка материала для парафиновых блоков: фрагменты лёгкого размерами с наличием на разрезах плотного сероватого очага с черноватыми участками, также мелкие черновато-серые очажки, и, кроме того, буллы
Figure 3. Macro-preparation of the surgical material: a – from the operating room after removal; б – cutting of the material for paraffin blocks: fragments of light size with the presence of a dense grayish focus with blackish areas on the incisions, as well as small blackish-gray foci, and, in addition, bullae
б
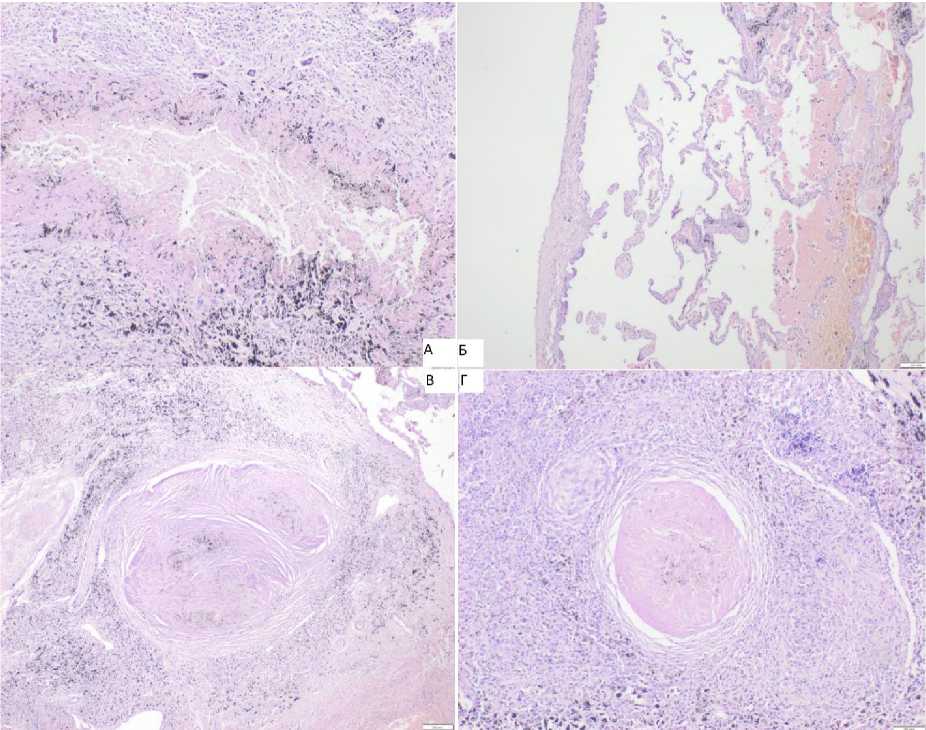
Рисунок 4. Патогистологическое исследование: А. Инкапсулированный очаг рыхлого эозинофильного некроза в лёгком. В капсуле и некротических массах – отложения угольного пигмента. Окраска гематоксилином и эозином. Увеличение ×40. Б. Буллёзная эмфизема лёгкого. Окраска гематоксилином и эозином. Увеличение ×40. В. Кониотический очажок в лёгком. Окраска гематоксилином и эозином. Увеличение ×100. Г. Кониоз внутрилёгочного лимфатического узла. Окраска гематоксилином и эозином. Увеличение ×100
Figure 4. Pathohistological examination: А. Encapsulated focus of loose eosinophilic necrosis in the lung. There are deposits of charcoal pigment in the capsule and necrotic masses. Staining with hematoxylin and eosin. Magnification ×40. Б. Bullous emphysema of the lung. Staining with hematoxylin and eosin. Magnification ×40. В. Coniotic lesion in the lung. Staining with hematoxylin and eosin. Magnification ×100. Г. Conio-sis of the intrapulmonary lymph node. Staining with hematoxylin and eosin. Magnification ×100
Послеоперационный период протекал без осложнений, дренажи удалены по срокам. Комплексное лечение было продолжено в прежнем объёме с удовлетворительной переносимостью.
Динамика через 3 месяца лечения и 1 месяц после оперативного этапа лечения.
Состояние больного оценивалось как удовлетворительное, жалоб не предъявлял.
В общем анализе крови, в общем анализе мочи, биохимическом анализе крови патологических изменений не выявлено. В коагулограмме сохраняется тенденция к гиперкоагуляции;
В анализах мокроты – ДНК МБТ не обнаружена, КУМ не обнаружены, получены отрицательные росты МБТ методом посева на жидкие питательные среды.
При спирометрии – сохраняется снижение вентиляционной способности лёгких по обструктивно- му типу. В динамике: снижение ОФВ1 – с 63,5% до 62,4%, ФЖЕЛ – с 97,8% до 89,7%, увеличение мИТ – с 0,65 до 0,68.
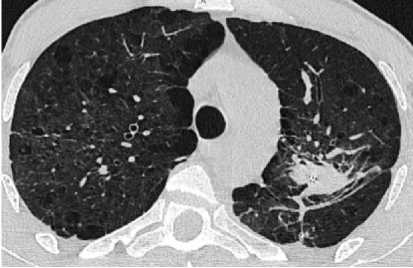
На контрольной КТ ОГК (25.07.2024) – апикальная плевра деформирована плевропульмональными спайками. «Свежих» очаговых изменений не выявлено. Левое лёгкое уменьшено в объёме из-за хирургического лечения. В прикорневой зоне на фоне утолщённого междолькового интерстиция прослеживаются цепочки металлических швов в локальном участке уплотнения со сближенными и деформированными просветами бронхов, с локальным утолщением костальной и междолевой плевры с незначительным количеством плеврального выпота пара-костально. В апикальном отделе S1 правого лёгкого сохраняется субплевральный участок консолидации с видимыми просветами бронхов в структуре (рис. 5).
а
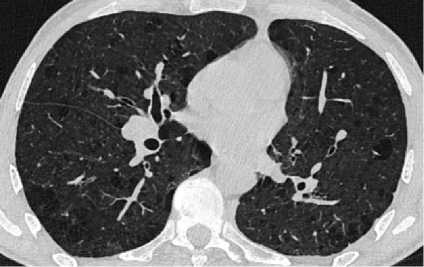
Рисунок 5. Аксиальные срезы КТ органов грудной клетки, лёгочное окно: а – левое лёгкое уменьшено в объёме из-за хирургического лечения. В прикорневой зоне на фоне утолщенного междолькового интерстиция прослеживаются цепочки металлических швов; б – на фоне выраженных фиброзных и буллезно-дистрофических изменений визуализируются множественные мелкие очаги вдоль междолевой плевры обоих лёгких
Figure 5. Axial CT scans of the chest organs, pulmonary window: a – the left lung is reduced in volume due to surgical treatment. In the basal zone, chains of metal sutures are traced against the background of a thickened interlobular interstitium; b – against the background of pronounced fibrous and bullous-dystrophic changes, multiple small foci are visualized along the interlobular pleura of both lungs
б
Пациент был выписан в ПТД по месту жительства для продолжения лечения в амбулаторных условиях. Стоит отметить, что больной полностью отказался от потребления табака.
ОБСУЖДЕНИЕ И РЕЗУЛЬТАТЫ
В современных условиях работы противотуберкулёзной службы актуальной проблемой является рост больных туберкулёзом с сопутствующими заболеваниями и значимыми факторами риска. К наиболее значимым относится табакокурение и ХОБЛ, которые имеют широкую распространённость среди пациентов с туберкулёзом лёгких, вызывая трудности в ведении и лечении данной категории больных. Кроме того, табакокурение является важнейшей причиной развития ХОБЛ и способствует неуклонному прогрессированию заболевания. В связи с чем лечение данной категории пациентов должно содержать комплексный характер, который направлен на купирование бронхообструктивных нарушений и отказ от табакокурения.
Кроме того, к факторам риска развития туберкулёза необходимо отнести профессиональные заболевания, к которым относятся пневмокониозы. Пневмокониозы – неизлечимое фиброзное заболевание лёгких, вызываемое дозозависимым воздействием вдыхаемой пыли. Обычно заболевание проявляется через десятилетия после воздействия, но высокие дозы воздействия могут привести к ускоренному заболеванию и дыхательной недостаточности в течение 1–2 лет. По данным различных авторов, при наличии пневмокониоза риск развития туберкулёза лёгких повышается от 2 до 5 раз [8, 9, 10]. Кроме того, данное заболевание является частой причиной развития ХОБЛ. Наличие нескольких значимых факторов у одного пациента может приводить к повышению риска развития активного туберкулёзного процесса, что было продемонстрировано в данной работе.
Данное клиническое наблюдение демонстрирует высокую эффективность комплексного подхода в лечении курящего больного туберкулёзом лёгких с ХОБЛ и пневмокониозом лёгких. При поступлении у пациента наблюдалась выраженная респираторная симптоматика и синдром интоксикации, рентгенологически отмечался распространённый двусторонний туберкулёзный процесс с бактериовыделением в мокроте. Учитывая отягощённый профессиональный анамнез, у больного диагностирован пневмокониоз лёгких с формированием буллезной эмфиземы лёгких. Также отягощающим фактором являлся длительный стаж табакокурения, в связи с чем больному проведена диагностика статуса курения и предложена антитабачная программа в виде никотинзаместительной терапии, которая способствовала отказу от табакокурения и повлияла на прирост функциональных показателей лёгких.
Благодаря применению комплексного подхода уже через 2 месяца лечения наблюдалась выраженная положительная клинико-лабораторная и рентгенологическая динамика в виде прекращения бактериовыделения, снижение системных воспалительных маркеров, а также рассасывания очаговоинфильтративных изменений в лёгочной ткани.
Несомненно, выполнение хирургического вмешательства у пациентов с выраженными эмфизема- тозными изменениями сопряжено с высоким риском длительного воздухотечения в послеоперационном периоде и развитие в дальнейшем спонтанного пневмоторакса при перерастяжении и без того изменённой лёгочной ткани [11–15]. Благодаря применению хирургического этапа лечения у пациента ликвидирован очаг туберкулёзной инфекции в лёгочной ткани. При патогистологическом исследовании операционного материала выявлена картина гранулематозно-некротического воспаления лёгочной ткани по туберкулёзному типу с признаками слабо выраженного прогрессирования и бронхогенной диссеминации. На этом фоне отмечены умеренные эмфизематозные изменения в виде булл. Кроме того, в лёгком, внутрилёгочном и внутриг-рудных лимфатических узлах были обнаружены множественные кониотические узелки, что подтверждает сочетание туберкулёза и пневмокониоза.
ЗАКЛЮЧЕНИЕ
В условиях роста больных туберкулёзом с сопутствующими заболеваниями и значимыми факторами риска существует необходимость разработки комплексного подхода в лечении данной категории пациентов. Данное клиническое наблюдение демонстрирует высокую эффективность применения комплексного подхода, направленного на лечение туберкулёзной инфекции, ХОБЛ и табакокурения у пациента с отягощённым профессиональным анамнезом.


