Особенности метаболизма лекарственных препаратов у пациентов с синдромом Жильбера
Автор: Ипатова М.Г.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.11, 2016 года.
Бесплатный доступ
Освещена современные представления о метаболизме лекарственных препаратов у пациентов с синдромом Жильбера. В основе заболевания синдрома Жильбера лежит снижение активности фермента глюкуронилтрансферазы, который, является ключевым ферментом во второй фазе биотрансформации лекарственных препаратов. В статье особое внимание уделено препаратам, которые метаболизируются с участием глюкуронилтрансферазы. Медикаментозная терапия у пациентов с синдромом Жильбера должна проводиться с учетом выявленных генетических дефектов в семействе UGT1A и особенностей метаболизма ЛП, что позволяет минимизировать побочные эффекты.
Синдром жильбера, уридилдифосфатглюкуронилтрансфераза (удф-гтф), метаболизм лекарственных препаратов, побочные эффекты лекарственных препаратов (лп)
Короткий адрес: https://sciup.org/140188506
IDR: 140188506 | УДК: 616.36-008.6:616-008.9:615.5
Features of pharmacotherapy in patients with Gilbert’s syndrome
Present the modern understanding of the problem of drug toxicity and liver damage in patients with Gilbert’s syndrome. Gilbert’s syndrome is based on reduced activity of the enzyme glucuronyltransferase, which is the main enzyme in the second phase of drug biotransformation. Focus of the article is on the medicines, on which metabolism presents glucuronyltransferase. Drug therapy in patients with Gilbert’s syndrome should be composed in view of these genetics defects and special aspects of drug metabolism to minimize drug side effects.
Текст научной статьи Особенности метаболизма лекарственных препаратов у пациентов с синдромом Жильбера
На сегодняшний день многие клиницисты рассматривают синдром Жильбера (СЖ) как хроническую семейную неконъюгированную гипербилирубинемию, имеющую доброкачественное течение. Это обусловлено изолированным повышением уровня билирубина в крови до умеренных значений (уровень билирубина в пределах 21–85 мкмоль/л) без нарушения других биохимических показателей функции печени и ее структуры [1, 2].
В основе СЖ лежит нарушение конъюгации билирубина (рис. 1) Непрямой билирубин (НБ), образованный в результате разрушения эритроцитов и гем-содержащих белков, циркулирует в плазме преимущественно в связанном с альбумином состоянии. Альбумин транспортирует НБ в печень, где он, связанный с лигандами, диффундирует в цитозоль с помощью белков-переносчиков семейства OATP. В эндоплазматическом ретикулуме (ЭР) происходит конъюгация билирубина в моно- и диглюкуронид с помощью фермента глюкуронилтрансферазы (UGT-1). Образовавшийся связанный билирубин (прямой билирубин, ПБ) экспортируется в желчный каналец с помощью транспортных белков семейства MRP2 (белок множественной лекарственной устойчивости-2) и небольшое количество с помощью белков MRP3 может выделяться через синусоидальную мембрану в кровь. Если в физиологических условиях экспрессия MRP1 и MRP3 находится на очень низком уровне, то при холестазе эти транспортеры начинают активно экспрессироваться [3].
Генетический дефект СЖ обусловлен наличием дополнительного динуклеотида ТА на промоторном участке А(ТА)6ТАА гена, кодирующего фермент УДФГТ, что ведет к образованию участка А(ТА)7ТАА. Удлинение промо-торной последовательности приводит к уменьшению образования фермента уридилдифосфатглюкуронил- трансферазы. Эта мутация обозначается UGT1A1 *28 и является наиболее распространенной и изученной [4].
Частота мутантного аллеля UGT1A1*28 в различных популяциях варьирует: 32–39% для европеоидов, 16–33% – для азиатских популяций, 40–43% – для негроидной популяций [5, 6, 7]. Мутантные аллели UGT1A1*36 и UGT1A1*37 обнаружены, главным образом, в негроидных популяциях, с частотой от 3 до 16% [5, 6, 8].
Есть данные о наличии до 113 вариантов мутаций данного гена (UGT1A1*1-*113) [1]. При варианте А(TA)7ТАА уровень продукции фермента может быть снижен до 80% от нормы у гетеро- и до 20% у гомозигот, соответственно.
Для пациентов с СЖ характерна интермиттирующая иктеричность склер и кожи на фоне голодания, инфекционных заболеваний, эмоциональной и физической нагрузки [9]. СЖ ассоциируется с высоким риском развития холелитиаза [10]. Это подтверждено мета-анализом, в который были включены 2816 пациентов с желчнокаменной болезнью (ЖКБ) и 1617 пациентов без ЖКБ. В результате исследования выявлено, что риск развития ЖКБ при СЖ повышался на 21,2%, причем чаще среди мужчин [10, 11]. Следует отметить, что при СЖ развитие ЖКБ может формироваться уже в детском возрасте. В исследовании (1992–2010 гг.), проведенном А.Р. Рейзис, было показано, что у 76,5% детей с СЖ имелась дисфункция билиарного тракта, почти у половины из них со сладж-синдромом. У 11,8% детей диагностировали уже развившуюся ЖКБ [12].
Клинической особенностью СЖ является появление или усиление желтухи, связанной с приемом некоторых лекарственных средств. В условиях дефицита фермента УДФГТ лекарственные средства конкурируют с билируби-

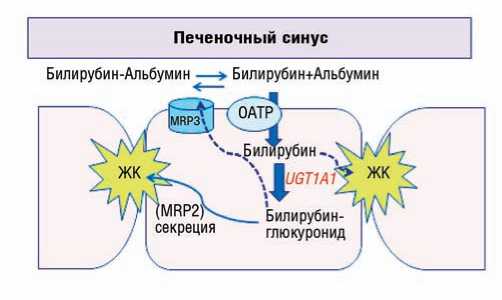
Рис. 1. Метаболизм и выведение билирубина в гепатоцитах
гепатоцид
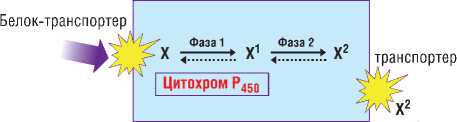
Фаза 1 - химическая модификация (окисление, восстановление, гидролиз)

Желчь Моча
Фаза 2 - трансформация метаболитов (конъюгация с эндогенными соединениями)
Фаза 3 - элиминация метаболитов ЛП
Рис. 2. Схема метаболизма лекарственных препаратов в гепатоците ном за фермент, что ведет к повышению НБ в сыворотке крови. Такие препараты называются аглюконами. К ним относятся: анаболические стероиды, глюкокортикостероиды, андрогены, рифампицин, циметидин, левомицетин, стрептомицин, салицилат натрия, ампициллин, кофеин, этинил-эстрадиол, парацетамол, ибупрофен, кетопрофен, сульфаниламиды, диакарб, ментол, кофеин, статины и др. [1]. Следовательно, применение препаратов-аглюконов у пациентов с СЖ может служить причиной развития лекарственного поражения печени. Поэтому перед специалистами стоит задача ранней диагностики СЖ и обдуманного назначения лекарственных средств с учетом особенностей их метаболизма у данной группы пациентов.
Метаболизм (биотрансформация) – это изменение химической структуры лекарственных веществ и их физикохимических свойств под действием ферментов организма. Метаболизм лекарственных препаратов включает в себя 3 фазы: Фаза I или химическая модификация с участием ферментов CYP450, Фаза II или трансформация метаболитов с помощью реакции коньюгации с глюкуроновой, серной, уксусной кислотами или аминокислотами и Фаза III – активный транспорт и элиминация продуктов биотрансформированных метаболитов с желчью и мочой (рис. 2).
Целью химической модификации в Фазе I является образование окисленных гидрофильных соединений за счет включения в их структуру функциональных групп: -OH, -NH2, -SH или -COOH. Введение гидроксильных групп в гидрофобный субстрат повышает полярность и растворимость молекулы ксенобиотика и облегчает ее выведение из организма.
Повышение водорастворимости химических соединений продолжается в реакциях биотрансформации (Фаза II). Ко второй фазе метаболизма ксенобиотиков относятся реакции глюкуронирования, сульфатирования, ацетилирования, метилирования, конъюгации с глютатионом и конъюгация с аминокислотами, такими как глицин, таурин, глутаминовая кислота. В результате реакций Фазы III ксенобиотики обычно полностью утрачивают биологическую активность, однако возможно образование активных метаболитов и канцерогенов. Метаболизм ЛП может осуществляться в реакциях исключительно Фазы I или II, одновременно в обеих (одна часть ЛП – в первой, другая – во второй), либо последовательно в каждой [13].
Конъюгация лекарственного препарата (ЛП) и его метаболитов с глюкуроновой кислотой, протекающая под действием глюкуронилтрансфераз, является одной из ключевых реакций Фазы II. Ферменты УДФ-глюкуронил-трансферазы подразделяют на 2 семейства UGT1 и UGT2, и описаны более 20 изоферментов. Глюкуронированию подвергаются ЛП, которые содержат функциональные группы, являющиеся акцепторами для УДФ-глюкуро-новой кислоты (фенолы, спирты, алифатические амины, карбоновые и карбоксильные кислоты).
Примером реакции может служить образование фенилглюкуронида:
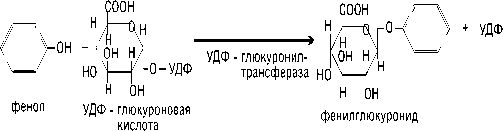
Примеры некоторых ЛП, подвергаемых глюкурони-рованию, представлены в табл. 1.
УДФ-глюкуронилтрансферазы также участвуют в метаболизме тироксина и трийодтиронина, стероидных гормонов, желчных кислот, ретиноидов, однако эти реакции в настоящее время изучены недостаточно.
Благодаря гидрофильности глюкурониды легко выводятся с мочой и желчью. Большинство реакций II фазы метаболизма происходят в цитозоле, но глюкуронил-трансферазы относятся к микросомальным ферментам, поэтому продукты протекающей в микросомах I фазы метаболизма здесь же подвергаются конъюгации [13].

Табл. 1. ЛП, подвергаемые глюкуронированию различными изоферментами УДФГТ
|
UGT1А1 |
UGT1А4 |
UGT1А6 |
UGT1А9 |
UGT1В7 |
UGT2В7 |
|
Бупренофин |
Имипрамин |
Фенол |
Фенол |
Клофибрат |
Морфин |
|
Амитриптилин |
Парацетамол |
Вальпроевая кислота |
Фенопрофен |
||
|
Хлорпромазин |
Буметанид |
Напроксен |
Зомепирак |
||
|
Ламотриджин |
Ибупрофен |
Кетопрофен |
Дифлунизал |
||
|
Доксепин |
Вальпроевая кислота |
Лабетолол |
Фенопрофен |
||
|
Прометазин |
Этинил- эстрадиол |
Ибупрофен |
|||
|
Ципрогептидин |
Дапсон |
Кетопрофен |
|||
|
Кетотифен |
Микофенольная кислота |
Оксазепам |
|||
|
Морфин |
Учитывая то, что ряд препаратов является субстратом для глюкуроновой кислоты, можно предположить, что у пациентов с СЖ при сниженной активности данного фермента, будет преобладать альтернативный путь его метаболизма. Образующиеся при этом метаболиты способны вызывать гепатотоксические реакции у пациентов с СЖ, либо усиливать побочные эффекты данных препаратов. В зарубежной литературе имеются данные о доказанном лекарственном поражении печени у пациентов с СЖ на фоне приема Иринотекана, Атазанавира [1, 14, 15]. Иринотекан (камптотецин), используемый для лечения колоректального рака и других солидных опухолей, в организме превращается в активную форму SN-38 под действием карбоксилестеразы [1, 15, 16]. SN-38 метаболизируется глюкуроновой кислотой в неактивные метаболиты и выводится с желчью или через почки. Побочные реакции иринотекана связаны с миелосупрес-сией (лейкопения, тромбоцитопения, анемия), а также с возникновением диареи. Было установлено, что чаще всего возникновение таких побочных эффектов ассоциировано с сочетанием мутации UGT1A1 *28 и мутации в гене UGT1A7 , что в значительной степени способствует снижению активности УДФГТ. В результате активный токсичный метаболит иринотекана оказывает большее воздействие на кишечник и костный мозг, усиливая проявление побочных реакций [1].
Другое проведенное исследование – метаболизм атазанавира у пациентов с СЖ. Данное вещество относится к ингибиторам протеаз, которые используются в антиретровирусной терапии. У ВИЧ-инфицированных пациентов с одним из генетических вариантов СЖ наблюдалось нарастание гипербилирубинемии во время терапии данным лекарственным средством. Однако это связано не с путем элиминации, а со способностью ата-занавира ингибировать активность УДФГТ. Вероятно, что тем же эффектом обладают другие лекарственные средства из группы ингибиторов протеазы, так как желтуха является частым побочным эффектом у препаратов из данной группы [1, 17].
Следует отметить, что токсичные метаболиты некоторых ЛП могут вызывать развитие гипербилирубинемии с внутрипеченочным холестазом вследствие повреждения белков-переносчиков семейства BSEP (bile salt export pump), экспортирующих желчные кислоты, либо белков-транспортеров семейства MRP2, участвующих в экспорте билирубина и других молекул, из гепатоцита в желчные канальцы (рис. 3) [18]. К таким препаратам относятся андрогены (метилтестостерон, ретаболил, неробол) и эстрогены (регивидон, триквилар, ноновлон), цитостатики (циклоспорин А), хлорпромазин, сульфаниламиды, полусинтетические и синтетические пенициллины (оксациллин, ампициллин, амоксициллин, карбенициллин, метициллин, флуклоксациллин), макролиды (эритромицин, олеандомицин), цефалоспорины (цефтриаксон и цефтазидим), блокаторы гистаминовых рецепторов (циметидин, ранитидин), пероральные сахароснижающие препараты – производные сульфанилмочевины (глибурид, гликлазид, глибенкламид) и другие [19, 20].
Выбор гепатопротектора при лекарственном поражении печени осуществляется в зависимости от клиникоморфологических проявлений поражения печени. На сегодняшний день препаратом выбора в лечении холестаза, в том числе лекарственно- индуцированного, является урсодезоксихолевая кислота (УДХК). В многочисленных исследованиях было показано, что УДХК стимулирует как канальцевые белки-транспортеры (MRP2, BSEP), так и базолатеральные транспортные белки (MRP3, MRP4). Это способствует элиминации потенциально токсических субстратов из гепатоцитов [20].
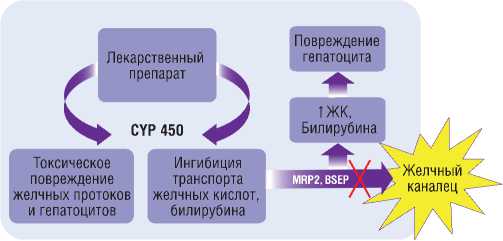
Рис. 3. Схема развития холестаза метаболитами лекарственных препаратов

Также доказана эффективность УДХК в качестве превентивного лечения холелитиаза у пациентов с СЖ. В исследовании Рейзис А.Р. (2011 г.) было показано, что количество больных ЖКБ сократилось в 4,5 раза на фоне приема УДХК [6].
Урсофальк является референтным препаратом урсодезоксихолевой кислоты (УДХК). Большая часть исследований по эффективности и безопасности применения УДХК в Европе проведена именно на препарате Урсофальк. Все другие препараты УДХК при регистрации в соответствующих странах мира должны представить доказательства о фармакологической и клинической эквивалентности Урсофальку. Подавляющая часть исследований по эффективности и безопасности УДХК в Европе проведена с применением Урсофалька (более 4000 научных работ) [21].
Приведем клинический пример, наглядно демонстрирующий поражение печени в виде патологического изменения биохимических показателей на фоне анти-хеликобактерной терапии у пациента с СЖ.
Мальчик-подросток 16 лет 3 месяцев поступил в стационар на обследование и лечение с диагнозом: язва луковицы двенадцатиперстной кишки в стадии открытого дефекта. Хронический гастродуоденит, обострение, ассоциированный с Helicobacter pylori (по данным эзофагогастродуоденоскопии с Хелпил-тестом).
При поступлении: жалобы на боли в эпигастрии, купирующиеся приемом пищи. Кожные покровы бледные, легкая краевая субиктеричность склер. Физическое развитие: без отклонений от нормы. В общем анализе крови и мочи – без патологических изменений. Реакция на скрытую кровь в кале – слабоположительная. В биохимическом исследовании крови: гипербилирубинемия до 28 мкмоль/л (норма до 20,5 мкмоль/л), за счет непрямой фракции 24 мкмоль/л. Остальные показатели были в пределах референтных значений. Маркеры вирусных гепатитов В и С – отрицательные. При ультразвуковом исследовании органов брюшной полости патологии не было выявлено. Семейный анамнез: у папы СЖ (генетически подтвержденный), язвенная болезнь двенадцатиперстной кишки; у мамы – хронический гастродуоденит. Ребенку генетическое обследование на СЖ не проводилось.
В условиях стационара назначена антихеликобак-терная квадротерапия, включающая висмута трикалия дицитрат, омепразол, амоксициллин, кларитромицин на 10 дней. На 8 сутки от начала лечения у ребенка появилась иктеричность склер и кожных покровов. Было рекомендовано контрольное биохимическое исследование крови и молекулярно-генетическое исследование на СЖ. В биохимическом анализе отмечалось нарастание общего билирубина (ОБ) до 3 норм (66 мкмоль/л) за счет НБ до 61 мкмоль/л без синдрома цитолиза и холестаза. Молекулярно-генетическое исследование выявило мутацию в промоторной области гена UGT1A1, установлен генотип А(ТА)7ТАА/А(ТА)7ТА, что является основанием для постановки диагноза СЖ.
Было решено в терапию включить препарат УДХК (Урсофальк) в дозе 10 мг/кг. На фоне отмены антибактериальной терапии и приеме Урсофалька у ребенка при контрольном проведении биохимического анализа крови отмечалось снижение ОБ до 45 мкмоль/л (НБ – 41 мкмоль/л). Через 3 недели от начала лечения на эзофагогастродуоденоскопии выявлена полная эпителизация язвенного дефекта. Хелпил тест – отрицательный. Прием УДХК был рекомендован курсом до 1 месяца.
Данный клинический пример наглядно показывает, что прием некоторых лекарственных препаратов у пациентов с синдромом Жильбера может приводить к нарастанию желтухи за счет дефицита фермента УДФГТ и/или повреждения белков-транспортеров семейства MRP2, участвующих в экспорте билирубина из гепатоцита в желчные канальцы.
Заключение
Исследования, направленные на выявление генетических дефектов в семействе UGT1A, позволяет врачам более рационально назначать ЛП пациентам с учетом их генетических особенностей. Одним из направлений ведения пациентов с СЖ должна стать минимизация лекарственных воздействий, а при необходимости длительной терапии потенциально токсичными лекарственными средствами – индивидуальный подбор препаратов с учетом особенностей метаболизма лекарств.
Включение фармакогенетического тестирования в стандарты обследования пациентов с СЖ позволит предотвратить возможные токсические эффекты от применения препаратов-аглюконов.
Для профилактики и лечения неблагоприятных последствий СЖ целесообразно применение урсодезоксихолевой кислоты (Урсофальк).
Список литературы Особенности метаболизма лекарственных препаратов у пациентов с синдромом Жильбера
- Cristian P. Pharmacogenetics of Gilbert’s syndrome./Pharmacogenomics (2008) 9 (6) P: 706-715.
- Подымова С.Д. Болезни печени. -М.: Медицина, 1998. -704 с.
- Fretzayas A., Moustaki M., Liapi O., Karpathios T./Eponym. Gilbert syndrome./Ear J Pediatr (2012) 171: 11-15.
- Thomas D. Boyer MD, Michael P. Manns MD, "Zakim and Boyer’s Hepatology: A Textbook of Liver Disease -Expert Consult, 6th edition” 2011/ISBN: 1437708811/1408 p.
- Beutler E., Gelbart T., Demina A. (1998) Racial variability in the UDP-glucuronosyltransferase 1 (UGT1A1)promoter: a balanced polymorphism for regulation of bilirubin metabolism? -Proc. Natl. Acad. Sci. USA, 95 (14), 8170-8174.
- Farrar J.S., Palais R.A., Wittwer C.T. (2011) Snapback primer genotyping of the Gilbert syndrome UGT1A1(TA)(n) promoter polymorphism by high-resolution melting. -Clin. Chem., 57 (9), 1303-1310.
- Fertrin K.Y., Gonçalves M.S., Saad S.T., Costa F.F. (2002) Frequencies of UDP glucuronosyltransferase 1 (UGT1A1) gene promoter polymorphisms among distinct ethnic groups from Brazil. -Am. J. Med. Genet., 108 (2), 117-119.
- Premawardhena A., Fisher C.A., Liu Y.T., Verma I.C., de Silva S., Arambepola M., Clegg J.B., Weatherall D.J. (2003) The global distribution of length polymorphisms of the promoters of the glucuronosyltransferase 1 gene(UGT1A1): hematologic and evolutionary implications. -Blood Cells Mol. Dis., 31 (1), 98-101. PMID: 12850492.
- Еселев М.М. Синдром Жильбера/М.М. Еселев, П.Г. Сцепуро. -Саратов: Изд-во Саратов. ун-та, 1991. -68 с.
- Gilbert syndrome as a predisposing factor for cholelithiasis risk in the Greek adult population/A. Tsezou //Genet. Test. Mol. Biomarkers. 2009. Vol. 13. № 1. P. 143-146.
- Loci from a genome-wide analyses of bilirubin levels are associated with gallstone risk and composition/S. Buch //Gastroenterology. 2010. Vol. 139. № 6. P. 1942-1951.
- Рейзис А.Р., Хохлова О.Н., Никитина Т.С./Синдром Жильбера: современные воззрения, исходы и терапия.//Доктор.ру №3 (71) -2012.
- Кукес В.Г. Клиническая фармакология. -М.: ГЭОТАР Медицина, 2004. -936 с.
- Ali Rasa, John Vierling, Khozema B. Hussain. Genetics of Drug-Induced Hepatotoxity in Gilbert’s syndrome./The American Journal of Gastroenterology (2013) 108: P. 1936-1937.
- Douillard JY,Cunningham D, Roth AD et al: Irinotecan combined with fluorouracil compared with fluorouracil alone as first line treatment for metastatic colorectal cancer:a multicantral randomized trail. Lancet 355 (9209),1041-1047 (2000).
- Folprecht G, Kohne CH: The role of new agents in the treatment of colorectal cancer. Oncology 66 (1),1-17 (2004).
- McLeod HL, et al. Pharmacogenetic predictors of adverse events and response to chemotherapy in metastatic colorectal cancer: results from North American Gastrointestinal Intergroup Trial N9741. J Clin Oncol 2010;28: 3227-33.
- Полунина Т.Е., Маев И.В. Лекарственные поражения печени//Consilium medicum. -2011. -Гастроэнтерология № 2. -С. 54-60.
- С.Г. Хомерики, Н.М. Хомерики лекарственные поражения печени учебное пособие для врачей. Москва 2012 с. 40.
- Paumgartner G, Beuers U. Mechanisms of action and therapeutic efficacy of ursodeoxycholic acid in cholestatic liver disease. Clin Liver Dis. 2004;8: 67-81. vi.
- Морозов С.В. Гепатопротекторы в клинической практике: рациональные аспекты использования: Пособие для врачей/С.В. Морозов, Ю.А. Кучерявый. -М.: 4 ТЕ Арт, 2011. -28 с.


