Особенности микробного пейзажа при разных типах перипротезной инфекции тазобедренного сустава
Автор: Прокопьев Д.С., Аминева П.Г., Бугаев Г.А., Виноградский А.Е., Борзунов Д.Ю.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.32, 2026 года.
Бесплатный доступ
Введение. При стабильном росте количества выполняемых операций первичного тотального эндопротезирования крупных суставов актуальной становиться проблема ликвидации перипротезной инфекции (ППИ). Рост возбудителей ППИ, устойчивых к антимикробным препаратам, значительно усложняет и затягивает процесс лечения, способствуют формированию хронической инфекции, в ряде случаев со стертыми клиническими проявлениями. Цель работы — выявить особенности микробного пейзажа при разных типах ППИ тазобедренного сустава (ТБС). Материалы и методы. Проведен анализ микробиологических исследований 96 пациентов с ППИ ТБС: группа 1 (n = 16) — I тип ППИ; группа 2 (n = 80) — II и III типы ППИ. Пациентам группы 1 выполняли процедуру DAIR, группы 2 — двухэтапное ревизионное эндопротезирование. Результаты. У 96 пациентов получено 103 микробных изолята: Гр(–) — 16 (15,5 %), Гр(+) — 87 (84,5 %). Среди Гр(+) MRSA, MRSE, MRSH встречали в 18 изолятах, у Гр(–) БЛРС+ — в 16 исследованиях. В структуре ППИ преобладали S. aureus (52,9 %), S. epidermidis (19,5 %), E. сloacae (37,5 %), P. aeruginosa (18,6 %) и E. Coli (18,6 %). Ассоциации при I типе ППИ (25 %) встречались чаще, чем при хронических формах (18,4 %). В 20 (19,4 %) случаях обнаружены микробные ассоциации. У 16 (16,7 %) пациентов обеих групп выявлена культурально-негативная инфекция (КНИ). Рецидив ППИ у пациентов с микробными ассоциациями произошел в трех (15 %) случаях. У пациентов с КНИ рецидив — в четырех (25 %) случаях. Обсуждение. Рост Гр(–) флоры при ранних формах ППИ превышал показатели хронических форм, — 31,3 % и 9,2 % соответственно. DAIR в таких условиях малоэффективен. S. aureus как возбудитель инфекций костей и суставов существует в квазидремлющем состоянии, что способствует хронизации. Заключение. В структуре этиологии ранней ППИ (I тип) преобладали грамотрицательные микроорганизмы и их ассоциации, при хронических формах (II и III тип) — грамположительные патогены. Культурально-негативная инфекция являлась причиной развития ранних форм ППИ чаще, чем хронических (25,0 % и 16,1 % соответственно). Статистически значимых различий между группами по выделению метициллинрезистентного стафилококка, а также грамотрицательных бактерий БЛРС+ не выявлено.
Тазобедренный сустав, перипротезная инфекция, ревизионное эндопротезирование, культурально-негативная инфекция, микробный пейзаж
Короткий адрес: https://sciup.org/142247044
IDR: 142247044 | УДК: 616.728.2-022.1-089.843-77-089.193.4:579.8 | DOI: 10.18019/1028-4427-2026-32-1-5-13
Microbial landscape in different types of periprosthetic hip joint infection
Introduction Due to the steady increase in the number of primary total hip arthroplasties, the problem of eliminating periprosthetic joint infection (PJI) has become pressing. The rise of antimicrobial-resistant PJI pathogens significantly complicates and prolongs treatment, contributing to the development of chronic infection, sometimes with latent clinical manifestations. The aim of this study was to identify the microbial landscape characteristics in different types of hip joint PJI. Materials and Methods Microbiological studies of 96 patients with hip joint PJI were analyzed: Group 1 (n = 16) with type I PJI; Group 2 (n = 80) with type II and type III PJI. Patients in Group 1 underwent the DAIR procedure and those in Group 2 underwent two-stage revision hip replacement. Results A total of 103 microbial isolates were obtained from 96 patients: 16 (15.5 %) Gr(–) and 87 (84.5 %) Gr(+). Among Gr(+), MRSA, MRSE, and MRSH were detected in 18 isolates, and among Gr(–), ESBL+ was detected in 16 isolates. The predominant pathogens in the PJI structure were S. aureus (52.9 %), S. epidermidis (19.5 %), E. cloacae (37.5 %), P. aeruginosa (18.6 %), and E. coli (18.6 %). Associations were more common in type 1 PJI (25 %) than in chronic forms (18.4 %). Microbial associations were detected in 20 cases (19.4 %). Culture-negative infection (CNI) was detected in 16 patients (16.7 %) in both groups. Relapse of PJI in patients with microbial associations occurred in three cases (15 %). In CNI cases, recurrence developed in four cases (25 %). Discussion The growth of Gr(–) flora in early PJI exceeded that in the chronic one: 31.3 % and 9.2 %, respectively. DAIR is ineffective in such conditions. S. aureus, as a causative agent of bone and joint infections, exists in a quasi-dormant state which contributes to chronicity. Conclusion Gram-negative microorganisms and their associations dominate in the etiology of early PJI (type I), while gram-positive pathogens predominated in chronic types (types II and III). Culture-negative infection was a more common cause of early PJI than of chronic types (25.0 % and 16.1 %, respectively). No statistically significant differences were found between the groups in the detection of methicillin-resistant staphylococci or gram-negative bacteria ESBL+.
Текст научной статьи Особенности микробного пейзажа при разных типах перипротезной инфекции тазобедренного сустава
При стабильном росте количества выполняемых в мире операций первичного тотального эндопротезирования крупных суставов актуальной становиться проблема ликвидации осложнений, в первую очередь перипротезной инфекции (ППИ) [1, 2, 3]. Диагностика ППИ является сложной задачей. Идентификация соответствующих патогенов важна и является основой для целевого применения антибактериальных препаратов [4]. Традиционно возбудителей инфекции идентифицируют путем микробиологического исследования (МБИ) синовиальной жидкости и тканевых интраоперационных биоптатов. Тем не менее, отсутствие роста микроорганизмов при культивировании достигает 40 % по разным причинам:
-
— формирование биопленок;
-
— образование инертных патогенов;
-
— идентификация возбудителей в неподходящей питательной среде;
-
— применение до верификации возбудителя антибиотиков;
-
— колонизация остеоцитарно-лакунарно-канальцевой сети кортикальной кости [5];
Рост возбудителей ППИ, устойчивых к антимикробным препаратам, значительно усложняет и затягивает процесс лечения. К таким патогенам относятся штаммы стафилококков, резистентные к препаратам трех и более классов, фторхинолон-резистентные и карбапенем-резистентные грамо-трицательные микроорганизмы, грибковая микрофлора [6, 7, 8].
Всё вышеуказанное способствуют формированию хронической инфекции, в ряде случаев со стертыми клиническими проявлениями. Это затрудняет диагностику и определяет значительную долю неудач при лечении пациентов с ортопедической инфекцией [6, 9].
Цель работы — выявить особенности микробного пейзажа при разных типах перипротезной инфекции тазобедренного сустава.
МАТЕРИАЛЫ И МЕТОДЫ
Дизайн исследования . Проведен ретроспективный анализ результатов МБИ пунктатов и тканевых интраоперационных биоптатов от 96 пациентов с ППИ тазобедренного сустава (МКБ-10: Z96.6), проходивших лечение с 2015 по 2020 гг. в гнойном хирургическом отделении Свердловского областного клинического психоневрологического госпиталя для ветеранов войн.
Критерии включения : пациенты с клинико-лабораторными признаками ППИ, которым в условиях стационара выполнен о оперативное лечение.
Критерии невключения : пациенты без признаков ППИ.
Исследование одобрено локальным этическим комитетом Госпиталя ветеранов войн (Екатеринбург, протокол от 09.11.2015 г., No 9.2/2015) и проведено в соответствии с Хельсинской декларацией 1975 г. (пересмотр в 2008 г.). Все пациенты подписали информированное согласие на исследование. Детализирующая информация, способствующая персонификации включенных в исследование пациентов, отсутствует.
В соответствии с классификацией глубокой инфекции после полной артропластики тазобедренного сустава (Coventry – Fitzgerald – Tsukayama, [10]) исследуемые разделены на две группы. В группу 1 вошли 16 пациентов с ранней формой ППИ, соответствующей I типу по классификации Tsukayama. В группу 2 включено 80 (83,3 %) пациентов с хронической ППИ, среди которых 39 случаев (48,75 %) составили тип II и 41 случай (51,25 %) — тип III. В наше исследование не вошли пациенты с IV типом ППИ.
В большинстве случаев пациентам группы 1 выполняли процедуру DAIR ( англ .: Debridement, Antibiotics, and Implant Retention). В группу 1 также включены больные с обширными костно-мышечными дефектами после предшествующих оперативных вмешательств и тяжелым соматическим состоянием, выполнение ревизионного эндопротезирования у которых не представлялось возможным. Таким больным выполняли резекционную артропластику тазобедренного сустава и удаление компонентов эндопротеза.
Пациентам группы 2 выполняли двухэтапное ревизионное эндопротезирование тазобедренного сустава.
Исследуемые группы были сопоставимы по поло-возрастным характеристикам ( p > 0,05) (табл. 1). Анализ показал отсутствие статистически значимых различий между группами ранней ( n = 16) и хронической ППИ ( n = 80). При стратификации по возрасту < 65 лет и ≥ 65 лет также не выявлено статистически значимых различий ( p = 0,059).
Таблица 1
Поло-возрастные характеристики пациентов
|
Параметры сравнения |
Группа 1 |
Группа 2 |
P -value |
|
|
Ранняя ППИ ( n = 16) |
Хроническая ППИ ( n = 80) |
|||
|
Мужчины |
абс. |
10 |
42 |
0,464 |
|
% |
62,5 |
52,5 |
||
|
Женщины |
абс. |
6 |
38 |
|
|
% |
37,5 |
47,5 |
||
|
Возраст, лет (M ± SD) |
63,7 ± 11,1 |
57,9 ± 12,2 |
0,656 |
|
|
< 65 лет |
абс. |
8 |
59 |
0,059 |
|
% |
50,0 |
73,8 |
||
|
≥ 65 лет |
абс. |
8 |
21 |
|
|
% |
50,0 |
26,2 |
||
Гнойно-воспалительные осложнения после предшествующих ревизионных вмешательств возникли у восьми (50 %) пациентов группы 1 и у 41 (51,3 %) пациента группы 2.
В 41 (83,7 %) случае из 49 ревизионных вмешательств на предыдущих этапах лечения во время МБИ в тканевых биоптатах был обнаружен патоген.
После первого этапа двухэтапного ревизионного эндопротезирования у пациентов группы 2 рецидив инфекции возник в семи (8,8 %) случаях. Рецидив инфекции после выполнения процедуры DAIR отмечен у одного (6,25 %) пациента группы 1.
У 15 (18,75 %) пациентов группы 2 на I этапе ревизионного эндопротезирования использовали метод NPWT ( англ .: negative-pressure wound therapy), что связано с выраженным гнойным расплавлением мягких тканей, некрозами и склеротическими изменениями костной ткани [11–14]. В данной группе пациентов выявили один (6,7 %) случай рецидива ППИ.
При поступлении в стационар у всех больных собирали жалобы и анамнестические данные, выполняли общий и местный осмотр, выявляли местные признаки воспаления. Для выявления нестабильности имплантов и патологических изменений прилежащих костных структур всем пациентам выполнены рентгенологические исследования пораженных суставов, а при наличии наружных свищей, — рентге-нофистулография [1, 5].
Лабораторные исследования включали определение количества лейкоцитов, показателей СОЭ и С-реактивного белка крови и ее сыворотки [15, 16]. Для бактериологического и цитологического исследования пунктата выполняли диагностическую пункцию перипротезной полости вне зависимости от наличия свищевого хода [17, 18].
Микробиологическое (культуральное) исследование
Исследовали биоматериал, полученный при помощи диагностической пункции перипротезной полости, и интраоперационные тканевые биоптаты. Биоптаты перед посевом гомогенизировали. Биоматериал собирали в стерильный контейнер в соответствии с рекомендациями по забору проб и в течение двух часов доставляли в лабораторию.
После вортексирования 10 мкл пункционной жидкости с помощью стерильной калиброванной петли высевали на питательные среды методом истощающего посева.
Посев производили на питательные среды:
-
— 5 % агар c кровью барана (основа Колумбийский агар, Bio-Rad, Франция; кровь барана дефибриниро-ванная, E&O Laboratories, Шотландия),
-
— шоколадный агар (основа Колумбийский агар, Bio-Rad, Франция; кровь барана дефибринированная, E&O Laboratories, Шотландия),
-
— желточно-солевой агар (питательный агар для культивирования микроорганизмов ГРМ-агар, ФБУН ГНЦ ПМБ, Россия),
-
— агар Сабуро с 2 % глюкозы и хлорамфениколом (SIFIN diagnostics, Германия).
Для обогащения и выделения анаэробов 100 мкл пункционной жидкости засевали в тиогликолевую среду в пробирках с высоким столбиком (ФБУН ГНЦ ПМБ, Россия). Затем засеянные чашки Петри помещали в термостат с аэробными условиями при температуре (37 ± 1) ° С, чашки с кровяным и шоколадным агаром инкубировали в атмосфере, содержащей 5 % CO 2 . Посевы инкубировали до 72 часов, с оценкой роста через 24, 48, 72 часа.
Идентификацию выросших колоний производили фенотипическими методами (окраска по Граму, тесты на оксидазу, каталазу и др.) и с помощью бактериологического анализатора WalkAway 40 Plus (Beckman Coulter, США).
Чувствительность к антибиотикам определяли диско-диффузионным методом по стандартной методике, описанной EUCAST, а также с использованием бактериологического анализатора WalkAway 40 Plus (Beckman Coulter, США).
Интерпретацию категорий чувствительности осуществляли по актуальным критериям EUCAST: Clinical breakpoints — bacteria .
Статистический анализ проводили с применением программного обеспечения Jamovi (версия 2.6.17, Австралия) и Microsoft Excel (версия 16.75.2, США). Для описания количественных данных с нормальным распределением использовали среднее значение и стандартное отклонение (М ± SD), для отличных от нормального — медиану и межквартильный интервал (МКИ), соответствующий нижнему (Q1) и верхнему (Q3) квартилям. Проверку нормальности распределения данных проводили с помощью критерия Шапиро – Уилка. Категориальные данные описывали с указанием абсолютных значений и процентных долей ( n , %). Сравнение групп по количественному показателю с нормальным распределением данных выполняли с помощью t-тест Стьюдента или критерия Манна – Уитни U при распределении, отличном от нормального. Для оценки различий между группами по категориальным признакам составляли таблицы сопряжённости 2 × 2. В случаях, когда ожидаемая частота в ячейках превышала 5, использовался критерий χ ² Пирсона. При наличии малых ожидаемых частот (< 5) применяли точный критерий Фишера. Статистическую значимость различий между группами принимали при p < 0,05.
РЕЗУЛЬТАТЫ
Анализ клинических проявлений перипротезной инфекции при поступлении в стационар (табл. 2) показал высокую частоту свищей и ран, которые выявляли у 93,8 % пациентов группы 1 с ранней ППИ и у 80,0 % пациентов группы 2 с хронической ППИ. Гиперемия кожных покровов в области поражённого сустава зарегистрирована в 87,5 % случаев в группе 1 и в 67,5 % случаев в группе 2. Болевой синдром в оперированном суставе отмечен у большинства пациентов обеих групп. Повышение температуры тела до фебрильных значений встречалось относительно редко. Статистически значимых различий по данным клиническим проявлениям между группами не выявлено ( p > 0,05).
Таблица 2
Частота выявления диагностически значимых клинических проявлений ППИ при поступлении в стационар
|
Клинические проявления |
Группа 1 |
Группа 2 |
P -value Точный тест Фишера |
||
|
Ранняя ППИ ( n = 16) |
Хроническая ППИ ( n = 80) |
||||
|
абс. |
% |
абс. |
% |
||
|
Свищи/раны |
15 |
93,8 |
64 |
80,0 |
0,289 |
|
Гиперемия кожных покровов в области пораженного сустава |
14 |
87,5 |
54 |
67,5 |
0,139 |
|
Болевой синдром в оперированном суставе |
13 |
81,3 |
71 |
88,8 |
0,415 |
|
Повышение температуры тела до фибрильных значений |
2 |
12,5 |
18 |
22,5 |
0,510 |
Рецидив ППИ после I этапа отмечен у семи (8,8 %) пациентов группы 2. II этап ревизионного эндопротезирования ТБС выполнен 64 (80 %) пациентам.
Одному пациенту с I типом ППИ в группе 1 после DAIR выполнили двухэтапное ревизионное эндопротезирование, давшее положительным результат.
Два и более сопутствующих заболевания (сахарный диабет, системные заболевания, ожирение, ВИЧ-инфекция, гепатиты В и С, инъекционная наркомания и др.), являющихся факторами риска развития ППИ [1], отмечали в девяти (56,3 %) случаях в группе 1 и в 58 (72,5 %) наблюдениях в группе 2.
Анализ лабораторных показателей воспалительной активности при поступлении (табл. 3) выявил отсутствие статистически значимых различий между группами ( p > 0,05). Среднее количество лейкоцитов было выше в группе ранней ППИ ( p = 0,298). Уровень СОЭ также был выше в группе 1, но различия не достигли статистической значимости ( p = 0,130). Концентрация С-реактивного белка имела тенденцию к более высоким значениям при ранней ППИ ( p = 0,055).
В МБИ 96 пациентов с ППИ получено 103 микробных изолята, из них 16 (15,5 %) — грамотрицательные микроорганизмы и 87 (84,5 %) — грамположительные (табл. 4, рис. 1, 2).
Таблица 3
Лабораторные показатели воспалительной активности у пациентов с ранней и хронической перипротезной инфекцией
|
Показатели |
Группа 1 |
Группа 2 |
P -value |
|
Ранняя ППИ ( n = 16) |
Хроническая ППИ ( n = 80) |
||
|
Количество лейкоцитов, 109/л |
7,85 ± 1,97 |
7,30 ± 2,60 |
0,298 |
|
СОЭ, мм/час |
41,25 ± 20,20 |
30,68 ± 18,65 |
0,130 |
|
С-реактивный белок, мг/л |
115,63 ± 44,73 |
74,97 ± 55,94 |
0,055 |
Таблица 4
Структура микробного пейзажа в изолятах исследуемых групп
|
Возбудитель/группа |
Группа 1 |
Группа 2 |
Всего ( n = 103) |
|||
|
Ранняя ППИ ( n = 17) |
Хроническая ППИ ( n = 86) |
|||||
|
абс. |
% |
абс. |
% |
абс. |
% |
|
|
Грамположительные микроорганизмы |
11 |
64,7 |
76 |
88,4 |
87 |
84,5 |
|
Staphylococcus аureus |
7 |
41,2 |
39 |
45,3 |
46 |
44,7 |
|
Staphylococcus epidermidis |
1 |
5,9 |
16 |
18,6 |
17 |
16,5 |
|
Enterococcus faecalis |
1 |
5,9 |
7 |
8,1 |
8 |
7,8 |
|
Другие КНС** |
2 |
11,8 |
12 |
13,9 |
14 |
13,6 |
|
Грамотрицательные микрооранизмы |
6* |
35,3* |
10* |
11,6* |
16 |
15,5 |
|
Enterobacter сloacae |
4 |
23,5 |
2 |
2,3 |
6 |
5,8 |
|
Pseudomonas aeruginosa |
1 |
5,9 |
2 |
2,3 |
3 |
2,9 |
|
Другие Грам– возбудители*** |
1 |
5,9 |
6 |
7,0 |
7 |
6,8 |
Примечание : * — различия между группами статистически значимы ( χ ² = 6,06; Критерий Пирсона p = 0,014); ** — в категорию «Другие коагулазонегативные стафилококки (КНС)» включены: Staphylococcus hominis , S. capitis , S. warneri , S. intermedius ; *** — в категорию «Другие Грам– возбудители» включены: Escherichia coli , Acinetobacter baumannii , Klebsiella pneumoniae , Proteus mirabilis .
Анализ микробного пейзажа по изолятам (табл. 4) выявил статистически значимые различия между ранней и хронической перипротезной инфекцией тазобедренного сустава ( χ ² = 6,06; p = 0,014). В группе ранней ППИ ( n = 17 изолятов) грамотрицательные микроорганизмы были выделены в 35,3 % случаях, тогда как при хронической форме ( n = 86 изолятов) — лишь в 11,6 % случаях. Напротив, грамположи-тельная флора преобладала при хронической ГППИ.
Среди грамположительных бактерий MRSA ( англ .: methicillin-resistant staphylococcus aureus ), MRSE ( англ .: methicillin-resistant staphylococcus epidermidis ), MRSH ( англ .: methicillin-resistant staphylococcus hominis ) встречали в 18 (20,7 %) изолятах (два изолята (11,1 %) — в группе 1, 16 (88,9 %) — в группе 2). В структуре грамотрицательных бактерий БЛРС+ встречали в 16 (25 %) исследованиях (два (12,5 %) — в группе 1, 14 (87,5 %) — в группе 2 соответственно).
Микробные ассоциации обнаружены в 20 (19,4 %) случаях из общего числа микроорганизмов ( n = 103): ассоциации из бактерий Гр(+) и Гр(–) встречали в семи (35 %) случаях; Гр(+) ассоциации — в 10 (50 %); Гр(–) — в трех (15 %) случаях. Обнаружены четыре (20 %) ассоциации, имеющие в составе три и более возбудителя.
У 16 (16,7 %) пациентов обеих групп, несмотря на клинико-лабораторную картину ППИ, результаты МБИ дали отрицательный результат.
Рецидивы ППИ у пациентов с микробными ассоциациями отмечали в трех (15 %) случаях из 20. Рецидив зарегистрирован у четырех (25 %) пациентов с культурально-негативной инфекцией (КНИ).
На рис 3. показана сравнительная оценка микробного пейзажа возбудителей 1 и 2 групп.
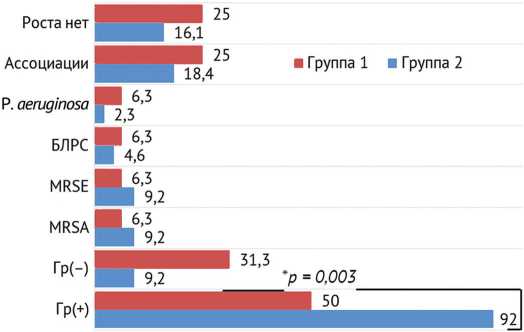
Рис. 3. Микробный пейзаж возбудителей ранней (I тип) и хронической (II–III тип) форм ППИ, %
Анализ микробного пейзажа среди пациентов также показал достоверные различия в распределении возбудителей ранней и хронической перипротезной инфекцией ( χ ² = 8,94, p = 0,003). В группе ранней ППИ ( n = 16) грамотрицательную флору выявили в 31,3 % случаев ( n = 5), что существенно чаще по сравнению с хронической ГППИ ( n = 80), где грамотрицательные микроорганизмы встречали лишь в 9,2 % случаев ( n = 7). Напротив, грамположительная флора преобладала при хронической инфекции — 92 % ( n = 74) против 50 % ( n = 8) случаев при ранней форме.
Полученные данные подтверждают, что гра-мотрицательные микроорганизмы оказыва- ют значимое влияние на развитие ранних форм перипротезной инфекции, в то время как хронический вариант заболевания преимущественно ассоциирован с грамположительной флорой.
Среди пациентов группы 2, которым на I этапе ревизионного эндопротезирования применяли NPWT ( n = 15), в интраоперационных МБИ встречали только грамположительную флору. Всего в этой группе получено 12 микробных изолята, в трех случаях (20 %) — КНИ. Ассоциации получены в одном (6,7 %) случае, MRSA/MRSE — в трех (20 %) случаях.
Среди пациентов с ревизионными вмешательствами на предшествующих этапах лечения ( n = 49) у 12 (24,5 %) обнаружены микробные ассоциации (четыре (33,3 %) — в группе 1, восемь (66,7 %) — в группе 2). У трех (25 %) из них отмечали рецидив ППИ, в дальнейшем двоим повторно выполнили дебридмент с заменой цементного спейсера. Рецидив инфекции отмечали у четырех (25 %) пациентов с КНИ в группе 2.
ОБСУЖДЕНИЕ
Анализируя микробный пейзаж, можно отметить лидирующую долю грамположительной флоры в причинах развития ППИ (в группе 1 — 50 %, в группе 2 — 92 %) [6, 19–22]. Рост грамотрицательной флоры при ранних формах ППИ значительно превышал аналогичные показатели хронических форм инфекции: 31,3 % и 9,2 % соответственно. Данные микроорганизмы представляют серьезную проблему для всех ортопедов, занимающихся первичным и ревизионным эндопротезированием, ввиду неуклонно возрастающей резистентности микрофлоры ко многим антибактериальным препаратам [23]. Вовлечение грамотрицательных бактерий в этиологию ППИ усложняет и пролонгирует процесс лечения [24]. Эффективность применения методики DAIR в таких условиях может значительно снижаться.
Частота встречаемости P. aeruginosa при ранней форме ППИ — 6,3 %, при хронической форме — 2,3 %. P. aeruginosa может являться причиной развития ранней/послеоперационной внутрибольничной инфекций [25]. По данным различных авторов, P. aeruginosa является причиной внутрибольничной инфекции более чем в 15 % случаев [26–28].
Проблемой в лечении пациентов с ППИ являются микробные ассоциации. В нашем исследовании частота встречаемости полимикробных инфекций при I типе ППИ составила 25 %, при II–III типах ППИ — 18,4 %. Микробные ассоциации усложняют выбор этиотропной антибиотикотерапии, что часто приводит к худшим исходам лечения в сравнении с мономикробной микрофлорой [29, 30].
При хронических формах ППИ в 52,9 % случаях выделяется золотистый стафилококк, характеризующийся ростом резистентных штаммов [6, 19–22]. Количества штаммов MRSA/MRSE/MRSH в нашем исследовании были сопоставимы.
Устойчивость к метициллину не является решающим фактором вирулентности, однако метициллин-резистентные штаммы S. aureus (MRSA) часто экспрессируют более высокий уровень факторов вирулентности, которые способствуют их выживанию и распространению [31].
В клинически сложных случаях с выраженной деструкцией мягких тканей мы применяли NPWT на первом этапе ревизионного эндопротезирования [11]. В 83,3 % изолятов данной группы пациентов выделен S. aureus. Поражению тканей способствует несколько существенных особенностей S. aureus, в частности при ППИ. S. aureus способны продуцировать ряд токсинов, включая альфа-токсин, эксфолиативные токсины (ETA, ETB, ETC), энтеротоксины и лейкоцидин Пантона – Валентина. Кроме того, у S. aureus существует множество секретируемых ферментов и белков клеточной стенки, опосредующих инвазию тканей, таких как коагулаза, ДНКаза, гиалуронидаза, коллагеназа и фибронектинсвязы- вающие белки. Большинство факторов вирулентности кодируются дополнительными генами, которые могут присутствовать или отсутствовать у отдельного штамма S. aureus. Также исследования in vitro показывают, что штаммы S. aureus быстро агрегируют в присутствии синовиальной жидкости человека и в течение 24 часов развиваются в макроскопические колонии, которые в конечном итоге преобразовываются в биопленку, устойчивую к антибиотикам [32]. Компоненты синовиальной жидкости, такие как фибриноген, фибронектин и свободная ДНК, могут вызывать агрегацию бактерий, которая, как предполагается, играет роль в патогенезе ППИ.
R. Proctor et al. изучали S. aureus в связи с его частой ассоциацией с инфекциями костей и суставов и хорошо охарактеризованной способностью существовать в квазидремлющем состоянии (так называемый фенотип малых колоний SCV), что потенциально способствует хронизации заболевания [33].
КНИ в нашем исследовании встречали в 25 % случаев в группе 1 и в 16,1 % в группе 2. Это согласуется с мировыми данными, по которым культурально-негативная ППИ встречается от 5 % до 42 % случаев [21, 34–38]. Этот факт часто осложняет выбор антимикробного препарата. В настоящее время рекомендуется при диагностике использовать молекулярные методы, включающие полимеразную цепную реакцию (ПЦР) и секвенирование. Эти методы продемонстрировали улучшение микробной идентификации при культурально-отрицательной ППИ [37, 38]. Кроме того, часто не выявленные, но присутствующие культуры при традиционном посеве являются результатом нахождения микроорганизмов в состоянии биопленки. Обнаружено, что культивирование пункционной жидкости и удаленных имплантов, обработанных ультразвуком, увеличивает выход микробов за счет разрушения бактериальной биопленки и чувствительность ПЦР [37].
ЗАКЛЮЧЕНИЕ
В структуре этиологии ранней ППИ (I тип) преобладали грамотрицательные микроорганизмы и их ассоциации, при хронических формах (II и III тип) — грамположительные патогены. Культурально-негативная инфекция являлась причиной развития ранних форм ППИ чаще, чем хронических (25,0 % и 16,1 % соответственно). Статистически значимых различий между группами по выделению мети-циллинрезистентного стафилококка, а также грамотрицательных бактерий БЛРС+ не выявлено.


