Особенности микроциркуляторных реакций в области экспериментального раневого дефекта у белых крыс
Автор: Лойко Д.Д., Савкина А.А., Степанова Т.В., Кириязи Т.С., Основин О.В., Андронова Т.А., Абдрахманова И.И., Федоров А.Н., Иванов А.Н.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Патологическая физиология
Статья в выпуске: 2 т.18, 2022 года.
Бесплатный доступ
Цель: выявить изменения параметров микроциркуляторного русла методом лазерной допплеровской флоуметрии в процессе заживления раневого дефекта и возможности их применения для модернизации технологий оценки эффективности средств для лечения ран. Материал и методы. Исследования выполнены на 25 белых крысах, разделенных на две группы: 10 контрольных интактных крыс, 15 животных с полнослойным экспериментальным дефектом кожи. У крыс оценивали параметры микроциркуляции кожи краев экспериментальной раны с помощью лазерной допплеровской флоуметрии, а также проводили анализ гистологических препаратов тканей области раневого дефекта. Результаты. Изменения микроциркуляции кожи краев раневого дефекта характеризуются воспалительной гиперемией, проявляющейся увеличением перфузионного показателя на 27% и нормированных амплитуд миогенных, дыхательных и сердечных колебаний. Изменения микроциркуляции верифицируются морфологической картиной воспаления, которая отражает увеличение количества полнокровных сосудов артериального и венозного русла, а также лейкоцитарную инфильтрацию дна и краев раны. Заключение. Мониторинг микроциркуляторных нарушений, возникающих в области кожных ран, позволяет оценить динамику репаративного процесса, что может быть использовано для разработки и оценки эффективности существующих медикаментозных и немедикаментозных методов стимуляции регенерации.
Микроциркуляция, полнослойный раневой дефект, регенерация
Короткий адрес: https://sciup.org/149141153
IDR: 149141153 | УДК: 616-003.9:616-018
Peculiarities of microcirculatory reactions in the area of experimental wound defect in white rats
Objective: to reveal changes of microbloodflow parameters by the laser Doppler flowmetry method in the process of wound defect healing and possibility of their application to modernization of the technologies forwound healing agents effectiveness evaluating. Material and methods. The studies were carried out on 25 white rats divided into 2 groups: 10 control intact rats, 15 animals with a full-thickness experimental skin defect. The microcirculatory parameters of the wound skin edges in rats were evaluated with laser Doppler flowmetry. Histological assay of the wound defect tissues were also performed. Results. It was established that changes in skin microcirculation at the wound defect edges were characterized by inflammatory hyperemia, which was manifested by 27% perfusion increase and increase of normalized amplitudes of myogenic, respiratory and cardiac oscillations. Changes in microcirculation are verified by the morphological picture of inflammation, which reflects an increase in the number of full-blooded vessels of the arterial and venous bed, as well as leukocyte infiltration of the bottom and edges of the wound. Conclusion. Monitoring of microcirculatory disorders occurring in the area of skin wounds allows us to assess the dynamics of the reparative process, which can be used to develop and evaluate the effectiveness of existing drug and non-drug methods of stimulating regeneration.
Текст научной статьи Особенности микроциркуляторных реакций в области экспериментального раневого дефекта у белых крыс
1 Введение. В настоящее время во всем мире распространенность острых и хронических ран остается на высоком уровне. Различные осложнения, которыми может сопровождаться процесс заживления ран, включая раневую инфекцию, формирование гипертрофированных рубцов и келоидов, оказывают негативное влияние как на качество жизни пациентов, так и на экономику системы здравоохранения в связи с увеличением продолжительности и стоимости лечения [1]. Одним из важных этапов создания новых средств для ухода и лечения ран является их апробация in vivo , что обусловливает актуальность совершенствования моделей и средств оценки эффектов инновационных продуктов.
По современным представлениям процесс заживления ран представляет собой сложную сеть физиологических изменений, включая реакции со стороны микрососудов зоны повреждения [2, 3]. Микроцирку-ляторные реакции в области раны оказывают непосредственное влияние на динамику и интенсивность репарации кожных ран, корригируя метаболические фазы течения раневого процесса [4]. Наблюдение за динамикой раневого процесса позволяет принять своевременное эффективное терапевтическое решение, что оказывает значительное влияние на конечный результат лечения.
Сегодня лазерная допплеровская флоуметрия — одна из самых современных неинвазивных методик, позволяющих оценить состояние микроциркулятор-ного русла [5]. Новизной методологического подхода, реализующегося в ходе настоящего исследования, является разработка возможности применения параметров лазерной допплеровской флоуметрии в оценке динамики репаративной регенерации кожных ран .
В связи с этим цель настоящего исследования — выявить изменения параметров микроциркулятор-ного русла методом лазерной допплеровской фло-уметрии в процессе заживления раневого дефекта и возможности их применения для модернизации технологий оценки эффективности средств для лечения ран.
Материалы и методы. Эксперимент выполнен на 25 белых крысах массой 250–320 г, разделенных на две группы: в контрольную группу были включены 10 интактных крыс, в опытную группу вошли 15 животных с полнослойным экспериментальным дефектом кожи.
На протяжении всего эксперимента животные находились в стандартных условиях вивария в индивидуальных клетках. Для общей анестезии животным вводились «Телазол» («ZoetisInc», Испания) в дозе
0,1 мл/кг и «Ксиланит» (ООО «Нита-Фарм», Россия) в дозе 1 мг/кг внутримышечно. Все исследования были выполнены в соответствии с Европейской конвенцией по защите позвоночных животных, используемых для экспериментов или в иных научных целях (1986), национальных руководств и правил учреждения по содержанию и использованию лабораторных животных и одобрены этическим комитетом Саратовского ГМУ имени В. И. Разумовского (протокол № 1 от 05.02.2019).
Контрольная группа, включавшая 10 интактных крыс, была сформирована для регистрации исходных параметров микроциркуляции кожи у крыс, которым не проводилась обработка антисептиками.
Моделирование полнослойного дефекта кожи осуществлялось хирургическим методом [6]. Для этого у животных опытной группы после депиляции и антисептической обработки кожи в межлопаточной области с помощью квадратного трафарета 5%-м йодом наносились контуры будущего раневого дефекта. По разметке с помощью скальпеля проводилось формирование полнослойного раневого дефекта размером 10×10 мм.
Для исследования состояния микрокровотока в зоне раневого дефекта использовали метод лазерной допплеровской флоуметрии, реализация которой выполнялась с помощью прибора «ЛАКК-ОП» (Россия). Измерение параметров микроциркуляции у животных опытной группы проводили на 14-е сутки эксперимента, располагая датчик анализатора на расстоянии 1 мм от верхнего края экспериментального дефекта. Оценивали перфузионный показатель и нормированные амплитуды эндотелиальных, нейрогенных, миогенных, дыхательных и сердечных колебаний [7].
Вывод животных из эксперимента осуществлялся передозировкой препаратов для наркоза. Для оценки морфологических изменений, происходящих в зоне экспериментальной полнослойной раны, мягкие ткани раневого дефекта забирались на 14-е сутки эксперимента и фиксировались в 10%-ном растворе формалина для дальнейшего гистологического исследования. Гистологические срезы толщиной 5 мкм окрашивались гематоксилином и эозином (ООО «Биовитрум», Россия). Микроскопию препаратов зоны раневого дефекта выполняли с помощью микровизора проходящего света серии μVizo-103 (ООО «ЛОМО ФОТОНИКА», Россия). Оценивали состояние и кровенаполнение сосудов микроциркуля-торного русла, а также инфильтрацию дна раны и ее перифокальной зоны клеточными элементами, участвующими в реализации раневого процесса, такими как фибробласты, лимфоциты, макрофаги.
Статистическую обработку полученных данных проводили с использованием программы Statistica 10.
Изменение показателей микроциркуляции в зоне раневого дефекта, Ме (Q25; Q75)
|
Показатели |
Группа |
|
|
контроля ( n =10) |
опытная ( n =15) |
|
|
Показатель перфузии, перф. ед. |
10,4 (9,6; 12,3) |
13,2 (11,3; 14,1) р =0,015 |
|
Амплитуда колебаний, усл. ед. |
||
|
эндотелиальных |
15,2 (11,5; 17,7) |
5,3 (4,04; 6,1) р <0,001 |
|
нейрогенных |
6,8 (6,7; 8,2) |
6,7 (5,4; 7,5) р =0,157 |
|
миогенных |
6,7 (5,9; 7,9) |
10,6 (7,3; 11,6) р <0,001 |
|
дыхательных |
9,1 (7,9; 11,6) |
14,7 (12,5; 18,8) р <0,001 |
|
сердечных |
3,8 (3,3; 4,7) |
18,6 (16,4; 20,1) р <0,001 |
П р и м еч а н и е : в каждом случае приведены медиана и интерквартильный размах; p — по сравнению с контролем.
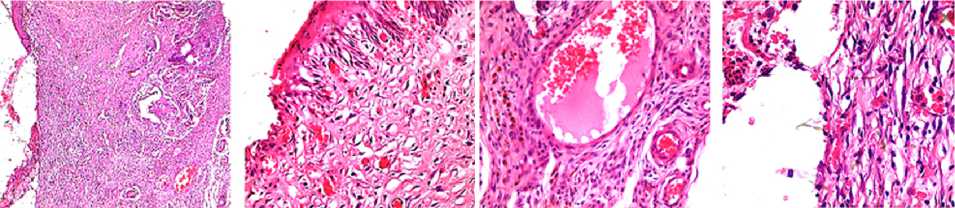
А Б В Г
Морфологические изменения в зоне раневого дефекта (окраска гематоксилином и эозином): А — зона раневого дефекта кожи (объектив ×5); Б — полнокровие сосудов перифокальной зоны, лимфоцитарная инфильтрация (объектив ×20); В — сладж и сепарация крови, лимфоцитарная инфильтрация, сидерофаги в перифокальной зоне (объектив ×40); Г — нейтрофильная инфильтрация края раневого дефекта (объектив ×40).
Полученные данные не соответствовали законам нормального распределения, поэтому представлены в таблице в виде медианы ( Ме ) и интерквартильного размаха (Q25; Q75). Сравнение между группами проведено с помощью критерия Манна — Уитни. Критический уровень значений показателя достоверности принимали равным 0,05.
Результаты. На 14-е сутки эксперимента у крыс опытной группы отмечалось уменьшение площади раневого дефекта до 6,3 (5;30) мм2 (уменьшение на 95% от исходной величины).
При оценке микроциркуляторных нарушений в зоне полнослойной кожной раны установлено, что у крыс опытной группы на 14-е сутки эксперимента перфузионный показатель кожи на границе раневого дефекта был статистически значимо выше контрольных значений на 27%. Повышение перфузии в данной группе животных сопровождалось перераспределением вклада активных и пассивных механизмов модуляции микрокровотока. При оценке активных механизмов модуляции выявлено статистически значимое снижение нормированных амплитуд эндотелиальных колебаний на 65% относительно контроля и, напротив, увеличение нормированных амплитуд миогенных колебаний на 58%. Значимых изменений нормированных амплитуд нейрогенных колебаний перфузии кожи на границе раневого дефекта у крыс опытной группы через 2 недели не вы- явлено. Установлено, что большой вклад в изменение микроциркуляторных реакций кожи на границе раневого дефекта вносят пассивные механизмы модуляции кровотока. Это проявлялось статистически значимым увеличением относительно контрольных значений нормированных амплитуд дыхательных колебаний на 6l %, а сердечных — в 4,9 раза (таблица).
При морфологическом исследовании препаратов зоны раневого дефекта установлено, что соединительная ткань перифокальной зоны богата кровеносными сосудами артериального и венозного русла (рис. А, Б). Отмечается их полнокровие (рис. Б), в отдельных сосудах присутствует сладж и сепарация крови (рис. В). При анализе клеточных популяций области кожной раны обнаружено, что преобладающей клеточной популяцией являются фибробласты. Наблюдается выраженная лимфоцитарная инфильтрация, присутствуют единичные сидерофаги. Края и дно раны инфильтрированы нейтрофилами (рис. Г).
Обсуждение. Полученные в ходе эксперимента данные о темпах регенерации полнослойной кожной раны согласуются с данными литературы, свидетельствующими о том, что раневой дефект кожи у крыс к 14-му дню эксперимента эпителизирует-ся более чем на 90% [8]. Вместе с тем результаты проведенного исследования подтверждают, что заживление кожной раны у крыс опытной группы сопровождается выраженными изменениями микро- кровотока, проявляющимися повышением перфузии краев раневого дефекта, а также изменением вклада активных и пассивных механизмов в регуляции кровотока. Полученный результат соответствует данным других авторов, которые продемонстрировали активацию коллатерального кровотока на модели полнослойного дефекта кожи [3].
Выявленные особенности микроциркуляторных реакций соответствуют морфологическим изменениям, происходящим в области раневого дефекта. Так, повышение перфузии краев кожной раны согласуется с наличием большого количества сосудов по периферии раны. Кроме того, отмечается их выраженное кровенаполнение, что непосредственно приводит к увеличению перфузионного показателя.
Увеличение вклада пассивных механизмов модуляции микрокровотока краев раневого дефекта у крыс опытной группы на 14-е сутки эксперимента, проявляющееся повышением сердечных и дыхательных колебаний в спектре ЛДФ-грамм, характеризует усиление притока и затруднения оттока крови в микроциркуляторном русле соответственно [9]. Это подтверждает визуализированное полнокровие сосудов как артериального, так и венозного русла. Наличие сладжа и сепарации крови в отдельных венулах свидетельствует о резком снижении оттока крови, что, вероятно, является одной из причин выраженного увеличения вклада дыхательных колебаний в модуляцию кровотока в микроциркуляторном русле кожи краев раневого дефекта.
Следует отметить, что эффективное заживление ран и образование грануляционной ткани невозможно без ангиогенеза. Процесс образования новых сосудов в физиологических и патологических условиях регулируется различными биологически активными веществами, среди которых особая роль отводится цитокинам и ростовым факторам. Согласно данным литературы, нейтрофилы, которые первыми мигрирует в область раневого дефекта, способны синтезировать и высвобождать широкий спектр цитокинов и проангиогенных факторов, таких как VEGF, TNFα, IL-1β, IL-8, которые прямо или косвенно способствуют росту и миграции эндотелиальных клеток, что вызывает образование новых кровеносных сосудов [10]. В то же время источниками цитокинов и ростовых факторов, влияющих на ангиогенные реакции, могут быть и другие клетки лейкоцитарного ряда, в частности лимфоциты, а также тканевые макрофаги и пролиферирующие фибробласты [11]. Присутствие в зоне экспериментального раневого дефекта клеток указанных ранее популяций, включая нейтрофилы, макрофаги, лимфоциты и фибробласты, и продукция ими регуляторных молекул может объяснять выявленные изменения микроциркуляции. В частности, обнаруженное в ходе исследования снижение миогенного тонуса сосудов, сопровождающееся увеличением нормированных амплитуд миогенных колебаний, может быть связано с продукцией различных провоспалительных цитокинов лейкоцитами, присутствующими в тканях зоны раневого дефекта в большом количестве. Помимо этого, в очаге воспаления развивается локальный ацидоз и гипоксия тканей, которые, в свою очередь, приводят к снижению миогенного тонуса и дилатации прекапиллярных сфинктеров, что выражается в увеличении амплитуд миогенных колебаний [9].
Заключение. Особенности микрокровотока в области раневого дефекта, выявленные с помощью лазерной допплеровской флоуметрии, соответствуют морфологическим характеристикам динамики раневого процесса. Мониторинг микроциркуляторных нарушений, возникающих в области кожных ран, позволяет неинвазивно оценить динамику репаративного процесса, что может быть использовано для патогенетической разработки и оценки эффективности существующих и медикаментозных и немедикаментозных методов стимуляции регенерации.
Список литературы Особенности микроциркуляторных реакций в области экспериментального раневого дефекта у белых крыс
- Sen CK. Human wound and its burden: updated 2020 compendium of estimates. Adv Wound Care (New Rochelle) 2021; 10 (5): 281–92.
- Haller HL, Sander F, Popp D, et al. Oxygen, pH, lactate, and metabolism-how old knowledge and new insights might be combined for new wound treatment. Medicina (Kaunas) 2021; 57 (11): 1190.
- Yousefi S, Qin J, Dziennis S, et al. Assessment of microcirculation dynamics during cutaneous wound healing phases in vivo using optical microangiography. J Biomed Opt 2014; 19 (7): 76015.
- Sоrensen MA, Petersen LJ, Bundgaard L, et al. Regional disturbances in blood flow and metabolism in equine limb wound healing with formation of exuberant granulation tissue. Wound Repair Regen 2014; 22 (5): 647–53.
- Kulikov DA, Glazkov AA, Kovaleva YuA. et al. Prospects of laser Doppler flowmetry application in assessment of skin microcirculation in diabetes. Diabetes Mellitus 2017; 20 (4): 279–85. Russian (Куликов Д. А., Глазков А. А., Ковалева Ю. А. и др. Перспективы использования лазерной допплеровской флоуметрии в оценке кожной микроциркуляции крови при сахарном диабете. Сахарный диабет 2017; 20 (4): 279–85).
- Smotrin SM, Dovnar RI, Vasil`kov AYU, et al. Effect of a dressing containing gold or silver nanoparticles on experimental wound healing. Journal of the Grodno State Medical University 2012; 1 (37): 75–80. Russian (Смотрин С. М., Довнар Р. И., Васильков А. Ю. и др. Влияние перевязочного материала, содержащего наночастицы золота или серебра, на заживление экспериментальной раны. Журнал Гродненского государственного медицинского университета 2012; 1 (37): 75–80).
- Humeau A, Koïtka A, Abraham P, et al. Time-frequency analysis of laser Doppler flowmetry signals recorded in response to a progressive pressure applied locally on anaesthetized healthy rats. Phys Med Biol 2004; 49 (5): 843–57.
- Bi H, Feng T, Li B, et al. In vitro and in vivo comparison study of electrospun pla and pla / pva / sa fiber membranes for wound healing. Polymers (Basel) 2020; 12 (4): 839.
- Krupatkin AI. Blood flow oscillations — new diagnostic language in microvascular research. Regional Blood Circulation and Microcirculation 2014; 13 (1): 83–99. Russian (Крупаткин А. И. Колебания кровотока — новый диагностический язык в исследовании микроциркуляции. Регионарное кровообращение и микроциркуляция 2014; 1 (49): 83–99).
- Tecchio C, Cassatella MA. Neutrophil-derived cytokines involved in physiological and pathological angiogenesis. Chem Immunol Allergy 2014; (99): 123–37.
- Wang Z, Qi F, Luo H, Xu G, et al. Inflammatory microenvironment of skin wounds. Front Immunol 2022; (13): 789274.


