Особенности профилактики специфических осложнений при хирургическом лечении больных с заболеваниями щитовидной железы
Автор: Мумладзе Р.Б., Долидзе Д.Д., Васильев И.Т., Марков И.Н., Якушин В.И., Варданян А.В., Царев М.И., Нуждин О.И., Султыгов А.Х., Джигкаев Т.Д., Сиукаев О.Н., Шие М., Олимпиев М.Ю.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 3 (31), 2013 года.
Бесплатный доступ
В данной работе приводятся результаты лечения 425 больных с различными заболеваниями щитовидной железы (ЩЖ), находившихся для обследования и оперативного вмешательства в ГКБ им. С. П. Боткина с 2008 по 2012 гг. Всем пациентам были выполнены экстрафасциальные вмешательства под эндотрахеальным наркозом. Минимальным объемом операции являлась гемитиреоидэктомия, максимальным - тиреоидэктомия с футлярно-фасциальным иссечением клетчатки шеи. Для профилактики пареза гортани проводили визуализацию и выделение возвратного и, в ряде случаев, верхнего гортанного нервов (ГН). При этом использовали прецизионную технику, увеличительные приборы и нейромиограф. Для предотвращения развития гипопаратиреоза также проводили визуализацию и выделение околощитовидных желез (ОЩЖ). Для этого, в том числе, использовали методику фотодинамической визуализации ОЩЖ с применением фотосенсибилизатора и источника синего света. В послеоперационном периоде отмечено 2 (0,5%) случая временного пареза гортани и 4 - (0,9%) транзиторного гипопаратиреоза. Таким образом, применение указанных методических подходов и современной медицинской техники при хирургическом лечении больных с различными заболеваниями ЩЖ позволило избежать развитие специфических осложнений со стойкими изменениями и повысить безопасность и радикальность оперативного вмешательства.
Хирургия, щитовидная железа, микрохирургия, эндокринология, онкология, нейромониторинг, фотодинамика, возвратный гортанный нерв, верхний гортанный нерв, околощитовидная железа
Короткий адрес: https://sciup.org/142211092
IDR: 142211092 | УДК: 616.441:089:06:08
Текст научной статьи Особенности профилактики специфических осложнений при хирургическом лечении больных с заболеваниями щитовидной железы
В последнее время во всем мире, в том числе и в России, отмечается значительное распространение заболеваний ЩЖ [4, 8, 10].
50 млн. человек с заболеваниями ЩЖ в России
Население РФ – 142 млн. человек
Рис. 1. Распространенность заболеваний ЩЖ
Сегодня в мире зарегистрировано более 200 млн, а в России – более 50 млн человек с различными расстройствами и заболеваниями ЩЖ. По темпу прироста рак щитовидной железы (РЩЖ) занимает первое место среди злокачественных опухолей и превышает 5% в год. В Европе еже- годно диагностируется более 200 тыс. новых случаев РЩЖ и 1500–2000 человек умирают от этого заболевания. Такой рост заболеваемости, помимо других причин, обусловлен значительной чувствительностью ткани ЩЖ к йодному дефициту, высокому радиационному фону и загрязнению окружающей среды [1, 5, 7, 16]. Особенное анатомическое расположение ЩЖ, сложное гистологическое строение и специфика ее физиологических механизмов функционирования вызывает значительные трудности как при обследовании, так и при лечении больных с тиреоидной патологией [14, 15, 17]. Это в полной мере касается и хирургического способа лечения, который, к сожалению, все еще является основным у большинства пациентов [2, 11, 12, 13]. Следует отметить, что только в России в год выполняется более 40 000 операции на ЩЖ, и существует целый ряд спорных вопросов и проблем, касающихся тактики хирургического лечения больных данной категорий, которые десятилетиями остаются нерешенными [3, 6, 9].
Оперативное вмешательство на ЩЖ, несмотря на кажущуюся простоту и многовековую историю существования, все еще является одним из самих сложных в хирургии, нередко сопровождающимся развитием специфических осложнений [3, 9]. Среди последних следует выделить по-
Таблица 1
Частота повреждения верхнего ГН при операциях на ЩЖ
Все это свидетельствует о неоднозначности методики оперирования на ЩЖ и неполноценности некоторых технических приемов, необходимых для профилактики возможных осложнений. В связи с этим, для сохранения качества жизни пациентов после хирургического вмешательства на ЩЖ, нужно не только не ослаблять внимание к данной проблеме, но и стараться совершенствовать существующие и искать новые возможности профилактики вышеуказанных специфических осложнений.
Материал и методы
Работа основана на результатах лечения 425 больных с заболеваниями ЩЖ, находившихся для обследования и оперативного вмешательства в ГКБ им. С. П. Боткина с 2008 по 2012 гг. У 282 (66,3%) пациентов был диагностирован узловой нетоксический зоб (УНЗ) и многоузловой нетоксический зоб (МНЗ), у 21 (4,9%) – диффузный токсический зоб (ДТЗ), у 18 (4,2%) – аутоиммунный тиреоидит (АИТ), у 11 (2,5%) – токсическая аденома (ТА) ЩЖ и у 93 (22%) больных – РЩЖ (рис. 2).Среди наблюдаемых пациен-
Таблица 2
Частота повреждения возвратного ГН при операциях на ЩЖ
|
Авторы |
Год |
Колич. опер. |
Повреждение возвратн. ГН |
|
|
Абс. число |
% |
|||
|
Г. И. Захарова и соавт. |
1986 |
1829 |
23 |
1,2 |
|
Г. И. Зеновко |
1989 |
451 |
4 |
0,9 |
|
П. П. Ананикян |
1991 |
2855 |
10 |
0,35 |
|
И. С. Брейдо |
1998 |
793 |
14 |
1,76 |
|
Р. Б. Магомедов |
2000 |
727 |
5 |
0,7 |
|
Э.В.Савенок |
2003 |
150 |
4 |
2,7 |
|
R. Hermann et al. |
1991 |
7566 |
395 |
5,2 |
|
W. Miller et al. |
1995 |
1147 |
96 |
8,3 |
|
A. Echeverri et al. |
1998 |
70 |
5 |
7,1 |
|
L. Kasemsuvan et al. |
1998 |
361 |
57 |
15,8 |
|
I. A. Chyaudhary et al. |
2007 |
310 |
10 |
3,2 |
|
O.Alimoglu |
2008 |
581 |
29 |
5 |
|
H. M. Zakaria et al. |
2011 |
340 |
14 |
4 |
Таблица 3
Частота послеоперационного гипопаратиреоза
Все пациенты были оперированы после соответствующего обследования под эндотрахеальным наркозом. Им были выполнены экстрафасциальные вмешательства с соблюдением определенной этапности. Минимальным объемом операции являлась гемитиреоидэктомия, максимальным – тиреоидэктомия с футлярно-фасциальным иссечением клетчатки шеи. Сведения о характере выполненных вмешательств представлены в табл. 4.
Во время хирургического вмешательства у ряда пациентов, особенно при одностороннем поражении ЩЖ, выполняли срочное гистологическое исследование для уточнения объема операции. На операции использовали современную медицинскую аппаратуру, такую как: генератор для прошивания сосудов «LigasureTM», ультразвуковой скальпель «UltraCision», эндоскопическую оптическую систему «Storz», бинокулярные лупы и операционный микроскоп фирмы «ZEISS», нейрофизиологический комплекс «Нейро-МВП» компании «Нейрософт», и портативный источник синего света «Биоспек». Все они применялись на различных этапах проводимых нами хирургических вмешательств.
Методика операции: воротниковый разрез, по возможности минимальный, от 4,5 до 6,5 см длиной, чаще всего выполняли в типичном месте таким образом, чтобы углы раны располагались у медиальных краев грудино-ключичнососцевидных мышц (рис. 3).
При недостаточном доступе к ЩЖ предгортанные мышцы пересекали на разных уровнях. Грудино-подъязычные мыш-
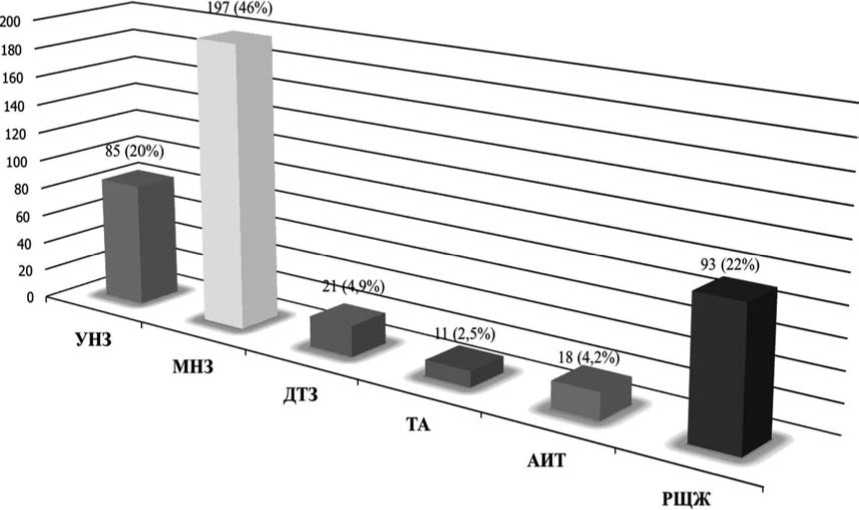
Рис. 2. Контингент наблюдаемых больных
Таблица 4
Характер оперативных вмешательств у больных с различными заболеваниями ЩЖ
|
Объем операции |
Заболевание ЩЖ |
Итого |
|||||
|
УНЗ |
МНЗ |
ДТЗ |
ТА |
АИТ |
РЩЖ |
||
|
Гемитиреоидэктомия |
85 (86,7%) |
3 (3%) |
– |
8 (8,2%) |
– |
2 (2%) |
98 (23%) |
|
Гемитиреоидэктомияс резекцией противоп. доли ЩЖ |
– |
3 (100%) |
– |
– |
– |
– |
3 (0,7%) |
|
Предельно-субтотальная резекция ЩЖ |
– |
1 (50%) |
– |
– |
1 (50%) |
– |
2 (0,5%) |
|
Тиреоидэктомия |
– |
190 (67%) |
21 (7,4%) |
3 (1%) |
17 (6%) |
52 (18,4%) |
283 (66,6%) |
|
Тиреоидэктомия с центральной лимфодиссекцией |
– |
– |
– |
– |
– |
31 (100%) |
31 (7,3%) |
|
Тиреоидэктомия с футлярно-фасц. иссеч. клетч. шеи |
– |
– |
– |
– |
– |
8 (100%) |
8 (1,9%) |
|
Всего |
85 (20%) |
197 (46,4%) |
21 (4,9%) |
11(2,5%) |
18 (4,2%) |
93 (22%) |
425 (100%) |
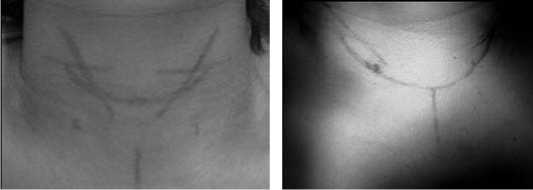
Рис. 3. Нанесение ориентиров для хирургического доступа перед операцией на ЩЖ

Рис. 4. Этапы доступа к ЩЖ без разделения и с пересечением предгортанных мышц цы разделяли у нижнего, а грудино-щитовидные – у верхнего края раны, так, чтобы в конце операции можно было избежать деформацию шеи при их восстановлении (рис. 4).
Для уменьшения кровоточивости и профилактики кровотечения, что является первым важным моментом при подобных операциях, а также с целью предотвращения распространения гематогенных метастазов, все манипуляции на ЩЖ начинали после перевязки и последующего пересечения тиреоидных сосудов.
При мобилизации доли ткань железы не прошивали. В стандартных случаях освобождали сначала верхний, затем нижний полюс и боковые поверхности ЩЖ. Для уточнения анатомических ориентиров в первую очередь открывали переднюю поверхность гортани.
При выделении верхнего полюса обычно существует опасность повреждения верхнего ГН. Чаще всего повреж- дается наружная ветвь данного нерва, которая обычно менее 1 мм в диаметре, и в 10–15% опускается ниже верхней границы тиреоидного полюса. При этом наружную ветвь легко можно спутать с мелкими сосудистыми структурами и фасциальными тяжами.
В связи с этим при мобилизации верхнего полюса все сосудистые элементы: артерии, вены и лимфатические сосуды ЩЖ перевязывали, коагулировали и потом, только после их идентификации на глаз, пересекали у тиреоидной капсулы.
При наличии факторов риска – высокого расположения верхнего полюса, наличия рецидивного и опухолевого процессов и большой пирамидальной доли, что составило 55 (13%) наблюдений (рис. 5), производили визуализацию верхнего ГН с использованием прецизионной техники и увеличительных приборов у 20 (4,6%) больных и применением нейромиографа – у 35 (8,2%) пациентов (рис. 6).
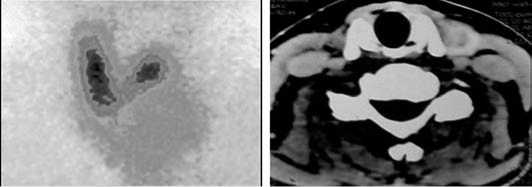
Рис. 5. Высокое расположение верхнего полюса, выявленное при сцинтиграфии ЩЖ и компьютерной томографии шеи
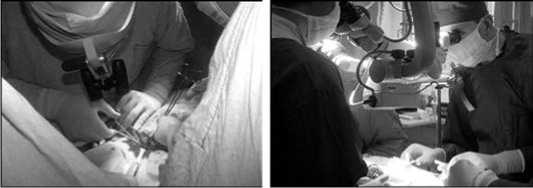
Рис. 6. Этапы операции на ЩЖ с использованием бинокулярных луп и операционного микроскопа
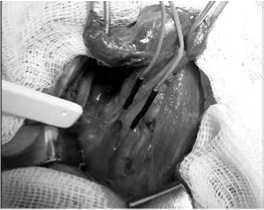
Рис. 7. Укладка электродов для электрофизиологической идентификации верхнего ГН
Нейромониторинг проводился непосредственно во время выделения верхнего полюса ЩЖ от окружающих структур.
Для этого сначала парные игольчатые электроды устанавливали в перстнещитовидной мышце, кото- рая иннервируется наружной ветвью верхнего ГН и определяет натяжение и тонус голосовой складки. Электроидентификацию осущест- вляли путем прямого контакта стимуляционного электрода с дифференцируемыми образованиями (рис. 7).
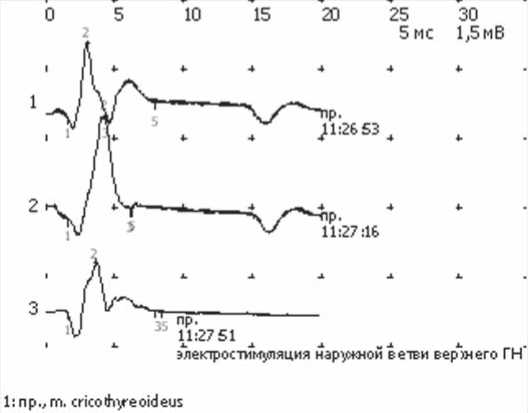
Рис. 8. М-ответ при интраоперационной электростимуляции наружной ветви верхнего ГН
При наличии наружной ветви верхнего ГН получали сокращение перстнещитовидной мышцы и регистрировали аудиосигнал и графическое изображение на экране монито-
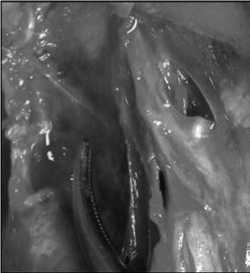
Рис. 9. Этап визуализации наружной ветви верхнего ГН
ра (рис. 8).
Такой подход позволил почти во всех случаях визуализировать наружную ветвь верхнего ГН, которая располагалась чаще всего по ходу косых волокон перстнещитовидной мышцы (рис. 9).
После верхнего переходили на мобилизацию нижнего полюса ЩЖ с раздельной перевязкой и пересечением основных стволов и ветвей нижних щитовидных сосу- дов у тиреоидной капсулы (рис. 10).
При этом сохраняли артерии, питающие ОЩЖ. Последние визуализировали для профилактики очередной опасности – гипопаратиреоза, а при наличии интимного контакта с удаляемой тканью, рецидивных, опухолевых и аутоиммунных процессах у 66 (15,5%) больных их выде-
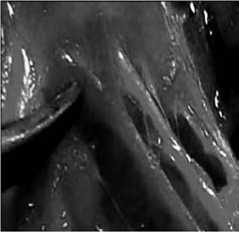
Рис. 10. Этап выделения нижних щитовидных сосудов
ляли с использованием тонких сосудистых и микрохирургических инструментов и в ряде случаев – увеличительных приборов (рис. 11).
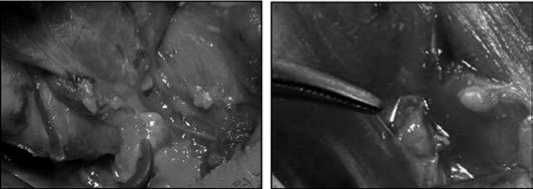
Рис. 11. Этапы визуализации верхней и нижней артерий ЩЖ
При выделении ОЩЖ учитывали, что они обычно имеют диаметр в 4–6 мм и встречаются чаще всего парами у нижних полюсов и заднебоковых поверхностей ЩЖ. Эпителиальные тельца имеют четкую капсулу и питающие их сосудистые веточки. Цвет ОЩЖ коричневый, но в зависимости от возраста и жировой инфильтрации могут иметь и желтоватый оттенок. Кроме того, ОЩЖ крайне чувствительны к гипоксии и травматизации. При манипуляциях и контакте с хирургическими инструментами на поверхности ОЩЖ появляется гиперемия с инъекцией сосудов, которая особенно хорошо видна при увеличении, чем они и выделяются от жировых долек клетчатки.
Следует отметить, что у 39 (9,2%) больных был применен метод фотодинамической визуализации ОЩЖ. Для этого пациентам за 2 часа до операции давали выпить раз- веденный в 50 мл воды фотосенсибилизатор «Аласенс», в количестве 1,5 гр, который накапливается и длительное время задерживается в ОЩЖ. При направлении на них синего света с использованием оптической систем «Storz» и портативного источника «Биоспек» (рис. 12) в темной
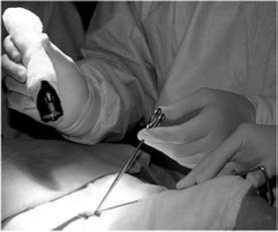
Рис. 12. Фотодинамическая визуализация ОЩЖ
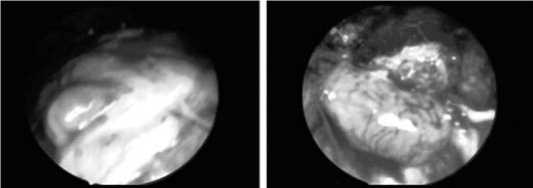
Рис. 13. Этапы фотодинамической визуализации ОЩЖ
операционной получали эффект люминесценции розовым цветом (рис. 13).
Особенно важна фотодинамическая визуализация ОЩЖ при рецидивных процессах и лимфодиссекции, когда при сложной анатомической ситуации и выраженной жировой клетчатке найти и сохранить эпителиальные тельца становится крайне сложно.
Во время мобилизации нижнего полюса существует следующая, основная опасность в виде повреждения возвратного ГН, который может располагаться как спереди, так и между ветвями и сзади от нижних щитовидных артерии. Поэтому для сохранения целостности данного нерва нужно либо его выделить на протяжении, либо применить тот же прием, и все сосудистые и тяжистые структуры пересекать у капсулы ЩЖ на глаз, отходя от нее на несколько миллиметров.
Мобилизация заднебоковых поверхностей долей осуществлялась раздельным легированием сосудистых коллатералей. На данном этапе производилась визуализация верхних ОЩЖ и возвратного ГН. Последний чаще выделяли у входа его в гортань, в области связки Бэрри (рис. 14).
Мы умышленно остерегались выделения возвратного ГН на протяжении для профилактики рубцовых парезов, и производили данную манипуляцию только при наличии рецидивного, распространенного опухолевого процесса и в случаях, требующих лимфодиссекцию, что составило 62 (14,6%) больных (рис. 15). При этом обязательно учитывали возможность наличия «невозвращающегося» возвратного ГН. Такой вариант мы встретили у 6 (1,4 %) пациентов.
Выделение возвратного ГН почти во всех случаях про- ходило с использованием тонких сосудистых и микрохирургических инструментов. При этом у 19 (4,5%) больных
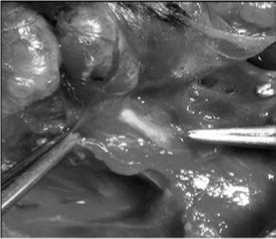
Рис. 14. Этап визуализации возвратного ГН
со сложными анатомическими особенностями мы использовали увеличительные приборы, которые облегчали наши действия позволяя более точно и четко идентифицировать анатомические структуры.
А у 29 (6,8%) больных при наличии рецидивного и рубцового процесса применили методику электро- физиологической идентификации возвратного ГН. В этом случае на интубационную трубку устанавливали электроды, которые при интубации соприкасались с голосовыми складками (рис. 16). Второй электрод использовали для дифференциации тяжи-стых структур в ране. При контакте данного
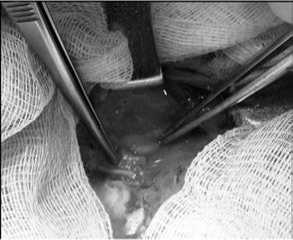
Рис. 15. Этап операции на ЩЖ с выделением возвратного ГН и ОЩЖ
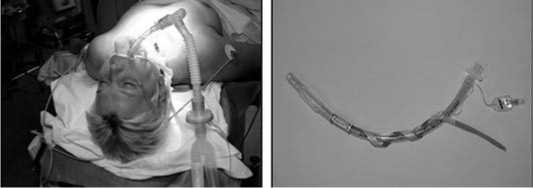
Рис. 16. Подготовка к операционному вмешательству, установлена интубационная трубка с фиксированным на ней электродом электрода с исследуемым образованием в случае наличия возвратного ГН получали сокращение иннервируемых им голосовых мышц, и разность потенциалов регистрировали звуковым и графическим способом.
После выделения возвратного ГН, долю скальпелем отсекали от трахеи без оставления тиреоидной ткани, кроме нескольких случаев предельно-субтотальной резекции ЩЖ. При этом целью в данном случае являлась не выделение возвратного ГН, а выполнение нужного объема операции с сохранением целостности данной анатомической структуры (рис. 17).
Следует отметить, что при наличии заболеваний загру-динно расположенной ЩЖ, у 25 (5.9%) больных, последовательность этапов операции несколько менялась.
Поскольку здесь для профилактики осложнений очень важно, чтобы мобилизация доли проходила без грубой тракции нижнего полюса ЩЖ, в первую очередь пересекался перешеек. Дальше начиналась мобилизация доли сверху вниз, поэтапным разделением всех сосудистых структур, фасциальных и рубцовых тяжей у тиреоидной капсулы, по-
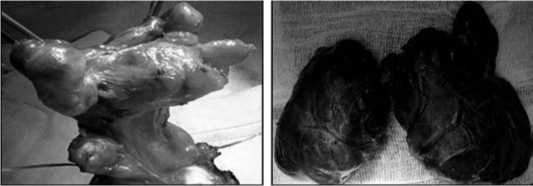
Рис. 17. Мобилизованная тиреоидная доля и удаленная ЩЖ
стоянным подтягиванием доли вверх. Так, под четким зрительным контролем, мобилизовывали сначала верхний полюс, далее – заднебоковую поверхность и нижний полюс ЩЖ и без грубых и резких движений поднимали загрудинный компонент в шейную часть тиреоидного ложа (рис. 18).
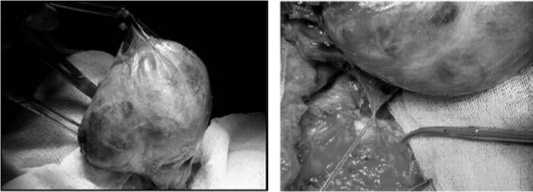
Рис. 18. Этапы выделения загрудинного компонента при загрудинном МНЗ, справа инструментом указан возвратный ГН
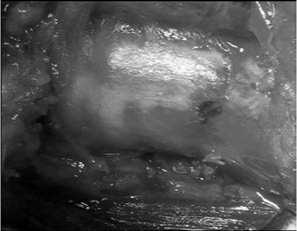
Рис. 19. Операционная область после геми- и тиреоидэктомии
Вмешательство завершали ревизией ложа ЩЖ и окружающих структур (рис. 19).
Для предупреждения рубцовой деформации шеи производили тщательное восста- новление мышечнофасциального каркаса. Рану закрывали вну- трикожными швами с оставлением микродренажей на активной аспирации.
Для выявления повреждения ГН после операции проводили ларингоскопию, электромиографию перстнещитовидной мышцы и в ряде случаев – рентгенкинемато-графию. Функциональное состояние ОЩЖ исследовали определением уровня Са и Р в крови.
Объем выполненного хирургического вмешательства у пациентов с тиреоидной карциномой контролировался с помощью сцинтиграфии ЩЖ.
Результаты
В послеоперационном периоде в результате наших хирургических вмешательств были зафиксированы 6 (1,4%) осложнений. В 1 (0,2%) случае – парез гортани на фоне повреждения верхнего ГН развился у больной с тиреоидной карциномой, у которой верхний полюс был интимно связан с перстнещитовидной мышцей. В данном наблюдении была выполнена тиреоидэктомия с центральной лимфодиссекцией.
В другом наблюдении – после тиреоидэктомии с футлярно-фасциальным иссечением клетчатки шеи у больной, в результате выделения возвратного ГН было отмечено ограничение подвижности одной голосовой связки с голосовым дефектом. Подвижность восстановилась через 1,5–2 месяца после операции.
Еще у 4 (0,9%) пациентов с рецидивным зобом, тиреоидной карциномой и АИТ – обнаружен транзиторный гипопаратиреоз при выделении ОЩЖ из рубцов и спаек.
Таким образом, парез гортани (временный) был отмечен в 0,5% (2 больных)
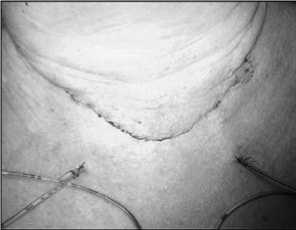
Рис. 20. Операционная область после тиреоидэктомии у больной с загрудинным МНЗ
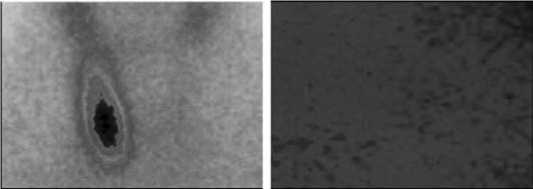
Рис. 21. Сцинтиграфия ЩЖ после геми- и тиреоидэктомии по поводу тиреоидной карциномы
случаев в результате повреждения верхнего и возвратного ГН, а транзиторный гипопаратиреоз – в 0,9% (4 больных) наблюдений. Послеоперационные осложнения по нозологиям имели следующий характер: при ДТЗ (рецидивный процесс) – 4,8 % (1 больная); при МНЗ (рецидивный процесс) – 0,5% (1 больная); при АИТ – 5,5 % (1 больной); при РЩЖ – 3,2% (3 больных).
Повторных операции у наблюдаемых больных не было. У всех пациентов косметический эффект был удовлетворительным (рис. 22).
Обсуждение
Таким образом, использованные методические подходы дали возможность избежать развития специфических осложнений со стойкими изменениями и позволили повысить безопасность и радикальность оперативного вмешательства. И хотя использованные способы, аппаратура и инструментарии могут пригодиться не у всех пациентов, тем не менее, иметь их в арсенале вместе с базовой методи-
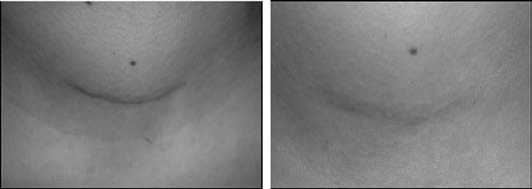
Рис. 22. Вид послеоперационного рубца через 3 и 7 месяцев после хирургического вмешательства кой, по нашему мнению, полезно и рекомендовано во время операции у всех больных с заболеваниями ЩЖ.
В заключение надо отметить, что каждый больной исключительно индивидуален, и бывают сложные пациенты, у которых с применением самых современных способов трудно получить нужную эффективность оперативного вмешательства. В связи с этим необходимым является продолжение традиции наших предшественников и поиск новых возможностей, которые позволяют постепенно улучшать результаты хирургического лечения пациентов с заболеваниями ЩЖ.
Выводы
Для эффективной профилактики специфических осложнений при операциях на ЩЖ важными являются:
-
1. Выбор оптимального доступа к ЩЖ.
-
2. Соблюдение строгой этапности при мобилизации ЩЖ.
-
3. Использование специального инструментария, современной медицинской аппаратуры и увеличительных приборов.
-
4. Перевязка (или коагуляция) и в последующем пересечение всех сосудистых структур под зрительным контролем у тиреоидной капсулы.
-
5. Визуализация и выделение верхнего и возвратного ГН с использованием прецизионной техники, увеличительных приборов и метода нейрофизиологической идентификации.
-
6. Визуализация или выделение 2–3 ОЩЖ с применением прецизионной техники, увеличительных приборов и методики фотодинамической визуализации.
Список литературы Особенности профилактики специфических осложнений при хирургическом лечении больных с заболеваниями щитовидной железы
- Анчикова Л.И., Кривошеев С.С., Поздняк А.О. Применение энтеросорбента и микроэлементов при зобе у работников цехов с вредными производственными факторами в условиях дефицита йода//Мат. IV Всерос. конгр. эндокринол.: «Актуальные проблемы современ. эндокринол». СПб., 2001. С. 261.
- Бржезовский В.Ж., Любаев В.Л. Диагностика и лечение медуллярного рака щитовидной железы//Практ. онкол. 2007. Т. 8, № 1. С. 29-34.
- Ветшев П.С., Карпова О.Ю., Чилингариди К.Е., Салиба М.Б. Профилактика и лечение нарушений подвижности голосовых складок при операциях на щитовидной железе//Хиругрия. 2005. № 5. С. 28-34.
- Дедов И.И., Кузнецов Н.С., Мельниченко Г.А. Эндокринная хирургия. М.: Литтерра, 2011. 338 с.
- Комиссаренко И.В., Рыбаков С.И., Коваленко А.Е., Омельчук А.В. Хирургическое лечение рака щитовидной железы в Украине после аварии на Чернобыльской АЭС//Материалы XI (13) Рос. симп. с межд. участием по хирург. эндокринол. СПб., 2003. С. 66-72.
- Попова Ю.В., Романчишен А.Ф. Послеоперационные осложнения в хирургии щитовидной железы//Матер. 15-го Рос. симп. по хир. эндокринол.: «Современные аспекты хирургической эндокринологии». Рязань, 2005. С. 265-269.
- Румянцев П.О., Ильин А.А., Румянцева У. В., Саенко В.А. Рак щитовидной железы: современные подходы к диагностике и лечению. М.: ГЭОТАР-Медиа, 2009.447 с.
- Фадеев В.В. Заболевания щитовидной железы в регионе легкого йодного дефицита: эпидемиология, диагностика, лечение. М.: Издательский дом Видар-М, 2005. 240 с.
- Фадеев В.В., Ванушко В.Э. Послеоперационный гипотиреоз и профилактики рецидива заболеваний щитовидной железы. М.: Издательский дом Видар, 2011. 70 с.
- Шулутко А.М., Семиков В.И., Ветшев П.С. Непальпируе-мые узловые образования щитовидной железы. М.:Профиль-2С, 2011.144 с.
- Bononi M., De-Cesare A., Atella F. et al. Surgicaltreatmentofm ultinodulargoiter: incidenceoflesionsoftherecurrentnervesaftertotalthyr oidectomy//Int. Surg. 2000. Vol. 85, № 3. P. 190-193.
- Hossain M. M., Haque M. R., Rashid A. et al. Surgical management of thyroid diseases -a study on 78 cases//Mymensingh Med. J. 2002. Vol. 11, № 1. P. 6-8.
- Mishra A., Mishra S. Total thyroidectomy for differentiated thyroid cancer: Primary compared with completion thyroidectomy//Eur. J. Surg. 2002. Vol. 168, № 5. P. 283-287.
- Shigemura N., Akashi A., Nakagiri T. et al. VATS with a supraclavicular window for huge substernal goiter: an alternative technique for preventing recurrent laryngeal nerve injury//Thorac. Cardiovasc. Surg. 2005. Vol. 53, № 4. P. 231-233.
- Testini M., Logoluso F., Lissidini G. et al. Emergency total thyroidectomy due to non traumatic disease. Experience of a surgical unit and literature review//World Journal of Emergence Surgery. 2012. Vol. 7, № 9. P. 5-10.
- Tuttle R.M., Becker D. The Chernobyl accident and its consequences: Update at the millenium//Semin. Nucl. Med. 2000. Vol. 30, № 2. P. 133-140.
- White M.L., Doherty G.M., Gauger P.G. Evidence-based surgical management of substernal goiter//World J. Surg. 2008. Vol. 32, № 7. P. 1285-1300.


