Особенности строения полифункциональных карбоксилатов тетраарилсурьмы
Автор: Шарутин В.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 2 т.16, 2024 года.
Бесплатный доступ
Из ферроцендикарбоновой кислоты, сульфосалициловой кислоты и пентаарилсурьмы Ar5Sb (Ar = Ph, p-Tol) в бензоле получены сполна замещенные сурьмаорганические производные ферроцендикарбоновой и сульфосалициловой кислот 1-3, строение которых после перекристаллизации из смеси бензол-октан доказано методом рентгеноструктурного анализа. Строение 1-3 установлено методом РСА. Кристаллы 1 [C68H64FeO4Sb2, M 1244,54; сингония моноклинная, группа симметрии С21/с; параметры ячейки: a = 16,9983(2), b = 10,94570(10), c = 30,3224(3) Å; β = 99,8220(10)°; V = 5559,04(10) Å3; Z = 4; rвыч = 1,487 г/см3; 2q 5,28-138,76 град.; всего отражений 32707; независимых отражений 10281; число уточняемых параметров 684; Rint = 0,0496; GOOF 1,062; R1 = 0,0345, wR2 = 0,0853; остаточная электронная плотность (max/min); 0,76/-0,90 e/Å3], 2 [C60H48FeO4Sb2, M 1132,33; сингония моноклинная, группа симметрии P21/n; параметры ячейки: a = 12,40720(10), b = 10,30830(10), c = 36,7290(4) Å; β = 94,1110(10) град., V = 4685,45(8) Å3, Z = 4; rвыч = 1,605 г/см3; 2q 4,82-138,56 град.; всего отражений 27748; независимых отражений 8680; число уточняемых параметров 604; Rint = 0,0367; GOOF 1,033; R1 = 0,0277, wR2 = 0,0709; остаточная электронная плотность (max/min); 0,86/-0,81 e/Å3], 3 [C63H62O7SSb2, M 1206,78; сингония моноклинная, группа симметрии P21/c; параметры ячейки: a = 20,9246(3), b = 13,5375(2), c = 21,4222(3) Å; β = 111,284(2) град., V = 5654,30(16) Å3, Z = 4; rвыч = 1,4175 г/см3; 2q 4,54-160 град.; всего отражений 48463; независимых отражений 11892; число уточняемых параметров 699; Rint = 0,0443; GOOF 1,024; R1 = 0,0327, wR2 = 0,0907; остаточная электронная плотность (max/min); 0,93/-0,85 e/Å3]. Атомы сурьмы в молекулах 1, 2 имеют с учетом координации карбонильных атомов кислорода на атом металла искаженную октаэдрическую конфигурацию. В структуре 3 присутствуют тетраэдрические тетраарилстибониевые катионы, атомы сурьмы в которых координированы с атомами кислорода сульфогрупп (Sb∙∙∙O(5)=S 2,601 Å), причем этот же атом кислорода координирован с орто-атомом водорода одной из толильных групп (Н(46)∙∙∙O(5)=S 2,60 Å). Молекулы воды структурируют кристалл 3 (Н(7)∙∙∙O(4)=S 1,98 Å, Н(7)∙∙∙O(5)=S 2,6 Å). (CCDC 2320709 для 1, 2320711 для 2, 2320717 для 3, deposit@ccdc.cam.ac.uk; http://www.ccdc. cam.ac.uk).
Особенности строения, арильные сурьмаорганические производные ферроцендикарбоновой и сульфосалициловой кислот, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147244637
IDR: 147244637 | УДК: 546.865+547.53.024+548.312.5 | DOI: 10.14529/chem240207
Structural features of polyfunctional tetraarylantimony carboxylates
From ferrocenedicarboxylic acid, sulfosalicylic acid and pentaarylantimony Ar5Sb (Ar = Ph, p-Tol) in benzene, fully substituted organoantimony derivatives of ferrocenedicarboxylic and sulfosalicylic acids 1-3 were obtained, the structure of which after recrystallization from a benzene-octane mixture was proven by X-ray diffraction analysis. Structures 1-3 were established by X-ray diffraction. Crystals 1 [C68H64FeO4Sb2, M 1244.54; monoclinic syngony, symmetry group C21/c; cell parameters: a = 16.9983(2), b = 10.94570(10), c = 30.3224(3) Å; β = 99.8220(10)°; V = 5559.04(10) Å3; Z = 4; rcalc = 1.487 g/cm3; 2q 5.28-138.76 degrees; total reflections 32707; independent reflections 10281; number of specified parameters 684; Rint = 0.0496; GOOF 1.062; R1 = 0.0345, wR2 = 0.0853; residual electron density (max/min) 0.76/-0.90 e/Å3], 2 [C60H48FeO4Sb2, M 1132.33; monoclinic syngony, symmetry group P21/n; cell parameters: a = 12.40720(10), b = 10.30830(10), c = 36.7290(4) Å; β = 94.1110(10) deg., V = 4685.45(8) Å3, Z = 4; rcalc = 1.605 g/cm3; 2q 4.82-138.56 degrees; total reflections 27748; independent reflections 8680; number of specified parameters 604; Rint = 0.0367; GOOF 1.033; R1 = 0.0277, wR2 = 0.0709; residual electron density (max/min) 0.86/-0.81 e/Å3], 3 [C63H62O7SSb2, M 1206.78; monoclinic syngony, symmetry group P21/c; cell parameters: a = 20.9246(3), b = 13.5375(2), c = 21.4222(3) Å; β = 111.284(2) deg., V = 5654.30(16) Å3, Z = 4; rcalc = 1.4175 g/cm3; 2q 4.54-160 degrees; total reflections 48463; independent reflections 11892; number of specified parameters 699; Rint = 0.0443; GOOF 1.024; R1 = 0.0327, wR2 = 0.0907; residual electron density (max/min) 0.93/-0.85 e/Å3]. The antimony atoms in molecules 1, 2 have a distorted octahedral configuration, taking into account the coordination of the carbonyl oxygen atoms to the metal atom. Structure 3 contains tetrahedral tetraaryl stibonium cations, the antimony atoms in which are coordinated with the oxygen atoms of sulfo groups (Sb∙∙∙O(5)=S 2.601 Å), and the same oxygen atom is coordinated with the ortho-hydrogen atom of one of the tolyl groups (H(46)∙∙∙O(5)=S 2.60 Å). Water molecules provide a structure to crystal 3 (H(7)∙∙∙O(4)=S 1.98 Å, H(7)∙∙∙O(5)=S 2.60 Å). (CCDC 2320709 for 1, 2320711 for 2, 2320717 for 3; deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
Текст научной статьи Особенности строения полифункциональных карбоксилатов тетраарилсурьмы
Интерес к синтезу новых соединений сурьмы во многом определяется расширяющимся потенциалом различных областей применения в практической деятельности: в фармацевтической промышленности, в качестве биоцидов, фунгицидов, антиоксидантов, реагентов в тонком органическом синтезе, а также компонентов каталитических систем при полимеризации [1].
В основе эффективного получения производных сурьмы общей формулы Ar4SbOC(O)R лежат реакции пентаарилсурьмы с соединениями, содержащими подвижный атом водорода. В этом случае синтез целевого продукта происходит в одну стадию, а его выделение не является трудоемким. Так, взаимодействием эквимолярных количеств пентафенилсурьмы и малоновой кислоты в толуоле получен кислый малонат тетрафенилсурьмы [2]:
CH2 ph5sb
HOOC'" "COOH -рьн
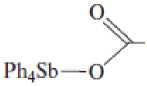
CH2
COOH
В то же время реакции двухосновных карбоновых кислот (янтарной, яблочной и винной) с двумя молями пентафенилсурьмы (толуол, 48 ч) приводят к образованию биядерных производных сурьмы с выходом до 98 % [3]:
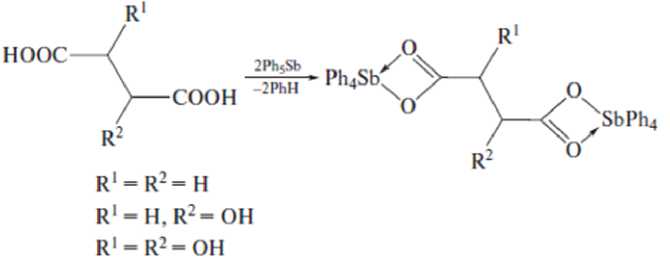
Продуктом реакции ацетилендикарбоновой кислоты с пентафенилсурьмой (толуол, 24 ч, 23 °С, мольное соотношение 1:2) является ацетилендикарбоксилат бис (тетрафенилсурьмы) [4]:
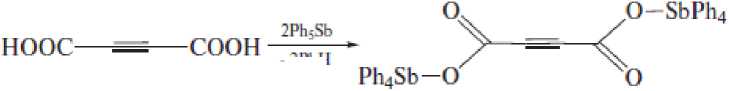
-2PhH
Особенность взаимодействия пентафенилсурьмы с тетрахлорфталевой кислотой заключается в том, что даже при соотношении реагентов 1:1 продуктом реакции является биядерное соединение [5]. Если продуктом реакции пентафенилсурьмы с карборандикарбоновой кислотой при мольном соотношении исходных реагентов 2:1 (толуол, 24 °С, 18 ч) является биядерное производное сурьмы (94 %), то взаимодействие эквимолярных количеств протекает с элиминированием углекислого газа и образованием монокарбоксилата тетрафенилсурьмы [6]:
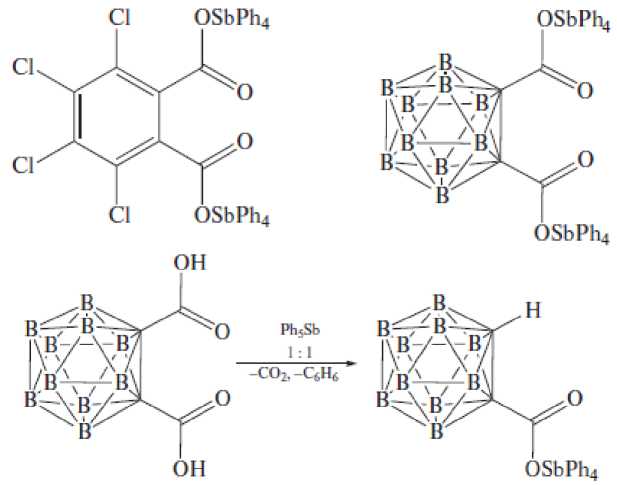
Отметим, что взаимодействие эквимолярных количеств ацетилендикарбоновой кислоты и пентафенилсурьмы также сопровождалось элиминированием углекислого газа, при этом имело место образование пропиолата тетрафенилсурьмы, который синтезировали также из пентафенил-сурьмы и пропиоловой кислоты [7]. В то же время мета -карборандикарбоновая кислота реагирует в растворе бензола с пентафенилсурьмой независимо от соотношения исходных реагентов с образованием только биядерного дикарбоксилата [8]. Показано, что взаимодействие пентафенил-сурьмы с 2,4-дигидроксибензойной кислотой независимо от соотношения реагентов протекает с участием карбоксильной и пара- гидроксильной групп и приводит к образованию 2-гидрокси-4-тетрафенилстибоксибензоата тетрафенилсурьмы(V), в молекуле которого тригонально-бипирамидальная координация двух атомов сурьмы искажена в разной степени [9]:
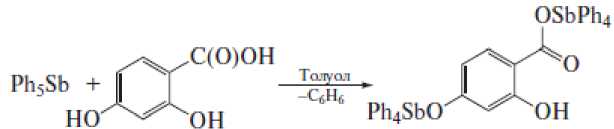
Установлено, что в реакции пентафенилсурьмы с 2,5- и 2,6-дигидроксибензойными кислотами участвуют только карбоксильные группы, продуктами являются 2,5-дигидроксибензоат тетрафенилсурьмы и 2,6-дигидроксибензоат тетрафенилсурьмы соответственно [10]:
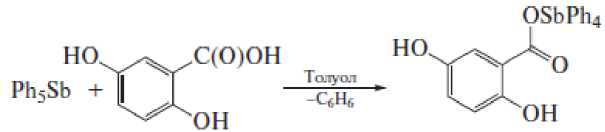
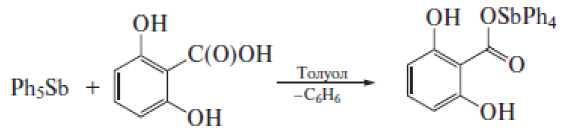
2,3-Дигидроксибензойная кислота при взаимодействии с пентафенилсурьмой проявляет свойства дигидроксибензола, при этом карбоксильная группа остается инертной даже при нагревании реакционной смеси, содержащей избыток пентафенилсурьмы. Единственным продуктом реакции является ионный комплекс 2-карбоксикатехолатотетрафенилстиботат(V) тетрафенилстибония, в анионе которого присутствует пятичленный металлоцикл:
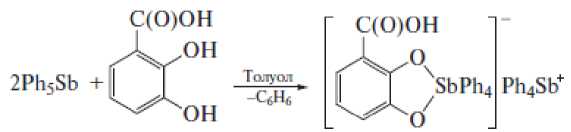
Ацетат тетрафенилсурьмы может реагировать с избыточным количеством уксусной кислоты с образованием аддукта Ph 4 SbOC(O)CH3 • CH3C(O)OH [11].
Первые Y-алкилацетилацетонаты тетрафенилсурьмы, в которых атомы сурьмы имеют октаэдрическую координацию с бидентатным ацетилацетонатным лигандом, получили взаимодействием пентафенилсурьмы с у -этилацетилацетоном, y -аллилацетилацетоном, y -фенилацетилацетоном и y -тиобутилацетилацетоном (толуол, 90 °С, 10 ч) [12, 13]. В гетероциклах SbO2C3 длины связей Sb—O близки к сумме ковалентных радиусов атомов сурьмы и кислорода:
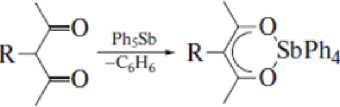
R= Et.All.Ph.BuS
Взаимодействием пентафенилсурьмы с октантетраоном-2,4,5,7 (мольное соотношение 2:1) в толуоле синтезирован биядерный комплекс Ph4Sb[oC(Ме)CHC(O)-(O)CCH(Ме)CO]SbPh4 [14]:
SbPh4 о о о чо
нзс'^^ТХХГСНз ~^^ HjC^WCH’
ОО О ZO
SbPh4
Найдено, что пентаарилсурьма и ферроцендикарбоновая кислота в растворе толуола (24 ° С, 24 ч) реагируют с образованием биядерных производных сурьмы, строение одного из них (толильного производного) ранее было доказано методом рентгеноструктурного анализа [15].
Известно, что пентаарилсурьма реагирует с алкил- или арилсульфоновыми кислотами с образованием соединений общей формулы Ar4SbOSO2R [16 - 22], однако только в случае сульфосалициловой кислоты, содержащей в своем составе гидрокси-, карбокси- и сульфогруппу, имело место замещение кислых атомов водорода вначале в сульфогруппе, а затем и в карбоксильном заместителе [16].
В настоящей работе описаны синтез и строение ферроценилдикарбоксилатов тетраарилсурьмы ( 1 , Ar = Ph и 2 , Ar = p -Tol), причем структура толильного производного уточнена с большей точностью, и сульфосалицилата тетра( пара -толил)сурьмы ( 3 ), описанного в работе [23], строение которого установлено впервые.
Экспериментальная часть
Соединения 1 ( t разл = 226 °С) и 2 ( t пл = 185 °С) синтезировали по методике, описанной в [15], из пентаарилсурьмы и ферроцендикарбоновой кислоты. Комплекс 3 ( t пл = 156 ° С) получали из пента( пара -толил)сурьмы и сульфосалициловой кислоты по методике, описанной в [23].
ИК-спектры соединений записывали на ИК-Фурье спектрометре Shimadzu IRAffinity-1S; образец готовили таблетированием с KBr (область поглощения 4000 - 400 см - 1).
Температуры разложения и плавления измерены на синхронном термоанализаторе Netzsch 449C Jupiter. Элементный анализ проводился на анализаторе Euro EA3028-НТ.
Рентгеноструктурный анализ проводили при 100(2) К на дифрактометре Rigaku XtaLAB Synergy-S (детектор типа HyPix-6000HE) с использованием Cu Kα ( λ = 1,54184 Å) излучения (графитовый монохроматор). Структуры были решены с помощью программы решения структуры ShelXT [24] с использованием внутренней фазировки и уточнены с помощью пакета уточнений ShelXL [25], включенного в пакет программ OLEX2 [26], с использованием минимизации методом наименьших квадратов. Эмпирическая коррекция поглощения применялась в программном комплексе CrysAlisPro [27] с использованием сферических гармоник, реализованных в алгоритме масштабирования SCALE3 ABSPACK. Положения атомов водорода были зафиксированы геометрически на рассчитанных расстояниях и позволяли им перемещаться на родительских атомах. Кристаллографические данные и результаты уточнения структур приведены в таблице.
Кристаллографические данные, параметры эксперимента и уточнения структур 1–3
|
Параметр |
1 |
2 |
3 |
|
Формула |
C 68 H 64 FeO 4 Sb 2 |
C 60 H 48 FeO 4 Sb 2 |
C 63 H 62 O 7 SSb 2 |
|
М |
1244,54 |
1132,33 |
1206,78 |
|
Сингония |
Моноклинная |
Моноклинная |
Моноклинная |
|
Пр. группа |
P 2 1 / с |
P 2 1 / n |
P 2 1 / с |
|
a , Å |
16,9983(2) |
12,40720(10) |
20,9246(3) |
|
b, Å |
10,94570(10) |
10,30830(10) |
13,5375(2) |
|
c, Å |
30,32204(3) |
36,7290(4) |
21,4222(3) |
|
α, град. |
90,00 |
90,00 |
90,00 |
|
β, град. |
99,8220(10) |
94,1110(10) |
111,284(2) |
|
γ, град. |
90,00 |
90,00 |
90,00 |
|
V , Å3 |
5559,04(10) |
4685,45(8) |
5654,30(16) |
|
Z |
4 |
4 |
4 |
|
р (выч.), г/см3 |
1,487 |
1,605 |
1,4175 |
|
-1 ц , мм |
10,100 |
11,925 |
8,335 |
|
F (000) |
2528,0 |
2272,0 |
2463,8 |
|
Размер кристалла (мм) |
0,1 × 0,16 × 0,18 |
0,11 × 0,15 × 0,19 |
0,09 × 0,13 × 0,17 |
|
Область сбора данных по 2 0 , град. |
5,28–138,76 |
4,82–138,56 |
4,54–160 |
|
Интервалы индексов отражений |
–20 ≤ h ≤ 20, –13 ≤ k ≤ 13, –36 ≤ l ≤ 36 |
–14 ≤ h ≤ 9, –12 ≤ k ≤ 12, –44 ≤ l ≤ 44 |
–25 ≤ h ≤ 26, –17 ≤ k ≤ 17, –27 ≤ l ≤ 21 |
|
Измерено отражений |
32707 |
27748 |
48463 |
|
Независимых отражений |
10281 |
8680 |
11892 |
|
Переменных уточнения |
684 |
604 |
699 |
|
GOOF |
1,062 |
1,033 |
1,024 |
|
R -факторы по F 2 > 2 с ( F 2) |
R 1 = 0,0345, wR 2 = 0,0853 |
R 1 = 0,0277, wR 2 = 0,0709 |
R 1 = 0,0327, wR 2 = 0,0907 |
|
R -факторы по всем отражениям |
R 1 = 0,0400, wR 2 = 0,0881 |
R 1 = 0,0317, wR 2 = 0,0728 |
R 1 = 0,0361, wR 2 = 0,0935 |
|
Остаточная электронная плотность (min/max), e /Å3 |
0,76/–0,90 |
0,86/–0,81 |
0,93/–0,85 |
Полные таблицы координат атомов, длин связей и валентных углов соединения 1, 2, 3 депонированы в Кембриджском банке структурных данных (CCDC 2320709 для 1, 2320711 для 2, 2320717 для 3; ; .
Обсуждение результатов
Сурьмаорганические производные ферроцена Fc[OC(O)SbTol 4 ] 2 ( 1 ) и Fc[OC(O)SbPh 4 ] 2 ( 2 )
были получены деарилированием пентаарилсурьмы в бензоле при 80 ° С в течение 1 ч:
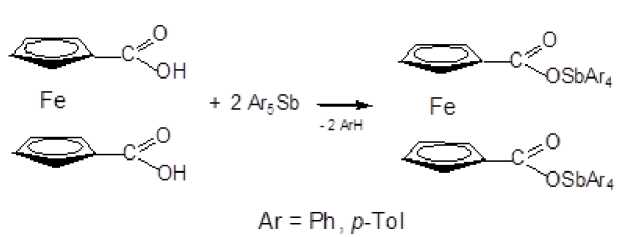
Ход реакции контролировали методом ТСХ. После перекристаллизации целевых продуктов из смеси бензол-октан получили светло-коричневые кристаллы, которые анализировали при помощи элементного анализа, ИК-спектроскопии и методом рентгеноструктурного анализа.
По аналогичной схеме синтезировали гидрат сульфосалицилата тетра( пара -толил)сурьмы (4-MeC 6 H 4 ) 4 Sb[OSO 2 C 6 H 3 (OH-1)(COOH-2)] 2 ( 3 ):
2(4-MeC 6 H 4 ) 5 Sb + НО8О 2 С б Н з (ОН-1)(СООН-2)]-2Н 2 О ^
^ [(4-MeC 6 H 4 ) 4 Sb][OSO 2 C 6 H 3 (OH-1)[C(O)OSb(C 6 H 4 Me-4) 4 )]^H 2 O
Полученные соединения растворимы в большинстве органических растворителей и имеют высокие температуры разложения/плавления.
Строение соединений 1 и 2 доказано методом РСА, причем структура первого (рис. 1) уточнена с большей точностью, чем в работе [15]. Найдено, что в соединениях 1 и 2 (рис. 2) наблюдается заметное искажение тригонально-бипирамидальной конфигурации молекул, как и в ряду ацилокситетраарильных соединений сурьмы общей формулы Ar 4 SbOC(O)R [1], причем наибольшие отклонения величин аксиальных углов СSbO наблюдаются в 1 (166,92(10) и 170,91(10)°) против 170,18(9) и 176,48(8)° в 2 .
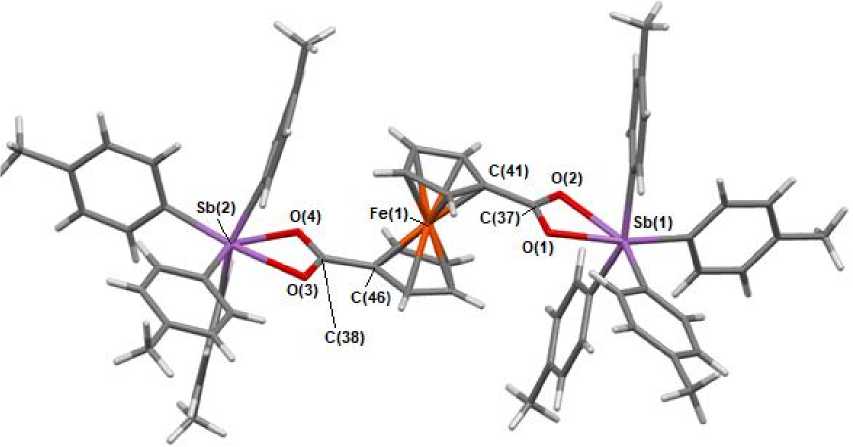
Рис. 1. Строение комплекса Fc[C(O)OSb(Tol-p) 4 )] 2 (1)
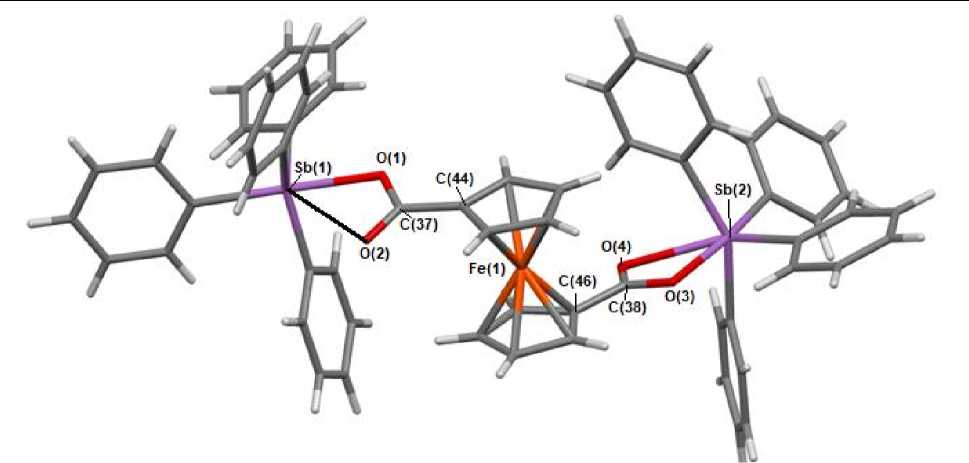
Рис. 2. Строение комплекса Fc[C(O)OSbPh 4 )] 2 (2)
Длины связей Sb - C в 1 находятся в интервале 2,131(3) - 2,173(3) А, что сравнимо с наблюдаемыми в 2 (2,130(3) - 2,182(3) А), приближающимися по своему значению к сумме ковалентных радиусов атомов-партнеров (2,12 А [28]). Прочность связей Sb - O в карбоксильных лигандах (2,290(3) Å в 1 и 2,241(3), 2,257(3) Å в 2 ) выше, чем связей Sb∙∙∙O=С (2,437(3), 2,478(3) Å в 1 и 2,571(3), 2,929(3) А в 2 ), что значительно меньше суммы ван-дер-ваальсовых радиусов атомов-партнеров (3,70 А) и больше суммы ковалентных радиусов атомов Sb и O (2,07 А [28]). Взаимодействие атомов Sb···O=С в полученных карбоксилатах тетраарилсурьмы подтверждается увеличением экваториальных углов со стороны контакта до 154,25(2), 155,05(2)° в 1 и 13 8,49(2), 151,50(2)° в 2 , при этом два других угла уменьшаются (100,28(2), 101,44(2)° в 1 и 102,09(2), 111,63(2)° в 2 ) по сравнению с идеальным значением 120°. Таким образом, внутримолекулярные контакты в 1 и 2 приводят к существенным искажениям в координационной сфере атомов сурьмы, и можно поэтому констатировать в них октаэдрическое окружение атомов металла, которое проявляется в большей степени для молекул 1 , очевидно, из-за присутствия донорных метильных групп в ароматических заместителях при атомах сурьмы. Действительно, в этих случаях карбоксилатные лиганды являются в полном смысле хелатирующими и координируются на атом сурьмы двумя атомами кислорода. Так, в молекулах ферроценилдикарбоксилатах тетраарилсурьмы отношение d (Sb'"O=C)Z d (Sb-О) близко к 1 (1,06 для 1 и 1,20 для 2 ). Вследствие этого координация атома сурьмы в них становится искаженной октаэдрической. Бидентатный характер карбоксилатных лигандов в 1 и 2 усиливает делокализация подвижной электронной плотности ферроценового фрагмента по карбоксильным группам. Донорные свойства ферроценильного заместителя (Fc) были ранее отмечены на примере диферроценилтитаноцена, когда прочность а -связи Ti - C усиливалась донорно-акцепторным взаимодействием Fc ^ Ti [29, 30].
О синтезе сульфосалицилата тетрафенилсурьмы и его сольвата со спиртом ранее сообщалось в [23], а об особенностях строения последнего - в работе [31]. В частности, было показано, что в его кристалле взаимодействий молекул спирта и производного сурьмы практически не наблюдалось. Поэтому было интересно исследовать строение гидрата сульфосалицилата тет-ра( пара -толил)сурьмы ( 3 ), несколько отличающегося от аналогичного фенильного производного (рис. 3).
Показано, что кристалл 3 содержит катионы тетра( пара -толил)стибония, атомы сурьмы в которых координированы с атомами кислорода сульфогрупп (Sb∙∙∙O(5)=S 2,601 Å) молекулярной формы соединения, причем гидроксильная группа остатка сульфосалициловой кислоты О(2)Н(3) участвует в образовании шестичленного цикла O(2)C(87)C(81)C(86)O(3)H(3) (H(3)^^^O(2)=C 1,80 А). Молекулы воды структурируют кристалл 3 (H(7)—O(4)=S 1,98 А, H(7)—O(5)=S 2,6 А).
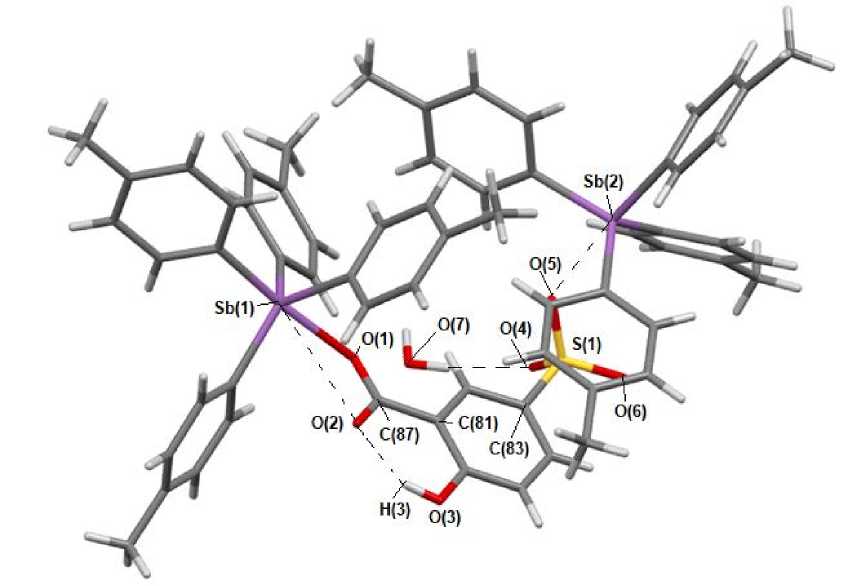
Рис. 3. Строение комплекса [(4-MeC 6 H 4 ) 4 Sb][OSO 2 C 6 H 3 (OH-1)[C(O)OSb(4-MeC 6 H 4 ) 4 )]∙H 2 O (3)
Заключение
Таким образом, из ферроцендикарбоновой кислоты, сульфосалициловой кислот и пентаарил-сурьмы (бензол, 1 ч, 80 ° С) получены сполна замещенные сурьмаорганические производные ферроцендикарбоновой и сульфосалициловой кислот 1 – 3 , строение которых доказано методом рентгеноструктурного анализа. Атомы сурьмы в молекулах 1 , 2 имеют в первом приближении искаженную тригонально-бипирамидальной конфигурацию с атомами кислорода в аксиальных положениях, однако с учетом координации карбонильных атомов кислорода на атом металла (Sb—O=C 2,437 - 2,829 А) его координационное число возрастает до шести. В структуре 3 присутствуют тетраэдрические тетраарилстибониевые катионы, атомы сурьмы в которых координированы с атомами кислорода сульфогрупп (Sb∙∙∙O(5)=S 2,601 Å) молекулярной формы соединения, причем этот же атом кислорода координирован с орто -атомом водорода одной из толильных групп (Н(46)∙∙∙O(5)=S 2,60 Å). Молекулы воды структурируют кристалл 3 (Н(7)∙∙∙O(4)=S 1,98 Å, Н(7)∙∙∙O(5)=S 2,6 Å).
Список литературы Особенности строения полифункциональных карбоксилатов тетраарилсурьмы
- Шарутин В.В., Поддельский А.И., Шарутина О.К. // Коорд. химия. 2020. Т. 46, № 10. С. 579. DOI: 10.31857/S0132344X20100011.
- Sharutin V.V., Senchurin V.S., Sharutina O.K. // Russ. J. Inorg. Chem. 2014. V. 59. P. 115. DOI: 10.1134/S003602361402017Xю
- Sharutin V.V., Sharutina O.K. // Russ. J. Coord. Chem. 2014. V. 40, No. 9. P. 643. DOI: 10.1134/S1070328414090073ю
- Sharutin V.V., Sharutina O.K., Gubanova Yu.O. // Bull. South Ural State Univ. Ser. Chem. 2015. V. 7. P. 17. DOI: 10.14529/chem150403.
- Sharutin V.V., Sharutina O.K. // Russ. J. Inorg. Chem. 2015. V. 60, No. 3. P. 292. DOI: 10.1134/S0036023615030171.
- Sharutin V.V., Sharutina O.K., Gubanova Y.O. et al. // J. Organomet. Chem. 2015. V. 798. P. 41. DOI: 10.1016/j.jorganchem.2015.09.002.
- Sharutin V.V., Sharutina O.K., Senchurin V.S. // Russ. J. Coord. Chem. 2014. V. 40, No. 2. P. 109. DOI: 10.1134/S1070328414020109
- Sharutin V.V., Sharutina O.K., Gubanova Y.O. et al. // Mendeleev Commun. 2018. V. 28. P. 621. DOI: 10.1016/j.mencom.2018.11.019.
- Шарутин В.В., Шарутина О.К., Губанова Ю.О. // Вест. Южно-Урал. гос. ун-та. Сер. хим. 2017. Т. 9. № 4. С. 56. DOI: 10.14529/chem170409.
- Sharutin V.V., Sharutina O.K., Gubanova Y.O., Eltsov O.S. // Inorg. Chim. Acta. 2019. V. 494. P. 211. DOI: 10.1016/j.ica.2019.05.029.
- Sharutin V.V., Senchurin V.S., Sharutina O.K., Panova L.P. // Russ. J. Inorg. Chem. 2008. V. 53. № 7. С. 1110. DOI: 10.1134/S0036023608070206.
- Sharutin V.V., Sharutina O.K., Zadachina O.P. et al. // Russ. J. Coord. Chem. 2003. V. 29, No. 1. P. 6. DOI: 10.1023/A:1021878530695
- Sharutin V.V., Pakusina A.P., Egorova I.V. et al. // Russ. J. Coord. Chem. 2008. V. 34, No. 4. P. 259. DOI: 10.1134/S1070328408040040
- Sharutin V.V., Sharutina O.K., Senchurin V.S., Mukovoz P.P. // Russ. J. Inorg. Chem. 2014. V. 59, No. 5. С. 508. DOI: 10.1134/S0036023614050155.
- Шарутин В.В. // Вестник ЮУрГУ. Серия «Химия». 2023. Т. 15, № 3. С. 89. DOI: 10.14529/chem230303.
- Шарутин В.В., Шарутина О.К., Панова Л.П., Бельский В.К. // Журн. общ. химии. 1997. Т. 67, вып. 9. С. 1531.
- Шарутин В.В., Шарутина О. К., Тарасова Т.А. и др. // Журн. общ. химии. 1999. Т. 69, Вып. 12. С. 1979.
- Шарутин В.В., Шарутина О.К., Тарасова Т.А. и др. // Журн. общ. химии. 2000. Т. 70, Вып. 8. С. 1311.
- Шарутин В.В., Пакусина А.П., Егорова И.В. и др. // Коорд. химия. 2003. Т. 29, № 5. С. 336. EDN: OOFOOD.
- Шарутин В.В., Шарутина О.К., Пакусина А.П. и др. // Коорд химия. 2004. Т. 30, № 1. С. 15. EDN: OVZSPL.
- Шарутин В.В., Егорова И.В., Пакусина А.П. и др. // Коорд. химия. 2007. Т. 33, № 3. С. 176. EDN: IADDTV.
- Шарутин В.В., Шарутина О.К., Сенчурин В.С. // Журн. неорган. химии. 2013. Т. 58, № 11. С. 1454. DOI: 10.7868/S0044457X13110196.
- Панова Л.П. Аренсульфонаты тетра- и триарилсурьмы. Синтез и строение: дис. … канд. хим. наук. Иркутск. 1999. 104 с.
- Sheldrick G. SHELXT – Integrated space-group and crystal-structure determination. Acta Crystallographica. Section A. 2015, 71, 3–8.
- Sheldrick G.M. Crystal structure refinement with SHELXL. Acta Crystallographica Section C. 2015; 71, 3–8.
- Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Cryst. 2009. V. 42. P. 339. DOI: 10.1107/S0021889808042726.
- CrysAlisPro 1.171.41.103a (Rigaku OD, 2021).
- Бацанов С.С. Атомные радиусы элементов // Журн. неорг. химии. 1991. Т. 36, № 12. С. 3015.
- Razuvaev G.A., Domrachev G.A., Sharutin V.V., Suvorova O.N. // J. Organometal. Chem. 1977. V. 141. P. 313. DOI: 10.1016/S0022-328X(00)90854-4.
- Zakharov L.N., Struchkov Yu.T., Sharutin V.V., Suvorova O.N. // Cryst. Struct. Comm. 1979. V. 8. P. 439.
- Шарутин В.В., Шарутина О.К., Панова Л.П., Бельский В.К. // Коорд. химия. 1997. Т. 23, № 7. С. 513.


