Особенности строения производных тетра(пара-толил)сурьмы p-Tol4SbX (X = Br, Oc(O)Ph•PhH, OSO2C6H2Me3-2,4,6)
Автор: Шарутин В.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 4 т.15, 2023 года.
Бесплатный доступ
Строение соединений тетра( пара -толил)сурьмы p -Tol4SbX [X = Br (1), OC(O)Ph∙PhH (2), OSO2C6Me3-2,4,6 (3)] установлено методом рентгеноструктурного анализа (РСА). По данным РСА, атомы сурьмы в комплексах 1-3 имеют координацию искаженной тригональной бипирамиды с тремя арильными лигандами в экваториальной плоскости, при этом аксиальные углы CSbX составляют 174,75(8), 175,13(9) и 174,51(6)°. Данные РСА: (1) [C28H28BrSb, M = 566,16; моноклинная сингония, пр. гр. P 21/ n ; параметры ячейки: a = 9,868(6) Å, b = 23,312(11) Å, c = 12,106(6) Å; β = 113,15(2)°, V = 2561(2) Å3, Z = 4; r(выч.) = 1,469 г/см3; m = 2,649 мм-1; F (000) = 1128,0; обл. сбора по 2q: 6,4-56,76°; -13 ≤ h ≤ 13, -31 ≤ k ≤ 31, -16 ≤ l ≤ 16; всего отражений 42998; независимых отражений 6359 ( R int = 0,0346); GOOF = 1,080; R -фактор 0,0325]; (2) [C41H39O2Sb, M = 685,47; моноклинная сингония, пр. гр. С 2/ с ; параметры ячейки: a = 28,186(13) Å, b = 15,116(6) Å, c = 17,629(8) Å; β = 91,73(2)°, V = 7507(6) Å3, Z = 8; r(выч.) = 1,213 г/см3; m = 0,765 мм-1; F (000) = 2816,0; обл. сбора по 2q: 6,572-56,996°; -37 ≤ h ≤ 37, -20 ≤ k ≤ 20, -23 ≤ l ≤ 23; всего отражений 116806; независимых отражений 9489 ( R int = 0,0492); GOOF = 1,102; R -фактор 0,0363]; (3) [C37H39O3SSb, M = 685,49; моноклинная сингония, пр. гр. P 21/ n ; параметры ячейки: a = 12,172(4) Å, b = 18,802(5) Å, c = 15,433(6) Å; β = 108,744(12)°, V = 3345(2) Å3, Z = 4; r(выч.) = 1,361 г/см3; m = 0,921 мм-1; F (000) = 1408,0; обл. сбора по 2 q : 5,96-63,02°; -16 ≤ h ≤ 17, -27 ≤ k ≤ 27, -22 ≤ l ≤ 21; всего отражений 138835; независимых отражений 11081 ( R int = 0,0373); GOOF = 1,045; R -фактор 0,0304]. Полные таблицы координат атомов, длин связей и валентных углов соединений 1-3 депонированы в Кембриджском банке структурных данных (№ 2182608, 2149953, 2171918; deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
Пента(пара-толил)сурьма, реакции с кислотами, бромид, бензоат, мезитиленсульфонат, тетра(пара-толил)сурьма, особенности строения, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147242672
IDR: 147242672 | УДК: 546.865+547.53.024+548.312.5 | DOI: 10.14529/chem230402
Features of the structure of tetra(para- tolyl)antimony derivatives p-Tol4SbX (X = Br, Oc(O)Ph•PhH, OSO2C6H2Me3-2,4,6)
The structure of tetra( para -tolyl)antimony compounds p-Tol4SbX [X = Br (1), OC(O)Ph∙PhH (2), OSO2C6Me3-2,4,6 (3)] was established by X-ray diffraction analysis (XRD). According to the X-ray diffraction data, the antimony atoms in complexes 1-3 have a distorted trigonal bipyramidal coordination with three aryl ligands in the equatorial plane, while the axial angles CSbX are 174.75(8), 175.13(9), and 174.51(6)°. The X-ray diffraction data: (1) [C28H28BrSb, M = 566.16; monoclinic syngony, sp. gr. P 21/ n ; cell parameters: a = 9.868(6) Å, b = 23.312(11) Å, c = 12.106(6) Å; β = 113.15(2)°, V = 2561(2) Å3, Z = 4; rcalc = 1.469 g/cm3; m = 2.649 mm-1; F(000) = 1128.0; region 2q collection: 6.4-56.76°; -13 ≤ h ≤ 13, -31 ≤ k ≤ 31, -16 ≤ l ≤ 16; total reflections 42998; independent reflections 6359 (Rint = 0.0346); GOOF = 1.080; R-factor 0.0325]; (2) [C41H39O2Sb, M = 685.47; monoclinic syngony, sp. gr. C 2/ c ; cell parameters: a = 28.186(13) Å, b = 15.116(6) Å, c = 17.629(8) Å; β = 91.73(2)°, V = 7507(6) Å3, Z = 8; rcalc = 1.213 g/cm3; m = 0.765 mm-1; F(000) = 2816.0; region 2q collection: 6.572-56.996°; -37 ≤ h ≤ 37, -20 ≤ k ≤ 20, -23 ≤ l ≤ 23; total reflections 116806; independent reflections 9489 (Rint = 0.0492); GOOF = 1.102; R -factor 0.0363]; (3) [C37H39O3SSb, M = 685.49; monoclinic syngony, sp. gr. P 21/ n ; cell options: a = 12.172(4) Å, b = 18.802(5) Å, c = 15.433(6) Å; β = 108.744(12)°, V = 3345(2) Å3, Z = 4; r calc = 1.361 g/cm3; m = 0.921 mm-1; F(000) = 1408.0; region 2q collection: 5.96-63.02°; -16 ≤ h ≤ 17, -27 ≤ k ≤ 27, -22 ≤ l ≤ 21; total reflections 138835; independent reflections 11081 ( R int = 0.0373); GOOF = 1.045; R -factor 0.0304]. Complete tables of atomic coordinates, bond lengths, and bond angles for compounds 1-3 have been deposited at the Cambridge Crystallographic Data Center (CCDC 2182608, 2149953, 2171918; deposit@ccdc.cam.ac.uk; http://www.ccdc.cam. ac.uk).
Текст научной статьи Особенности строения производных тетра(пара-толил)сурьмы p-Tol4SbX (X = Br, Oc(O)Ph•PhH, OSO2C6H2Me3-2,4,6)
Возрастающий интерес к органическим соединениям сурьмы во многом определяется растущим потенциалом их применения в самых разнообразных областях практической деятельности: в качестве лекарственных препаратов, биоцидов, фунгицидов, в качестве реагентов и компонентов каталитических систем при полимеризации, в тонком органическом синтезе, в качестве антиоксидантов и др. [1]. Одними из наиболее исследованных сурьмаорганических соединений являются фенильные производные пятивалентной сурьмы общей формулы Ph 4 SbX (Х – электроотрицательная группа) [2]. В меньшей степени изучены подобные толильные производные [3 - 25].
В молекулах органических соединений сурьмы(V) центральный атом содержит пять электронных пар на валентной оболочке. Согласно теории ОЭПВО (отталкивание электронных пар валентных орбиталей) предпочтительной конфигурацией для пяти отталкивающихся точек (электронных пар), расположенных на поверхности сферы, является тригональная бипирамида. Отличительная особенность этой конфигурации – то, что экваториальные электронные пары должны быть расположены ближе к центральному остову, чем аксиальные, исходя из баланса между взаимным отталкиванием и притяжением электронных пар. В рамках модели жестких сфер для молекул с пятью электронными парами на валентной оболочке центрального атома оказывается возможной любая структура, промежуточная между квадратной пирамидой и тригональной бипирамидой с валентными углами между экваториальными связями в интервале от 90 до 120°.
Тригональная бипирамида оказывается энергетически немногим более стабильной, чем квадратная пирамида [26].
В производных сурьмы общей формулы Ar 4 SbX электроотрицательный лиганд Х всегда находится в аксиальном положении, что полностью согласуется с теорией ОЭПВО, причем чаще всего происходит увеличение длины связи Sb-X, по сравнению с суммой ковалентных радиусов связанных между собой атомов. Это наблюдается, например, в хлоридах тетрафенил- и тетра- п -толилсурьмы [3, 27], где расстояния Sb–Cl равны 2,740(6) и 2,72(1) Å соответственно, что значительно больше суммы ковалентных радиусов атомов Sb и Cl (2,40 Å) [28]. Аналогичное удлинение связи Sb–Br (2,965 Å [29]; 2,950 Å [30]) наблюдается для бромидов тетрафенил- и тетра( пара -толил)сурьмы (сумма ковалентных радиусов атомов Sb и Br равна 2,55 Å [28]).
В настоящей работе изучены особенности строения производных тетра( пара -толил)сурьмы: p -Tol 4 SbX [X = Br ( 1 ), OC(O)Ph∙PhH ( 2 ), OSO 2 C 6 Me 3 -2,4,6 ( 3 )].
Экспериментальная часть
Соединения 1 - 3 синтезировали по методике, описанной в [1], из эквимолярных количеств пента( пара -толил)сурьмы и кислоты в растворе бензола. После перекристаллизации целевого продукта из смеси бензол-октан (1:2 объем.) получали бесцветные кристаллы 1 - 3 , которые анализировали методами элементного анализа, РСА и ИК-спектроскопии.
ИК-спектры соединений записывали на ИК-Фурье спектрометре Shimadzu IRAffinity-1S; образец готовили таблетированием с KBr (область поглощения 4000 - 400 см - 1).
Рентгеноструктурный анализ проводили на автоматическом четырехкружном дифрактометре Bruker D8 QUEST (Mo K α -излучение, λ = 0,71073 Å, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [31]. Все расчеты по определению и уточнению структур выполнены по программам SHELXL/PC [32] и OLEX2 [33]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Кристаллографические данные и результаты уточнения структур приведены в таблице.
Таблица
Кристаллографические данные, параметры эксперимента и уточнения структур 1–3
|
Параметр |
1 |
2 |
3 |
|
1 |
2 |
3 |
4 |
|
Формула |
C 28 H 28 BrSb |
C 41 H 39 O 2 Sb |
C 37 H 39 O 3 SSb |
|
М |
566,16 |
685,47 |
685,49 |
|
Сингония |
Моноклинная |
Моноклинная |
Моноклинная |
|
Пространственная группа |
P 2 1 / n |
C 2/c |
P 2 1 / n |
|
a , Å |
9,868(6) |
28,186(13) |
12,172(4) |
|
b, Å |
23,312(11) |
15,116(6) |
18,802(8) |
|
c, Å |
12,106(6) |
17,629(8) |
15,433(6) |
|
α, град. |
90,00 |
90,00 |
90,00 |
|
β, град. |
113,15(2) |
91,73(2) |
108,744(12) |
|
γ, град. |
90,00 |
90,00 |
90,00 |
|
V , Å3 |
2561(2) |
7507(6) |
3345(2) |
|
Z |
4 |
8 |
4 |
|
ρ (выч.), г/см3 |
1,469 |
1,213 |
1,361 |
|
µ , мм–1 |
2,649 |
0,765 |
0,921 |
|
F (000) |
1128,0 |
2816,0 |
1408,0 |
|
Размер кристалла (мм) |
0,39 × 0,3 × 0,12 |
0,5 × 0,4 × 0,06 |
0,45 × 0,28 × 0,06 |
|
Область сбора данных по 2 θ , град. |
6,4–56,76 |
6,572–56,996 |
5,96–63,02 |
|
Интервалы индексов отражений |
–13 ≤ h ≤ 13, –31 ≤ k ≤ 31, –16 ≤ l ≤ 16 |
–37 ≤ h ≤ 37, –20 ≤ k ≤ 20, –23 ≤ l ≤ 23 |
–16 ≤ h ≤ 17, –27 ≤ k ≤ 27, –22 ≤ l ≤ 21 |
|
Измерено отражений |
42998 |
116806 |
138835 |
|
Независимых отражений |
6359 |
9489 |
11081 |
Окончание таблицы
|
1 |
2 |
3 |
4 |
|
Отражений с I > 2 σ ( I ) |
5068 |
7621 |
8404 |
|
Переменных уточнения |
275 |
473 |
386 |
|
GOOF |
1,080 |
1,102 |
1,045 |
|
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0325, wR 2 = 0,0665 |
R 1 = 0,0363, wR 2 = 0,0987 |
R 1 = 0,0304, wR 2 = 0,0708 |
|
R -факторы по всем отражениям |
R 1 = 0,0494, wR 2 = 0,0734 |
R 1 = 0,0516, wR 2 = 0,1083 |
R 1 = 0,0504, wR 2 = 0,0795 |
|
Остаточная электронная плотность (min/max), e /Å3 |
–0,71/0,54 |
–0,66/0,80 |
–0,73/0,32 |
Полные таблицы координат атомов, длин связей и валентных углов соединений 1-3 депонированы в Кембриджском банке структурных данных (CCDC 2182608, 2149953, 2171918; ; .
Обсуждение результатов
Кристаллическая структура бромида тетра( пара -толил)сурьмы была ранее определена в [29, 30]. В настоящей работе строение указанного производного сурьмы уточнено до R = 3,25 %. Установлено, что ароматические кольца в экваториальной плоскости имеют пропеллерную конформацию, при этом углы между плоскостями циклов и экваториальной плоскостью равны 13,51; 34,96; 67,75° (рис. 1).
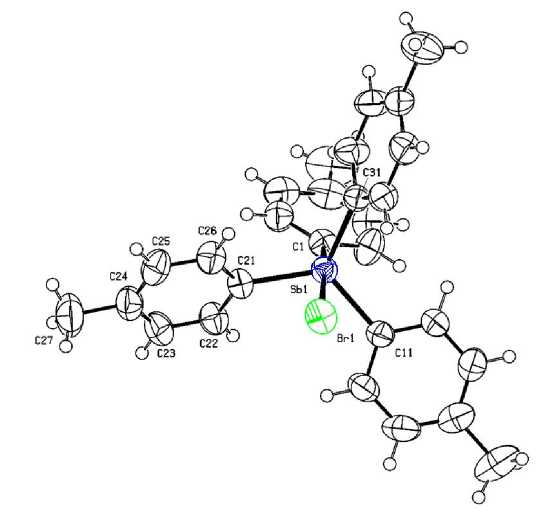
Рис. 1. Строение бромида тетра( пара -толил)сурьмы p -Tol 4 SbBr (1)
Большое значение одного из углов является, вероятно, причиной возникновения внутримолекулярного контакта между атомом брома и мета-атомом водорода толильного кольца Br···H(15) (2,95 Å) при сумме ван-дер-ваальсовых радиусов атомов 3,1 Å [28]). Стремлением к увеличению сокращенного расстояния можно объяснить наблюдаемое искажение аксиального угла C(1)SbBr [174,75(8)°], которое при идеальном значении последнего было бы еще короче. Нарушение линейности фрагмента BrSbC(1) происходит за счет отклонения связи Sb–Br в сторону толильного кольца С(11)–С(17), находящегося практически в экваториальной плоскости. Атом Sb выходит из экваториальной плоскости [С3] к атому углерода аксиальной толильной группы на 0,287 Å, вследствие чего углы Br(1)SbСeq [79,01(8)–88,40(8)°] меньше идеального значения (90°), а углы СaxSbCeq [96,83(11)–99,11(11)°] – больше. Сумма углов в экваториальной плоскости равна 354,4°, при этом их значения различаются между собой [114,66(11), 117,44(11), 122,44(12)°]. Отношение длины аксиальной связи Sb–Cax [2,153(3) Å] к среднему значению экваториальных связей Sb–Ceq [2,103(3), 2,108(3), 2,118(3) Å] равно 1,02, т. е. приближается к 1. Все наблюдаемые параметры демонстрируют тенденцию фрагмента С4Sb к переходу в тетраэдрическую структуру. Расстояние Sb–Br [2,9637(15) Å] превышает сумму ковалентных радиусов атомов Sb и Br (2,55 Å [28]), что свидетельствует о координационном характере связи.
В описаных ранее структурах карбоксилатов тетра( пара -толил)сурьмы атомы сурьмы имеют искаженную тригонально-бипирамидальную координацию с аксиально расположенными карбокси- и толильной группами с дополнительной координацией атома кислорода карбонильной группы на атом металла [8, 16 - 18, 20, 22, 25, 34, 35], при этом внутримолекулярные расстояния Sb⋅⋅⋅O(=С) в их молекулах значительно меньше суммы ван-дер-ваальсовых радиусов атомов сурьмы и кислорода (3,58 Å) [29], однако в сурьмаорганических производных фумаровой кислоты подобная координация отсутствует [36]. Аксиальные углы OSbС и суммы углов CSbC в экваториальной плоскости близки к значениям 180 и 360 ° .
Установлено, что в кристалле сольвата p -Tol4SbOC(O)Ph∙PhH ( 2 ) присутствуют молекулы бензола, разупорядоченные по трем положениям; атомы сурьмы имеют искаженную тригональ-но-бипирамидальную координацию с аксиально расположенными карбоксильной группой и атомом углерода одной из толильных групп (рис. 2).
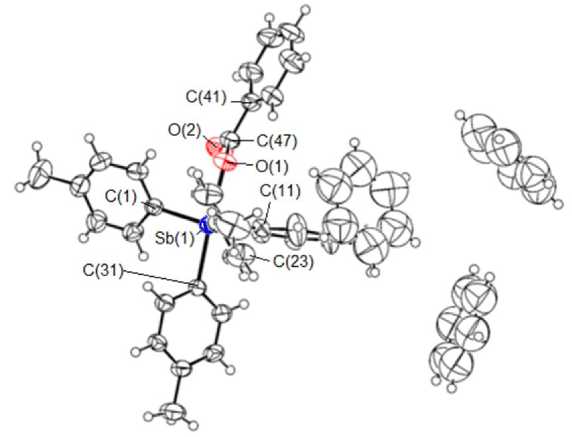
Рис. 2. Строение сольвата бензоатотетра( пара -толил)сурьмы с бензолом p -Tol 4 SbOC(O)Ph∙PhH (2)
Искажение координационного полиэдра атома сурьмы в 2 проявляется в выходе центрального атома из экваториальной плоскости в сторону аксиального атома углерода С(31) на 0,196 Å, что сопровождается уменьшением суммы углов в экваториальной плоскости (357,43°) по сравнению с 360°, при этом интервалы изменения углов CSbC составляют 115,17(11)-125,62(11)°. Толильные кольца в экваториальной плоскости имеют пропеллерную конформацию, при этом углы между плоскостями циклов и экваториальной плоскостью равны 10,71; 51,23; 62,02°. Наличие карбоксильной группы в ацилатах тетраарилсурьмы допускает реализацию в этих соединениях дополнительной внутримолекулярной координации атома сурьмы с карбонильным кислородом, т. е. увеличение координационного числа атома сурьмы до 6. Расстояние между атомом сурьмы и карбонильным кислородом, формально не связанными друг с другом, в соединении 2 составляет 3,272 Å при сумме ван-дер-ваальсовых радиусов атомов сурьмы и кислорода равной 3,70 Å [29]. Взаимодействие атомов Sb···O=С в 2 подтверждается увеличением экваториальных углов (со стороны контакта) до 125,62(11)º и уменьшением двух других углов [115,17(11), 116,64(11)º] по сравнению с идеальным значением 120º. Таким образом, внутримолекулярный контакт приводит к существенным искажениям в координационной сфере атомов сурьмы. Необходимо отметить, что внутримолекулярные контакты Sb—O(=C) в монокарбоксилатах тетрарилсурьмы изме- няются в интервалах 2,594-3,309 Å [37]. Длина связи Sb–O(1) (2,246(2) Å) значительно превышает по значению длины экваториальных связей Sb–C (2,113(3)–2,120(3) Å). Отношение растояний Sb-X к сумме ковалентных радиусов атомов-партнеров в соединениях p-Tol4SbХ (X = Br 1, O 2) одинаково (1,16), что позволяет рассматривать комплексы 1 и 2 как тесные ионные пары с тет-ра(пара-толил)стибониевыми катионами [p-Tol4Sb]+ и анионами Х-.
Согласно одному из правил, сформулированных в рамках теории ОЭПВО, увеличение электроотрицательности лиганда коррелирует с увеличением длины его связи с центральным атомом, поэтому можно ожидать, что замена электроотрицательного лиганда Х в комплексах p -Tol 4 SbХ на аренсульфонатную группу приведет к увеличению ионного характера связи Sb - O. Действительно, в бензолсульфонате тетра( пара -толил)сурьмы расстояние Sb - O составляет 2,400(7) Å [39], а в толуолсульфонате тетра( пара -толил)сурьмы длина Sb - O равна 2,404 Å [7,9]. В синтезированном мезитиленсульфонате тетра( пара -толил)сурьмы ( 3 ) длина Sb - O(1) равна 2,5424(14) Å, а отношение d Sb - O / Σ (r Sb + r O ) = 1,23, что свидетельствует о более ионном характере этой связи по сравнению с комплексами 1 и 2 . С учетом координации сульфонатного лиганда атом сурьмы в 3 имеет сильно искаженную тригонально-бипирамидальную координацию с атомами кислорода и углерода в аксиальных положениях (рис. 3).
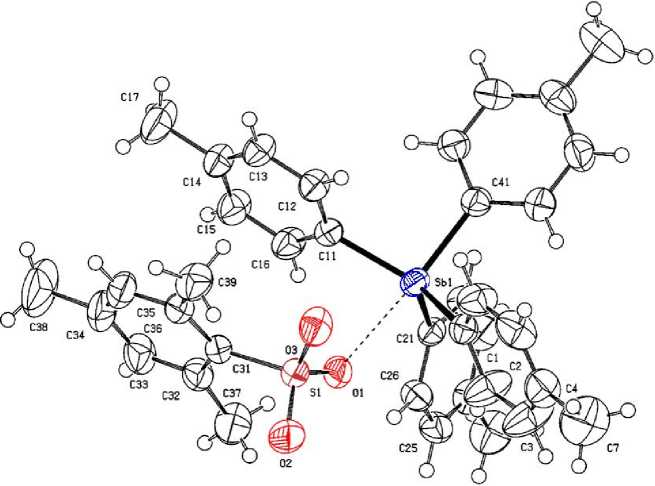
Рис. 3. Строение 2,4,6-триметилбензолсульфоната тетра( пара -толил)сурьмы p -Tol 4 SbOSO 2 С 6 H 2 (Me 3 -2,4,6) (3)
Аксиальный угол O(1)Sb(1)C(41) равен 174,51(6)°. Атом сурьмы выходит из экваториальной плоскости к аксиальному атому углерода С(41) на 0,33 Å, поэтому углы C eq Sb(1)C ax больше 90° (97,32(7)° - 101,66(7)°). Толильные кольца в экваториальной плоскости имеют пропеллерную конформацию, при этом углы между плоскостями циклов и экваториальной плоскостью равны 25,15, 27,27, 72,42°. Сумма валентных углов СSbC в экваториальной плоскости составляет 352,44(7)°, их значения изменяются в интервале 108,62(7)°–131,56(7)°. Аксиальная связь Sb(1)– С(41) (2,1396(19) Å) длиннее экваториальных связей Sb(1)–С(1,11,21) (2,1067(19), 2,1046(18), 2,1182(18) Å). Отношение длины аксиальной связи к среднему значению экваториальных связей (2,1098 Å) равно 1,014, т. е. приближается к единице. Расстояние Sb(1)–O(1) в 3 близко к аналогичному расстоянию в бензолсульфонате тетра( пара -толилсурьмы (2,400(7) Å) [38]. Наличие координационной связи Sb(1)∙∙∙O(1) в 3 приводит к искажению валентных углов при атоме серы в мезитиленсульфонатном лиганде по сравнению с тетраэдрическим (углы OSO и OSC изменяются в интервалах 110,13(9)°–115,55(11)° и 105,20(8)°–108,66(9)° соответственно). В мезитиленсульфонатном лиганде соединения 3 связи S–O неравноценны: связь S(1)–O(1) (1,4833(14) Å) длиннее двух других S(1)=O(2) (1,4438(16) Å) и S(1)=O(3) (1,4408(15) Å).
Заключение
Таким образом, искажение тригонально-бипирамидальной конфигурации молекул p -Tol4SbХ в сторону тетраэдрической и удлинение связи Sb - Х определяется электроотрицательностью группы Х. При этом следует также учитывать эффекты кристаллической упаковки и стерические затруднения в молекулах, вызванные объемом заместителя Х, однако малое число примеров в этом ряду не позволяло провести более точную корреляцию.
Список литературы Особенности строения производных тетра(пара-толил)сурьмы p-Tol4SbX (X = Br, Oc(O)Ph•PhH, OSO2C6H2Me3-2,4,6)
- Кочешков К.А., Сколдинов А.П., Землянский Н.Н. Методы элементоорганической химии. Сурьма, висмут. М.: Наука, 1976. 483 с.
- Шарутин В.В., Поддельский А.И., Шарутина О.К. // Коорд. химия. 2020. Т. 46, № 10. С. 579. DOI: 10.31857/S0132344X20100011.
- Акатова К.Н., Бочкова Р.И., Лебедев В.А. и др. // Докл. АН СССР. 1983. Т. 268, № 6. С. 1389.
- Шарутин В.В., Шарутина О.К., Пакусина А.П. и др. // Коорд. химия. 2005. Т. 31, № 2. С. 117. EDN: HRZYJR.
- Шарутин В.В., Шарутина О.К., Платонова Т.П. и др. // Коорд. химия. 2003. Т. 29, № 1. С. 13. EDN: OOFNKD.
- Шарутин В.В., Шарутина О.К., Панова Л.П. и др. // Журн. общ. химии. 1997. Т. 67, №. 9. С. 1531.
- Шарутин В.В., Пакусина А.П., Егорова И.В. и др. // Коорд. химия. 2003. Т. 29, № 5. С. 336. EDN: OOFOOD.
- Шарутин В.В., Шарутина О.К., Пакусина А.П. и др. // Журн. общ. химии. 1997. Т. 67, № 9. С. 1536. EDN: PFLFSA.
- Шарутин В.В., Шарутина О.К., Тарасова Т.А. и др. // Журн. общ. химии. 1999. Т. 69, № 12. С. 1979.
- Шарутин В.В., Шарутина О.К., Платонова Т.П. и др. // Журн. общ. химии. 2000. Т. 70, № 11. С. 1932. EDN: BAWNYU.
- Шарутин В.В., Шарутина О.К., Молокова О.В. и др. // Коорд. химия. 2002. Т. 28, № 8. С. 581–590. EDN: QEXAWC.
- Шарутин В.В., Шарутина О.К., Молокова О.В. и др. // Журн. общ. химии. 2001. Т. 71, № 8. С. 1317.
- Шарутин В.В., Шарутина О.К., Осипов П.Е. и др. // Журн. общ. химии. 2000. Т. 70, № 6. С. 931.
- Сопшина Д.М. // Вестник ЮУрГУ. Сер. «Химия». 2022. Т. 14, № 1. С. 50. DOI: 10.14529/chem220106.
- Ефремов А.Н., Шарутин В.В. // Вестник ЮУрГУ. Сер. «Химия». 2021. Т. 13, № 1. С. 47. DOI: 10.14529/chem210105.
- Шарутина О.К. // Вестник ЮУрГУ. Сер. «Химия». 2021. Т. 13, № 4. С. 63. DOI: 10.14529/chem210404.
- Сенчурин В.С., Орленко Е.Д. // Вестник ЮУрГУ. Сер. «Химия». 2019. Т. 11, № 2. С. 66. DOI: 10.14529/chem190207.
- Шарутин В.В., Шарутина О.К., Бондарь Е.А. и др. // Коорд. химия. 2002. Т. 28, № 5. С. 356. EDN: EOICYB.
- Шарутин В.В., Шарутина О.К., Ефремов А.Н. и др. // Журн. неорг. химии. 2017. Т. 62, № 10. С. 1330. DOI: 10.7868/S0044457X17100075.
- Шарутин В.В., Шарутина О.К. // Журн. неорган. химии. 2017. Т. 62, № 7. С. 925. DOI: 10.7868/S0044457X17070224.
- Шарутин В.В., Шарутина О.К., Сенчурин В.С. и др. // Журн. неорган. химии. 2016. Т. 61, № 8. С. 1017. DOI: 10.7868/S0044457X16080146.
- Шарутин В.В., Шарутина О.К., Ефремов А.Н. // Журн. структ. химии. 2020. Т. 61, № 9. С. 1490. DOI: 10.26902/JSC_id60682.
- Шарутин В.В., Шарутина О.К., Ефремов А.Н. // Журн. неорган. химии. 2020. Т. 65, № 1. С. 49. DOI: 10.31857/S0044457X20010158.
- Шарутин В.В., Шарутина О.К., Ефремов А.Н. и др. // Журн. неорган. химии. 2020. Т. 65, № 4. С. 482. DOI: 10.31857/S0044457X20040170.
- Шарутин В.В. // Вестник ЮУрГУ. Серия «Химия». 2023. Т. 15, № 1. С. 50. DOI: 10.14529/chem230105.
- Гиллеспи Р., Харгиттаи И. Модель отталкивания электронных пар валентной оболочки и строение молекул. М.: Мир. 1992. С.75.
- Лебедев В.А., Бочкова Р.И., Кузьмин Э.А. и др. // Докл. АН СССР. 1981. Т. 260, № 5. С. 1124.
- Бацанов С.С. // Журн. неорган. химии. 1991. Т. 36, Вып. 12. С. 3015.
- Ferguson G., Glidewell C., Lloyd D., Metcalfe S. // J. Chem. Soc. Perkin Trans. II. 1988. P. 731.
- Шарутин В.В., Шарутина О.К. // Журн. общ. химии. 2014. Т. 84, № 3. С. 457.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and processing software for the SMART system. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An integrated system for solving, refining and display-ing crystal structures from diffraction data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Cryst. 2009. Vol. 42. P. 339. DOI: 10.1107/S0021889808042726
- Шарутин В.В., Галиуллина Д.Р., Головин М.С. // Вестник ЮУрГУ. Серия «Химия». 2023. Т. 15, № 2. С. 66. DOI: 10.14529/chem230205
- Галиуллина Д.Р., Ефремов А.Н. // Вестник ЮУрГУ. Серия «Химия». 2022. Т. 14, № 3. С. 23. DOI: 10.14529/chem220303
- Шарутин В.В., Семенова А.Д. // Вестник ЮУрГУ. Серия «Химия». 2023. Т. 15, № 2. С. 44. DOI: 10.14529/chem230203
- Cambridge Crystallographic Database. Release 2022. Cambridge. deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk
- Шарутин В.В., Шарутина О.К., Сенчурин В.С. // Журн. неорган. химии. 2013. Т. 58. № 11. С. 1454. DOI: 10.7868/S0044457X13110196


