Особенности строения сольвата трис(2-метокси-5-хлорфенил)висмута с бензолом
Автор: Шарутин В.В., Шарутина О.К.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 4 т.16, 2024 года.
Бесплатный доступ
По данным рентгеноструктурного анализа, атомы висмута в двух молекулах трифенилвисмута (1) [C36H30Bi2, M 880,56; сингония триклинная, группа симметрии P1 ; параметры ячейки: a = 5,787(3), b = 14,203(7), c = 19,667(14) Å; a = 72,61(3), β = 81,68(4), g = 78,34(2) град.; V = 1504,5(16) Å3; размер кристалла 0,46×0,16×0,15 мм; интервалы индексов отражений -7 ≤ h ≤ 7, -18 ≤ k ≤ 18, -25 ≤ l ≤ 25; всего отражений 32105; независимых отражений 6933; Rint 0,0437; GOOF 1,093; R1 = 0,0290, wR2 = 0,0609; остаточная электронная плотность 0,48/-1,87 e/Å3] имеют искаженную тригональную координацию с неподеленной электронной парой на атоме металла. Длины связей Bi-C изменяются в интервале 2,246(5)-2,260(5) Å, углы CBiC 92,56(16)-95,24(15)°. В сольвате трис(2-метокси-5-хлорфенил)висмута с бензолом (2) [C24H21O3Cl3Bi, M 672,74; сингония моноклинная, группа симметрии P21/n; параметры ячейки: a = 8,920(5), b = 21,362(7), c = 13,649(5) Å; a = 90,00, β = 107,33(2), g = 90,00 град.; V = 2482,8(17) Å3; размер кристалла 0,5 × 0,11 × 0,09 мм; интервалы индексов отражений -11 ≤ h ≤ 11, -28 ≤ k ≤ 28, -17 ≤ l ≤ 17; всего отражений 40401; независимых отражений 5924; Rint 0,0334; GOOF 1,150; R1 = 0,0269, wR2 = 0,0623; остаточная электронная плотность 0,48/-2,02 e/Å3] атом висмута имеет аналогичную координацию. Длины связей Bi-C (2,253(3)-2,267(3) Å) длиннее связей в 1 из-за присутствия внутримолекулярных контактов Bi∙∙∙O (3,09, 3,08, 3,05 Å). Несмотря на увеличение объема 2-метокси-5-хлорфенильных лигандов, значения углов CBiC (90,26(12)-92,96(12)°) заметно меньше. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2333440 (1), 2044008 (2); deposit@ccdc.cam.ac.uk; https://www.ccdc.cam.ac.uk).
Сольват, трис(2-метокси-5-хлорфенил)висмут, бензол, строение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147246064
IDR: 147246064 | УДК: 546.865+547.47+548.312.5 | DOI: 10.14529/chem240403
Structural features of tris(2-metoxy-5-chlorophenyl)bismuth solvate with benzene
According to X-ray diffraction analysis, the bismuth atoms in two triphenylbismuth molecules (1) [C36H30Bi2, M 880.56; triclinic system, symmetry group P1 ; cell parameters: a = 5.787(3), b = 14.203(7), c = 19.667(14) Å; a = 72.61(3), β = 81.68(4), g = 78.34(2) deg.; V = 1504.5(16) Å3; crystal size 0.46×0.16×0.15 mm; reflection index intervals -7 ≤ h ≤ 7, -18 ≤ k ≤ 18, -25 ≤ l ≤ 25; total reflections 32105; independent reflections 6933; Rint 0,0437; GOOF 1.093; R1 = 0.0290, wR2 = 0.0609; residual electron density 0.48/-1.87 e/Å3] have a distorted trigonal coordination with a lone electron pair at the fourth vertex. The Bi-C bond lengths vary in the range 2.246(5)-2.260(5) Å, the CBiC angles are 92.56(16)-95.24(15)°. In the tris(2-methoxy-5-chlorophenyl)bismuth solvate with benzene (2) [C24H21O3Cl3Bi, M 672.74; monoclinic system, symmetry group P21/n; cell parameters: a = 8.920(5), b = 21.362(7), c = 13.649(5) Å; a = 90.00, β = 107.33(2), g = 90.00 deg.; V = 2482.8(17) Å3; crystal size 0.5×0.11×0.09 mm; reflection index intervals -11 ≤ h ≤ 11, -28 ≤ k ≤ 28, -17 ≤ l ≤ 17; total reflections 40401; independent reflections 5924; Rint 0.0334; GOOF 1.150; R1 = 0.0269, wR2 = 0.0623; residual electron density 0.48/-2.02 e/Å3] a distorted trigonal coordination with a lone electron pair at the fourth vertex is also observed. The Bi-C bond lengths (2.253(3)-2.267(3) Å) are significantly longer than similar bonds in 1 due to the presence of intramolecular Bi∙∙∙O contacts (3.09, 3.08, 3.05 Å). Despite the increase in the volume of bidentate 2-methoxy-5-chlorophenyl ligands, the values of the CBiC angles (90.26(12)-92.96(12)°) are noticeably lower, indicating less steric hindrance in 2. Complete tables of atomic coordinates, bond lengths, and bond angles were deposited in the Cambridge Structural Data Bank (No. 2333440 (1), 2044008 (2); deposit@ccdc.cam.ac.uk; https://www.ccdc.cam.ac.uk).
Текст научной статьи Особенности строения сольвата трис(2-метокси-5-хлорфенил)висмута с бензолом
Аннотация. По данным рентгеноструктурного анализа, атомы висмута в двух молекулах трифенилвисмута (1) [C36H30Bi2, M 880,56; сингония триклинная, группа симметрии P1; параметры ячейки: a = 5,787(3), b = 14,203(7), c = 19,667(14) A; a = 72,61(3), в = 81,68(4), Y = 78,34(2) град.; V = 1504,5(16) Å3; размер кристалла 0,46×0,16×0,15 мм; интервалы индексов отражений –7 ≤ h ≤ 7, –18 ≤ k ≤ 18, –25 ≤ l ≤ 25; всего отражений 32105; независимых отражений 6933; Rint 0,0437; GOOF 1,093; R1 = 0,0290, wR2 = 0,0609; остаточная электронная плотность 0,48/–1,87 e/Å3] имеют искаженную тригональную координацию с неподеленной электронной парой на атоме металла. Длины связей Bi-C изменяются в интервале 2,246(5)-2,260(5) A, углы CBiC 92,56(16)-95,24(15)°. В сольвате трис(2-метокси-5-хлорфенил)висмута с бензолом (2) [C24H21O3Cl3Bi, M 672,74; сингония моноклинная, группа симметрии P21/n; параметры ячейки: a = 8,920(5), b = 21,362(7), c = 13,649(5) Å; a = 90,00, в = 107,33(2), Y = 90,00 град.; V = 2482,8(17) A3; размер кристалла 0,5 х 0,11 х 0,09 мм; интервалы индексов отражений –11 ≤ h ≤ 11, –28 ≤ k ≤ 28, –17 ≤ l ≤ 17; всего отражений 40401; независимых отражений 5924; Rint 0,0334; GOOF 1,150; R1 = 0,0269, wR2 = 0,0623; остаточная электронная плотность 0,48/-2,02 e/A3] атом висмута имеет аналогичную координацию. Длины связей Bi-C (2,253(3)–2,267(3) Å) длиннее связей в 1 из-за присутствия внутримолекулярных контактов Bi∙∙∙O (3,09, 3,08, 3,05 Å). Несмотря на увеличение объема 2-метокси-5-хлорфенильных лигандов, значения углов CBiC (90,26(12)-92,96(12)°) заметно меньше. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2333440 (1), 2044008 (2); ; .
Наиболее изученными арильными производными трехвалентного висмута являются соединения с фенильными и, в меньшей степени, толильными лигандами. Наличие вакантных d -орбиталей у атомов висмута позволяет образовывать дополнительные координационные связи металла с лигандами, содержащими потенциальные координирующие центры, что приводит к увеличению координационного числа атома Bi. Сравнение структуры трифенилвисмута ( 1 ) с арильными соединениями висмута, содержащих потенциальные координирующие центры в арильных лигандах, может позволить выявить влияние природы заместителей при атоме висмута на геометрические параметры указанных молекул. С целью дальнейшего исследования арильных соединений висмута(III) [1, 2] были получены трис (5-бром-2-метоксифенил)висмут [3], трис (5-хлор-2-метоксифенил)висмут [4] и его сольват с бензолом ( 2 ), строение которого изучено в настоящей работе.
Экспериментальная часть
Синтез 1 и 2 осуществляли по методикам, приведенным в монографии [5] и работе [4] соответственно. Кристаллы 2 выделяли при перекристаллизации целевого продукта из смеси бензол-октан.
Рентгеноструктурный анализ (РСА) кристаллов соединения 1 и 2 проводили на автоматическом четырехкружном дифрактометре D8 QUEST фирмы Bruker (Mo K„-излучение, 1 = 0,71073 Å, графитовый монохроматор) при 293 К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены с помощью программ SMART и SAINT-Plus [6]. Все расчеты по определению и уточнению структур выполнены с помощью программ SHELXL/PC [7] и OLEX2 [8]. Структура определена прямым методом и уточнена методом наименьших квадратов в анизотропном приближении для неводородных атомов. Положение атомов водорода уточняли по модели наездника. Кристаллографические данные и результаты уточнения структуры приведены в табл. 1, геометрические характеристики координационного полиэдра атома висмута – в табл. 2. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2333440 (1), 2044008 (2); или .
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структур 1 и 2
|
Параметр |
1 |
2 |
|
Формула |
C 36 H 30 Bi 2 |
C 24 H 21 O 3 Cl 3 Bi |
|
М |
880,56 |
672,74 |
|
Сингония |
триклинная |
моноклинная |
|
Пр. группа |
P 1 |
P 2 1 / n |
Окончание табл. 1
|
Параметр |
1 |
2 |
|
a , Å |
5,787(3) |
8,920(5) |
|
b, Å |
14,203(7) |
21,362(7) |
|
c, Å |
19,667(14) |
13,649(5) |
|
а , град. |
72,61(3) |
90,00 |
|
β, град. |
81,68(4) |
107,33(2) |
|
Y , град. |
78,34(2) |
90,00 |
|
V , Å3 |
1504,5(16) |
2482,8(17) |
|
Z |
2 |
4 |
|
р (выч.), г/см 3 |
1,944 |
1,800 |
|
ц , мм-1 |
11,703 |
7,446 |
|
F (000) |
824,0 |
1292,0 |
|
Размер кристалла, мм |
0,46 × 0,16 × 0,15 |
0,5 × 0,11 × 0,09 |
|
Область сбора данных по 2 0 , град |
5,88–55,16 |
6,12–55,82 |
|
Интервалы индексов отражений |
–7 ≤ h ≤ 7, –18 ≤ k ≤ 18, –25 ≤ l ≤ 25 |
–11 ≤ h ≤ 11, –28 ≤ k ≤ 28, –17 ≤ l ≤ 17 |
|
Измерено отражений |
32105 |
40401 |
|
Независимых отражений |
6933 |
5924 |
|
R int |
0,0437 |
0,0334 |
|
Переменных уточнения |
343 |
283 |
|
GOOF |
1,093 |
1,150 |
|
R -факторы по F2 > 2 c (F2) |
R 1 = 0,0290, wR 2 = 0,0609 |
R 1 = 0,0269, wR 2 = 0,0623 |
|
R-факторы по всем отражениям |
R 1 = 0,0455, wR 2 = 0,0654 |
R 1 = 0,0330, wR 2 = 0,0654 |
|
Остаточная электронная плотность (max/min), e/A3 |
0,48/–1,87 |
0,48/–2,02 |
Таблица 2
|
Связь |
d , Å |
Угол |
го , град. |
|
1 |
|||
|
Bi(1)–С(1) |
2,246(5) |
С(1)Bi(1)С(11) |
92,67(16) |
|
Bi(1)–С(11) |
2,253(5) |
C(1)Bi(1)С(21) |
94,80(16) |
|
Bi(1)–C(21) |
2,254(4) |
C(11)Bi(1)С(21) |
95,03(15) |
|
Bi(2)–С(31) |
2,250(5) |
C(31)Bi(2)C(41) |
92,56(16) |
|
Bi(2)–С(41) |
2,260(5) |
C(51)Bi(2)C(31) |
94,68(16) |
|
Bi(2)–C(51) |
2,249(4) |
C(51)Bi(2)C(41) |
95,24(15) |
|
2 |
|||
|
Bi(1)–С(1) |
2,267(3) |
C(11)Bi(1)C(1) |
92,96(12) |
|
Bi(1)–С(11) |
2,261(3) |
C(21)Bi(1)C(1) |
90,26(12) |
|
Bi(1)–C(21) |
2,253(3) |
C(21)Bi(1)C(11) |
92,96(12) |
|
O(3)∙∙∙Bi(1) |
3,049(7) |
O(3)Bi(1)C(11) |
141,82(13) |
|
O(2)∙∙∙Bi(1) |
3,079(8) |
O(2)Bi(1)C(1) |
141,47(12) |
|
O(1)∙∙∙Bi(1) |
3,090(7) |
O(1)Bi(1)C(21) |
139,08(12) |
|
Преобразования симметрии: 1–x, –y, 1–z |
|||
Длины связей и валентные углы в молекулах соединений 1 и 2
Обсуждение результатов
Согласно теории отталкивания электронных пар валентных орбиталей (ОЭПВО) и правилам, разработанным Гиллеспи [9], четыре электронные пары, расположенные на валентных орбиталях центрального атома, должны располагаться в вершинах правильного тетраэдра. Искажение тетраэдрической конфигурации обусловлено наличием неподеленных электронных пар, которые занимают бóльший объем, чем связывающие электронные пары, что приводит к уменьшению углов между связями по сравнению с теоретическим значением 109 ° 28 ' . Другой причиной отклонения углов от этого значения является наличие внутримолекулярных невалентных взаимодействий центрального атома с лигандами.
Строение арильных соединений висмута общей формулы Ar 3 Bi, содержащих потенциальные координирующие центры в арильных лигандах, описано в работах [1 - 4, 10 - 16]. Сравнение геометрических характеристик указанных соединений с геометрическими параметрами простейших триарильных производных висмута [17 - 20] помогает выявить общие закономерности в строении триарильных соединений висмута. С этой целью в настоящей работе определено строение трифенилвисмута ( 1 ) и сольвата трис (2-метокси-5-хлорфенил)висмута с бензолом ( 2 ), полученного при перекристаллизации продукта из смеси бензол-октан. Отметим, что соединение 2 изоструктурно аналогичному соединению сурьмы [21, 22]. Строение координационного узла атома металла схоже с ранее описанными структурами триарилвисмута.
Молекулы 1 , 2 имеют конфигурацию искаженного тетраэдра с тремя атомами углерода трех арильных лигандов и неподеленной электронной парой в его вершинах (рис. 1, 2). Среднее значение длины связи Bi - C в 2 (2,260(3) Å, интервал 2,253(3) - 2,267(3) Å) несколько превышает таковое в 1 (2,252 Å, интервалы 2,246(5)–2,254(4) Å и 2,249(4) - 2,260(5) Å в двух кристаллографически независимых типах молекул), при этом сумма ковалентных радиусов атомов-партнеров связи равна 2,31 Å [23]. Удлинение связей в 2 объясняется, вероятно, присутствием внутримолекулярных контактов Bi∙∙∙O - СН 3 (3,09, 3,08, 3,05 Å). Отметим, что наблюдаемое расстояние значительно меньше суммы ван-дер-ваальсовых радиусов атомов висмута и кислорода, которая равна 3,9 Å [24]. Более заметное увеличение расстояний Bi - C имеет место в молекуле тримезитилвисмута (2,291 Å [20]), что обусловлено большим объемом лигандов.
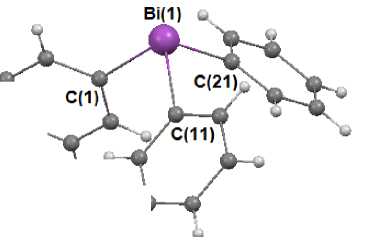
Рис. 1. Строение трифенилвисмута (1) (приведена молекула одного из двух кристаллографически независимых типов)
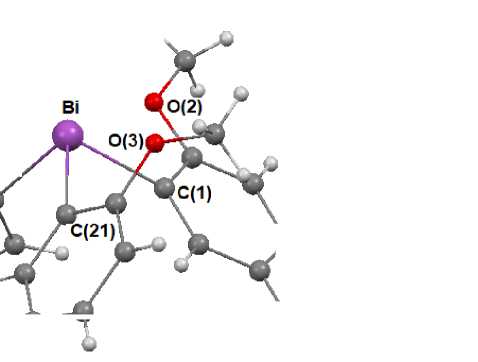
Рис. 2. Строение сольвата трис (2-метокси-5хлорфенил)висмута с бензолом (2) (сольватная молекула бензола не показана)
Несмотря на увеличение объема 2-метокси-5-хлорфенильных лигандов по сравнению с фенильными, значения углов CBiC (90,26(12)-92,96(12) ° ) в 2 несколько меньше, чем в 1 (92,67(16) - 95,03(15) и 92,56(16)-95,24(15) ° ), что может быть обусловлено направлением дополнительных взаимодействий Bi-"O - CH3 (рис. 3).
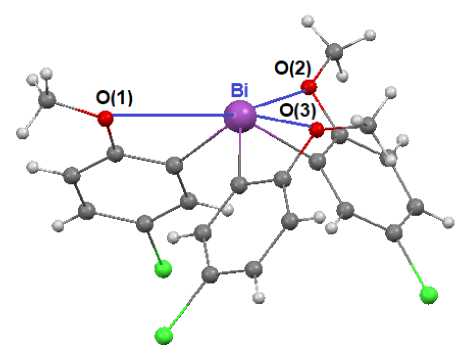
Рис. 3. Направление контактов Bi—O-CH3 в молекуле трис (2-метокси-5хлорфенил)висмута
Максимальное значение валентных углов (среднее 102,71 ° ) имеет место в молекуле тримезитилвисмута с большим объемом радикалов [20] и молекуле трис(2,6-диметоксифенил)висмута (среднее 99,41 ° ), имеющей метоксигруппы в орто- положениях [15]. Отметим, что в молекуле трис (5-бром-2-метоксифенил)висмута среднее значение валентных углов (92,05 ° [25]) совпадает с найденным в 2 .
В молекуле 2 двугранные углы между плоскостями арильных колец [C(1) - C(6)] - [C(11) - C(16)], [C(1) - C(6)] - [C(21) - C(26)], [C(11) - C(16)] - [C(21) - C(26)] составляют 79,63 ° , 75,80 ° , 89,21 ° , в молекуле 1 подобные углы принимают значения 65,95 ° , 69,53 ° , 72,48 ° .
В кристалле 2 молекулы трис (5-хлор-2-метоксифенил)висмута образуют цепи (короткие контакты Cl(1) --- C(11) 3,401 А и Cl(1) --- C(12) 3,371 А, расположенные вдоль кристаллографической оси b . В пространстве между цепями находятся молекулы сольватного бензола, кратчайшее расстояние Н(3) --- С(9) составляет 2,90 А (рис. 4).
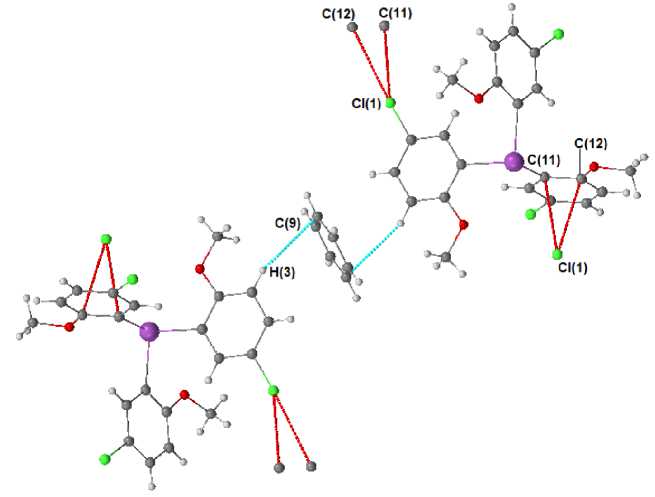
Рис. 4. Межмолекулярные контакты в кристалле 2
Молекулы сольватного бензола располагаются на середине четырех ребер и в центрах двух граней элементарной кристаллической ячейки (рис. 5).
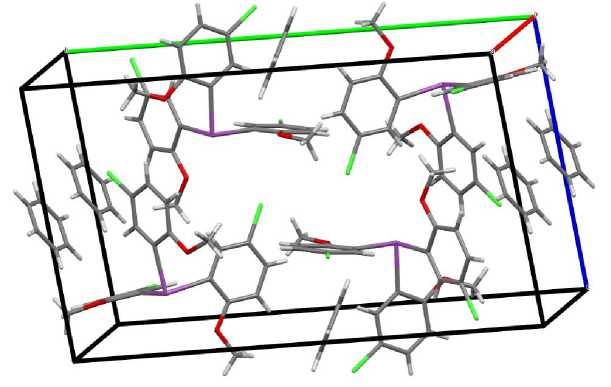
Рис. 5. Упаковка молекул 2 в элементарной кристаллической ячейке (проекция вдоль кристаллографической оси а )
Выводы
Таким образом, удлинение связей Bi - C в производных Ar3Bi по сравнению с Ph3Bi обусловлено, в первую очередь, увеличением объема арильного лиганда, а также наличием в лигандах групп, способных к формированию дополнительных взаимодействий с центральным атомом. Присутствие потенциальных координирующих центров в арильных лигандах, как правило, приводит к уменьшению валентных углов CBiC, в то время как большой объем арильного заместителя способствует увеличению углов.
Список литературы Особенности строения сольвата трис(2-метокси-5-хлорфенил)висмута с бензолом
- Kamepalli S., Carmalt C.J., Culp R.D. et al. // Inorg. Chem. 1996. V. 35, No. 21. P. 6179. DOI: 10.1021/ic960516c
- Шарутин В.В., Поддельский А.И., Шарутина О.К. // Коорд. химия. 2021. Т. 47, № 12. С. 719. DOI: 10.31857/S0132344X21120021
- Шарутин В.В., Сенчурин В.С., Шарутина О.К., Казаков М.В. // Бутлеровские сообщения. 2011. Т. 27, № 14. С. 43. EDN: NJRIHT
- Шарутин В.В., Шарутина О.К., Ефремов А.Н. // Коорд. химия. 2021. Т. 47, № 9. С. 568. EDN: RURAHX
- Кочешков К.А., Сколдинов А.П., Землянский Н.Н. Методы элементоорганической химии. Сурьма, висмут. М.: Наука, 1976. 483 с.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures from Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Cryst. 2009. V. 42. P. 339. DOI: 10.1107/S0021889808042726
- Гиллеспи Р., Харгиттаи И. Модель отталкивания электронных пар валентной оболочки и строение молекул. М.: Мир, 1992. 296 с.
- Шарутин В.В., Сенчурин В.С., Шарутина О.К., Чагарова О.В. // Журн. неорган. химии. 2012. Т. 57, № 8. С. 1149. EDN: OZLDRJ
- Plajer A.J., Colebatch A.L., Rizzuto F.J. et al. // Angew. Chem., Int. Ed. 2018. V. 57. P. 6648. DOI: 10.1002/anie.201802350
- Vranova I., Jambor R., Ruzicka A. et al. // Organometallics. 2015. V. 34. P. 534. DOI: 10.1021/om5011879
- Hebert M., Petiot P., Benoit E. et al. // J. Org. Chem. 2016. V. 81. P. 5401. DOI: 10.1021/acs.joc.6b00767
- Ohshita J., Yamaji K., Ooyama Y. et al. // Organometallics. 2019. V. 38. P. 1516. DOI: 10.1021/acs.organomet.8b00945
- Ogawa T., Ikegami T., Hikasa T. et al. // J. Chem. Soc., Perkin Trans.1. 1994. P.3479. DOI: 10.1039/P19940003479
- Шарутин В.В., Шарутина О.К., Сенчурин В.С. // Бутлеровские сообщения. 2013. Т. 34, № 4. С. 55. EDN: RAVMKT
- Jones P.G., Blaschette A., Henschel D., Henschel A. // Z. Kristallogr. Crystalline Materials. 1995. V. 210, No. 5. P. 377. DOI: 10.1524/zkri.1995.210.5.377
- Stavila V., Thurston J.H., Prieto-Centurión D., Whitmire K.H. // Organometallics. 2007. V. 26, No. 27. P. 6864. DOI: 10.1021/om7009667
- Шарутин В.В., Шарутина О.К. // Бутлеровские сообщения. 2013. Т. 36, № 10. С. 111. EDN: RURAHX
- Соболев A.H., Ромм И.П., Бельский В.К., Гурьянова E.H. // Kooрд. химия. 1980. Т. 6, № 6. С. 945.
- Шарутин В.В., Шарутина О.К. II Журн. общ. химии. 2020. Т. 90, № 10. С. 1577. DOI: 10.31857/S0044460X20100133
- Шарутин В.В., Шарутина О.К. II Журн. неорган. химии. 2021. Т. 66, № 3. С. 358. DOI: 10.31857/S0044457X21030156
- Cordero B., Gómez V., Platero-Prats A.E. et al. // Dalton Trans. 2008. V. 21. P. 2832. DOI: 10.1039/B801115J
- Mantina M., Chamberlin A.C., Valero R. et al. // J. Phys. Chem. A. 2009. V. 113, No. 19. P. 5806. DOI: 10.1021/jp8111556
- Sharutin V.V., Sharutina O.K., Ermakova V.A. et al. // Russ. J. Inorg. Chem. 2017. V. 62, No. 8. P. 1043. DOI: 10.1134/S0036023617080174


