Особенности влияния различных доз йодида калия на содержание тиреотропного гормона и гипофизарных гонадотропинов в гипофизе и крови у самок крыс
Автор: Басалаева Н.Л., Стрижиков В.К., Дружинина О.В., Сычугов Г.В., Кузнецова Ю.М.
Журнал: Человек. Спорт. Медицина @hsm-susu
Рубрика: Проблемы здравоохранения
Статья в выпуске: 28 (287), 2012 года.
Бесплатный доступ
Выявлено, что йодид калия в различных дозах оказывает влияние на тиреотропный гормон и гонадотропины у эутиреоидных самок крыс. Влияние оказывается как на уровень гипофизарных гормонов в крови, так и на их экспрессию в тканях гипофиза.
Йодид калия, тиреотропный гормон, гипофизарные гонадотропины
Короткий адрес: https://sciup.org/147153446
IDR: 147153446 | УДК: 636.02:612.018:619:615.31
Characteristic of different doses of potassium iodide effect on the content of thyroid hormone and gonadotropins in pituitary and blood of female rats
It was revealed, that potassium iodide at different doses has an effect on thyroid-stimulating hormone and gonadotropins of euthyroid female rats. They influence both the levels of pituitary hormones in the blood, and their expression in the tissues of the pituitary gland.
Текст научной статьи Особенности влияния различных доз йодида калия на содержание тиреотропного гормона и гипофизарных гонадотропинов в гипофизе и крови у самок крыс
Накопление йода при йодной нагрузке происходит и в гипофизе самок крыс, однако при проведении исследования была выявлена особенность аккумуляции йодидов в гипофизе: интенсивность накопления йода зависела от дозировки [8]. Была сделана попытка провести аналогию между дозой йодидов и содержанием йода в гипофизе и щитовидной железе самок крыс. Уровень йода в вышеназванных органах был определен с помощью количественного рентгеноспектрального микроанализа [6].
Накопление йода в гипофизе начиналось, когда доза KI соответствовала уровню йода в йод-пози-тивных точках гипофиза (ПИПП) (1 мкг/100 г массы животного (м. ж.)). Аккумуляция йода достигала максимума при дозе, 10-кратно превышающей уровень йода в ПИПП и в 1,5 раза превышающей средний уровень йода в щитовидной железе (8 мкг/100 г м. ж.). При дальнейшем повышении дозы KI (25 мкг/100 г м. ж.) внутриорганный йод в гипофизе не увеличивался и не отличался от контрольных показателей [8].
При исследовании гормонального статуса у самок крыс было выявлено, что введение вышеназванных доз йодида калия оказывает тормозящее влияние на функциональную активность гипофиза:
калия, тиреотропный гормон, гипофизарные гонадо- снижается уровень тиреотропного гармона (ТТГ) и растут показатели фолликулостимулирующего (ФСГ) и лютеинизирующего (ЛГ) гармонов, причем выраженность изменений не зависела от дозы KI [3, 4].
Встал вопрос: реагируют ли на введение йодидов морфологические структуры гипофиза – изменяется ли экспрессия гипофизарных гормонов в клеточных структурах гипофиза? Совпадают ли эти изменения с колебаниями уровней гормонов вкрови?
Целью настоящего исследования стало изучение влияния различных доз йодида калия на содержание ТТГ и гипофизарных гонадотропинов в крови и их экспрессию в тканях гипофиза у эутиреоидных самок крыс.
Материалы и методы. В эксперименте, выполненном на кафедре анатомии и гистологии Уральской академии ветеринарной медицины Минсельхоза России (зав. кафедрой – проф. В.К. Стри-жиков), были использованы 34 беспородные крысы-самки 6-месячного возраста со средней массой 250 ± 30 г. Животные содержались в виварии со стандартным световым режимом (12 ч света : 12 ч темноты (дневная фаза – с 7:00 до 19:00 летнего времени)) и получали стандартный корм и воду. Эксперимент проводился в соответствии с «Правилами проведения работ с использованием экспериментальных животных» (Приложение к Приказу Министерства здравоохранения СССР от 12.08.1977 г. № 775). Самки были взяты на опыт в фазы диэструса и метаэструса. 9 животных составили контрольную группу, 7 – первую. По 6 крыс вошло во 2, 3 и 4-ю группы. Анализ цикличности функционирования гонад проводился на основании определения гормонов репродуктивной сферы в сыворотке крови и исследования вагинальных мазков.
Крысам 1, 2, 3 и 4-й групп однократно через желудочный зонд вводили йодид калия из расчета соответственно 1 мкг/100 г, 4 мкг/100 г, 8 мкг/100 г и 25 мкг/100 г м. ж.
Все животные были подвержены эвтаназии под эфирным наркозом в период с 11 до 13 ч дневной фазы экспериментальных суток через 48 ч после введения йодида калия. Предварительно у животных проводился забор крови из яремной вены. У всех крыс были изъяты гипофизы.
В сыворотке крови животных определяли содержание ТТГ, ФСГ и ЛГ методом иммунофер-ментного анализа с использованием стандартных наборов тест-систем ОАО «Алкор-Био» (Санкт-Петербург, Россия). Исследования проводили на иммуноферментном автоматическом анализаторе (фотометр «BIO-RAD model 680 MR 12726», США) в иммунологической лаборатории НУЗ «Дорожная клиническая больница ОАО „РЖД“ на ст. Челябинск».
Морфологический раздел работы был выполнен в Областном патологоанатомическом бюро Министерства здравоохранения Челябинской области (начальник – канд. мед. наук Г.В. Сычугов) и на кафедре анатомии и гистологии Уральской академии ветеринарной медицины Минсельхоза России (зав. кафедрой – профессор В.К. Стрижиков).
Определение экспрессии ТТГ, ФСГ и ЛГ в тканях гипофиза осуществляли стрептавидин-биоти-новым методом с помощью моноклональных антител (МКАТ) к ТТГ (clone QB2/6, 1:200 v/v), ФСГ (clone INN-hFSH-60, 1:2500 v/v) и ЛГ (clone C93, 1:75 v/v) (Novocastra, Newcastle upon Tyne, UK).
Иммуногистохимическому исследованию были подвергнуты 34 гипофиза. Материал фиксировали 10%-ным нейтральным формалином в течение 24 ч, обезвоживали и подвергали парафиновой заливке. Срезы ткани толщиной 5 мкм помещали на покрытые силаном предметные стекла, депарафинировали, обезвоживали и отмывали в растворе трисбуфера при pH 7,2–7,4.
Для восстановления антигенной активности срезы обрабатывали 0,01 М – цитратным буфером с pH 6,0 в течение 30 мин в СВЧ печи при 95 °С. Затем срезы инкубировали с 0,3%-ным пероксидом водорода для блокирования эндогенной активности пероксидазы в течение 5 мин, обрабатывали нормальной 1%-ной лошадиной сывороткой в течение 30 мин при комнатной температуре для снижения неспецифического связывания и инкубировали со специфическими первичными антителами в рабочих разведениях при 40 °С в течение 12 ч.
Для визуализации антигенреактивных клеток использовали тест-систему «Novostain Universal Detection Kit» (Novocastra, Newcastle upon Tyne, UK ) . После окончания инкубации с первичными антителами препараты обрабатывали сначала вторичными биотинилированными, затем третичными стрептавидиновыми антителами. После проведения иммуногистохимической реакции срезы окрашивали гематоксилином и заключали в канадский бальзам.
Препараты исследовались с помощью светового микроскопа Axiostar plus (Carl Zeiss Jena, Germany), оснащенного 35-мм фотоаппаратом (Cannon Power Shot A520). При просмотре препаратов на светооптическом уровне антигенпозитив-ные клетки идентифицировали по их коричневому окрашиванию. Подсчет числа клеток с позитивным иммуногистохимическим окрашиванием проводился при увеличении × 400. Результаты реакции с антигенами оценивали с помощью автоматизированного количественного анализа с использованием программного обеспечения BioVision Professional 3.0 (West Medica Handels GmbH, Vienna, Austria) по проценту окрашенных клеток (positive area % (PA%)).
Комплексный статистический анализ был выполнен с использованием пакета прикладных программ Statistica for Windows 6.0. Достоверность различий между группами вычисляли с помощью t -критерия Стьюдента. Достоверными считали значения при p ≤ 0,05.
Результаты исследования и обсуждение. Результаты исследования гипофизарных гормонов приведены на рис. 1–3.
В контрольной группе показатели ТТГ соответствовали эутиреоидному состоянию животных,
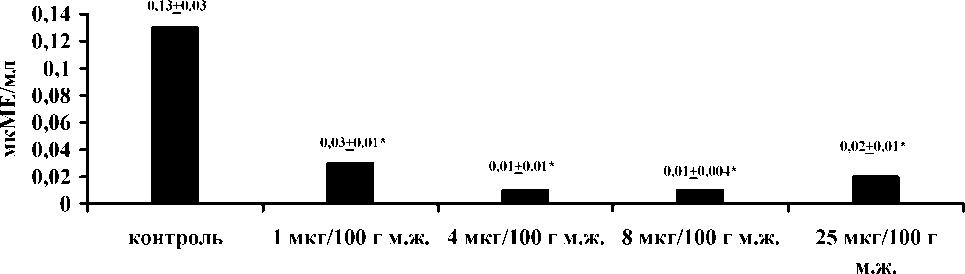
Рис. 1. Динамика изменений ТТГ в крови при различных дозах йодида калия. Здесь и на рис. 2, 3 знак * – p ≤ 0,05 – различия с контрольной группой
■ ттг
Басалаева Н.Л., Стрижиков В.К., Дружинина О.В. и др.
ФСГ и ЛГ – диэструсу и метаэструсу, не отличаясь от литературных данных [1, 2].
После введения йодида калия у всех крыс в крови наблюдалось снижение ТТГ в сочетании с подъемом ФСГ и ЛГ. Эти изменения были максимально выражены при дозах KI 4 и 8 мкг/100 г м. ж.
Динамика изменений экспрессии ТТГ, ФСГ и ЛГ в гипофизе несколько отличалась от динамики изменений параметров гормонов в крови. Так, достоверное снижение уровня экспрессии ТТГ (более чем в 2 раза) начиналось с дозы 4 мкг/100 г м. ж. При нарастании дозы йодида калия выраженность снижения экспрессии ТТГ уменьшалась.
Экспрессия ФСГ и ЛГ в тканях гипофиза максимально (более чем в 2 раза) возрастала также при дозе 4 мкг/100 г м. ж. При увеличении дозы KI сохранялось повышение экспрессии ФСГ, а показатели ЛГ достоверно не отличались от уровня контрольной группы.
При анализе результатов проведенного нами исследования можно предположить, что воздействие доз йодида калия, соответствующих содержанию йода в гипофизе и щитовидной железе, привело к снижению функции гипофиза у самок крыс – гипофизарному гипотиреозу и персистирующему эструсу.
Было установлено, что ФСГ и ЛГ реагировали на йодид калия сочетанно с изменениями ТТГ. Реакция происходила как на уровне показателей в крови, так и на уровне морфологических структур. Однако если изменения уровня гормонов в крови наблюдались при всех исследуемых дозах йодида калия, то одновременная вариабельность экспрес- сии гормонов в гипофизе – только при дозе KI, 5-кратно превышающей уровень йода в ПИПП (4 мкг/100 г м. ж.).
Уровень гипофизарных гормонов в крови изменялся начиная с дозы йодида калия, соответствующей уровню йода в йод-позитивных точках гипофиза (1 мкг/100 г м. ж.). Экспрессия гипофизарных гормонов в тканях гипофиза начинала варьировать при дозе KI, 5-кратно превышающей уровень йода в ПИПП (4 мкг/100 г м. ж.).
При дозе йодида, соответствующей среднему уровню йода в щитовидной железе (8 мкг/100 г м. ж.), достоверно менялась только экспрессия ТТГ.
При воздействии 25 мкг/100 г м. ж. наблюдался интересный феномен: изменилась экспрессия не только ТТГ, но и ФСГ, однако экспрессия ЛГ достоверно не отличалась от показателей контроля . Эти данные соответствовали полученным ранее результатам: при дозе 25 мкг/100 г м. ж. прогестерон, в отличие от эстрадиола, не отличался от уровня контрольной группы [8]. Можно предположить, что гипофизарные гонадотропины индивидуально чувствительны к различным дозам йода.
Ранее исследователями проводились попытки оценить экспрессию ТТГ в гипофизе при воздействии различных доз йодидов. Однако авторы применяли значительно большие дозы препаратов, и оценка экспрессии ТТГ была затруднена выраженными явлениями гипертрофии аденоцитов гипофиза [7].
Таким образом, при анализе результатов проведенного нами исследования выявлено, что калий-йодид в дозах, кратных содержанию йода в гипофизе и щитовидной железе, влиял на экспрессию
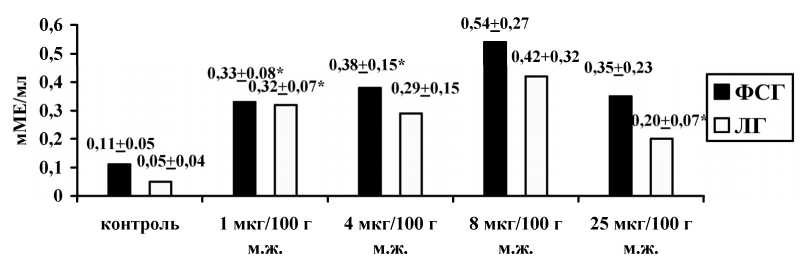
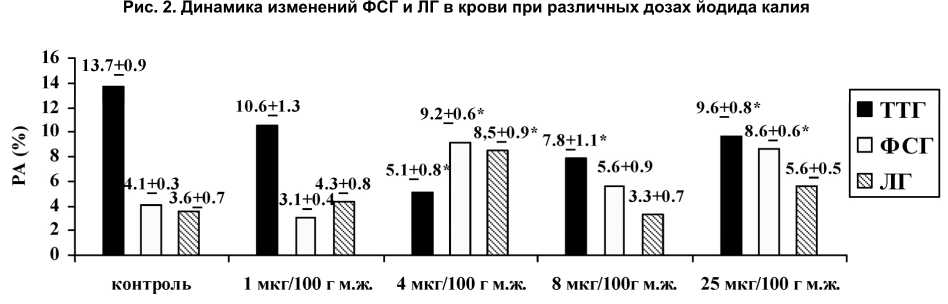
Рис. 3. Динамика изменений экспрессии ТТГ, ФСГ и ЛГ в гипофизе при различных дозах йодида калия
гипофизарных гормонов в клеточных структурах гипофиза, причем дозозависимо. Одновременно гуморальные и местные иммуногистохимические параметры ТТГ, ФСГ и ЛГ изменялись начиная с концентраций KI, 5-кратно превышающих уровень йода в йод-позитивных точках гипофиза.
Список литературы Особенности влияния различных доз йодида калия на содержание тиреотропного гормона и гипофизарных гонадотропинов в гипофизе и крови у самок крыс
- Анисимов, В.Н. Световой режим, мелатонин и риск развития рака/В.Н. Анисимов, И.А. Виноградова//Вопросы онкологии. -2006. -Т. 52, № 5. -С. 491-498.
- Козлов, В.Н. Интегральная оценка и коррекция тиреоидзависимых морфофункциональных нарушений у животных: автореф. дис.... д-ра биол. наук/В.Н. Козлов -М., 2008. -38 с.
- ОСОБЕННОСТИ ВЛИЯНИЯ ЙОДИДА КАЛИЯ НА ФУНКЦИОНАЛЬНЫЕ ПАРАМЕТРЫ ТИРЕОИДНОЙ И РЕПРОДУКТИВНОЙ СИСТЕМ САМОК-КРЫС/Н.Л. Басалаева, В.К. Стрижиков, Н.Т. Мифтахутдинов и др.//Вестник ЮУрГУ. «Образование, здравоохранение, физическая культура». -2010. -№ 19 (195). -С. 77-79.
- Особенности влияния различных доз йодида калия на функциональные параметры тиреоидной и репродуктивной системы самок крыс/Н.Л. Басалаева, В.К. Стрижиков, Н.Т. Мифтахутдинов и др.//Вестник ЮУрГУ. «Образование, здравоохранение, физическая культура». -2011. -Вып. 26. -№ 7 (224). -С. 72-74.
- Cann, S. Hypothesis: Dietary Iodine Intake in the Etiology of Cardiovascular Disease/S. Cann//J. Amer. Coll. Nutrition. -2006. -Vol. 25. -Р. 1-11.
- Expression of NIS in the thyroid and pituitary of female rats after a single dose of potassium iodide/N. Basalaeva, G. Sychugov, V. Strizhikov, E. Mikhailova//Endocr. Regul. -2011. -Vol. 45. -Р. 23-28.
- Histological Study on TSH Cells of Postnatal Rats with Iodine Excess/Li Jin-ru, Li-na Zheng, Hao Liu, Jin-bao Liu//Chinese Journal of Comparative Medicine. -2007. -Vol. 7. -Р. 390-392.
- Iodine concentration and signs of apoptosis in the thyroid and pituitary of female rats after different single doses of potassium iodide/N. Basalaeva, G. Sychugov, V. Strizhikov, E. Mikhailova//Endocr. Regul. -2011. -Vol. 45. -Р. 183-190.


