Остеохондральный трансплантат из преахиллярной зоны для замещения дефектов и повреждений суставных поверхностей голеностопного сустава
Автор: Кузнецов Василий Викторович, Пахомов Игорь Анатальевич, Зайдман Алла Михайловна, Корель Анастасия Викторовна, Корочкин Сергей Борисович, Репин А.В., Гуди С.М.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 4, 2017 года.
Бесплатный доступ
Введение. Лечение остеохондральных дефектов при поражениях блока таранной кости предполагает хирургическую санацию зоны некроза хряща и подлежащей кости, заполнение возникшего дефекта остеохондральным аутотрансплантатом. Использование МСКТ, МРТ позволяет выявить изменения в голеностопном суставе на начальной стадии, когда эффективна органосохраняющая операция. Цель. Гистологическое обоснование возможности использования ОА из преахиллярной зоны пяточной кости для лечения остеохондральных дефектов при поражениях блока таранной кости. Материалы и методы. Нами предложен новый способ получения остеохондрального аутотрансплантата для замещения остеохондральных дефектов при поражениях блока таранной кости различного генеза. Применение данного метода для хирургического лечения пациентов с остеохондральным дефектом при поражении блока таранной кости позволяет восстановить анатомическое строение голеностопного сустава. Для обоснования использования нового способа получения остеохондрального аутотрансплантата для замещения остеохондральных дефектов при поражениях блока таранной кости различного генеза морфологически были исследованы микропрепараты суставного хряща и подлежащей костной ткани блока таранной кости (кадаверный материал), зоны некроза таранной кости, хрящевой зоны преахиллярной зоны пяточной кости. Для сравнения с уже известными и описанными хрящевыми тканями были исследованы препараты хрящевой ткани латерального мыщелка бедренной кости. Результаты. Исследование препаратов хряща преахиллярной зоны пяточной кости выявило большое количество хондроцитов в межклеточном матриксе, наличие всех зон (поверхностная зона, промежуточная зона, глубокая зона), что свидетельствует о том, что данный хрящ структурно-функционально сохранен. Заключение. Полученные данные позволяют сделать предположение, что хрящ преахиллярной зоны может быть рассмотрен в качестве материала для аутотрансплантации.
Преахиллярная зона, костно-хрящевой дефект, таранная кость, блок, остеохондральные поражения, хондроциты,
Короткий адрес: https://sciup.org/142213584
IDR: 142213584 | УДК: 616.718.71-018.3-007.21-089.844 | DOI: 10.18019/1028-4427-2017-23-4-405-410
Osteochondral graft from the pre-Achilles area for repair of ankle joint articular surface defects and lesions
Introduction Management of osteochondral lesions of the talus trochlea involves surgical debridement of the necrotic cartilage and underlying bone, and then repair of the defect with an osteochondral autologous graft. The use of MSCT, MRI allows us to detect changes in the ankle joint at the initial stage, when the salvage operation is effective. Purpose Histological substantiation of the possibility to use osteochondral autologous grafts from the pre-Achilles area of the calcaneus for management of osteochondral defects in the damaged talus trochlea. Material and methods We substantiate a new technique for obtaining an osteochondral autologous graft to repair osteochondral defects of the talar trochlea resulting from various lesions by means of a morphological study of the following microslides: cartilage and underlying bone tissue of the talar trochlea (cadaver material), necrotic area of the talus, and the cartilage portion of the pre-Achilles area of the calcaneus. For comparison, preparations of the cartilage tissue from the lateral condyle of the femur were investigated. Results Investigations of the specimens of the pre-Achilles cartilage of the calcaneus revealed a large number of chondrocytes in the extracellular matrix, presence of its all cartilage zones (superficial, middle, and deep ones). This was a proof that this cartilage was preserved both structurally and functionally. Conclusion On the basis of the findings, it is assumed that pre-Achilles area cartilage can be considered as an autograft material.
Текст научной статьи Остеохондральный трансплантат из преахиллярной зоны для замещения дефектов и повреждений суставных поверхностей голеностопного сустава
Проблема лечения остеохондральных дефектов при поражениях блока таранной кости (далее – ОПБТК) актуальна в настоящее время [1, 2]. На сегодняшний день существует несколько направлений хирургического лечения ОПБТК, каждое из которых имеет свои достоинства и недостатки: проблема «болезненного донорского места», трудности сопоставления трансплантата с «принимающим ложем» на блоке таранной кости, наличие нескольких инвазивных этапов лечения по забору, культивации и имплантации донорского материала. Применение мозаичной остеохондропластики с использованием остеохондрального аутотрансплантата (далее – ОА) при лечении ОПБТК отвечает поставленным задачам
лечения, т.к. способствует радикальной санации очага некроза, ликвидации очага хронического воспаления в суставе, восстановлению биомеханики в голеностопном суставе. Это ведет к снижению инвалидизации пациентов, сокращению реабилитационного периода. В настоящее время в ФГБУ «ННИИТО им. Я.Л. Цивьяна» Минздрава России применяется запатентованный способ хирургического лечения ОПБТК с применением ОА из преахиллярной зоны пяточной кости [3].
Целью настоящей работы является гистологическое обоснование возможности использования ОА из преахиллярной зоны пяточной кости для лечения остеохондральных дефектов при поражениях блока
таранной кости. Для этого были проведены морфологические исследования микропрепаратов хрящевой и костной ткани преахиллярной зоны пяточной кости.
Для сравнения были исследованы препараты суставного хряща и прилежащая костная ткань латерального мыщелка бедренной кости.
МАТЕРИАЛЫ И МЕТОДЫ
С разрешения локального этического комитета ФГБУ «ННИИТО им. Я.Л. Цивьяна» Минздрава России (протокол заседания № 006/14 от 12 сентября 2014 года) исследованы микропрепараты суставного хряща и подлежащей костной ткани блока таранной кости (када-верный материал), хрящевой зоны преахиллярной зоны пяточной кости, хрящевая ткань латерального мыщелка бедренной кости и зоны некроза таранной кости. Возраст
пациентов составил от 30 до 60 лет, количество пациентов – 12 человек. Препараты фиксировались в 10 % растворе нейтрального формалина. После декальцинации в растворе ЭДТА и парафиновой проводки препараты окрашивались гематоксилином и эозином. Полученные препараты анализировали и оцифровывали с помощью микроскопа Axio Observer Z1 (Carl Zeiss, Германия) и программного обеспечения ZEN 2012 (blue edition).
РЕЗУЛЬТАТЫ
Хрящевая и подлежащая костная ткани блока таранной кости
В суставном хряще блока таранной кости нет четкого деления на зоны, присутствуют поверхностные уплощенной формы хондроциты (рис. 1); хондроциты верхней части промежуточной зоны, расположенные по 1–2 в лакуне, и хондроциты, расположенные колонками в более глубокой части промежуточной зоны, и гипертрофированные хондроциты глубокой зоны. В гомогенно эозинофильном плотном матриксе глубокой хрящевой зоны располагаются дистрофически измененные клетки, в основном безъядерные. Встречаются клетки с сохраненным ядром, но с кальцифицированной цитоплазмой. Хрящевая и костная ткани разделены четкой интенсивно базофильной линией, пограничной зоной суставного хряща, обеспечивающей сохранность хрящевой ткани (рис. 1, б). За базофильной линией располагается зона обызвествленного хряща, прилежащая к костной ткани. Костная ткань пластинчатого типа с неравномерными линиями склеивания, большим количеством остеобластов, что указывает на процесс перестройки.
Зона некроза блока таранной кости
На препарате видны фрагменты кости, некротизированный костный мозг. Тонкая костная ткань практически лишена клеток, в сохранившей архитектонику части кости встречаются безъядерные клетки. В некоторых местах видны некротические массы. Выявляются макрофаги. В зоне регенерации наблюдается фибротизация ткани, характеризующаяся фибриновыми волокнами и редкими веретеновидными клетками. Процесс некроза происходит при практически сохранной хрящевой ткани (местами некротические изменения проникают в хрящевую ткань). Выявляются все характерные для суставной хрящевой ткани зоны: поверхностная, промежуточная и глубокая. Межклеточный матрикс разволокнен, неравномерно окрашен. Базофильная линия местами разрушена, и процесс некроза внедряется в хрящевую ткань (рис. 2). Определяется отслоение хрящевой ткани от кости. Выявленные изменения в хрящевой ткани подтверждают необходимость проведения операции по замене этой хрящевой ткани трансплантатом из здоровой хрящевой ткани.
Преахиллярная зона пяточной кости (хрящевая и подлежащая костная ткани)
Хрящевая ткань представлена межклеточным матриксом с погруженными в него хондроцитами.
Выделены хрящевые зоны: поверхностная зона, промежуточная, глубокая зона, можно выявить базофильную линию и кальцифицированную зону, прилежащую к базофильной линии со стороны костной ткани. Матрикс поверхностной зоны интенсивно окрашен. Хондроциты этой зоны имеют уплощенную цитоплазму, округлое базофильное ядро. Клетки расположены параллельными рядами (рис. 3, а). Далее хондроциты располагаются по 1–2 в лакуне, матрикс окрашен неравномерно. Ближе к базофильной линии располагаются немногочисленные цепочки хондроцитов, образующих колонки или стопки. Матрикс этой зоны наиболее интенсивно окрашен по отношению к другим зонам. Базофильная линия четко очерчена (рис. 3, б). Местами в нее погружены хондроциты. Зона кальцифицированного хряща, прилежащая к базофильной линии, тонкая, местами отсутствует. Ко сть незрелая: много остеобластов и нечеткие линии склеивания. При исследовании препаратов в зависимости от возраста было установлено, что с увеличением возраста общее число хондроцитов снижается, нарастают дистрофические изменения, затрагивающие межклеточный матрикс.
Большое количество хондроцитов в межклеточном матриксе; наличие всех зон (поверхностная, промежуточная зона, глубокая зона), а также наличие хорошо выраженной базофильной линии и прилежащей кальцифицированной зоны свидетельствует о том, что данный хрящ структурно-функционально сохранен и может быть использован для трансплантации.
Суставной хрящ и прилежащая костная ткань латерального мыщелка бедренной кости
В суставном хряще латерального мыщелка бедренной ко сти представлены все зоны, характерные для ткани этого типа: тонкий поверхностный слой (интенсивно окрашенный барьер), промежуточная зона с изогенно расположенными группами клеток (рис. 4, а) и хаотично расположенными колонками хондроцитов, глубокая зона с гипертрофированными хондроцитами. Группы клеток располагаются в лакунах, границы которых сливаются между собой. Базофильная линия узкая, встречаются участки, где она граничит с костью, оссифицированная зона почти не выявляется. Визуализируется тонкий слой субхондральной кости (рис. 4, б).
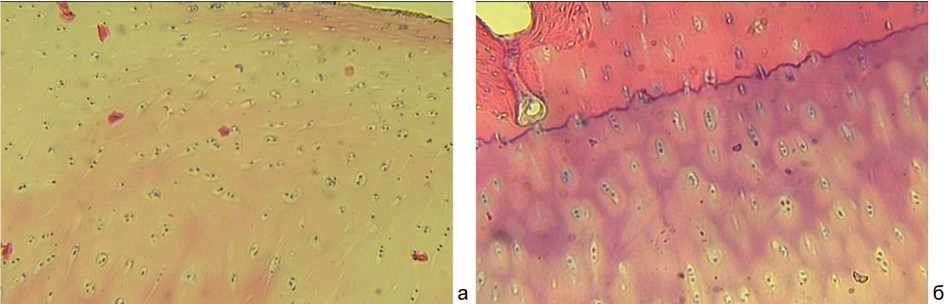
Рис. 1. Парафиновые срезы, окраска гематоксилин-эозин, увеличение 100: а – поверхностная зона суставного хряща таранной кости; б – базофильная линия и хондроциты промежуточной и глубокой зон суставного хряща таранной кости
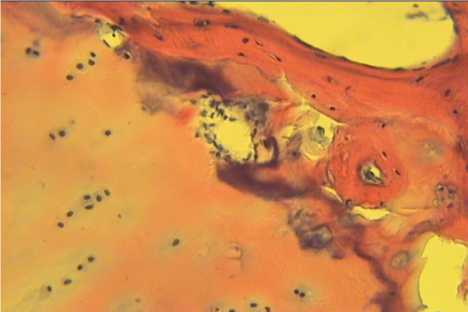
Рис. 2. Парафиновые срезы, окраска гематоксилин-эозин, увеличение 200. Зона некроза блока таранной кости. Разрушение базофильной линии, внедрение процесса некроза в хрящевую ткань
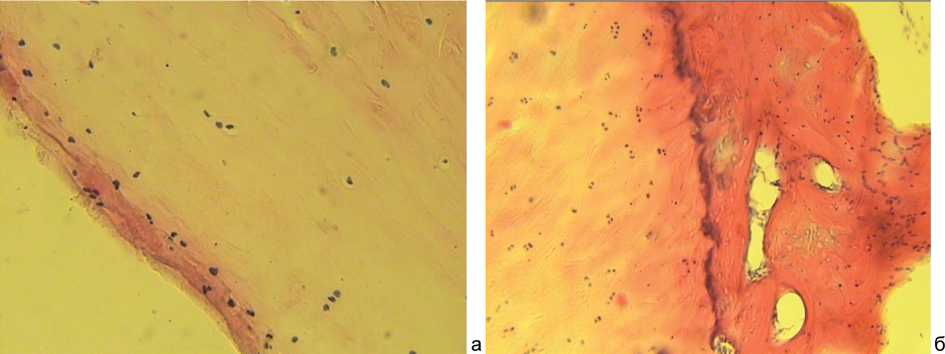
Рис. 3. Парафиновые срезы, окраска гематоксилин-эозин, увеличение 200: а – хондроциты поверхностной, промежуточной и глубокой зон преахиллярной зоны пяточной кости; б – базофильная линия и колонковые хондроциты преахиллярной зоны пяточной кости
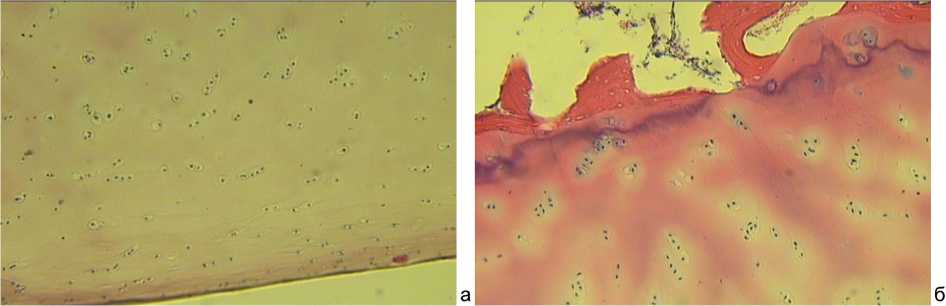
Рис. 4. Парафиновые срезы, окраска гематоксилин-эозин, увеличение 100: а – хондроциты поверхностной и промежуточной зон хрящевой ткани суставного хряща латерального мыщелка бедра; б – базофильная линия и хондроциты промежуточной и глубокой зон хрящевой ткани суставного хряща и латерального мыщелка бедра
ДИСКУССИЯ
В ходе работы выяснилось, что у большинства молодых трудоспособных пациентов причиной «крузалгии неясного генеза» являются остеохондральные поражения [4]. Предложенные разными авторами различные рентгенологические укладки не позволяют надежно диагностировать ОПБТК. Создается впечатление, что должно стать правилом назначение мультиспиральной компьютерной томографии (далее МСКТ) пациентам с «беспричинными» болями в голеностопном суставе. Действительно, МСКТ является методом выбора для диагностики ОПБТК [5]. С этим нельзя согласиться полностью, поскольку МСКТ не позволяет оценить распространенность сопутствующего отека губчатого костного вещества пораженного блока таранной кости. Дополнительную информацию позволяет получить МРТ. Необходимость данной информации дискуссионная, при этом есть работы, подчеркивающие необходимость предоперационного консервативного лечения в качестве предоперационной подготовки для профилактики отторжения трансплантата, прогрессии асептического некроза в зоне ОПБТК [6].
Также дискуссионными остаются хирургические подходы к лечению ОПБТК. Несмотря на сомнительную эффективность по причине нерадикальности, рядом авторов сообщается о продолжении использования мультилокальной остеоперфорации блока таранной кости как самостоятельного метода [7]. Безусловно, в качестве дополнительного метода мультилокальная остеоперфорация занимает свое заслуженное место в комплексе хирургического лечения [8]. Время подтвердило необходимость радикального вмешательства на кистовидном образовании, в связи с чем такие нерадикальные операции как субхондральное микрофрак-турирование, дебрайдмент, экскохлеация зоны некроза и т.д. перестали использоваться ортопедами как самостоятельные методы. Причиной этого является необходимость замещения возникающего дефекта. В этом направлении с конца ХХ века наблюдается значительный прогресс [9, 10, 11, 12]. Для замещения возникающего дефекта использовались имплантация аутологичных хондроцитов, костный аутотрансплантат, аллотрансплантат, аллогемиартропластика [13, 14].
На сегодняшний день перечисленные методы носят экзотический характер, так как проявляют свои положительные свойства, по-видимому, только в руках авторов. Методом выбора, судя по всему, до сих пор остается замещение дефекта остеохондральным аутотрансплантатом по методике Hangoody. Тем не менее, несомненные положительные характеристики методики Hangoody нивелируются ее неприемлемым недостатком, а именно – возникающее «болезненное» донорское место в области коленного сустава [15]. Различные авторы предлагали приемы, снижающие травматичность техники Hangoody, что не решило проблемы. Предлагаемая в нашей клинике методика позволяет решить данную проблему, но, безусловно, необ-
ходимо продолжение набора клинического материала для доказательства ее жизнеспособности. Внедряя ее, нам потребовались доказательства правомочности использования остеохондрального аутотрансплантата из преахиллярной зоны для клинических целей. Представленные в ряде исследований данные позволили утверждать, что этот трансплантат является остеохон-дральным и по своим морфологическим свойствам подходит для достижения целей лечения ОПБТК.
Безусловно, методы лечения ОПБТК будут развиваться дальше. Очень ценным будет снижение ин-вазивности хирургического вмешательства за счет внедрения мозаичной остеохондропластики малоинвазивными методами под контролем артроскомии, что позволит отказаться от необходимости остеотомии лодыжек. Но на сегодняшний день мозаичная остеохондропластика, по мнению многих специалистов, остается методом выбора.
В доступной отечественной и иностранной литературе отсутствуют данные по описанию и характеристике хрящевой ткани из преахиллярной зоны пяточной кости. Поэтому для выявления структурно-функциональных особенностей данной хрящевой ткани было проведено морфологическое исследование хрящевой ткани из пре-ахиллярной зоны пяточной кости. Также был проведен сравнительный анализ препаратов суставного хряща и подлежащей костной ткани блока таранной кости, хрящевой зоны преахиллярной зоны пяточной кости, хрящевой ткани латерального мыщелка бедра и зоны некроза таранной кости. Суставной хрящ блока таранной кости представлен равномерно гомогенным матриксом, в котором клетки располагаются диффузно. Обычно в суставном хряще различают три зоны: поверхностная, промежуточная и глубокая (базальная) [16]. Хондроциты различных зон имеют различия по объему, форме, способности к дифференцировке, плотности распределения в матриксе, ультраструктурной организации. Наименее дифференцированные клетки в суставном хряще расположены в верхней части промежуточной зоны, а наиболее дифференцированные в глубокой зоне [17]. Во всех исследованных хрящевых тканях присутствуют поверхностные уплощенной формы хондроциты, промежуточные, расположенные изогенно по 1–2 в лакуне, и отдельные группы клеток, расположенные колонками, глубинные гипертрофированные хондроциты. Также выявлено наличие разделяющей базофильной зоны, обеспечивающей сохранность хрящевой ткани, костной ткани с признаками перестройки. Полученные данные подтвердили возможность использования костно-хрящевого ОА из преахиллярной зоны пяточной кости. Исследование зоны некроза блока таранной кости выявило все признаки разрушения: фрагменты костной ткани, некротизированный костный мозг, местами некротические изменения проникают в хрящевую ткань. Все выявленные изменения свидетельствуют о необходимости замены пораженной ткани аутотрансплантатом.
ЗАКЛЮЧЕНИЕ
Исследование препаратов хряща преахиллярной зоны пяточной кости показало большое количество хондроцитов в гомогенно окрашенном межклеточном матриксе, наличие всех зон (поверхностная, промежуточ-
ная, глубокая), а также сохранной базофильной линии, что свидетельствует о том, что данный хрящ структурно-функционально сохранен и может быть рассмотрен в качестве материала для аутотрансплантации.
Список литературы Остеохондральный трансплантат из преахиллярной зоны для замещения дефектов и повреждений суставных поверхностей голеностопного сустава
- Пахомов И.А., Прохоренко В.М., Садовой М.А. Диагностика и хирургическое лечение асептического некроза таранной кости (болезнь Муше)//Вестник травматологии и ортопедии им. Н.Н. Приорова. 2008. №1. С.75-81.
- Ступина Т.А., Щудло М.М. Суставной хрящ: изменения при чрескостном дистракционном остеосинтезе, физиологическая и репаративная регенерация (обзор литературы)//Гений Ортопедии 2012. № 4. С.137-141.
- Способ забора остеохондрального аутотрансплантата: пат. 2562706 Российская Федерация. МПК A61B17/56./Пахомов И.А., Кузнецов В.В., Садовой М.А. № 2014142130; заявл. 17.10.2014; опубл. 2015.
- Autologous osteochondral grafting for talar cartilage defects/R.A. Al-Shaikh, L.B. Chou, J.A. Mann, S.M. Dreeben, D. Prieskorn//Foot Ankle Int. 2002. Vol.23,No 5. P. 381-389 DOI: 10.1177/107110070202300502
- Кузнецов В.В., Пахомов И.А. Остеохондральные поражения блока таранной кости, современные подходы к хирургическому лечению (обзор литературы)//Сибирский научный медицинский журнал. 2016. Т.36, №2. С.56-61
- Садовой М.А., Зедгенидзе И.В., Пахомов И.А. Повреждения суставного хряща при пронационно-абдукционном механизме травмы голеностопного сустава.//Травматология и ортопедия России. 2008. №3 (49). С.5-19.
- Ahmad J., Jones K. Comparison of osteochondral autografts and allografts for treatment of recurrent or large talar osteochondral lesions//Foot Ankle Int. 2016.Vol. 37, No 1. P. 40-50 DOI: 10.1177/1071100715603191
- Shapiro F., Koide S., Glimcher M.J. Cell origin and differentiation in the repair of full-thickness defects of articular cartilage//J. Bone Joint Surg. Am. 1993. Vol. 75, No 4. P. 532-553.
- Мозаичная аутологичная остеохондропластика в лечении локального асептического некроза блока таранной кости/Н.А. Корышков, А.П. Хапилин, А.С. Ходжиев, И.А. Воронкевич, Е.В. Огарёв, А.Б. Симонов, О.В. Зайцев//Травматология и ортопедия России. 2014. №4 (74). С. 90-98
- Berndt A.L., Harty M. Transchondral fractures (osteochondritis dissecans) of the talus//J. Bone Joint Surg. Am. 2004. Vol. 86-A, No 6. P. 1336.
- Woelfle J.V., Reichel H., Nelitz M. Indications and limitations of osteochondral autologous transplantation in osteochondritis dissecans of the talus//Knee Surg. Sports Traumatol. Arthrosc. 2013. Vol. 21, No 8. P. 1925-1930 DOI: 10.1007/s00167-013-2483-2
- Murawski C.D., Kennedy J.G. Operative treatment of osteochondral lesions of the talus//J. Bone Joint Surg. Am. 2013. Vol. 95, No 11. P. 1045-1054 DOI: 10.2106/JBJS.L.00773
- Сустав: морфология, клиника, диагностика, лечение/В.Н. Павлова, Г.Г. Павлов, Н.А. Шостак, Л.И. Слуцкий. М.: Медицинское Информационное Агентство (МИА), 2011. 552 с.
- Gautier E., Kolker D., Jakob R.P. Treatment of cartilage defects of the talus by autologous osteochondral grafts//J. Bone Joint Surg. Br. 2002. Vol. 84, No 2. P. 237-244.
- Knee donor-site morbidity after mosaicplasty -a systematic review/R. Andrade, S. Vasta, R. Pereira, H. Pereira, R. Papalia, M. Karahan, J.M. Oliveira, R.L. Reis, J. Espregueira-Mendes//J. Exp. Orthop. 2016. Vol. 3, No 1. P. 31 DOI: 10.1186/s40634-016-0066-0
- Ранняя диагностика аваскулярного некроза блока таранной кости/Т.М. Исакова, С.В. Гюльназарова, Г.В. Дьячкова, М.В. Налесник//Гений ортопедии. 2011. №3. C. 66-70.
- Алгоритм лучевой диагностики застарелых повреждений голеностопного сустава/Т.М. Исакова, С.В. Гюльназарова, Г.В. Дьячкова, М.В. Налесник//Вестник травматологии и ортопедии Урала. 2012. Т.5, № 1-2. С. 21-27.
- Knee-to-ankle mosaicplasty for the treatment of osteochondral lesions of the ankle joint/V. Valderrabano, A. Leumann, H. Rasch, T. Egelhof, B. Hintermann, G. Pagenstert//Am. J. Sports Med. 2009. Vol. 37, No Suppl. 1. P.105S-111S DOI: 10.1177/0363546509351481


