Остеосинтез при микрососудистых операциях в хирургии кисти
Автор: Фоминых А.А., Горячев А.Н., Быков В.В.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 2, 2003 года.
Бесплатный доступ
Представлен опыт лечения 84 пациентов, у которых при тяжелых травмах кисти, в том числе полных и неполных травматических отчленениях сегментов кисти, выполнены микрососудистые операции. Для остеосинтеза применялись спицы, спицы и аппараты внешней фиксации, конструкции с памятью формы. Наибольший процент восстановления функции кисти и ее сегментов достигнут при использовании аппаратов внешней фиксации и конструкций с памятью формы.
Кисть, отчленение, микрореплантация, конструкции с памятью формы, аппарат внешней фиксации
Короткий адрес: https://sciup.org/142120590
IDR: 142120590
Osteosynthesis for microvascular operations in hand surgery
The work deals with the experience of treatment of 84 patients subjected to microvascular operations for severe hand injuries including complete and partial traumatic avulsions of the hand segments. Wires, wires with external fixators, shape-memory implants were used for osteosynthesis. The greatest percentage of functional recovery of the hand and its segments was achieved when the external fixators and shape-memory implants were used.
Текст научной статьи Остеосинтез при микрососудистых операциях в хирургии кисти
Возможности микрохирургии в настоящее время значительно расширились, и органосохраняющие операции при травматических от-членениях пальцев и сегментов кисти хотя и не стали рутинными, тем не менее распространены достаточно широко [1, 2, 8, 9, 10]. Все это обусловливает повышение требований к функциональному результату лечения, где роль остеосинтеза занимает не последнее место [8, 9, 10]. В доступной нам литературе описанию методов фиксации кости при реваскуляризациях и микрореплантациях сегментов кисти уделено недостаточно внимания. В связи с этим отсутствует анализ функциональных результатов лечения в зависимости от вида выполненного остеосинтеза сегмента, а рекомендации по вопросам не только лечебной и хирургической тактики, но и экспертной оценки требуют доработки [3-6, 9, 10]. Поэтому поиск новых медико-технических решений, способных качественно улучшить функциональные результаты лечения больных с тяжелыми травмами кисти, актуален и в наши дни.
Целью данного исследования являлось изучение особенностей постреплантационного периода у больных с отчленениями пальцев и сегментов кисти в зависимости от вида проведенного остеосинтеза.
МАТЕРИАЛЫ И МЕТОДЫ
Нами изучены материалы лечения 84 пациентов межрегионального центра микрохирургии и хирургии кисти города Омска, в котором за период с 1992 по 2000 год были проведены органосохраняющие операции, в том числе - реваскуляризации и микрореплантации пальцев и сегментов кисти. Мужчин было 68, женщин – 16 (табл. 1). Большая часть пациентов (71,4%) находились в возрасте от 18 до 55 лет (табл. 2). Микрореплантации пальцев и их блоков были выполнены
48 больным при неполных травматических от-членениях, у 24 больных – при полных; 12 пациентам были выполнены артериальные и венозные реваскуляризации в сочетании с различными видами остеосинтеза, шва нервов, кожной пластики. Медикаментозная терапия была направлена на улучшение периферического кровообращения, профилактику гнойных осложнений, коррекцию нарушений гомеостаза. Как правило, назначали антикоагулянты прямого действия (гепарин
20000-30000 ЕД в сутки) в течение 7 дней с последующим переходом на антикоагулянты непрямого действия. Инфузионная терапия включала в себя внутривенное введение растворов низкомолекулярного декстрана (реополиглюкин -400/800 мл) и глюкозо-новокаиновой смеси (новокаин 0,25 % - 200,0; глюкоза 5 % - 500,0). С целью профилактики гнойно-септических осложнений проводилась медикаментозная терапия, включавшая антибиотики и сульфаниламиды. Для повязок использовался 10% раствор ди-мексида в новокаине с добавлением антибиотиков, к которым выделенная из раны культура сохранила чувствительность. Сроки наблюдения составили от 6 месяцев до 8 лет. Клиникофункциональные изменения в реплантированном сегменте и конечности в целом исследовались с помощью стандартных методов клинической и рентгенологической диагностики, реографии, электротермометрии, миографии. Оценка функционального результата проводилась на основании системы Американской ассоциации хирургов кисти.
Наиболее часто повреждения являлись следствием работы на строгальном станке и циркулярной пиле (57,1%). В большинстве своем это наиболее тяжелый вид травм. При этом, как правило, имеются не только костные, но и мяг-ко-тканные дефекты, повреждения сухожилий и нервов.
Основной контингент пострадавших составили лица наиболее трудоспособного возраста – 60 пациентов (71,4%).
У всех пациентов имелись нарушения кровообращения. И только у 10 они имели компенсированный характер. В результате проведенных лечебных мероприятий процент приживления составил 85,7%. Пиявки использовались эффективно для ликвидации венозного стаза у 56 пациентов. Курс лечебной физкультуры начинали с 3-5 дня после операции. До сращения поврежденных анатомических структур кисти проводилась дозированная пассивная разработка дви- жений в смежных суставах поврежденного сегмента. В это время проводили курс УВЧ - терапии, а при наличии отека - магнитотерапии. В первом периоде ЛФК проводилась строго индивидуально. Пассивные движения выполнялись медленно, до порога боли, чтобы избежать рефлекторного сокращения мышц и блокирования суставов. Стремились научить больного произвольному расслаблению и напряжению мышц предплечья и кисти. Продолжительность этого периода заканчивалась вместе с периодом иммобилизации. Второй период ЛФК начинали с проведения упражнений, направленных на восстановление функции поврежденного сегмента, исключавших боль. Кроме ЛФК проводили курс массажа, электростимуляции, электрофореза с лидазой, иглорефлексотерапии. Методы рефлексотерапии применялись со второго дня после операции, при этом использовались классическая акупунктура, аурикулоакупунктура, электроакупунктура.
Проведенный анализ материалов лечения больных с успешными микрососудистыми операциями на кисти позволил нам определить, что наибольший прирост функции получен при использовании аппаратов внешней фиксации и конструкций с памятью формы. Сроки консолидации в обеих группах (табл. 5) практически идентичны: 54,2±0,31 дня для аппаратов внешней фиксации и 52,3±0,12 дня – для конструкций с памятью формы. Существенно отличаются сроки реабилитации – они значительно меньше при использовании конструкций с памятью формы. Это может быть объяснено тем, что конструкции с памятью формы значительно легче переносятся пациентами, не требуют постоянных перевязок и, соответственно, имеют минимальный процент гнойно-септических осложнений. Длительность иммобилизации определялась сроками восстановления сухожилий. Кроме того, необходимо отметить, что в силу биоинертности конструкций из никелида практически не было необходимости в их извлечении.
Таблица 1.
Распределение лиц мужского и женского пола среди пострадавших, в зависимости от локализации патологии
|
Пол |
Повреждённый сегмент |
||||
|
пястье |
основная фаланга |
средняя фаланга |
дистальная фаланга |
итого |
|
|
Мужской |
17 |
22 |
19 |
10 |
68 |
|
Женский |
4 |
5 |
5 |
2 |
16 |
|
Итого |
21 |
27 |
24 |
12 |
84 |
Таблица 2.
Распределение больных в зависимости локализации патологии и возраста
|
Возраст (лет) |
Повреждённый сегмент |
||||
|
пястье |
основная фаланга |
средняя фаланга |
дистальная фаланга |
итого |
|
|
От 0 до 10 |
2 |
3 |
2 |
2 |
9 |
|
От 10 до 20 |
4 |
3 |
2 |
1 |
10 |
|
От 20 до 30 |
8 |
8 |
4 |
3 |
23 |
|
От 30 до 40 |
6 |
9 |
12 |
4 |
31 |
|
От 40 до 50 |
1 |
2 |
2 |
1 |
6 |
|
От 50 до 60 |
1 |
1 |
1 |
3 |
|
|
Старше 60 |
1 |
1 |
2 |
||
Итого 21 27 24 12 84
Таблица 3.
Механизм повреждения сегментов кисти
|
Механизм повреждения |
Повреждённый сегмент |
||||
|
пястье |
основная фаланга |
средняя фаланга |
дистальная фаланга |
итого |
|
|
Ранение острыми предметами (нож, топор, стекло) |
3 |
5 |
6 |
1 |
15 |
|
Резано-рваные ранения (электропила, станок) |
10 |
16 |
15 |
7 |
48 |
|
Сдавление, размозжение |
2 |
1 |
1 |
2 |
6 |
|
Сдавление, отрыв, скальпирование |
2 |
1 |
1 |
1 |
5 |
|
Комбинированный |
1 |
2 |
3 |
||
|
Огнестрельный |
3 |
2 |
1 |
1 |
7 |
|
Итого |
21 |
27 |
24 |
12 |
84 |
Таблица 4.
Степень приживления в зависимости от нарушения кровообращения у больных с открытыми сочетанными повреждениями кисти
|
Характер кровообращения |
Сегмент |
||||
|
пястье |
основная фаланга |
средняя фаланга |
дистальная фаланга |
итого |
|
|
Декомпенсированное |
5 |
7 |
8 |
6 |
26 |
|
Приживление |
4 |
6 |
6 |
5 |
21 |
|
Субкомпенсированное |
14 |
15 |
14 |
5 |
48 |
|
Приживление |
13 |
13 |
11 |
4 |
41 |
|
Компенсированное |
2 |
5 |
2 |
1 |
10 |
|
Приживление |
2 |
5 |
2 |
1 |
10 |
|
Итого сегментов |
21 |
27 |
24 |
12 |
84 |
Таблица 5.
Сроки лечения при остеосинтезе костей кисти
|
Способ остеосинтеза |
Число больных |
Сроки сращения (дни) |
Пребывание в стационаре (дни) |
Сроки реабилитации (дни) |
|
Спицы Киршнера |
27 |
62,1±0,32 |
24,3±0.28 |
181,5±0,22 |
|
Аппараты внешней фиксации |
28 |
54,2±0.31 |
19,2±0,17 |
162,4±0,14 |
|
Конструкции с памятью формы |
29 |
52,3±0,12 |
17,5±0,13 |
139,3±0,21 |
Реплантации дистальных фаланг всегда сопряжены с определенными техническими трудностями, так как диаметр пальцевых артерий на этом уровне редко превышает 0,5 мм, кроме того часто возникает необходимость в анкило-зировании поврежденного сустава. Однако, в силу анатомических особенностей кровеносного русла на уровне дистального межфалангового сустава, сохранение костного дефекта для выполнения сосудистого анастомоза может оказаться полезным. Анкилозирование сустава может быть успешно выполнено аппаратом внешней фиксации в послеоперационном периоде с постепенной компрессией, когда уже нет риска сосудистых осложнений. Это подтверждается следующим клиническим примером.
Клинический пример № 1. Больной Г. (и/б № 2549), 43 лет, доставлен в отделение микрохирургии через 2 часа после травмы (1 палец правой кисти поврежден диском циркулярной пилы). Локально: дистальная фаланга 1 пальца держится на узком кожном лоскуте до 3,5 мм, не включающим в себя никаких значимых анатомических структур. На рентгенограммах в прямой и боковой проекциях выявлен многооскольчатый перелом дистального метаэпифиза проксимальной фаланги (ДМЭПФ) с обширным дефектом кости. Однако рентгенологическая картина не соответствовала клинической, поэтому при ревизии раны обнаружен практически тотальный дефект (ДМЭПФ). Во время первичной хирургической обработки мелкие костные фрагменты удалены. Первичный артродез был опасен тем, что мог деформировать анастомоз во время компрессии. Поэтому при реплантации остеосинтез был выполнен спицей Киршнера с сохранением дефекта кости. Это позволило без дополнительной резекции поврежденных сосудов наложить анастомоз на артерию – 0,4 мм и восстановить две тыльные вены – 0,3-0,4 мм в диаметре, а также пальцевой нерв. В послеоперационном периоде внутривенно вводились низкомолекулярные декстраны, физраствор с тренталом, аспирин в порошках по 0,25 г 3 раза и обезболивающие. Рана зажила первично. На 18 сутки после реплантации с целью ранней реабилитации поврежденного сегмента и создания анкилоза межфалангового сустава выполнен остеосинтез 1пальца мини-фиксатором (авт. свид. 1789206). Длительность фиксации в аппарате 2 месяца. Через 4 месяца после травмы больной вернулся к труду в прежнем качестве.
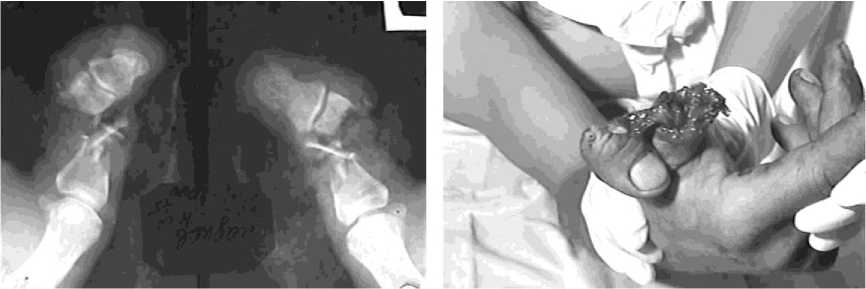
а
б
Рис. 1. Пример 1. Больной Г., 43 лет. Неполное травматическое отчленение ДФ 1 пальца правой кисти: а – фоторентгенограмма перед операцией, б – внешний вид пальца перед операцией.
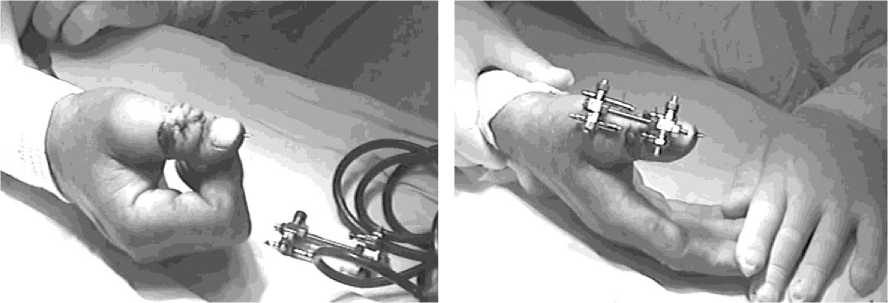
б
а
Рис. 2. Пример 1. Больной Г., 43 лет: а - внешний вид пальца через 7 дней после реплантации, б – после остеосинтеза минификсатором (авт. свид 1789206).
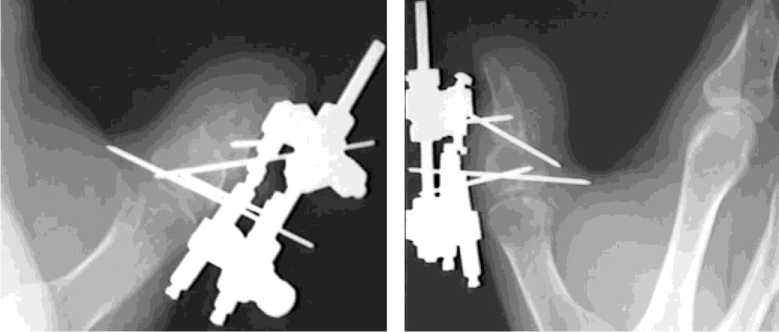
а б
Рис. 3. Пример 1. Больной Г., 43 лет: а, б – фоторентгенограммы в процессе лечения.
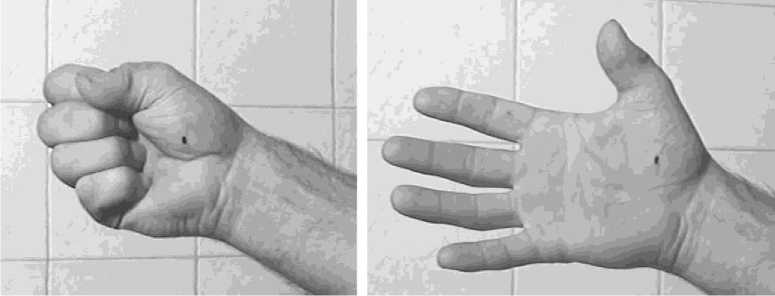
а б
Рис. 4. Пример 1. Больной Г., 43. лет: а, б – функциональный результат через 4 месяца.
Клинический пример № 2. Больной А. (и/б. 1876.), 33 лет, доставлен в отделение микрохирургии через 1,5 часа после травмы (1 палец левой кисти поврежден топором). Локально: дистальная фаланга (ДФ) и часть ПФ 1 пальца держатся на узком кожном ладонном лоскуте до 3мм. Палец прохладен, синюшен, оттока по венам нет. На рентгенограммах в прямой и боковой проекциях выявлен поперечный перелом ПФ 1 пальца. При выполнении первичной хирургической обработки удален суставной хрящ
ДФ и выполнен остеосинтез ПФ 1 пальца спицей Киршнера и стяжкой с памятью формы. Анастомозы пальцевой артерии и двух вен диаметром 0,4-0,5 мм выполнены нитью 10/0 Prolene Послеоперационное ведение стандартное. Заживление первичное. Спица удалена через 2 недели. Иммобилизация прекращена через 4 недели. Через 2 месяца после травмы рентгенологически подтверждено сращение, 1 палец опороспособен. Больной вернулся к труду в прежнем качестве.
б
а
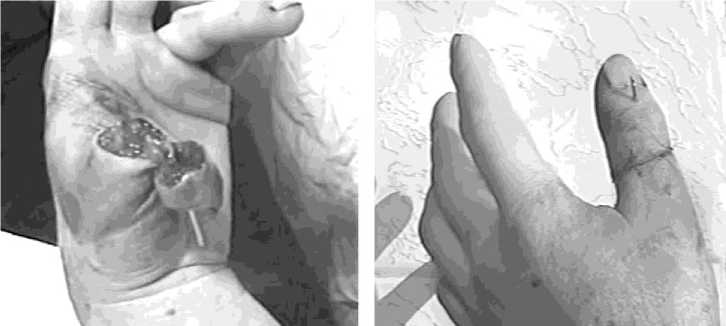
Рис. 5. Пример 2. Больной А., 33. лет. Неполное травматическое отчленение ДФ 1 пальца правой кисти: а - во время операции, б – через неделю после реплантации.
б
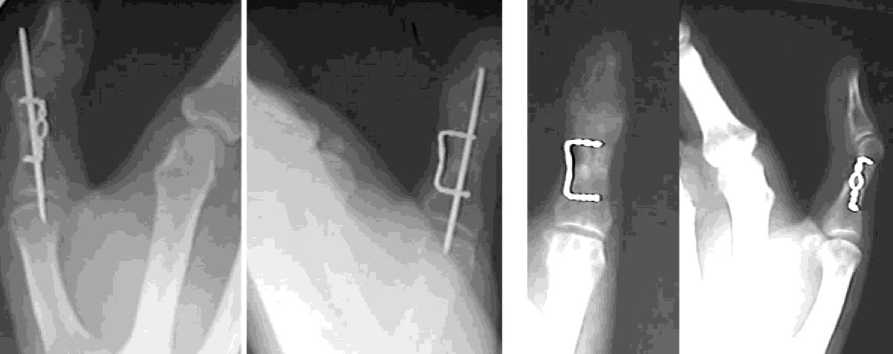
Рис. 6. Пример 2. Больной А., 33 лет. Фоторентгенограммы: а – через неделю после операции, б – через 2 месяца после реплантации.
а б
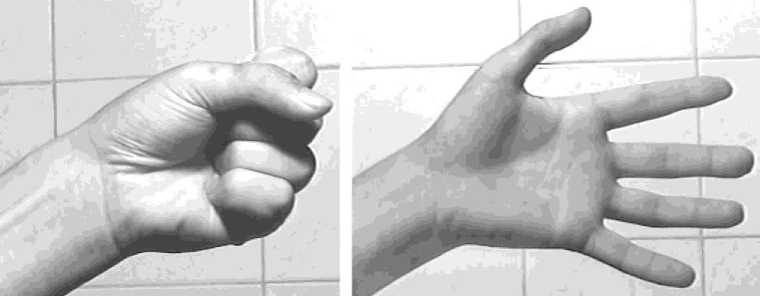
Рис. 7. Пример 2. Больной А., 33 лет. Функциональный результат через 5 месяцев после реплантации.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Остеосинтез при тяжелых травмах кисти, сопровождающихся нарушением кровообращения, должен быть по возможности простым и быстрым, так как, несмотря на успехи восстановительной хирургии сосудов верхней конечности, количество осложнений, связанных с тромбозом артериального и венозного русла, по-прежнему остается достаточно высоким. Если при макрореплантациях самым грозным осложнением может быть миоренальный синдром вследствие запоздалого включения конечности в кровоток и всасывания в кровь продуктов распада, то при микрореплантациях самыми частыми осложнениями являются артериальные и венозные тромбозы. Потеря времени при выполнении остеосинтеза может пагубно сказаться даже при реплантациях фаланг пальцев, поэтому до сих пор самым распространенным видом остеосинтеза в этой области был и остается остеосинтез спицами Киршнера. Достоинства и недостатки его очевидны. Из-за этого многие хирурги после заживления ран стремятся перейти на более функциональный способ – накостный или чре-скостный. Остеосинтез аппаратами внешней фиксации позволяет создать стабильность фрагментов при сохранении активной функции смежных суставов, способствуя улучшению функциональных результатов и укорочению сроков восстановительного лечения. Это, пожалуй, единственный способ, позволяющий одновременно решить две задачи – осуществить компрессию места перелома и компенсировать укорочение сегмента, которое часто сопровождает микрореплантации сегментов кисти. Однако, несмотря на все преимущества чрескостного остеосинтеза, он не удобен при первичной операции так, как ограничивает возможности хирургов при ревизии раны, пластики сосудов, нервов, сухожилий и закрытии мягкотканных дефектов. Поэтому использование внешней фиксации возможно не раньше второй, третьей недели после реплантации или реваскуляризации. Накостный остеосинтез при лечении тяжелых травм кисти дает хорошие функциональные результаты, но высокий риск гнойносептических осложнений сдерживает хирургов от широкого применения этого метода, особенно в острый период. Кроме того, для выполнения накостного остеосинтеза требуется значительно больше времени, чем при остеосинтезе спицами и аппаратами внешней фиксации, что также неблагоприятно сказывается на количестве осложнений, а для удаления пластины требуется повторная, не менее травматичная операция. Применение материалов и имплантатов с памятью формы последние 10 лет показало их высокую эффективность. Простота и надежность конструкций, оптимальные условия компрессии, которая длится весь период лечения, возможность быстро и прочно фиксировать поврежденный сегмент создали благоприятные условия для повсеместного распространения этого метода не только в травматологии и ортопедии, но и в сосудистой, абдоминальной, челюстно-лицевой хирургии, а также в микрохирургии и хирургии кисти. Высокая пластичность материалов из никелида титана, приближает его механические свойства к тканям человека. Химически сплав является биоинертным, что позволяет в ряде случаев отказаться от извлечения конструкций. К недостаткам конструкций с памятью формы следует отнести необходимость в наличии хладагентов (хлорэтил или жидкий азот), отсутствие четких критериев деформации конструкции, малая управляемость процессом компрессии. Ряд недостатков легко устраним по мере накопления опыта работы.
ЗАКЛЮЧЕНИЕ
Применение аппаратов внешней фиксации при микрососудистых операциях в хирургии кисти наиболее целесообразно для компенсации длины поврежденного сегмента или его дозированного укорочения.
Конструкции с памятью формы при микро- реплантациях и реваскуляризациях кисти и ее сегментов значительно упрощают оперативное вмешательство, обеспечивают компрессию на весь период лечения, легко переносятся пациентами, значительно сокращают сроки реабилитации.


