Острая дисфункция эндотелия у больных с хирургической инфекцией мочевыводящих путей
Автор: Рахметов Н.Р., Телеуов М.К., Исаханов Е.Е.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Опыт регионов
Статья в выпуске: 1-2 т.23, 2008 года.
Бесплатный доступ
Исследованы две группы больных в количестве 150 человек. В исследуемой группе пациентов в количестве 50 человек дополнительно применялся L-аргинин. Данные, полученные в результате исследования, могут быть использованы для прогнозирования течения послеоперационного периода, возможности развития хирургической инфекции и ее ранней диагностики. Метод профилактики и лечения хирургической инфекции, основанный на профилактике дисфункции эндотелия путем применения L-аргинина, может использоваться в клинических условиях для лечения хирургических больных в послеоперационном периоде, в том числе оперированных на органах мочевыделительной системы
L-аргинин, оксид азота, хирургическая инфекция, эндотелиальная дисфункция
Короткий адрес: https://sciup.org/14918841
IDR: 14918841 | УДК: 616.62-002-006.55-089.85+546.174
Acute endothelial dysfunction in patients having surgical infection of urinary tracts
The results which were received in the study can be used for prognosis of postoperative period's flow, possibility of development of surgical infection and its early diagnosis. approved method of prevention and treatment of surgical infection based on correction of vascular endothelium function by usinga l-arginine can be used in clinical conditions to treat surgical patients in the postoperative period including patients who underwent operations on urinary tracts.
Текст научной статьи Острая дисфункция эндотелия у больных с хирургической инфекцией мочевыводящих путей
В общей структуре хирургической заболеваемости одно из ведущих мест занимают гнойновоспалительные процессы, которые наблюдаются у 35-45% хирургических больных. Инфекция является причиной и многочисленных послеоперационных осложнений – от нагноения послеоперационной раны до развития сепсиса, который часто приводит к смерти больного.
В последнее десятилетие значительно изменились представления о патогенезе сепсиса [1, 2, 3, 4]. По современным данным, сепсис и его осложнения являются прогрессирующими стадиями одного и того же патологического процесса – синдрома системной воспалительной реакции (ССВР) или синдрома системного воспалительного ответа (ССВО).
В настоящее время считается, что в основе патогенеза острой хирургической патологии лежит недостаточность гемоперфузии тканей в системе микроциркуляции, приводящая к тяжелым нарушениям в клеточных структурах, зачастую приобретающих необратимый характер [5]. Нарушение гемоперфузии тканей и, как следствие, тканевая гипоксия обусловлены рядом составляющих факторов: вазоспазмом, нарушением проницаемости сосудистой стенки, изменением вязкости крови, в регуляции которых основная роль принадлежит сосудистому эндотелию. Следовательно, основное значение в патогенезе нарушений микроциркуляции и тканевых повреждений при острой хирургической патологии принадлежит нарушениям функций сосудистого эндотелия. В число перспективных методов коррекции эндотелиальной дисфункции входит применение L-аргинина.
В 1998 г. группа российских исследователей впервые обнаружила выраженный ранозаживляющий эффект при обработке гнойных ран охлажденным газовым потоком, содержащим оксид азота – NO, который генерировался воздушно-плазменным аппаратом Плазон, созданным в МГТУ им. Баумана [6]. В результате этих исследований в медицине и, в частности, в хирургии начало развиваться новое направление – NO-терапия ран и воспалительных процессов.
В случае достижения задачи адекватной защиты эндотелия в послеоперационном периоде можно одновременно решить проблемы, связанные с нормализацией гемостаза, предупреждением нарушений гемодинамики, эффективной антибактериальной защитой пациента. Одной из важнейших функций сосудистого эндотелия, по которой также можно судить о его функциональном состоянии, является синтезирование эндотелиоцитами оксида азота – NO.
Оксид азота в организме синтезируется с помощью фермента NO-синтазы (NOS), которая осуществляет присоединение молекулярного кислорода к конечному атому азота в гуанидиновой группе L-аргинина, конечными продуктами этой реакции являются оксид азота и цитруллин.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
В работу включались больные, оперированные по поводу мочекаменной болезни (МКБ) и доброкачественной гиперплазии предстательной железы (ДГПЖ). Всего в рамках работы обследованы 150 человек, из них 52 пациента (34,7%) – с МКБ и 98 (65,3%) – с ДГПЖ. Распределение больных в зависимости от пола и возраста представлено в таблице 1.
Из 98 больных ДГПЖ операция аденомэктомия была произведена в два этапа в 47 (47,9%) случаях, одномоментно в 44 (45%) случаях и в 7 (7,1%) случаях больным была произведена трансуретральная резекция предстательной железы (ТУР ПЖ). При МКБ уретеролитотомия проведена у 31 больного, не-фролитостомия – у 8, пиелолитотомия – у 13.
Из исследования были исключены больные с тяжелой сопутствующей соматической патологией: бронхиальной астмой, ишемической болезнью сердца, с сердечной недостаточностью НIIб, с артериальной гипертонией II и III степеней, с дыхательной недостаточностью ДНII-III, декомпенсированным и субкомпен-сированным сахарным диабетом, злокачественными новообразованиями.
Таблица 1
Распределение больных в зависимости от пола и возраста
|
Возраст (в годах) |
Мужчины |
Женщины |
Всего |
|||
|
абс. ч. |
% |
абс. ч. |
% |
абс. ч. |
% |
|
|
До 20 |
1 |
0,8 |
1 |
4,5 |
2 |
1,3 |
|
20-29 |
2 |
1,6 |
3 |
13,6 |
5 |
3,3 |
|
30-39 |
5 |
3,9 |
4 |
18,2 |
9 |
6 |
|
40-49 |
5 |
3,9 |
4 |
18,2 |
9 |
6 |
|
50-59 |
11 |
8,6 |
6 |
27,3 |
17 |
11,4 |
|
60 и старше |
104 |
81,2 |
4 |
18,2 |
108 |
72 |
|
Итого |
128 |
100,0 |
22 |
100,0 |
150 |
100,0 |
Все больные были разделены на 2 группы: А – группу сравнения в количестве 100 пациентов и В – основную в количестве 50 пациентов. Также была обследована контрольная группа из 35 здоровых лиц.
Все больные в послеоперационном периоде получали стандартную терапию, включающую в себя базовую инфузионно-трансфузионную терапию, антибактериальную терапию по стандартной схеме: цефалоспорин I генерации + антианаэробный препарат, анальгетики, гемостатики, симптоматическую терапию.
В основной группе (В) все больные получали дополнительно в качестве источника L-аргинина, донатора оксида азота (NO), препарат «инфезол 40» (Berlin Chemie, Германия) по 500 мл интраоперационно и 1 раз в сутки в течение 2 суток после операции подряд (всего 3 инфузии).
Дополнительно производилось: определение метаболитов оксида азота (по методике J.A. Navarro, J.A. Molina, 1993 в модификации В.Б. Карпюк и соавт., 1998); исследование показателей эндотелийзависимой вазодилятации (измерения проводили линейным методом, предложенным D. Celermajer и соавт., 1992; в модификации Д.А. Затейщикова, 1998); определение показателей сосудисто-тромбоцитарного звена гемостаза (фактора Виллебранда по З.С. Баркаган, 1999, АДФ-зависимой агрегации тромбоцитов по Born, 1995; в модификации Е.А. Захарьи – М.В. Кинах, 1998). Дополнительные исследования проводились до операции и далее на 1-е, 3-и, 6-е сутки – после операции в условиях клинической лаборатории Почечного центра г. Семипалатинска и Централизованной научноисследовательской лаборатории СГМА.
Для определения статистической значимости различий между двумя показателями проверялись гипотезы о равенстве генеральных средних или относительных частот (интенсивных показателей) для независимых, несвязанных выборок по t-критерию Стьюдента. Критический уровень значимости принимался равным p=0,05.
Мерой разброса относительной частоты (интенсивного показателя) служила эмпирическая оценка ее стандартного отклонения, вычисляемая по формуле:
P ⋅ q mР = ,
n где Р – интенсивный показатель, полученный в результате исследования;
n – число всех наблюдений;
q=1–P (q=100–P, если P выражается в %, и q=1000–P, если P выражается в ‰).
После статистической обработки в программе Statistica 6.0 все полученные данные с помощью пакета прикладных программ Microsoft Office переводились в таблицы и графики.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
В результате проведенных исследований были получены данные о повышенном содержании метаболита 72
NO – нитрита (NO2) в крови больных с окклюзией мочевых путей. В таблице 2 отражены данные о содержании нитрита в крови у больных общей группы до и после операции.
Особый интерес представляли данные о продукции NO у больных в послеоперационном периоде и исходя из цели и задач исследования – особенностей его динамики в зависимости от наличия и течения хирургической инфекции.
После операции уровень содержания в крови метаболита NO в среднем по обеим группам обследованных возрос относительно исходного. Степень превышения над показателем практически здоровых
Таблица 2
Сравнительная характеристика содержания в крови метаболита NO (мкг/мл) у здоровых лиц и обследованных больных (общая группа)
|
Группа |
До операции |
После операции |
|
Здоровые лица, n=35 |
0,49±0,03 |
0,49±0,03 |
|
Больные МКБ, n=52 |
1,09±0,05* |
1,28±0,07* |
|
Больные ДГПЖ, n=98 |
1,02±0,06* |
1,14±0,06 |
Примечание: * – различия с показателями группы здоровых лиц статистически значимы, р<0,01
Таблица 3
Разделение больных по степени тяжести хирургической инфекции
В обеих группах имелись осложнения, связанные с развитием хирургической инфекции, при этом разделение по степени тяжести осуществлялось по виду сопутствующей нозологии и клиническим проявлениям. Разделение больных по степени тяжести хирургической инфекции представлено в таблице 3.
У прооперированных пациентов без хирургической инфекции фактически не отмечалось динамики уровня метаболита NO в крови после операции (в сроки развития осложнений в сравниваемой группе), хотя статистически значимые различия с контрольной группой сохранялись. На фоне развития хирургической инфекции в среднем по подгруппе отмечался дополнительный рост показателя до 1,39±0,07 мкг/мл, и различия с контрольной группой достигли 2,84 раза, а между подгруппами – 1,32 раза (p<0,05).
Данные, характеризующие зависимость содержания метаболита NO в крови у больных с различной степенью тяжести хирургической инфекции, представлены в таблице 4.
Таблица 4
Содержание метаболита NO у больных с различной степенью тяжести хирургической инфекции
|
Группа |
Содержание NO2, мкг/мл |
|
Здоровые лица, n=35 |
0,49±0,03 |
|
Больные МКБ и ДГПЖ с развитием хирургической инфекции (контрольная группа), n=56 |
1,39±0,07* |
|
Больные МКБ и ДГПЖ с легкой хирургической инфекцией, n=46 |
1,31±0,05* |
|
Больные МКБ и ДГПЖ со среднетяжелой хирургической инфекцией, n=10 |
1,78±0,09* # |
Примечания: * – различия с показателями группы здоровых лиц статистически значимы, р<0,01; # – различия между подгруппами статистически значимы, р<0,01.
Нами был проведен анализ частоты развития легкой и среднетяжелой хирургической инфекции в зависимости от содержания метаболита NO в крови. При этом граничным значением показателя было установлено 1,3 мкг/мл как уровень, статистически значимо повышенный относительно зарегистрированного у здоровых лиц.
В результате такового было выявлено, что у пациентов, имевших после операции уровень содержания метаболита NO ниже 1,3 мкг/мл, частота развития легкой хирургической инфекции составила 33,3%, среднетяжелой – 5,1%, а в группе больных, имевших содержание нитрита в крови выше 1,3 мкг/мл, – 54,1% и 13,1% соответственно. Таким образом, относительный риск развития хирургической инфекции при повышенном содержании метаболита NO в крови составил 1,74, в том числе среднетяжелой – 2,57 (p<0,05).
После операции в общей группе на фоне повышения содержания метаболитов NO, отражающего его гиперпродукцию сосудистым эндотелием, отмечалось парадоксальное статистически значимое снижение показателя эндотелийзависимой вазодилятации (табл. 5).
Таблица 5
Сравнительная характеристика показателя эндотелийзависимой вазодилятации в пробе с реактивной гиперемией у здоровых лиц и больных после операции
|
Группа |
ЭЗВД, % |
|
Здоровые лица, n=35 |
26,2±0,9 |
|
Больные МКБ, n=36 |
12,6±2,7* |
|
Больные ДГПЖ, n=64 |
11,8±2,2* |
Примечание: * – различия с показателями группы здоровых лиц статистически значимы, р<0,01.
Как и по содержанию метаболита NO в крови, отчетливые различия прослеживались в отношении показателя ЭЗВД в зависимости от наличия и тяжести хирургической инфекции (табл. 6).
Одним из возможных механизмов реализации неблагоприятного влияния эндотелиальной дисфункции на развитие различных патологических состояний, в том числе хирургической инфекции, может служить патологическая активация системы гемостаза, в первую очередь – ее сосудисто-тромбоцитарных механизмов, непосредственно зависящих от состояния эндотелия.
Нами были получены данные, свидетельствующие о наличии четкой зависимости степени ее активации от уровня изменений продукции NO и степени снижения эндотелийзависимой вазодилятации, при этом максимально выраженной у больных с развитием
Таблица 6
Показатели эндотелийзависимой вазодилятации у больных с различной степенью тяжести хирургической инфекции
|
Группа |
Значения показателя ЭЗВД, % |
|
Здоровые лица, n=35 |
26,2±0,9 |
|
Больные МКБ и ДГПЖ с развитием хирургической инфекции (общая группа), n=56 |
8,7±0,8* |
|
Больные МКБ и ДГПЖ с легкой хирургической инфекцией, n=46 |
9,3±0,8* |
|
Больные МКБ и ДГПЖ со среднетяжелой хирургической инфекцией, n=10 |
5,9±0,4* # |
Примечания: * – различия с показателями группы здоровых лиц статистически значимы, р<0,01; # – различия между подгруппами статистически значимы, р<0,05.
хирургической инфекции. Полученные данные, как мы полагаем, являются дополнительным фактом в пользу повышения риска хирургической инфекции у оперированных больных с дисфункцией сосудистого эндотелия.
Снижение реакции сосудистого эндотелия на эндогенный оксид азота (выявленное нами в результате обследования больных с хирургической инфекцией на фоне повышения его продукции) не может, однако, служить основанием для заключения о патогенной роли данного важнейшего эндотелиального стимула. И в данной ситуации он остается важнейшим вазодилятатором. Поэтому дополнительное повышение его продукции, возможно, позволит преодолеть эндотелиальную дисфункцию.
Проведены исследования состояния NO-эргической системы, эндотелий-зависимой вазодилятации и системы гемостаза, а также особенностей клинического течения послеоперационного периода у больных на фоне применения в качестве донатора NO L-аргинина.
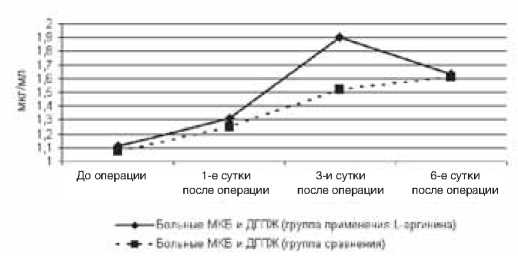
Данные, характеризующие динамику содержания нитрита NO2 в крови у больных с легкой хирургической инфекцией, представлены на рисунке 1.
В группе сравнения, как и в общем по подгруппам больных с МКБ и ДГПЖ, отмечалось значительное повышение показателя на 3-и и 6-е сутки после операции. Однако в группе применения L-аргинина повышение содержания метаболитов NO было выражено еще в большей степени и статистически значимо превышало показатель группы сравнения (на 25,0%, p<0,05). На 6-е сутки значения показателя в обеих группах практически уравнивались.
До операции
1-е сутки после операции
3-и сутки после операции
6-е сутки после операции
Рис. 1. Сравнительная характеристика содержания метаболита NO в крови больных в зависимости от проводимого лечения (группа больных с легкой хирургической инфекцией).
У больных со среднетяжелой хирургической инфекцией группы сравнения степень повышения уровня метаболитов NO в крови была несколько более высокой, чем в подгруппе с легкой инфекцией (рис. 2). Применение L-аргинина позволило добиться значительно более выраженного увеличения значений данного показателя, на 3-и сутки статистически значимо превысившего уровень NO2 группы сравнения (на 22,9%, p<0,05).
На 6-е сутки в данной подгруппе было зарегистрировано снижение содержания метаболитов NO отно-
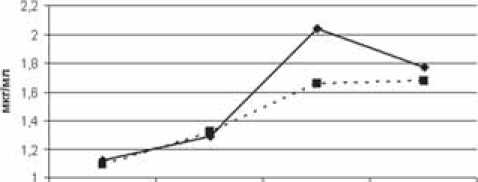
До операции 1-е сутки 3-и сутки 6-е сутки после операции после операции после операции
• Болы*» Wb и ДТП* (групп* применен»! L-аргинмна) ■ * - Болы*» WS и ДГПж (групп* сравнении)
Рис. 2. Сравнительная характеристика содержания нитрита NO2 в крови больных в зависимости от проводимого лечения (группа больных со среднетяжелой хирургической инфекцией).
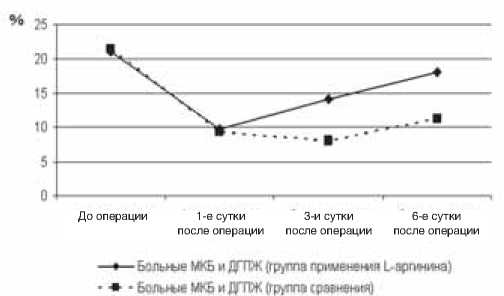
Рис. 3. Показатели ЭЗВД у больных в зависимости от проводимого лечения (группа с легкой хирургической инфекцией).
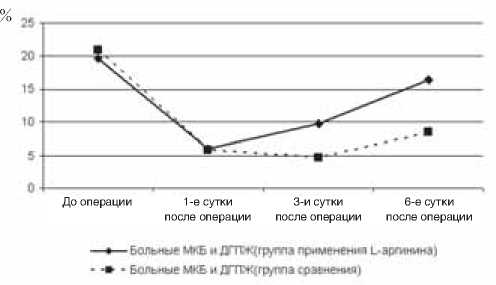
Рис. 4. Показатели ЭЗВД у больных в зависимости от проводимого лечения (группа со среднетяжелой хирургической инфекцией).
сительно исходного уровня, в то время как в группе традиционной терапии сохранялась тенденция к повышению показателя.
Как указано выше, применение L-аргинина как непосредственного донатора NO и стабилизатора функции сосудистого эндотелия могло бы способствовать коррекции эндотелиальной дисфункции и тем самым ликвидации общей и регионарной вазоконстрикции, улучшения кровообращения оперированного органа и зоны операционной раны. Для проверки данного предположения нами было проведено исследование значений показателей ЭЗВД в динамике лечения с использованием L-аргинина.
Таблица 7
Динамика содержания в крови фактора Виллебранда и функционального состояния тромбоцитов у больных МКБ и ДГПЖ в зависимости от проводимого лечения
|
Показатель |
До операции |
1-е сутки после операции |
3-и сутки после операции |
6-е сутки после операции |
|
Группа сравнения, n=100 |
||||
|
1 |
2 |
3 |
4 |
5 |
|
ФВ, % |
1,01±0,05 |
1,17±0,06* |
1,24±0,07* |
1,31±0,07* |
|
СИАТ, % |
43,5±2,9 |
51,6±3,1 |
59,6±2,8* |
60,4±3,0* |
|
ИДТ, % |
17,1±1,3 |
15,8±0,9 |
13,2±0,8* |
13,9±0,9* |
|
ПВ, с |
15,5±1,1 |
14,5±1,0 |
11,9±0,6* |
12,7±0,7* |
|
МНО усл. ед. |
0,89±0,07 |
0,81±0,06 |
0,76±0,05 |
0,80±0,06 |
|
ХII-а КЗФ-фибринолиз, мин |
4,4±0,2 |
4,2±0,2 |
4,6±0,1 |
4,9±0,2 |
|
Группа применения L-аргинина, n=50 |
||||
|
ФВ, % |
1,02±0,04 |
1,15±0,06 |
1,13±0,08 |
1,08±0,07# |
|
СИАТ, % |
44,8±2,5 |
52,0±3,0 |
53,7±3,3* |
49,4±2,9# |
|
ИДТ, % |
16,8±1,1 |
15,4±1,0 |
15,9±0,9# |
17,2±1,4 |
|
ПВ, с |
15,3±0,9 |
13,9±0,7 |
12,2±0,6* |
14,8±0,7# |
|
МНО усл. ед. |
0,90±0,06 |
0,80±0,05 |
0,79±0,06 |
0,86±0,07 |
|
ХII-а КЗФ-фибринолиз, мин |
4,5±0,2 |
4,3±0,1 |
4,4±0,1 |
4,5±0,2 |
Примечания: * – различия с показателем до операции статистически значимы, p<0,05; # – различия показателя с группой сравнения статистически значимы, p<0,05.
У больных с хирургической инфекцией степень снижения показателей ЭЗВД была выраженной, и даже при легких формах была на 3-и сутки почти 2-кратной. На 6-е сутки после операции намечалась минимальная тенденция к ее коррекции, однако только у больных с быстрым улучшением, хорошей эффективностью антимикробной терапии.
При применении L-аргинина наиболее выраженное снижение показателя среди всех обследований было зарегистрировано в 1-е сутки после операции, когда эффект от применения препарата еще не мог развиться в полной мере, далее, на 3-и и особенно 6-е сутки, имелась значительная динамика к увеличению показателя. В эти сроки превышение среднего уровня над группой сравнения было статистически значимым и составило 41,8% (p<0,05) и 60,2% (p<0,05) соответственно (рис. 3 и 4).
Таким образом, выраженность эффекта L-аргинина в отношении уровня ЭЗВД при развитии хирургической инфекции была большей, нежели в среднем по группе оперированных больных.
Нами также проведен анализ показателей различных механизмов гемостаза в сравнительном аспекте на фоне применения в лечении больных L-аргинина (табл. 7).
ОБСУЖДЕНИЕ
В качестве основных параметров, характеризующих эффективность применения L-аргинина в хирургической практике, нами использованы:
-
• частота развития синдрома системной реакции на воспаление (ССРВ) – определяли на 2-е сутки после операции;
-
• частота развития местных проявлений хирургической инфекции – определяли на 3-и сутки после операции;
-
• тяжесть течения хирургической инфекции – определяли на 6-е сутки после операции.
Синдром системной реакции на воспаление в контрольной группе развился в послеоперационном периоде в 56% случаев, в основной группе – в 38% случаев, т. е. на 32% реже, различия между подгруппами статистически значимы, р<0,05.
Частота местных проявлений хирургической инфекции была на 66,7% выше при традиционном ведении, различия между группами статистически незначимы (табл. 8).
Оценка тяжести течения хирургической инфекции на основании местного статуса и показателей ССРВ представлена в таблице 9.
Таблица 8
Частота местных проявлений хирургической инфекции у оперированных больных основной и контрольной групп
|
Традиционное ведение, n=100 |
Применение L-аргинина, n=50 |
||
|
абс. |
% |
абс. |
% |
|
10 |
10,0±3,0 |
3 |
6,0±3,4 |
Таблица 9
Сравнительный анализ тяжести течения хирургической инфекции у оперированных больных основной и контрольной групп
|
Традиционное ведение, n=100 |
Применение L-аргинина, n=50 |
||||||
|
Легкое течение |
Средней тяжести |
Легкое течение |
Средней тяжести |
||||
|
абс. |
% |
абс. |
% |
абс. |
% |
абс. |
% |
|
46 |
46,0±5 |
10 |
10,0±3,0 |
16 |
32,0±6,6 |
3 |
6,0±3,4 |
Из результатов анализа видно, что частота проявлений инфекционно-воспалительного процесса легкой степени (только ССРВ) была в группе L-аргинина ниже на 30,4%, а проявлений средней тяжести, включающих также местные признаки хирургической инфекции, – на 40%, различия между группами статистически незначимы.
Полученные в работе данные позволили нам сформулировать следующие выводы:
-
1. У больных с хирургической патологией мочевыделительной системы (мочекаменная болезнь, ДГПЖ) имеется статистически значимое повышение содержания метаболитов NO в крови (на 122% и 108%), сопровождающееся снижением эндотелийзависимой вазодилятации (на 17,2% и 26% соответственно), что свидетельствует о нарушениях функции сосудистого эндотелия. После оперативного лечения наблюдается дальнейший кратковременный рост содержания метаболитов NO в крови (до 161%) с одновременным статистически значимым угнетением вазодилятирующей функции эндотелия (на 51,9% и 55% соответственно).
-
2. Развитие хирургической инфекции сопровождается более значительными нарушениями функции сосудистого эндотелия, выражающимися в дополнительном повышении содержания метаболитов NO и глубоком угнетении показателя эндотелийзависимой вазодилятации и сопровождающимися активацией механизмов сосудисто-тромбоцитарного звена системы гемостаза. Тяжесть хирургической инфекции находится в прямой связи с выраженностью эндотелиальной дисфункции.
-
3. Применение L-аргинина при оперативном лечении больных мочекаменной болезнью и ДГПЖ дает дополнительное повышение эндотелиальной продукции NO, сопровождающееся увеличением показателя эн-дотелийзависимой вазодилятации (на 57%) и коррекцией нарушений со стороны сосудисто-тромбоцитарного звена гемостаза (снижение содержания ФВ в крови на 8,9%, СИАТ – на 10%, рост ИДТ – на 20,5%).
-
4. Коррекция эндотелиальной дисфункции и сосудисто-тромбоцитарного гемостаза путем применения L-аргинина позволяет добиться снижения частоты (на 32%) и тяжести хирургической инфекции, ускорения выздоровления.
-
5. Степанова Н. А., Лекманов А. У., Орбачевский Л. С. Диагностика и коррекция нарушений микроциркуляции, центральной гемодинамики и кислородного статуса при травматическом шоке у детей. Анестезиол. и реаниматол. 2005; 1; 26.
-
6. Шехтер А.Б., Кабисов Р.К., Пекшев А.В., Козлов Н.П., Перов Ю.Л. Экспериментально-клиническое обоснование плазмодинамической терапии ран оксидом азота. Бюллетень экспериментальной биологии и медицины, 1998, том 126, № 8.
Список литературы Острая дисфункция эндотелия у больных с хирургической инфекцией мочевыводящих путей
- Balk R.//Crit. Care Clin. -2000. -Vol. 16, № 2. -P. 214-226
- Вone R.//Crit. Care Med. -1996. -Vol. 24, № 7. -P. 1125-1127.
- Bone R.//Clin. Chest Med. -1996. -Vol. 17, № 2. -P. 175-181.
- Bone R., Grodzin Ch., Balk R.//Chest. -1997. -Vol. 112, № 1. -P. 235-243.
- Степанова Н. А., Лекманов А. У., Орбачевский Л. С. Диагностика и коррекция нарушений микроциркуляции, центральной гемодинамики и кислородного статуса при травматическом шоке у детей. Анестезиол. и реаниматол. 2005; 1; 26.
- Шехтер А.Б., Кабисов Р.К., Пекшев А.В., Козлов Н.П., Перов Ю.Л. Экспериментальноклиническое обоснование плазмодинамической терапии ран оксидом азота. Бюллетень экспериментальной биологии и медицины, 1998, том 126, № 8.


