Острое проксимальное расслоение аорты с отрывом устья правой коронарной артерии
Автор: Альсов Сергей Анатольевич, Хван Дмитрий Сергеевич, Сирота Дмитрий Андреевич, Ляшенко Максим Михайлович, Чернявский Александр Михайлович
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Случаи из клинической практики
Статья в выпуске: 3 т.19, 2015 года.
Бесплатный доступ
В клиническом случае описан опыт успешной хирургической коррекции острого проксимального расслоения аорты в сочетании с отрывом устья правой коронарной артерии у женщины 56 лет. Пациентке выполнено супракоронарное протезирование восходящего отдела аорты с аутовенозным шунтированием правой коронарной артерии.
Острое расслоение аорты, отрыв правой коронарной артерии
Короткий адрес: https://sciup.org/142140678
IDR: 142140678 | УДК: 616.1
Acute proximal aortic dissection complicated by right coronary artery detachment
This case report describes the experience of successful surgical repair of acute proximal aortic dissection complicated by the right coronary artery detachment in a 56-year-old woman. The patient underwent ascending aortic replacement with autovenous right coronary artery bypass.
Текст научной статьи Острое проксимальное расслоение аорты с отрывом устья правой коронарной артерии
Острое проксимальное расслоение аорты – жизнеугрожающее состояние: заболеваемость составляет, по данным разных авторов, до 3,5 случая на 100 тыс. человек в год [1]. В России ежегодно у более 3 тыс. человек происходит острое расслоение аорты. Госпитальная летальность при этой патологии составляет 20–30% даже при своевременном хирургическом лечении [2]. Несмотря на возросшее качество диагностики и лечения данных пациентов, неспецифическая симптоматика, симулирующая различные заболевания с болевым синдромом в грудной клетке, в первую очередь острый инфаркт миокарда, и организационные сложности до оперативного вмешательства уменьшают шансы пациента на выживание. Таким образом, случай острого расслоения аорты в сочетании с острым коронарным синдромом, возникший вследствие отрыва устья коронарной артерии, представляет клинический интерес.
В ФГБУ «ННИИПК им. акад. Е.Н. Мешалкина» Минздрава России поступила женщина 56 лет с жалобами на давящие загрудинные боли, характерные для острого коронарного синдрома. Из анамнеза известно, что болевой приступ возник внезапно в виде давящих болей за грудиной без иррадиации. В течение 25 лет пациентка страдает артериальной гипертензией с максимальным показателем систолического артериального давления (АД) до 240 мм рт. ст., на фоне медикаментозной терапии сред- нее систолическое АД – 160 мм рт. ст. Наследственностью по сердечно-сосудистой патологии не отягощена.
Болевой синдром не купировали в течение 5 ч. Бригада скорой медицинской помощи доставила в лечебно-профилактическое учреждение по месту жительства с подозрением на острый коронарный синдром. Пациентка получила нагрузочную дозу плавикса и аспирина в соответствии с рекомендациями по ведению больных с острым коронарным синдромом. Болевой синдром купировали наркотическими анальгетиками. Пациентке в экстренном порядке выполнили коронароангиографию, по результатам которой не выявили поражения коронарного русла (рис. 1). Давление стабилизировали на 130/80 мм рт. ст. В течение 10 дней пациентку наблюдали и лечили по поводу гипертонического криза. Тем не менее у нее сохранялся болевой синдром, мигрирующий в межлопаточную область и распространяющийся вдоль позвоночника. При дообследовании после проведения МСКТ-ангиографии выявили проксимальное расслоение аорты и признаки гидроперикарда, после чего пациентку перевели в ННИИПК им. акад. Е.Н. Мешалкина с показаниями к экстренному хирургическому лечению.
Из особенностей объективного статуса: в сознании, адекватна. Повышенного питания. Отеков нет. Ритм синусовый с частотой сердечных сокращений (ЧСС) 86 уд/ мин. АД на обеих руках 150/90 мм рт. ст. Пульсация на
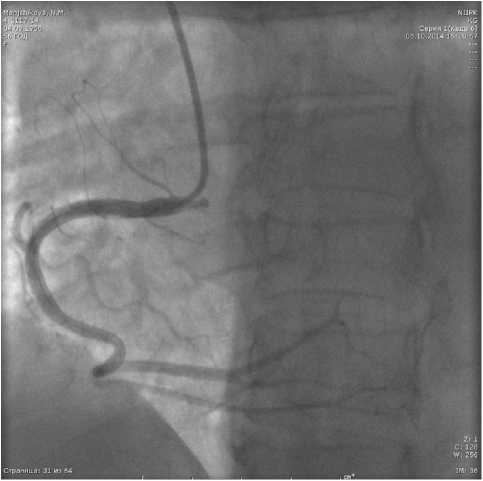
Рис. 1. Коронарограмма правой коронарной артерии
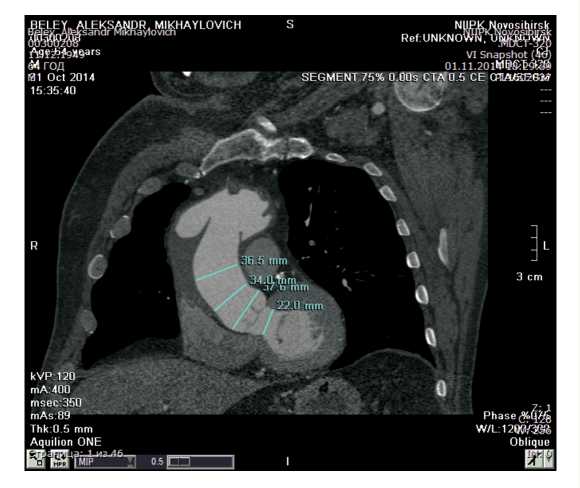
Рис. 2. МСКТ-ангиография восходящего отдела аорты. Расслоение восходящего отдела аорты с тромбозом ложного канала
магистральных артериях конечностей отчетливая, симметричная. Признаков ишемии нижних конечностей не выявлено. Признаков мальперфузии внутренних органов не обнаружено. Диурез достаточный.
Данные ЭКГ: ритм синусовый, неполная блокада правой ножки пучка Гиса, гипертрофия левого желудочка.
МСКТ-ангиография: расслоение от уровня синотубулярного гребня (СТГ) до инфраренального отдела аорты с распространением на левую почечную артерию. Диаметр восходящего отдела аорты 52 мм. Тромбоз ложного канала восходящего отдела аорты (рис. 2).
Маркеры повреждения миокарда: КФК МВ – 24. Интраоперационно выполнено дообследование с целью уточнения тактики лечения.
ЧПЭхоКГ: конечный диастолический объем 76 мл, фракция выброса 63%, нарушений локальной сократимости миокарда не выявлено, толщина межжелудочковой перегородки 1,5 см, аорта в восходящем отделе 4,7 см. Клапанный аппарат сердца без особенностей. От уровня СТГ фенестрацией начинается диссекция интимы с распространением на дугу аорты. В просвете ложного канала восходящего отдела аорты, вероятно, тромб.
УЗИ брахиоцефальных артерий: гемодинамически значимых изменений не выявлено, расслоение брахиоцефальных артерии не определяется.
УЗИ артерий нижних конечностей: расслоение артерий нижних конечностей не определяется.
Диагноз: острое проксимальное расслоение аорты. Гипертоническая болезнь III стадии. Артериальная гипертензия III степени. Хроническая сердечная недоста- точность IIа стадии по Стражеско – Василенко, функциональный класс II по NYHA. Ожирение I степени.
Хирургическая техника операции
Доступ – правая подключичная артерия для артериальной канюляции, срединная стернотомия. Аппарат искусственного кровообращения подключен по схеме: правое предсердие – правая подключичная артерия. Охлаждение больной до 25 °С. В полости перикарда около 200 мл серозно-геморрагической жидкости. При осмотре выявлено расширение восходящего отдела аорты до 6 см. Установлен дренаж левого желудочка через правую верхнюю легочную вену. Выделены устья брахиоцефальных артерий. Наложен зажим на аорту. Кардиоплегия антеградная. Кустодиол (20 мл/кг) в корень аорты. Аорта вскрыта поперечным разрезом.
При осмотре определяется циркулярное расслоение стенки аорты, начинающееся от фиброзного кольца правого коронарного синуса и распространяющееся по правой стенке восходящего отдела аорты. Ложный канал заполнен тромбами разной степени организации (рис. 3). При осмотре аортальный клапан трехстворчатый, створки тонкие, подвижные. Гидравлическая проба – коаптация полная, клапан признан состоятельным. Отмечается отрыв устья правой коронарной артерии (рис. 4). В области СТГ аорта пропускает калибр № 27.
По достижении температуры больного 25 °С наложены зажимы на брахиоцефальные артерии. Выполнен циркуляторный арест с антеградной унилатеральной перфузией головного мозга (объемная скорость перфу-
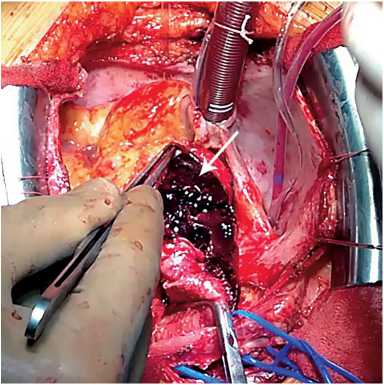
Рис. 3. Тромбоз ложного канала расслоеного восходящего отдела аорты
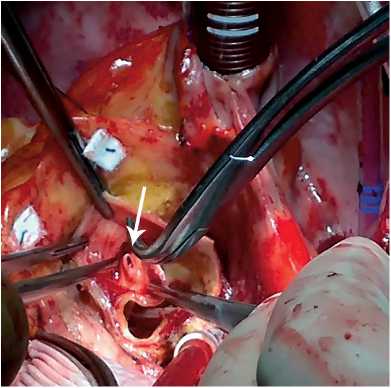
Рис. 4. Отрыв устья правой коронарной артерии
зии – 10 мл/кг/мин). При ревизии дуги аорты отмечалось распространение циркулярного расслоения на всю дугу аорты, фенестраций не обнаружено, брахиоцефальные артерии интактны. В просвете артерий (брахиоцефальный сосуд, левая общая сонная артерия) фрагментов отслоенной интимы не определялось, кровоток осуществлялся по истинному каналу. Стенка дуги аорты укреплена по сэндвич-методике. Сформирован косой дистальный анастомоз дуги аорты с синтетическим протезом Vascutek № 28. Аэропрофилактика. Наложен зажим на протез, возобновлено искусственное кровообращение в полном объеме. Начато согревание больного. Остиальное отверстие правой коронарной артерии ушито на синтетических прокладках. Выполнен проксимальный анастомоз СТГ с сосудистым протезом Vascutek № 28. Вскрыт просвет правой коронарной артерии на 3 см дистальнее ее устья. Выполнен анастомоз с аутовенозным трансплантатом (большая подкожная вена) по типу «конец в бок». Проксимальный конец шунта имплантирован в восходящий отдел аорты (протез). Профилактика воздушной эмболии, проверка состоятельности анастомозов. Снят зажим с протеза. Восстановление сердечной деятельности самостоятельное. После гемостаза и деканюляции выполнено послойное ушивание раны.
Интраоперационный контроль ЧПЭхоКГ: регургитации на аортальном клапане нет, нарушений локальной сократимости левого желудочка не отмечено.
Послеоперационный период протекал с явлениями коагулопатии и повышенной кровоточивости на фоне предшествующей антиагрегантной и антикоагулянтной терапии, по поводу чего проводили гемостатическую терапию в полном объеме с применением компонентов крови. Пациентку выписали на 16-е сутки.
Обсуждение
При остром проксимальном расслоении аорты операцией выбора является супракоронарное протезирование (с использованием или без использования сэнд-вич-техники на корне аорты), позволяющее быстро и с минимальным количеством осложнений устранить жизнеугрожающее состояние – профилактировать разрыв аорты. Обнаружение при этом расслоения, распространяющегося на устья коронарных артерий или тем более их отрыв, является неблагоприятным фактором как для пациента, так и хирурга и приводит к изменению хирургической тактики. Клиническая симптоматика может быть похожей на острый инфаркт миокарда. Так, по данным Hagen, нормальная электрокардиограмма наблюдалась только у 27% пациентов с острым расслоением аорты [3]. Как правило, данная группа пациентов получает антиагрегантную и антикоагулянтную терапию, согласно протоколу ведения пациентов с острым коронарным синдром. При расслоении аорты это приводит к неблагоприятным последствиям и увеличению смертности за счет кровопотери [4]. Основным дифференциальным диагнозом при остром расслоении является острый коронарный синдром, который также может быть проявлением расслоения аорты. Коронар- ная недостаточность при проксимальном расслоении аорты встречается примерно у 9,5% пациентов. Признаки тампонады сердца и развитие шока у пациентов данной группы наблюдались закономерно чаще, чем у пациентов без признаков ишемии миокарда [5]. Ишемия миокарда в предоперационном периоде, наряду с реанимационными мероприятиями, периферической и висцеральной мальперфузией, гемоперикардом, нестабильностью гемодинамики и комой, является фактором риска госпитальной смертности [6–8].
Основным методом лечения ишемии миокарда при остром расслоении аорты, конечно же, является хирургический. В литературе можно найти единичные примеры чрескожных вмешательств у больных с острым расслоением аорты. Однако в данных клинических случаях расслоение диагностировано лишь после коронарографии и стентирования, первоначально проводимых по поводу острого коронарного синдрома [9, 10]. Несмотря на сообщения об успешной ангиопластике у пациентов с расслоением аорты, первоочередным остается экстренное хирургическое вмешательство. Только своевременная операция может снизить летальность и увеличить выживаемость в ближайшем и отдаленном периодах и позволяет избежать прогрессирования расслоения с развитием неблагоприятных осложнений [11].
Neri описал механизмы развития коронарной недостаточности при остром проксимальном расслоении аорты. Выделены три типа, в зависимости от которых выполняется та или иная хирургическая пластика коронарных артерий [12]. Если расслоение достигает устья коронарной артерии, но не продолжается на ее стенку, реконструкция состоит в выкраивании устьев коронарных артерий по типу «кнопок». Когда расслоение распространяется на стенку коронарной артерии с образованием ложного канала, коронарная артерия продольно рассекается, куда затем вшивается заплата из аутоперикарда или большой подкожной вены. При отрыве коронарной артерии участок, подвергшийся расслоению, удаляется, и выполняется реконструкция по типу «конец в конец» большой подкожной веной. Но пластические операции на коронарных артериях не гарантируют стабильно положительного отдаленного результата, требуют много времени и удлиняют период интраоперационной ишемии миокарда. Как и другие авторы, мы считаем коронарное шунтирование более предпочтительным ввиду простоты, меньшей инвазив-ности и быстроты по сравнению с реконструктивными вмешательствами на коронарных артериях [13].
В нашем случае при полном отрыве правой коронарной артерии произошел циркулярный отрыв устья пра- вой коронарной артерии, в медии и интиме аорты образовалось отверстие диаметром около 5 мм. Остаток медии и адвентиции с устьем коронарной артерии был припаян к клетчатке правого желудочка, находился в состоянии отека, и выделение устья на «кнопке» было сопряжено с большими техническими трудностями. Главная проблема в условиях острого расслоения – надежно герметизировать отверстие в интиме и медии корня аорты. Во избежание проблем с последующим гемостазом в этой зоне следует выполнять протезирование синуса или имплантировать клапаносодержащий кондуит, после чего либо шунтировать (протезировать) вовлеченную в процесс коронарную артерию, либо реконструировать устья с реимплантацией в протез. В нашем случае, учитывая достаточную эластичность тканей, мы ушили отверстие в интиме-медии на отдельных П-образных швах с тефлоновыми прокладками и дополнили реконструкцию корня аорты сэндвич-техникой. Предварительно герметизировали устье правой коронарной артерии. Далее проводили стандартное аортокоронарное шунтирование правой коронарной артерии в проксимальном сегменте с использованием в качестве кондуита большой подкожной вены бедра. Это решение позволило достоверно не увеличивать время окклюзии аорты и отказаться от использования клапаносодержащего кондуита.
Данный клинический случай демонстрирует возможность хирургической коррекции острого проксимального расслоения аорты в сочетании с отрывом устья коронарной артерии. При возникновении подобной ситуации в арсенале хирурга должны быть алгоритмы, позволяющие изменять ход операции и проводить гемодинамическую коррекцию последствий острого проксимального расслоения аорты.
Список литературы Острое проксимальное расслоение аорты с отрывом устья правой коронарной артерии
- Clouse W.D., Hallett J.W. Jr, Schaff H.V., Spittell P.C., Rowland C.M., Ilstrup D.M., Melton L.J. 3rd. Acute aortic dissection: population-based incidence compared with degenerative aortic aneurysm rupture//Mayo Clin. Proc. 2004. Vol. 79. P. 176-180.
- Trimarchi S., Nienaber C.A., Rampoldi V., Myrmel T., Suzuki T., Mehta R.H., Bossone E., Cooper J.V., Smith D.E., Menicanti L., Frigiola A., Oh J.K., Deeb M.G., Isselbacher E.M., Eagle K.A.; International Registry of Acute Aortic Dissection. Contemporary results of surgery in acute type A aortic dissection: The International Registry of Acute Aortic Dissection experience//J. Thorac. Cardiovasc. Surg. 2005. Vol. 129. № 1. P. 112-122.
- Hagan P.G., Nienaber C.A., Isselbacher E.M., Bruckman D., Karavite D.J., Russman P.L., Evangelista A., Fattori R., Suzuki T., Oh J.K., Moore A.G., Malouf J.F., Pape L.A., Gaca C., Sechtem U., Lenferink S., Deutsch H.J., Diedrichs H., Marcos y Robles J., Llovet A., Gilon D., Das S.K. The International Registry of Acute Aortic Dissection (IRAD): new insights into an old disease//JAMA. 2000. Vol. 283. № 7. P. 897-903.
- Cannesson M., Burckard E., Lefévre M., Bastien O., Lehot J.J. Predictors of in-hospital mortality in the surgical management of acute type A aortic dissections: impact of anticoagulant therapies//Ann. Fr. Anesth. Reanim. 2004. Vol. 23. № 6. P. 568-574.
- Hirata K., Wake M., Kyushima M., Takahashi T., Nakazato J., Mototake H., Tengan T., Yasumoto H., Henzan E., Maeshiro M., Asato H. Electrocardiographic changes in patients with type A acute aortic dissection-incidence, patterns and underlying mechanisms in 159 cases//J. Cardiol. 2010. Vol. 56. № 2. P. 147-153.
- Chirillo F., Marchiori M.C., Andriolo L., Razzolini R., Mazzucco A., Gallucci V., Chioin R. Outcomes of 290 patients with aortic dissection. A 12-year multicentre experience//Eur. Heart J. 1990. Vol. 11. № 4. P. 311-319.
- Chiappini B., Schepens M., Tan E., Dell' Amore A., Morshuis W., Dossche K., Bergonzini M., Camurri N., Reggiani L.B., Marinelli G., Di Bartolomeo R. Early and late outcomes of acute type A aortic dissection: analysis of risk factors in 487 consecutive patients//Eur. Heart J. 2005. Vol. 26. № 2. P. 180-186.
- Чернявский А.М., Альсов С.А., Ляшенко М.М., Сирота Д.А., Хван Д.С., Виноградова Т.Е., Захаров С.Л., Ломиворотов В.В. Анализ неврологических осложнений после хирургической реконструкции дуги аорты у пациентов с проксимальным расслоением//Патология кровообращения и кардиохирургия. 2013. № 2. С. 35-40.
- Barabas M., Gosselin G., Crépeau J., Petitclerc R., Cartier R., Théroux P. Left main stenting-as a bridge to surgery-for acute type A aortic dissection and anterior myocardial infarction//Catheter Cardiovasc. Interv. 2000. Vol. 51. № 1. P. 74-77.
- Yunoki K., Naruko T., Itoh A., Furukawa A., Abe Yu., Nakagawa E., Komatsu R., Haze K. Stenting of right coronary ostial occlusion due to thrombosed type A aortic dissection: One-year follow-up results//J. Cardiol. Cases. 2010. Vol. 1. № 3. P. 166-170.
- Чернявский А.М., Ляшенко М.М., Альсов С.А., Сирота Д.А., Хван Д.С. Гибридный подход в хирургии расслоений аорты проксимального типа//Ангиология и сосудистая хирургия. 2014. Т. 20. № 3. С. 41-47.
- Neri E., Toscano T., Papalia U., Frati G., Massetti M., Capannini G., Tucci E., Buklas D., Muzzi L., Oricchio L., Sassi C. Proximal aortic dissection with coronary malperfusion: presentation, management, and outcome//J. Thorac. Cardiovasc. Surg. 2001. Vol. 121. № 3. P. 552-560.
- Kawahito K., Adachi H., Murata S., Yamaguchi A., Ino T. Coronary malperfusion due to type A aortic dissection: mechanism and surgical management//Ann. Thorac. Surg. 2003. Vol. 76. № 5. P. 1471-1476.


