Острый инфаркт миокарда как осложнение расслаивающей аневризмы грудного отдела аорты у пациента старческого возраста: клинический случай
Автор: Букатов В.В., Аль Гутани К., Леонова Н.А.
Журнал: Juvenis scientia @jscientia
Рубрика: Клинические случаи
Статья в выпуске: 6 т.11, 2025 года.
Бесплатный доступ
Несмотря на достигнутый за последние годы прогресс в лечении инфаркта миокарда, в том числе у пациентов пожилого и старческого возраста, в современных реалиях случаются неординарные клинические случаи, из-за редкости которых врачи испытывают трудности при определении тактики лечения этих пациентов. В данной статье представлен клинический случай развития острого инфаркта миокарда у мужчины 76 лет как осложнения расслаивающей аневризмы грудного отдела аорты. Скорой медицинской помощью в приемное отделение доставлен пациент 76 лет с входящим диагнозом: острый коронарный синдром (ОКС) с подъемом сегмента ST электрокардиограммы. Учитывая типичную клиническую картину и изменения электрокардиограммы, пациент немедленно, без дополнительной диагностики (эхокардиография) направлен в рентген-операционную для проведения экстренной коронароангиографии и возможного стентирования симптом-связанной артерии. При проведении коронароангиографии выявлена диссекция интимы с формированием окклюзии ствола левой коронарной артерии (ЛКА), интраоперационно консилиум из кардиолога, эндоваскулярного хирурга и кардиохирурга решил выполнить экстренное стентирование ствола ЛКА. Операция прошла без видимых осложнений, на контрольных сериях просвет ствола ЛКА ровный, кровоток по шкале Thrombolysis In Myocardial Infarction (TIMI) 3. После реваскуляризации, несмотря на положительную динамику по данным ангиографии и электрокардиограммы, у пациента сохранялся болевой синдром в грудной клетке. Дополнительные методы обследования (эхокардиография, СКТ-ангиография аорты) позволили диагностировать расслаивающую аневризму грудного отдела аорты, которая распространилась на ствол левой коронарной артерии, что привело к инфаркту миокарда. В дальнейшем удалось стабилизировать пациента и через месяц провести оперативное вмешательство в объеме протезирования аорты. Пациента выписали в удовлетворительном состоянии на дальнейшее амбулаторное лечение.
Инфаркт миокарда с подъемом сегмента ST, ОКС с подъемом ST, расслаивающая аневризма грудного отдела аорты
Короткий адрес: https://sciup.org/14134776
IDR: 14134776 | DOI: 10.32415/jscientia_2025_11_6_22-31
Acute Myocardial Infarction as a Complication of Thoracic Aortic Dissection in an Elderly Patient: а Case Report
Despite significant advances in the management of myocardial infarction, including in elderly patients, rare and diagnostically challenging clinical situations still occur. We report a clinical case of ST-segment elevation myocardial infarction (STEMI) in a 76-year-old man caused by thoracic aortic dissection. The patient was admitted to the emergency department with a preliminary diagnosis of ST-segment elevation acute coronary syndrome. Due to the typical clinical presentation and electrocardiographic findings, the patient was immediately transferred to the catheterization laboratory for emergency coronary angiography and possible culprit artery stenting without prior echocardiography. Coronary angiography revealed intimal dissection with occlusion of the left main coronary artery. During an intraoperative consultation involving a cardiologist, an endovascular specialist, and a cardiac surgeon, emergency stenting of the left main coronary artery was performed. The procedure was uneventful. Control angiographic images demonstrated restoration of the left main coronary artery lumen with TIMI 3 blood flow. However, despite successful revascularization, the patient continued to experience persistent chest pain. Additional imaging studies, including echocardiography and CT angiography of the aorta, revealed thoracic aortic dissection extending into the left main coronary artery, which caused myocardial infarction. The patient was stabilized and subsequently underwent surgical aortic replacement one month later. He was discharged in satisfactory condition for further outpatient follow-up.
Текст научной статьи Острый инфаркт миокарда как осложнение расслаивающей аневризмы грудного отдела аорты у пациента старческого возраста: клинический случай
Боли в грудной клетке — самый частый симптом, который встречается в отделениях неотложной помощи. При этом заболевания, требующие дифференциальной диагностики, могут как не представлять опасности для жизни, так и быть крайне опасными и сопряженными с высоким риском летальности. Одним из таких заболеваний является расслаивающая аневризма аорты. Частота развития этого заболевания, по разным данным, составляет 2,5–5 случаев на 100 000 населения [1].
Расслаивающая аневризма аорты — это угрожающее жизни состояние, при котором летальность среди нелеченых пациентов составляет 1% в час, и для его лечения требуется экстренное хирургическое вмешательство. Однако клинические проявления расслаивающей аневризмы пересекаются с острым инфарктом миокарда, что приводит к высоким показателям ошибочной диагностики на практике. Существующие клинические рекомендации не содержат целевых протоколов дифференциальной диагностики при одновременном наличии расслаивающей аневризмы аорты и острого инфаркта миокарда, что часто приводит к неправильной тактике ведения пациента, последующему неверному лечению, повышающему летальность больных [2]. Таким образом, необходим анализ клинических случаев для выявления диагностических дилемм и оптимизации клинических протоколов. Дифференциальная диагностика между инфарктом миокарда и расслаивающей аневризмой аорты, по данным последних исследований, затруднительна [3]. Ишемические изменения на электрокардиограмме (ЭКГ) у пациентов с расслаивающей аневризмой аорты регистрируются у 38,0%, при этом наиболее распространенным зарегистрированным отклонением является инверсия зубца Т, которая наблюдалась у 38,6% пациентов с расслаивающейся аневризмой грудного отдела аорты, девиация сегмента ST встречается значимо реже. Острый инфаркт миокарда с подъемом сегмента ST был выявлен у 16,3%. Уровень тропонина I повышался у 36,6% пациентов.
Пациенты с острым инфарктом миокарда в современных сосудистых центрах обычно подвергаются эндоваскулярному вмешательству, без траты времени на дополнительные обследования [4]. Расслаивающая аневризма аорты может осложняться острой коронарной окклюзией, что приводит к значительному увеличению летальности. Рекомендуемым лечением расслоения аорты является экстренная кардиохирургическая операция [5]. В некоторых случаях острый инфаркт миокарда может являться причиной расслоения восходящей аорты. Рутинное кардиохирургическое вмешательство с экстренной катетеризацией сердца может привести к более высокой летальности в этой группе пациентов [6]. Противоречия между методами лечения острого расслоения аорты и инфаркта миокарда с подъемом сегмента ST могут привести к клинической катастрофе [7]. Характерным признаком, который может помочь в ранней диагностике расслаивающей аневризмы аорты и определения дальнейшей тактики лечения — это выявление аортальной недостаточности и/или лабораторно повышенный уровень D-димера крови [8], однако учитывая необходимость принимать быстрое решение об экстренной реваскуляризации миокарда, у клиницистов нет времени или возможностей проведения трансторакального УЗИ сердца и анализа уровня D-димера крови в короткие сроки. Использование трансторакальной эхокардиографии повышает эффективность скрининга острого расслоения аорты у пациентов с инфарктом миокарда с подъемом сегмента ST. У пациентов с низкой клинической вероятностью расслаивающей аневризмы аорты прямые признаки, выявляемые с помощью трансторакальной эхокардиографии, могут быть использованы для быстрого определения тех, кому требуется расширенная визуализация [9].
В настоящее время остаются неразрешенные вопросы тактики лечения этих пациентов (проведение реваскуляризации коронарной артерии, стабилизация состояния и в последующем протезирование аорты, либо протезирование аорты и проведение аортокоронарного шунтирования в острый период заболевания). Данные медицинской литературы не дают однозначного ответа на вопрос о предпочтительной тактике. Описаны клинические случаи успеха обоих вариантов, однако летальность при этом состоянии сохраняется крайне высокой [10].
В качестве примера представлен клинический случай острого инфаркта миокарда как осложнения расслаивающей аневризмы грудного отдела аорты. Отмечены основные диагностические этапы, разъяснены причины выбора тактики введения пациента, представлено течение заболевания и его исход.
КЛИНИЧЕСКИЙ СЛУЧАЙ
Мужчина 76 лет экстренно доставлен в приемное отделение регионального кардиохирургического центра ОГБУЗ БОКБ Святителя Иоасафа бригадой скорой медицинской помощи с входящим диагнозом: острый коронарный синдром с подъемом сегмента ST электрокардиограммы. Жалобы на интенсивную давяще-распирающую боль в грудной клетке, с иррадиацией в левую верхнюю конечность, чувство нехватки воздуха, потливость, страх смерти. Из анамнеза известно, что пациент страдает гипертонической болезнью более 15 лет, периодически принимает гипотензивные препараты короткого действия, однако регулярной базовой терапии нет, регулярно артериальное давление не контролирует. Ранее физические нагрузки переносил удовлетворительно, соответственно возрасту, жалоб на боли в груди, одышку ранее не предъявлял, периодически отмечал головные боли в затылочной области, связывая их с повышением артериального давления. Настоящее ухудшение в течение двух часов, когда после умеренной физической нагрузки (принес домой 5 литров воды) возникли вышеописанные симптомы, самостоятельно попытался купировать симптоматику корвалолом, без эффекта. При измерении артериального давления — повышение до 200/120 мм рт.ст., в связи с чем была вызвана скорая помощь.
На догоспитальном этапе скорой медицинской помощью проведена следующая терапия: морфин 1% — 1,0 в/в дробно, гепарин 4000 ЕД в/в болюс, клопидогрел 600 мг per os , ацетилсалициловая кислота 250 мг per os , изокет спрей 2 дозы под язык. Учитывая ожидаемую длительность транспортировки в региональный сосудистый центр менее 2 часов, решено воздержаться от применения тромболитической терапии.
При осмотре в приемном отделении: общее состояние пациента тяжелое, сознание ясное, ориентирован, на вопросы отвечает правильно, несколько заторможено (в связи с действием наркотических анальгетиков). Кожные покровы обычной окраски, повышенной влажности, видимые слизистые розовые, в легких дыхание везикулярное, проводится во все отделы, хрипы не выслушиваются, тоны сердца приглушены, ритмичны, тахикардия 110 ударов в мин. Во втором межреберье у правого края грудины выслушивается мягкий диастолический шум. АД 180/110 мм рт.ст. Живот при пальпации мягкий, безболезненный во всех отделах, печень, селезенка не увеличены. Нижние конечности не отечны. Рост пациента 175 см, масса тела 82 кг.
На электрокардиограмме (после внутривенного введения бета-адреноблокаторов) фиксируется подъем сегмента ST в отв. I, II, aVL до 0,5 мм, в отведениях V1-V6 до 22 мм (рис. 1).
По прибытии в сосудистый центр болевой синдром выражен на 80% от исходного, электрокардиограмма без значимой динамики, артериальное давление 180/110 мм рт.ст. Пациенту в условиях палаты реанимации и интенсивной терапии начата инфузия гепарина 12 ЕД/кг и инфузия изосорбида динитрата 6 мг/час с целью стабилизации артериального давления, в/в введено 15 мг метопролола для урежения частоты сердечных сокращений и уменьшения потребности миокарда в кислороде. Учитывая типичную клинику болевого синдрома и закономерные изменения электрокардиограммы для инфаркта миокарда с подъемом ST, принято решение о проведение экстренной коронароангиографии (КАГ) с возможным стентированием инфаркт-связанной артерии, без ожидания дополнительных методов исследований, таких как ультразвуковое исследование сердца и анализы крови. Больной экстренно в течение 15 минут от поступления в приемное отделение транспортирован в рентген-операционную с параметрами гемодинамики: частота сердечных сокращений 92 удара в минуту, артериальное давление 160/100 мм рт.ст.
При выполнении КАГ определялась диссекция ствола левой коронарной артерии (ЛКА), привед-
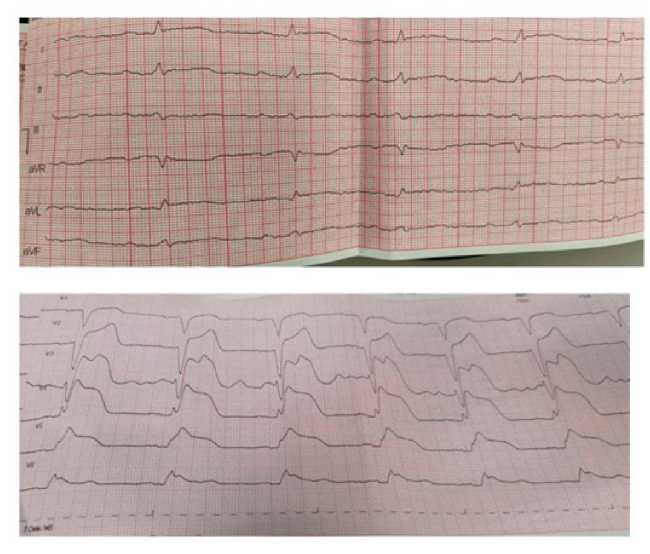
Рис. 1. Электрокардиограмма с подъемом сегмента ST у мужчины 76 лет с расслаивающей аневризмой грудного отдела аорты. Fig. 1. Electrocardiogram demonstrating ST-segment elevation in a 76-year-old man with thoracic aortic dissection.
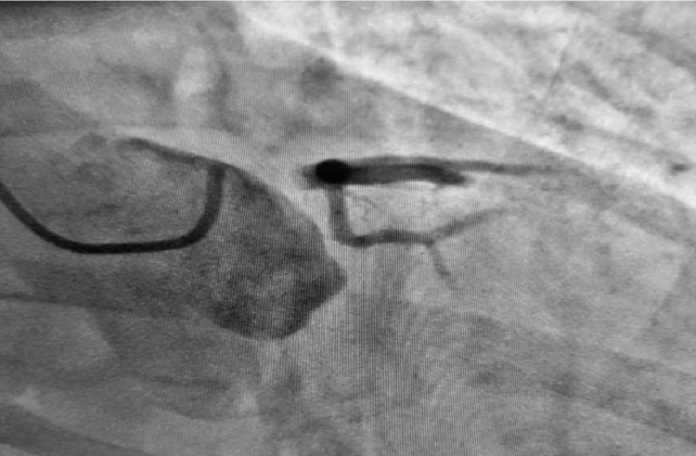
Рис. 2. Коронароангиография: диссекция, окклюзия левой коронарной артерии. Fig. 2. Coronary angiography showing dissection with occlusion of the left main coronary artery.
шая к полной окклюзии сосуда без гемодинамически значимого атеросклероза в других коронарных артериях (рис. 2).
Интраоперационно кардиолог совместно с эндоваскулярным хирургом и кардиохирургом приняли решение о проведении стентирования ствола левой коронарной артерии. Учитывая стабильные показатели гемодинамики пациента, отсутствие кардиогенного шока и отёка легких, решено воздержаться от механической поддержки кровообращения (внутриаортальной баллонной контрпульсации). Оперативное вмешательство прошло без особенностей, по окончанию стентирования ширина просвета ствола левой коронарной артерии полностью восстановлена, достигнут кровоток TIMI 3 (рис. 3).
Лабораторные исследования (набор при поступлении в палату интенсивной терапии, перед проведением коронароангиографии): общий анализ крови: эритроциты 4,07 × 1012/л гемоглобин 102 г/л, лейкоциты 11,9 × 109/л, тромбоциты 268 × 109/л. Коагулограмма: умеренная гипокоагуляция, обусловленная введением гепарина. В биохимическом анализе крови наблюдались типичные изменения, характерные для острого инфаркта миокарда, повышение уровня КФК до 1121 ЕД/л, КФК-МВ до 235 ЕД/л, высокочувствительного тропонина I до 5465 пг/л, АЛТ 125 ЕД/л, АСТ 125 ЕД/л креатинин 111 мкмоль/л, мочевина 10,1 ммоль/л.
Несмотря на реваскуляризацию инфаркт-зависимой артерии, положительную динамику
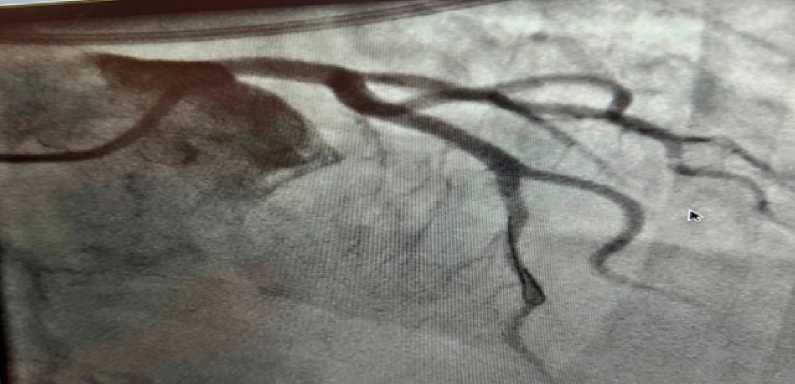
Рис. 3. Коронароангиография: восстановление кровотока по левой коронарной артерии. Fig. 3. Coronary angiography demonstrating restoration of blood flow in the left main coronary artery.
Пациент транспортирован из рентген-операци-онной в блок интенсивной терапии. При осмотре сохранялись распирающие боли в грудной клетке, выражены на 60% от исходного, на электрокардиограмме фиксировалась динамика снижения элевации сегмента ST более чем 50%, инверсия зубцов Т в грудных отведениях.
Параметры гемодинамики: частота сердечных сокращений 86 ударов в минуту, артериальное давление 155/90 мм рт.ст.
электрокардиограммы и повторное обезболивание наркотическими анальгетиками, у пациента сохранялся болевой синдром в грудной клетке. В связи с этим проведено экстренное эхокардиографическое исследование, через 1 час после реваскуляризации инфаркт-связанной артерии, по результатам которого: полости сердца не расширены, умеренное снижение сократимости верхушечных сегментов, фракция выброса 41%, отмечалась аортальная недостаточность II–III степени, при осмо-
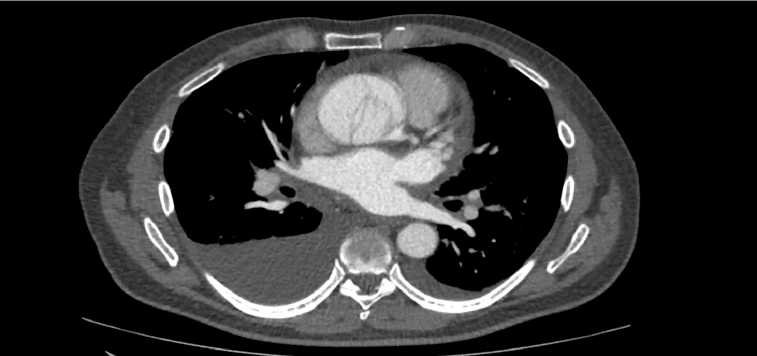
Рис. 4. СКТ-ангиография расслаивающей аневризмы грудного отдела аорты. Fig. 4. Computed tomography angiography demonstrating thoracic aortic dissection.
тре грудной аорты подозрение на расслоение — определялся двойной контур.
Учитывая данные эхокардиографии, выбрана тактика контролируемой гипотонии, также, несмотря на возраст, усилена терапия бета-адреноблокаторами, для контроля артериального давления начата инфузия урапидила со скоростью 10 мг/час после в/в введения 25 мг. Болевой синдром в грудной клетке удалось купировать на фоне удержания артериального давления (< 110/80 мм рт.ст.), частоты сердечных сокращений (< 65 уд/мин). После стабилизации состояния, для подтверждения диагноза пациент направлен на проведение СКТ-ангиографии грудной аорты с болюсным усилением, на которой выявили расслоение стенки восходящей части и дуги аорты (рис. 4) от аортального клапана до начальной части нисходящего отдела с формированием истинного и ложного просвета. Ложный просвет локально превосходил истинный более чем на 50% преимущественно на уровне восходящей аорты, диаметр истинного просвета на этом уровне — 15 мм, ложного — 30 мм.
Незамедлительно собран консилиум из кардиологов, эндоваскулярных хирургов и кардиохирургов.
По результатам консилиума, учитывая острый инфаркт миокарда, необходимость двойной антиагрегантной терапии и как следствие высокие риски кровотечения, общий высокий риск опе- ративного вмешательства в острый период заболевания, принята тактика дальнейшей консервативной терапии, направленной на стабилизацию гемодинамики для исключения прогрессирования расслоения аорты и проведения оперативного вмешательства в отсроченный, так называемый, «холодный» период через 1 месяц после события.
Пациент наблюдался в палате интенсивной терапии, первые 48 часов со значимым ограничением двигательного режима (постельный) и строгим контролем артериального давления (непрерывные инфузии изосорбида динитрата и урапидила), в контрольных анализах наблюдались характерные для острого инфаркта миокарда повышение маркеров повреждения миокарда (тропонин I более 50000 нг/л, КФК 1835 Ед/л, КФК-МВ 216 Ед/л, Д-димер 1,3 мг/л) и последующее закономерное снижение кардиоспецифических маркеров (тропонин I 34568 нг/л через 24 часа, 17240 нг/л через 48 часов и полная нормализация на 7-е сутки); показатели общего анализа крови и функции почек были без значимых сдвигов.
После 48 часов пребывания пациента в палате интенсивной терапии была начата реабилитация и активизация больного, проводились занятия лечебной физкультуры для профилактики пневмонии и мышечной атрофии, цифры артериального давления и частоты сердечных сокращений были в пределах 110–128/65–86 мм рт.ст. и 62–
68 уд в мин соответственно на приеме периндо-прила 4 мг × 1 раз в сутки, метопролола сукцината 50 мг × 1 раз в сутки, индапамида 1,5 мг × 1 раз в сутки, лерканидипина 5 мг × 1 раз в сутки. С 4-х суток началась активизация пациента по палатному режиму, болевой синдром в грудной клетке не рецидивировал, контрольная СКТ-аортография на 7-е сутки от первого исследования показала, что расслоение стенок аорты не прогрессирует, в дальнейшем, учитывая отсутствие рецидива болевого синдрома в грудной клетке, СКТ не повторялась.
Через месяц после эндоваскулярного вмешательства пациенту выполнена операция: протезирование корня аорты и восходящей аорты синтетическим кондуитом, содержащим биологический протез аортального клапана по методике Бенталла — Де Боно–Каучукоса. В послеоперационом периоде потребовалась инфузия свежезамороженной плазмы и эритроцитарной взвеси с удаленным лейкоцитарным слоем для коррекции кровотечения и гипокоагуляции.
На первые сутки после операции пациент был экстубирован, а через 72 часа больного перевели из отделения реанимации в общую палату кардиохирургического отделения.
Впоследствии проводилась комплексная реабилитация пациента, контроль лабораторных и гемодинамических показателей, УЗИ сердца и СКТ-ан-гиография аорты, все показатели соответствовали принятым нормативам в послеоперационном периоде. Пациент выписан на дальнейшее амбулаторное лечение с рекомендациями, в том числе по регулярному наблюдению кардиологом (через месяц, через полгода, через год). Осмотр через месяц показал, что коррекции лечения не требуется, пациент выполнял бытовые потребности без дополнительной помощи. При повторном осмотре через 6 месяцев выяснилось, что пациент полностью вернулся к полноценной жизни, смог выполнять расширенные бытовые нагрузки и не испытывал трудностей, одышки или болей в грудной клетке, артериальное давление пациента держалось стабильно на уровне 120–125/80–89 мм рт.ст., ЧСС — в пределах 60–64 уд. в мин.
ЗАКЛЮЧЕНИЕ
Представляя данный клинический случай, хотелось обратить внимание коллег на то, что такое серьезное заболевание как инфаркт миокарда может являться осложнением другого заболевания (расслаивающая аневризма аорты). В настоящей публикации представлен пациент с диагнозом: острая расслаивающая аневризма грудного отдела аорты тип А Stanford, осложненная инфарктом миокарда 2-го типа передне-боковой области левого желудочка. Инфаркт миокарда как осложнение расслаивающей аневризмы аорты является редким, но не казуистическим случаем, зачастую скрывающим основное заболевание. Задержка реваскуляризации инфаркт-зависимой артерии является недопустимой, и проведение СКТ-ангио-графии аорты не может быть причиной рутинной задержки лечения, однако в крупных сосудистых центрах при подозрении на расслаивающую аневризму аорты (диастолический шум над аортой, высокое пульсовое давление, анамнез аневризмы аорты) целесообразно проводить ультразвуковое исследование сердца перед проведением коро-нароангиографии для исключения расслоения.
Финансирование: Авторы заявляют об отсутствии финансирования.


