Отдаленная эффективность последовательной имплантации перекрывающихся краями сиролимус-элюирующих стентов у больных ишемической болезнью сердца с протяженными стенозами коронарных артерий
Автор: Марков В.В., Баев А.Е., Варваренко В.И., Гольцов С.Г., Торим Ю.Ю., Крылов А.Л.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 1-1 т.26, 2011 года.
Бесплатный доступ
Изучена отдаленная эффективность последовательной имплантации перекрывающихся краями сиролимус-элюирующих стентов (СЭС) и сочетания СЭС и голометаллического стента (ГМС). Эффективность реваскуляризации оценивали в процессе 11,1±0,6 мес. наблюдения. Установлено, что последовательная имплантация перекрывающихся краями СЭС при стентировании протяженных диффузных поражений позволяет снизить частоту рестенозов без увеличения количества тромбозов по сравнению с сочетанным использованием СЭС и ГМС.
Ишемическая болезнь сердца, сиролимус-элюирующий стент, голометаллический стент, протяженные поражения коронарных артерий
Короткий адрес: https://sciup.org/14919384
IDR: 14919384 | УДК: 616.132.2-007.271-089.819.5-07
Long-term efficacy of overlapping sirolimus eluting stents in long stenosis in patients with coronary heart disease
Long-term efficacy of overlapping sirolimus eluting stents (SES) versus combination SES and bare metal stents (BMS) is studied over 11,1±0,6 month monitoring. The following conclusions were made: implantation of overlapping SES in long diffuse coronary lesions reduc
Текст научной статьи Отдаленная эффективность последовательной имплантации перекрывающихся краями сиролимус-элюирующих стентов у больных ишемической болезнью сердца с протяженными стенозами коронарных артерий
Болезни системы кровообращения, включая ишемическую болезнь сердца (ИБС), продолжают занимать лидирующее место в структуре причин инвалидизации и смертности населения промышленно развитых стран, в том числе и России [2]. Наличие стенокардии и степень ее выраженности прямо коррелируют с тяжестью стено-тического поражения коронарных артерий (КА), состоянием сердечной мышцы и определяют прогноз заболевания в целом [9]. Наличие у пациента протяженного стенозирующего поражения КА, как правило, сопряжено с повышенным риском развития неблагоприятных сердечно-сосудистых событий. Нередко длина гемодинамически значимого стеноза превышает 40 мм. В таких случаях методом выбора может быть последовательная имплантация нескольких стентов с использованием техники “overlapping” – наложением края последующего стента на край предыдущего. Края стентов перекрываются на протяжении 1–5 мм. В завершении выполняется постдилатация участка перекрытия двух соседних стентов. Для постдилатации используют баллон диаметром, соответствующим диаметру большего стента. Давление в баллоне при этом должно превышать давление раскрытия большего по диаметру стента при его установке.
По мнению ряда авторов, такая методика сопряжена с определенными техническими сложностями, увеличи- вающими травму сосудистой стенки и способствующими нарушению процессов эндотелизации [10, 11, 16]. Увеличение металла на участках “overlap” может служить причиной гиперплазии неоинтимы, тромбозов и рестенозов стентов как при имплантации ГМС, так и стентов с лекарственным покрытием (СЛП) [10, 13, 14, 16]. На сегодняшний день частота применения техники “overlapping” в клинической практике составляет около 10% [13], поэтому отдаленные результаты последовательной имплантации стентов представляют большой интерес.
Цель исследования: изучить отдаленнyю эффективность стентирования протяженных стенозов КА путем последовательной имплантации перекрывающихся сиро-лимус-элюирующих стентов и в случаях сочетания си-ролимус-элюирующего и голометаллического стентов.
Материал и методы
В клинически и ангиографически контролируемое исследование включены 49 пациентов с ИБС, не имеющих противопоказаний к комбинированной антианги-нальной терапии (рис. 1.). Больные разделены на две группы. В 1-й группе (СЭС+ГМС, n=24) выполнена последовательная имплантация СЭС и ГМС. Во 2-й группе (СЭС+-СЭС), включавшей 25 пациентов, выполнена имплантация перекрывающихся СЭС.
По всем основным клиническим и демографическим показателям статистически значимых различий между группами не было (табл. 1). В обеих группах пациентов преобладала ИБС с симптомами стенокардии напряжения, соответствующими III функциональному классу (ФК).
Почти половина больных (45,8% в 1-й группе против 56% во 2-й; p=0,48) перенесли ИМ давностью 6 мес. и более. У большинства пациентов ИБС протекала на фоне артериальной гипертонии I–III степени и некорригиро-ванной гиперхолестеринемии. Симптомы сердечной недостаточности II–III ФК (по NYHA) сопутствовали проявлениям коронарной недостаточности у всех обследованных пациентов.
При проведении ангиографии у подавляющего большинства пациентов 1 и 2-й группы наряду с диффузным атеросклерозом диагностировано многососудистое стенозирующее поражение КА (79,2% против 84,0%; p=0,30). Реваскуляризация хронических окклюзий методом “overlapping” выполнена в 20,8% случаях в группе СЭС+ГМС и 20% – в группе СЭС+СЭС (p=0,94).
Перед выполнением стентирования всем пациентам назначали аспирин в дозе 125 мг/сут. Клопидогрел в дозе 75 мг/сут назначали за 5 суток до стентирования. После стентирования проводилась двойная антитромбоцитар-ная терапия (аспирин в дозе 125 мг/сут и клопидогрел в дозе 75 мг/сут до 12 мес.) и антикоагулянтная терапия (гепарин 1000 ЕД/ч внутривенно в течение первых суток, со вторых суток пациенты переводились на подкожное введение гепарина в дозе 20000 ЕД/сут в течение пяти суток и 10000 ЕД/сут – в течение последующих двух суток).
Контроль за эффективностью реваскуляризации осуществлялся через год. Всем больным проведена контрольная ангиография. При прогрессировании коронарной и сердечной недостаточности пациенты поступали в клинику независимо от контрольных точек.
В процессе наблюдения нами оценивались следу- I ющие ангиографические показатели:
Остаточный стеноз – сужение просвета стента сразу после стентирования (мм).
Поздняя потеря – сужение просвета стента, наступившее в течение контрольного периода в результате формирования неоинтимы, определяемое при контрольной коронарографии (мм).
Стеноз стента – сужение просвета стента за счет остаточного стеноза и сформированной неоинтимы, определяемое при контрольной коронарографии.
Бинарный рестеноз – стеноз артерии более 50%, выявленный на стентированном участке при контрольной коронарографии.
Тромбоз стента – ангиографически документированный (визуализированный) тромбоз стентированного участка с кровотоком Thrombolysis In Myocardial Infarction (TIMI) 0.
Полученные результаты обрабатывались с помо- щью пакета прикладных программ STATISTICA 6.0 for Windows. В условиях нормального распределения анализируемого признака статистическую значимость различий определяли с помощью t-критерия Стью- дента. При отсутствии нормального распределения признака в сформированной выборке использовался непараметрический критерий Манна–Уитни. Для определения различий качественных переменных проводился анализ таблиц сопряженности и применялся критерий χ2. Различия величин считали статистически значимыми при уровне p<0,05. Количественные данные представлены как М±m (среднее значение и стандартная ошибка среднего).
Результаты
При выполнении стентирования пациентам 1-й группы с использованием техники “overlapping” имплантировано 48 стентов (24 СЭС и 24 ГМС), во 2-й – 53 перекрывающихся СЭС. Суммарное количество перекрывающихся участков стентов составило 24 в 1-й группе и 28 – во 2-й.
Пациентам 1-й группы с использованием техники “overlapping” в переднюю нисходящую артерию (ПНА) установлено 40 (83,4%) стентов. В правую коронарную артерию (ПКА) и огибающую артерию (ОА) установлено по 4 (8,3%) стента. Во 2-й группе в ПНА имплантировано 25 (47,2%) перекрывающихся СЭС, в ПКА – 19 (35,8%) стентов, в ОА – 9 (17,0%) стентов.
При анализе ангиографических показателей (табл. 2) не выявлено статистически значимых различий по степени стеноза стентируемых КА (78,7±0,1% в 1-й группе против 79,8±1,3% – во 2-й; р=0,65) и степени стеноза на участке “overlap” (40,3±1,1% против 47,2±1,3%; p=0,59).
Средний диаметр стентируемой артерии в обеих группах превышал 3 мм (3,18±0,07 мм в 1-й группе и 3,07±0,04
Таблица 1
Клинические и демографические показатели (М±m)
|
Показатели |
1-я группа, СЭС+ГМС (n=24) |
2-я группа, СЭС+СЭС (n=25) |
p |
|
Возраст, годы |
53,6±1,5 |
52,9±2,2 |
<0,99 |
|
Половое соотношение, м.: ж. |
19 (100%):0 (0%) |
22 (88%):3(12%) |
0,67 |
|
Продолжительность ИБС, мес. |
47,3±8,9 |
49,6±11,4 |
<0,68 |
|
Стенокардия напряжения: |
0,86 |
||
|
I ФК |
0 |
0 |
|
|
II ФК |
5 (20,8%) |
6 (24,0%) |
|
|
III ФК |
16 (66,7%) |
17 (68,0%) |
|
|
IV ФК |
0 |
0 |
|
|
НС |
3 (12,5%) |
2 (8,0%) |
|
|
Перенесенный ИМ (>6 мес.) |
11 (45,8%) |
14 (56,0%) |
0,48 |
|
ХСН по NYHA: |
0,88 |
||
|
II ФК |
11 (45,8%) |
12 (48,0%) |
|
|
III ФК |
13 (54,2%) |
13 (52,0%) |
|
|
СД |
3 (12,5%) |
7 (28,0%) |
0,18 |
|
Гиперхолестеринемия |
21 (87,5%) |
24 (96,0%) |
0,28 |
|
АГ I–III степени |
22 (91,7%) |
23 (92,0%) |
0,97 |
|
ОНМК |
0 |
2 (8,0%) |
0,16 |
|
Курение |
18 (75,0%) |
16 (64,0%) |
0,40 |
|
Ожирение I–III степени |
6 (25,0%) |
8 (32,0%) |
0,59 |
Примечание: м. – мужчины; ж. – женщины; НС – нестабильная стенокардия; ХСН – хроническая сердечная недостаточность; АГ – артериальная гипертония;
ОНМК – острое нарушение мозгового кровообращения; СД – сахарный диабет.
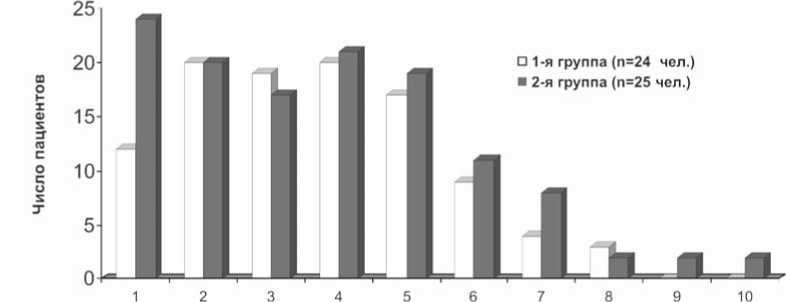
Рис. 1. Медикаментозная терапия у пациентов 1 и 2-й группы до стентирования
Реокклюзия на перекрывающихся участках стентов в 1-й группе ассоциировалась с развитием ИМ, во 2-й – с проявлениями НС. Поздняя потеря на участках “overlap” в группе СЭС+ГМС была в 3,5 раза выше по сравнению с группой СЭС+-СЭС и достигала в среднем 33,4±4,6% против 9,9±1,9% соответственно; p=0,0046.
мм – во 2-й; p=0,82). Длина участка поражения была в 1,3 раза больше в группе СЭС+СЭС по сравнению с группой СЭС+ГМС (32,2±1,9 мм в 1-й группе против 42,4±2,7 мм – во 2-й; р=0,005). Средняя длина стентированных участков также была статистически значимо выше в группе СЭС (38,4±1,5 мм в 1-й группе против 45,0±0,8 мм – во 2-й; р=0,01).
Согласно критериям оценки непосредственных ангиографических результатов, в 1-й группе успешными были признаны 23 вмешательства из 24 (95,8%). У одного пациента с наличием плотного эксцентрического стеноза степень остаточного стеноза составила 33,3% при кровотоке TIMI III. Во 2-й группе все процедуры были признаны удачными. Ни в одном из случаев в обеих группах не отмечали угрожающую диссекцию краевого участка артерии, а также кровоток менее TIMI III. Степень остаточного стеноза составила 13,04±3,92% в 1-й группе против 6,04±1,87% – во 2-й; р<0,004.
За время первичной госпитализации у 1 (4%) пациента 2-й группы развился повторный ИМ в результате подострого тромбоза СЭС на 5-е сут после имплантации. Больному выполнена экстренная ангиопластика целевого сосуда с хорошим ангиографическим результатом. За время первичной госпитализации летальных исходов не было.
Отдаленные (>30 сут) результаты прослежены у всех пациентов через 3–14 (в среднем 11,1± 0,6 мес.) после стентирования. Повторный ИМ в отдаленном периоде имел место всего у 1 (4,2%) пациента группы СЭС+ГМС. Причиной ИМ стала реокклюзия стентированного участка через 3 мес. после реваскуляризации (табл. 3). Пациенту выполнена повторная ангиопластика с хорошим ангиографическим результатом. Летальных исходов за время проспективного наблюдения не зарегистрировано.
Бинарный рестеноз на стентированном участке (с учетом 5 мм артерии у краев стентов) диагностирован в 7 (29,2%) случаях в 1-й группе и 2 (8%) – во 2-й (p=0,056). Частота бинарного рестеноза на перекрывающихся участках СЭС+ГМС достигала 5 (20,8%) случаев. В группе СЭС бинарный рестеноз диагностирован на 1 (3,8%) участке “overlap” (p=0,05).
Обсуждение
Как было отмечено ранее, проблема выбора оптимальной тактики лечения при протяженных коронарных стенозах является предметом споров и дискуссий в современной научной литературе. Возможности хирургической коррекции (коронарное шунтирование) при протяженном диффузном поражении КА ограничены. Это обусловлено как морфологически неблагоприятным поражением, затрудняющим процедуру шунтирования, так и наличием у таких больных тяжелой сопутствующей патологии, повышающей риск операции [3, 4].
При эндоваскулярном лечении наличие протяженного стеноза зачастую диктует необходимость последовательной имплантации нескольких стентов. Последовательная имплантация осуществляется двумя способами – с сохранением “непокрытого” между стентами участка (“gap” – в англоязычной литературе) и имплантации стентов перекрывающимися краями (техника “overlapping”). Непокрытый между стентами пораженный атеросклерозом участок артерии представляет собой потенциальную угрозу формирования клинически значимого рестеноза [8].
В настоящее время нет единого мнения относитель-
Таблица 2
Ангиографическая характеристика и динамика перекрывающихся (overlapping) участков стентов (М±m)
|
Показатели |
1-я группа, СЭС+ГМС, (n=24) |
2-я группа, СЭС+СЭС, (n=28) |
p |
|
Диаметр артерии, мм |
3,18±0,07 |
3,07±0,04 |
0,82 |
|
Длина участка поражения, мм |
32,2±1,9 |
42,4±2,7 |
0,005 |
|
Длина стеноза, мм |
18,3±2,9 |
23,8±2,8 |
0,04 |
|
Стеноз артерии, % |
78,7±0,1 |
79,8±1,3 |
0,65 |
|
Длина участка “overlap”, мм |
3,16±0,6 |
3,32±1,2 |
0,86 |
|
Диаметр стеноза на участке “overlap”, мм |
1,28±0,14 |
1,45±0,12 |
0,08 |
|
Диаметр стеноза на участке “overlap”, % |
40,3±1,1 |
47,2±1,3 |
0,59 |
|
Диаметр стента, мм |
3,13±0,06 |
3,17±0,03 |
0,21 |
|
Длина стентированного участка, мм |
38,4±1,5 |
45,0±0,8 |
0,01 |
|
Диаметр стентов на участке “overlap”, мм |
3,15±0,08 |
3,09±0,06 |
0,51 |
|
Остаточный стеноз на участке “overlap”, мм |
0,42±0,12 |
0,18±0,06 |
0,009 |
|
Остаточный стеноз на участке “overlap”, % |
13,04±3,92 |
6,04±1,87 |
0,004 |
Примечание: n – количество участков перекрывания стентов (“оverlap”).
но риска, обусловленного участками перекрывающихся краями стентов. Очевидно, что на участках “overlap” увеличивается “металлонасыщенность”, что может повышать риск рестенозов и тромбозов. Кроме того, в случае имплантации СЛП на участках “overlap” увеличивается доза антипролиферативного препарата, что может привести к токсическому эффекту, который проявляется резким угнетением митотического деления клеток, замедлением процесса формирования неоинтимы, истончением стенки сосуда и возникновением аневризматических расширений просвета артерии. Создается условие для развития поздних и очень поздних тромбозов стентированных участков [1].
Высокую частоту рестенозов перекрывающихся ГМС (у 41% пациентов через 6 мес.) отмечают в своих работах S.H. Lee c соавт. [12]. Для снижения рестеноза ряд авторов рекомендует последовательную имплантацию СЛП [5, 6, 11]. В 2007 г. F. Burzotta c соавт. обсуждают вопрос сочетанного использования двух типов стентов – с лекарственным покрытием и ГМС [7]. В исследовании SIRTAX через 8 мес. после имплантации перекрывающихся краями стентов потеря просвета достигала 0,33±0,61 мм против 0,15±0,38 мм в группе с имплантацией 1 стента и 0,18±0,43 мм в группе с имплантацией нескольких стентов без зон перекрытия. Через 3 года частота развития неблагоприятных сердечно-сосудистых событий достигала 24,4% против 14,0% и 21,1% в исследуемых группах больных соответственно; p<0,01. Повторная реваскуляризация выполнена 25 (20,2%) пациентам в группе “overlapping”, при этом в большинстве случаев максимальное сужение просвета наблюдалось именно в зоне перекрытия двух стентов, частота рестеноза здесь достигала 53,1% от всех случаев рестеноза стентов [13]. О высоком риске интралюминальных тромбозов после последовательной имплантации перекрывающихся краями пакли-таксель-элюирующих стентов сообщалось в патогисто-логическом исследовании T. Shinke и соавт., выполненном на лабораторных животных [14]. Через 1 мес. в группе СЛП поздняя потеря составила 0,46±0,63 мм против 1,30±0,50 мм в группе ГМС; p=0,01. При макроскопическом исследовании в стентах с паклитакселем определялись множественные тромбозы (p<0,001), причем преимущественно в зонах “overlap”, в то время как в группе ГМС регистрировались единичные внутренние тромбы.
Таблица 3
Результаты контрольной ангиографии перекрывающихся участков стентов через 11,1±0,6 мес. после стентирования
|
Показатели |
1-я группа, СЭС+ГМС, (n=24) |
2-я группа, СЭС+СЭС, (n=28) |
p |
|
Поздняя потеря на участке “overlap”, мм |
1,06±0,14 |
0,32±0,05 |
0,0021 |
|
Поздняя потеря на участке “overlap”, % |
33,4±4,6 |
9,9±1,9 |
0,0046 |
|
Общая потеря на участке “overlap”, мм |
1,23±0,15 |
0,51±0,10 |
0,0009 |
|
Общая потеря на участке “overlap”, % |
38,4±4,8 |
16,4±3,5 |
0,0004 |
|
Рестеноз >50% и <70% |
2 (8,3%) |
0 |
0,12 |
|
Рестеноз >70% |
2 (8,3%) |
0 |
0,12 |
|
Окклюзия |
1 (4,2) |
1 (3,6%) |
0,91 |
|
Всего рестенозов > 50% |
5 (20,8%) |
1 (3,6%) |
0,05 |
Примечание: n – количество участков перекрывания стентов (“оverlap”).
В исследовании T. Feng и соавт., включавшем 22 пациента с имплантацией перекрывающихся краями СЭС, при проведении оптической когерентной томографии через 12 мес. после вмешательства установлено, что полностью покрыты неоинтимой только 90% поверхности стентов. Различий по толщине неоинтимы на участках “overlap” и неперекрывающихся сегментах не выявлено. Сегменты, непокрытые неоинтимой, чаще регистрировались на участках “overlap”, но статистической значимости по количеству страт не достигнуто (1,4% страт на неперекрыва-ющихся участках против 5,2% – на участках “overlap”; p>0,05). Для предотвращения тромбозов на непокрытых неоинтимой участках авторы рекомендовали пролонгированную дезагрегантную терапию [15].
В нашем исследовании техника последовательной имплантации перекрывающимися краями стентов Cypher применена у 25 больных ИБС с диффузным коронарным атеросклерозом. Включенные в исследование пациенты представляли собой крайне тяжелые в клиническом и морфологическом плане группы. У подавляющего большинства клинике коронарной недостаточности сопутствовала тяжелая сердечная недостаточность, обусловленная морфологически неблагоприятным поражением КА. В ангиографической картине преобладало многососудистое стенозирующее поражение коронарного русла. Степень остаточного стеноза после реваскуляризации на участке “overlap” составляла 13,04±3,92% в 1-й группе и 6,04±1,87% – во 2-й (р<0,004). Несмотря на длинные участки стентирования и последовательную имплантацию нескольких стентов в одну артерию, мы не наблюдали случаев острого тромбоза в обеих группах больных. Подострый тромбоз стентов диагностирован у 0% пациентов в 1-й группе и у 1 (4%) больного – во 2-й (р=0,32). Таким образом, теоретические предпосылки увеличения частоты острых и подострых тромбозов СЭС в нашем исследовании не подтвердились.
Как отмечалось ранее, одним из факторов, ограничивающим отдаленную эффективность последовательной имплантации стентов, является гиперпролиферация на участке “overlap”. В нашем исследовании поздняя потеря на участках overlap была в 3 раза выше в 1-й группе по сравнению со 2-й (33,4±4,6% против 9,9±1,9%; p=0,0046), что свидетельствует о высокой степени гиперплазии неоинтимы на участках перекрывающихся краев стентов только в случае сочетания СЭС и ГМС. Частота бинарного рестеноза здесь составила 20,8% против 3,6% в случае имплантации только стентов с антипролиферативным покрытием (p=0,05). Необходимо отметить, что частота рестеноза 20,8% через 12 мес. после имплантации стента с лекарственным покрытием является недопустимо высокой, в связи с чем сочетанное применение перекрывающихся краями СЭС и ГМС в рутинной практике следует исключить.
Заключение
-
1. Эндоваскулярная реваскуляризация протяженных стенозов КА с применением двух и более перекрывающихся краями СЭС является клинически эффективной и безопасной.
-
2. Последовательная имплантация стентов Cypher в артерии диаметром >3 мм, при длине стентированного участка до 45 мм и длине участка “overlap” 3 мм, с выполнением постдилатации участка перекрытия не приводит к увеличению частоты рестенозов и тромбозов стентированного участка.
-
3. Сочетанное использование СЭС и ГМС при последовательном стентировании протяженных стенозов КА, сопровождается повышением частоты рестенозов на участках “overlap” по сравнению с имплантацией перекрывающихся СЭС.
Список литературы Отдаленная эффективность последовательной имплантации перекрывающихся краями сиролимус-элюирующих стентов у больных ишемической болезнью сердца с протяженными стенозами коронарных артерий
- Бабунашвили А.М., Юдин И.Е., Дундуа Д.П. и др. Стенты с лекарственным покрытием при лечении диффузных атеросклеротических поражений коронарных артерий//Consilium medicum. -2006. -Т. 1, №4. -С. 56-52.
- Бокерия Л.А., Гудкова Р.Г. Сердечно&сосудистая хирургия 2008. -М.: НЦССХ им. Бакулева РАМН, 2009. -162 с.
- Марков В.В., Баев А.Е., Варваренко В.И. Эффективность стентирования диффузного атеросклеротического поражения коронарного русла сиролимус-элюирующими стентами//Сибирский медицинский журнал (Томск). -2010. -№ 4 (1). -С. 37-43.
- Савченко А.П., Черкавская О.В., Руденко Б.А. и др. Интервенционная кардиология. Коронарная ангиография и стентирование: руководство. -М.: ГЭОТАР-Медиа, 2010. -343 с.
- Aoki J., Ong A., Rodriguez Granillo G. et al. "Full metal jacket" (stented length > or =64 mm) using drug&eluting stents for de novo coronary artery lesions//Am. Heart J. -2005. -Vol. 150(5). -Р. 994-999.
- Balakrishnan B., Tzafriri A.R., Seifert P. et al. Strut position, blood flow, and drug deposition: implications for single and overlapping drug&eluting stents//Circulation. -2005. -Vol. 111(22). -Р. 2958-2965.
- Burzotta F., Siviglia M., Altamura L. et al. Overlapping heterogenous drug&eluting stents and of overlapping drug-eluting and bare metal stents//Am. J. Cardiol. -2007. -Vol. 99(3). -Р. 364-368.
- Cook S., Wenaweser P., Togni M. et al. Incomplete Stent Apposition and Very Late Stent Thrombosis After Drug&Eluting Stent Implantation//Circulation. -2007. -Vol. 115. -P. 2426-2434.
- Daly C.А., De Stavola B., Sendon J.L. et al. Predicting prognosis in stabile angina -results from the Euro heart survey of stabile angina: prospective observational study//Br. Med. J. -2006. -Vol. 332. -P. 262-267.
- Finn A.V., Kolofgie D.F., Harnek J. et al. Differential response of delayed healing and persistent inflammation at sites of overlapping sirolimus&or paclitaxel&eluting stents//Circulation. -2005. -Vol. 112. -P. 270-278.
- Kereiakes D.J., Wang H., Popma J.J. et al. Periprocedural and late consequences of overlapping Cypher sirolimuseluting stents: pooled analysis of five clinical trials//J. Am. Coll. Cardiol. -2006. -Vol. 48(1). -Р. 21-31.
- Lee S.H., Jang Y., Oh S.J. et al. Overlapping vs. one long stenting in long coronary lesions//Catheter. Cardiovasc. Interv. -2004. -Vol. 62(3).-Р. 298-302.
- Raber L., Juni P. et al. Impact of Stent Overlap on Angiographic and Long-Term Clinical Outcome in Patients Undergoing Drug-Eluting Stent Implantation//J. Am. Coll. Cardiol. -2010. -Vol. 55. -P. 1178-1188.
- Shinke T., Li J., Chen J.P. High Incidence of Intramural Thrombus After Overlapping Paclitaxel-Eluting Stent Implantation//Circulation: Cardiovascular Interventions. -2008. -Vol. 1. -P. 28-35.
- Tian F., Chen Y.D., Sun Z.Y. Evaluation of neointimal coverage of overlapping sirolimus-eluting stents by optical coherence tomography//Chinese Medical J. -2009. -Vol. 122. -No. 6. -P. 670-674.
- Virmani R., Guagliumi G., Farb A. et al. Localized hypersensitivity and late coronary thrombosis secondary to a sirolimus&eluting stent: should we be cautious//Circulation. -2004. -Vol. 109. -P. 701-705.


