Отдаленные результаты комбинированного этапного подхода в лечении больных с фибрилляцией предсердий и коронарным шунтированием
Автор: Богданов Юрий Игоревич, Вечерский Юрий Юрьевич, Баталов Роман Ефимович, Затолокин Василий Викторович, Попов Сергей Валентинович
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 1 т.32, 2017 года.
Бесплатный доступ
Статья посвящена проблеме хирургического лечения ишемической болезни сердца (ИБС) в сочетании с фибрилляцией предсердий (ФП). Несмотря на увеличение хирургических вмешательств по коррекции ФП во время коронарного шунтирования (КШ), в среднем хирургическая аблация ФП выполняется лишь у 27,5% пациентов во время КШ. В статье приведены отдаленные результаты одноцентрового, проспективного исследования по оценке эффективности комбинированного этапного подхода в лечении больных с ФП и КШ в сравнении с одноэтапной хирургической аблацией ФП.
Ишемическая болезнь сердца, фибрилляция предсердий, коронарное шунтирование, хирургическая аблация
Короткий адрес: https://sciup.org/14920176
IDR: 14920176 | УДК: 616.12-008.313.2-089
Long-term results of combined stepwise approach in treatment of patients with atrial fibrillation and coronary artery bypass grafting
The article is devoted to surgical treatment of the coronary artery disease in combination with atrial fibrillation. Despite the growing number of surgical atrial fibrillation ablation procedures during coronary artery bypass grafting surgery, only 27.5% of patients receive intervention for atrial fibrillation correction in addition to CABG. Article comprises long-term results of the prospective, single-center trial on clinical efficacy of combined stepwise approach in treatment of patients with atrial fibrillation and CABG in comparison with surgical ablation alone.
Текст научной статьи Отдаленные результаты комбинированного этапного подхода в лечении больных с фибрилляцией предсердий и коронарным шунтированием
ФП является наиболее распространенным видом нарушения ритма сердца среди наджелудочковых тахиаритмий. По данным многоцентровых клинических исследований выявлено, что распространенность ФП составляет около 0,5% в возрасте от 50 до 59 лет, после 75 лет – до 9%, причем чаще регистрируется у мужчин. По данным Фремингемского исследования, наличие ФП увеличивает риск инсульта в 5 раз. У больных ИБС или сердечной недостаточностью ФП удваивает риск инсульта у мужчин, а у женщин утраивает. Для лиц в возрасте от 80 до 89 лет ФП является единственным сердечно-сосудистым заболеванием, которое независимо от других факторов влияет на частоту инсультов. Атрибутивный риск инсульта снижается с возрастом при всех сердечно-сосудистых состояниях, кроме ФП, при которой риск значительно увеличивается [1].
В ретроспективном исследовании, включавшем 21534 пациента после операции аортокоронарного шунтирования (АКШ), было показано, что ФП в предоперационном периоде является независимым предиктором ранней и отдаленной летальности [2]. Несколько когортных исследований признали ФП маркером для повышенной летальности [3]. Средний возраст пациентов, которым выполняется операция АКШ, увеличивается, следовательно, увеличивается число пациентов с ФП, подлежащих операции АКШ. По данным одного из исследований, распространенность ФП у пациентов с изолированной АКШ составляет от 2,7% у молодых пациентов до 22,3% для пациентов в возрасте 75–80 лет. Как правило, пациенты с ФП, подвергающиеся операции АКШ, более пожилые, со сниженной фракцией выброса (ФВ), они чаще страдают сахарным диабетом и артериальной гипертензией по сравнению с пациентами без ФП [5].
Тем не менее ФП как переменная никогда не входила в калькуляторы расчета периоперационного риска, такие как Euroscore и STS score. ФП особенно ухудшает прогноз у кардиохирургических пациентов с низкой ФВ и хронической сердечной недостаточностью [3, 4].
Материал и методы
Данное исследование относится к проспективным, одноцентровым, контролируемым исследованиям. В НИИ кардиологии (Томск) за период с 2012 по 2015 гг. выполнено 50 операций по коррекции ФП во время операции КШ. В исследование включены больные в возрасте от 18 до 90 лет с верифицированной ИБС, показаниями к КШ и подтвержденной ФП. В исследование включено 28 пациентов (24 мужчины и 4 женщины) в возрасте от 44 до 76 лет (средний возраст – 64,1±7,8 лет) с персистирующей и длительно персистирующей формами ФП и ИБС (табл. 1).
При поступлении в стационар большинство пациентов предъявляли жалобы на перебои в работе сердца (95%), учащенное сердцебиение, давящие боли за грудиной и одышку (91%). Все пациенты получали антиарит-мические терапию на догоспитальном этапе. Однако в 95% она оказалась неэффективна. На госпитальном этапе всем пациентам проводилось следующее обследование: электрокардиограмма (ЭКГ) в 12 отведениях, клинический и биохимический анализ крови, трансторакальная эхокардиография, чреспищеводная эхокардиография для исключения тромбов в ушке левого предсердия, коронарография выполнялась при ее отсутствии на догоспитальном этапе.
В зависимости от методики пациенты были распределены на 2 группы. Пациентам первой группы выполнялась прямая реваскуляризация миокарда и эпикардиальная биполярная радиочастотная аблация легочных вен и крыши левого предсердия с использованием биполярных электродов Atricure и резекцией ушка левого предсердия, а также электрофизиологического исследования через 16±7 дней после операции с катетерной эндокардиальной антральной изоляцией легочных вен, в случае обнаружения восстановления проведения в легочные вены
Таблица 1
Клиническая характеристика пациентов
|
Показатели Эпи+эндокардиальная аблация (n=18) |
Эпикардиальная аблация (n=10) |
|
|
Возраст 64±4 лет |
63±3,3 лет |
|
|
Длительно персистирующая ФП |
11 |
6 |
|
Персистирующая ФП |
7 |
4 |
|
Длительность пароксизма (мес.) |
9±3,2 |
10±2 |
|
ФВ% 65±2% |
62±3% |
|
|
Средние размеры ЛП, мм |
58±1,6 |
53,1±4,4 |
|
Аритмический анамнез (годы) |
3±0,7 |
3±1,3 |
|
NYHA class% I |
29,7% |
32,3% |
|
II |
70,3% |
66,7% |
|
Инфаркт в анамнезе% |
28,8% |
33,3% |
|
Объем поражения коронарного |
||
|
русла Syntax (средний балл) |
24,5 |
25,3 |
(n=18). Во второй (контрольной) группе пациентов выполнялась прямая реваскуляризация миокарда и только биполярная эпикардиальная аблация по вышеописанной схеме (n=10). Всем пациентам выполнена перевязка ушка левого предсердия для предотвращения образования тромбов. Результаты оценивались по суточному мониторированию ЭКГ.
Результаты и обсуждение
В раннем послеоперационном периоде и на 30-е сутки после операции пациентам проведено суточное мониторирование ЭКГ. У 1 пациента основной группы (5,6%) и у 3 пациентов контрольной группы (30%) зарегистрированы рецидивы ФП на госпитальном этапе. По данным ЭФИ, полная электрическая изоляция всех легочных вен после биполярной эпикардиальной аблации была достигнута у 5 пациентов (27,7%). В остальных случаях было выявлено восстановление проведения в легочные вены (72,3%). Во всех случаях обнаружения восстановления проведения выполнялась антральная изоляция легочных вен. Согласно последним данным, восстановление проведения в легочных венах очень часто наблюдается среди пациентов, свободных от ФП. Это было подчеркнуто в других исследованиях на пациентах без клинических рецидивов аритмии. Эти результаты подтверждают необходимость дальнейшего изучения роли восстановления проведения в легочных венах в развитии рецидивов после процедуры аблации. По результатам наблюдения, через 12 месяцев после вмешательства синусовый ритм сохранялся у 15 пациентов группы этапного подхода (83,3%), по сравнению с 6 пациентами контрольной группы (60%), рисунок 1. Осложнение в виде кровотечения зарегистрировано у одного пациента основной группы (5,6%), что потребовало ревизии в первые сутки после операции и переливания свежезамороженной плазмы (табл. 2). Источником кровотечения являлась коллатераль левой внутренней грудной артерии. Летальных исходов в обеих группах не зарегистрировано.
Заключение
Одним из преимуществ эндокардиальной аблации является возможность проведения ЭФИ, так как у пациентов после операции АКШ возникает необходимость верификации электрофизиологических изменений после эпикардиальной аблации.
За последнее десятилетие катетерная аблация и хирургическое лечение ФП достигли значительных результатов. Разработка новых источников энергии и миниин-вазивных подходов вывели лечение ФП на качественно новый уровень. На сегодняшний день аблация ФП при операции КШ улучшает прогноз без значительного увеличения операционного риска для пациента.
Хотя рутинное интраоперационное картирование в настоящее время недоступно для контроля эффективности аблации во время кардиохирургической операции, по всей вероятности, стратегия, основанная на комбинировании преимуществ хирургического метода при операции КШ и электрофизиологического исследования с
Таблица 2
Полученные результаты
|
Показатели |
Эпи+эндокардиальная аблация (n=18) |
Эпикардиальная аблация (n=10) |
|
Рецидив ФП (30 дней) |
5,6% |
30% |
|
Синусовый ритм через 12 мес. |
83,3% (p<0,05) |
60% (p<0,05) |
|
Осложнение (кровотечение) |
5,6% |
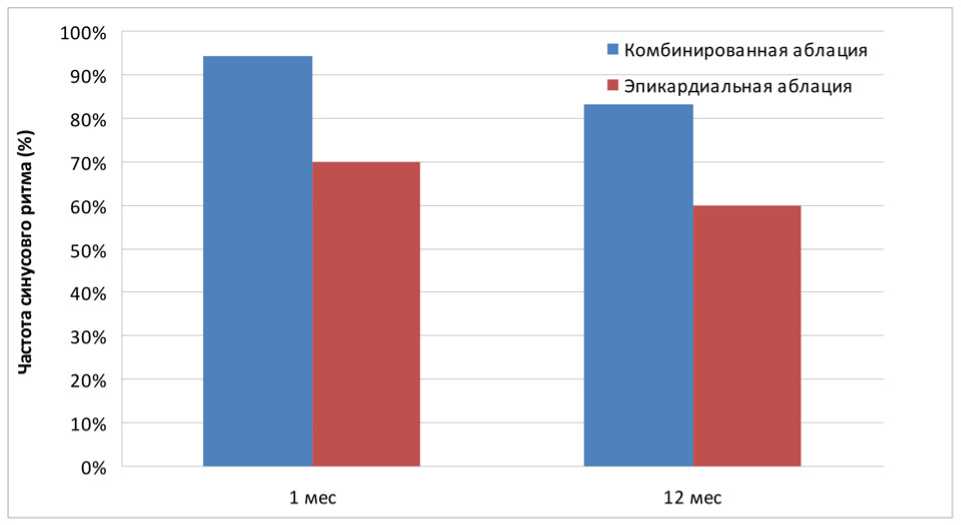
Рис. 1. Эффективность коррекции ФП через 12 мес.
катетерной аблацией, в раннем послеоперационном периоде способна улучшить результаты путем достижения большей трансмуральности, устранения прорывов абла-ционных линий и нанесения дополнительных воздействий на этапе электрофизиологического исследования и катетерной аблации.
Список литературы Отдаленные результаты комбинированного этапного подхода в лечении больных с фибрилляцией предсердий и коронарным шунтированием
- Wolf P.A., Abbott R.D., Kannel W.B. Atrial fibrillation as an independent risk factor for Stroke: the Framingham Study//Stroke. -1991. -No. 22. -P. 983-988.
- Saxena A., Kapoor J., Dinh D.T. et al. Preoperative atrial fibrillation is an independent predictor of worse early and late outcomes after isolated coronary artery bypass graft surgery//J. Cardiol. -2015. -Vol. 65. -P. 224-229.
- Benjamin E.J., Wolf P.A., D’Agostino R.B. et al. Impact of atrial fibrillation on the risk of death: the Framingham Heart Study//Circulation. -1998. -Vol. 98. -P. 946-952.
- Quader M.A., McCarthy P.M., Gillinov A.M. et al. Does preoperative atrial fibrillation reduce survival after coronary artery bypass grafting?//Ann. Thorac. Surg. -2004. -Vol. 77. -P. 1514-1524.
- Ad N., Barnett S.D., Haan C.K. et al. Does preoperative atrial fibrillation increase the risk for mortality and morbidity after coronary artery bypass grafting?//J. Thorac. Cardiovasc. Surg. -2009. -Vol. 137. -P. 901-906.


