Отдаленный прогноз неблагоприятных сердечнососудистых событий у пациентов с хронической сердечной недостаточностью в зависимости от полиморфизма RS1143634 гена интерлейкина-1
Автор: Хазова Е.В.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 4 т.39, 2024 года.
Бесплатный доступ
Течение и прогноз хронической сердечной недостаточности сопряжены с активацией воспалительных каскадов, выраженность которых имеет генетическую детерминированность.Цель: анализ неблагоприятных сердечно-сосудистых событий у пациентов с хронической сердечной недостаточностью на протяжении 5 лет в зависимости от полиморфизма rs1143634 гена интерлейкина-1β.Материал и методы. Изучены клинические признаки, проведено генотипирование по полиморфному локусу rs1143634 гена IL-1β пациентов с хронической сердечной недостаточностью ишемического генеза (n = 445, средний возраст - 66,4 ± 10,4 года). Информация об исходах пациентов в течение 5 лет получена методом телефонного опроса по конечным точкам: смерть от всех причин, сердечно-сосудистая смерть. Смертельные и несмертельные сердечно-сосудистые события сформировали комбинированную конечную точку. Время до наступления события анализировали методом Каплана - Мейера; отношение рисков - регрессией Кокса. Статистическую обработку проводили в программах Jamovi, R 4.3.1.Результаты и выводы. Встречаемость генотипов полиморфизма rs1143634 гена IL-1β у пациентов с хронической сердечной недостаточностью и группы генетического контроля не различалась и была соразмерна с теоретически ожидаемым равновесием Харди - Вайнберга. Носители ТТ генотипа характеризовались большим уровнем воспаления, развитием инфаркта миокарда в молодом возрасте. У пациентов с хронической сердечной недостаточностью ТТ генотипа риск смерти от всех причин был выше в 2,85 раза, достижения комбинированной конечной точки - в 3,3 раза, смертельного мозгового инсульта - в 17,1 раза в сравнении с CC генотипом, в 14,9 раза - в сравнении с СТ генотипом. У пациентов с хронической сердечной недостаточностью и хронической болезнью почек ТТ генотипа риск смерти от мозгового инсульта был в 29,33 раза выше, чем у пациентов СС генотипа, в 29,12 раза - чем у пациентов СТ генотипа. У пациентов с хронической сердечной недостаточностью в сочетании с сахарным диабетом частота госпитализаций по причине декомпенсации сердечной деятельности при ТТ генотипе была выше, чем при СС и СТ генотипах (χ2 = 6,33; р = 0,042).
Хроническая сердечная недостаточность, полиморфизм rs1143634 гена il-1β, прогноз, кардиоваскулярные осложнения
Короткий адрес: https://sciup.org/149147161
IDR: 149147161 | УДК: 616.12-008.46-002.2-079.3:575.174.015.3 | DOI: 10.29001/2073-8552-2024-39-4-142-149
Long-term prognosis of adverse cardiovascular events in patients with chronic heart failure depending on the RS1143634 polymorphism of the interleukin-1 gene
The course and prognosis of chronic heart failure (CHF) are associated with the activation of inflammatory cascades, the severity of which is genetically determined.Aim: To analyze adverse cardiovascular events in patients with chronic heart failure over 5 years depending on the rs1143634 polymorphism of the interleukin-1β gene.Material and Methods. Clinical signs were studied, genotyping was carried out at the polymorphic locus rs1143634 of the IL-1β gene in patients with CHF of ischemic origin (n = 445, average age 66.4 ± 10.4 years). Information on patient outcomes over 5 years was obtained by telephone interview with endpoints: all-cause death, cardiovascular death, fatal and non-fatal cardiovascular events formed a composite endpoint. Time to event was analyzed using the Kaplan-Meier method; hazard ratio - Cox regression. Statistical processing was carried out in the Jamovi, R 4.3.1 programs.Results and conclusions. The occurrence of genotypes of the rs1143634 polymorphism of the IL-1β gene in patients with CHF and the genetic control group did not differ and was commensurate with the theoretically expected Hardy-Weinberg equilibrium. Carriers of the TT genotype were characterized by a high level of inflammation and the development of myocardial infarction at a young age. In patients with CHF of the TT genotype, the risk of death from all causes is 2.85 times higher, achieving the combined endpoint is 3.3 times higher, fatal cerebral stroke is 17.1 times higher compared to CC, 14.9 times higher than compared to ST genotype. In patients with CHF and chronic kidney disease of the TT genotype, the risk of death from cerebral stroke is 29.33 times higher than the CC genotype, and 29.12 times higher for the CT genotype. In patients with CHF in combination with diabetes mellitus, the frequency of hospitalizations due to cardiac decompensation in the TT genotype is higher than in the CC and CT genotypes (χ2 = 6.33, p = 0.042).chronic heart failure; rs1143634 polymorphism of the IL-1β gene; prognosis; cardiovascular complications
Текст научной статьи Отдаленный прогноз неблагоприятных сердечнососудистых событий у пациентов с хронической сердечной недостаточностью в зависимости от полиморфизма RS1143634 гена интерлейкина-1
Генетические механизмы распространенных социально значимых многофакторных заболеваний с генетической предрасположенностью, к которым в том числе относится и хроническая сердечная недостаточность, подвергаются интенсивному изучению. В генную сеть хронической сердечной недостаточности, согласно существующим представлениям об этиологии и патогенезе, включают гены-кандидаты, кодирующие белки ренин-ан-гиотензин-альдостероновой системы, контролирующие липидный обмен, гены белков дисфункции эндотелия, коагуляции крови, фибринолиза, а также гены факторов роста и воспаления, участвующие в созревании и разрыве атеросклеротической бляшки в коронарных сосудах. Не вызывает сомнений участие провоспалительных цитокинов в патофизиологических механизмах кардиоваску- лярного риска и неблагоприятного течения хронической сердечной недостаточности [1, 2]. Интересен провоспа-лительный цитокин, интерлейкин-1 бета (IL-1β), инициирующий множество биологических каскадов – важных компонентов воспалительной реакции, а также атероге-неза [3]. Вариабельность воспалительного ответа может иметь генетическую детерминированность.
Однонуклеотидный полиморфизм rs1143634 гена IL-1β лоцируется в регионе 2q14.1 [4, 5] и заключается в замене в положении + 3954 цитозина на тимин, приводя к появлению низкочастотного аллеля Т, ассоциированного с гиперпродукцией и повышением сывороточного уровня IL-1β [6-8]. Минорный аллель Т определяется у 24,8% популяции Европы [9]. Анализ публикаций позволяет судить о функциональной значимости аллеля Т полиморфизма rs1143634 гена IL-1β в развитии атеросклероза коронарных артерий, ишемической болезни сердца [10–12].
Описана связь аллеля Т полиморфизма rs1143634 гена IL-1β с повышенным риском формирования артериальной гипертензии [13]. Противоположные данные приводятся в серии публикации в отношении риска развития хронической сердечной недостаточности, указывающие на больший риск при наличии аллеля С и генотипа СС полиморфизма rs1143634 гена IL-1β (OШ = 3,798: ДИ: 1,060–13,607), тогда как аллель Т (OШ = 0,53; ДИ: 0,360– 0,780), генотипы СТ (OШ = 0,453; ДИ: 0,275–0,746) и ТТ (OШ = 0,263; ДИ: 0,073–0,943) идентифицированы как протективные факторы [14, 15]. Таким образом, в настоящее время нет единого мнения о влиянии полиморфизма rs1143634 гена IL-1β на течение и прогноз хронической сердечной недостаточности.
Цель работы: анализ неблагоприятных сердечно-сосудистых событий у пациентов с хронической сердечной недостаточностью на протяжении 5 лет в зависимости от полиморфизма rs1143634 гена IL-1β.
Материал и методы
Проведено клинико-генетическое исследование 445 пациентов с хронической сердечной недостаточностью (235 мужчин и 210 женщин, средний возраст – 66,4 ± 10,4 года) и 118 пациентов группы генетического контроля. Все включенные в исследование пациенты были европеоидной расы, проживали в г. Казань, добровольно подписали форму информированного согласия. Проведение научной работы одобрено локальным этическим комитетом Казанского ГМУ Минздрава России (протокол № 5 от 23.05.2023 г.). В исследование включались пациенты старше 18 лет с верифицированной хронической сердечной недостаточностью, согласно Российскими рекомендациями по диагностике и лечению хронической сердечной недостаточности1. Критериями невключения были инфаркт миокарда, коронарное вмешательство, мозговой инсульт, декомпенсация сердечной недостаточности в течение 3 мес., предшествующих включению в исследование, гемодинамически значимые врожденные / приобретенные пороки сердца, наличие состояния с ожидаемой продолжительностью жизни менее одного год, беременность или лактация женщины, алкогольная / наркотическая зависимость, выраженные когнитивные расстройства.
Гематологическое (клиническое и биохимическое) исследование пациентов группы исследования проводилось в рамках рутинной клинической практики на базе Городской клинической больницы № 7 имени М.Н. Садыкова (г. Казань). Уровень N-терминального фрагмента мозгового натрийуретического пептида определялся в сыворотке крови иммунохемилюминесцентным методом на автоматическом иммунохимическом анализаторе Vitros 3600. Высокочувствительный С-реактивный белок определялся в сыворотке крови иммунотурбидиметриче-ским методом на анализаторе Roche Cobas 8000 с биохимическим модулем c702. По уровню высокочувствительного С-реактивного белка ранжировался относительный воспалительный риск развития и прогрессирования кардиоваскулярных событий: низкий (высокочувствительный С-реактивный белок < 1 мг/л), средний (1– 3 мг/л) и высокий (> 3 мг/л) [17].
Толерантность к физической нагрузке определяли по данным теста 6-минутной ходьбы, оценивали параметры электрокардиограммы. Размеры камер сердца и сократительную функции миокарда определяли при проведении трансторакальной эхокардиоскопии: при фракции выброса левого желудочка ≥ 50% диагностировали сердечную недостаточность с сохраненной (СНсФВ), при 40– 49% – с умеренно сниженной (СНу/сФВ), при < 40% – с низкой (СНнФВ) фракцией выброса2. Препарат дезоксирибонуклеиновой кислоты из лимфоцитов венозной крови выделяли сорбентным методом согласно инструкции производителя «ДНК-Сорб-В» (ФБУН ЦНИИ эпидемиологии Роспотребнадзора, Россия). Полимеразную цепную реакцию проводили в реальном времени по полиморфному локусу rs1143634 гена IL-1β в соответствии с инструкцией, прилагаемой к реагенту «ТестГен» (Ульяновск, Россия). Полиморфные сайты геномной ДНК генотипиро-вали на амплификаторе CFX96 (БиоРад, США).
Информация об исходах пациентов в течение 5 лет получена посредством телефонного опроса по конечным точкам: смерть от всех причин, сердечно-сосудистая смерть. Смертельные и несмертельные сердечно-сосудистые события сформировали комбинированную конечную точку. При отсутствии событий в течение 5 лет констатировалась бессобытийная выживаемость.
Для анализа и визуализации первичных данных использовали лицензионные программы Jamovi (version 2.3.16) [Computer Software], R 4.3.1 (R Foundation for Statistical Computing, Вена, Австрия). Нормальность распределения количественных переменных проводили с помощью критерия Шапиро – Уилка ( n ≤ 50) или критерия Колмогорова – Смирнова ( n > 50). Непрерывные переменные при нормальном распределении указаны как среднее и стандартное отклонение ( М ± SD ), при отличном от нормального – медиана и межквартильный диапазон ( Ме [25; 75%]). Категориальные переменные приведены в виде абсолютного значения и процента. Межгрупповые различия количественных переменных оценивали тестом Стьюдента либо тестом Манна – Уитни, категориальных – критерием χ2 Пирсона. Соответствие распределения генотипов равновесию Харди – Вайнберга определяли с помощью теста Фишера в Excel. Выявляли ассоциации по отношению шансов (ОШ) c определением 95% доверительного интервала (ДИ). Сравнительный анализ в отношении времени до наступления события проводили методом Каплана – Мейера и лог-рангового теста, для оценки отношения рисков (ОР) и соответствующих 95% ДИ – пропорциональных рисков Кокса. Значимыми различия считали при p < 0,05.
Результаты и обсуждение
У всех включенных в исследование пациентов хронической сердечной недостаточности предшествовала ишемическая болезнь сердца, в том числе у 82,3% пациентов в сочетании с артериальной гипертензией. Длительность хронической сердечной недостаточности составила 8 [5; 10] лет, уровень N-терминального фрагмента мозгового натрийуретического пептида – 825 [338;1209] пг/мл. Функциональный класс (ФК) хронической сердечной недостаточности определялся с учетом результатов теста 6-ми- нутной ходьбы: I ФК – 2,6%, II ФК – 34,3%, III ФК – 43,5%, IV ФК – 19,6% пациентов. В исследуемой когорте превалировала СНсФВ (67%); СНу/сФВ и СНнФВ были характерны для 19 и 14% пациентов соответственно.
До включения в исследование 45,1% пациентов перенесли инфаркт миокарда, 13,5% – коронарное вмешательство, 8,1% – мозговой инсульт. Факторы риска представлены отягощенной наследственностью по сердечно-сосудистым заболеваниям (37,3%), табакокурению (16,6%). Заболеваниями, сопутствующими хронической сердечной недостаточности, являлись:
– хроническая болезнь почек – 40%, (скорость клубочковой фильтрации (СКФ) по CKD-EPI 65,6 ± 19,2 мл/ мин/1,73 м2; умеренное снижение СКФ (С3А) было у 45,8%, существенное снижение (С3Б) – у 20%, резкое снижение (С4) и терминальная хроническая болезнь почек (С5) – у 3 и 2,5% пациентов соответственно. На момент госпитализации ни один пациент не получал заместительной почечной терапии);
– фибрилляция предсердий – 26,7% (в том числе постоянная форма – у 53,5%, пароксизмальная – у 43,3%, персистирующая – у 3,2% пациентов);
– хроническая обструктивная болезнь легких – 22,8% (по степени обструкции легких пациенты с хронической сердечной недостаточностью представлены следующим образом: легкая степень тяжести – 33,8%, средняя степень – 36,4%, тяжелая степень – 29,9%),
– сахарный диабет – 21,8%.
На момент включения в исследование 19,1% пациентов сообщили, что не принимают медикаментозную терапию на постоянной основе. Ингибиторы ангиотен-зинпревращающего фермента применяли 49,6% пациентов, блокаторы рецепторов ангиотензина II – 17,4%, β -адреноблокаторы – 48,7%, антагонисты минералокортикоидных рецепторов – 13,9% пациентов с хронической сердечной недостаточностью. Реже в структуре медикаментозной терапии присутствовали дезагреганты (35%), диуретики (34,6%), антагонисты кальция (22,7%), нитраты (15,7%), сердечные гликозиды (8,9%). На липид-сни-жающей терапии статинами не менее 1 года находились 28,8% пациентов.
Исследование частот встречаемости генотипов полиморфизма rs1143634 гена IL-1β у пациентов с хронической сердечной недостаточностью и группы генетического контроля не выявило различий: СС – 58,7 и 61%, СТ – 36,2 и 34,7%, ТТ – 5,2 и 4,2% ( χ2 = 0,304; р = 0,859) и было соразмерно с теоретически ожидаемым равновесием Харди – Вайнберга ( χ2 = 0,06; р = 0,81 и χ2 = 0,07; р = 0,78).
Сравнение распространенности факторов риска и клинических характеристик пациентов с хронической сердечной недостаточностью СС, СТ и ТТ генотипов полиморфизма rs1143634 гена IL-1β не выявило различий, за исключением дебюта инфаркта миокарда в молодом возрасте у пациентов с ТТ генотипом в сравнении с СТ генотипом (53,1 ± 13,9 и 64,0 ± 11,0 года, p = 0,044). Лабораторные параметры не отличались вариабельностью за исключением меньшего уровня гемоглобина у носителей ТТ генотипа полиморфизма rs1143634 гена IL-1β (124 ± 21,7 г/л) в сравнении с СС (137 ± 19,5 г/л; р = 0,006) и СТ генотипами (137 ± 20,8 г/л; р = 0,009).
Уровень высокочувствительного С-реактивного белка составил у пациентов СС генотипа полиморфизма rs1143634 гена IL-1β 2,65 [1,2; 6,7] мг/л, СТ – 3,37 [1,74;
6,43] мг/л, ТТ – 5,54 [3,32; 9,29] мг/л. Обращает на себя внимание тот факт, что у всех пациентов ТТ генотипа уровень высокочувствительного С-реактивного белка превышал 3 мг/л. Доля лиц с высоким относительным воспалительным риском была меньше при СТ генотипе (53,4%), СС генотипе полиморфизма rs1143634 гена IL-1β (44,6%) ( χ2 = 11,7; p = 0,019). Уровень α1-глобулина носителей ТТ генотипа (3,75 ± 0,65 мг/л) превышал таковой, характерный для СС (3,15 ± 0,63 мг/л; р = 0,006) и СТ генотипов (3,24 ± 0,71 мг/л; р = 0,027).
Структура и функция сердца не различались у пациентов с хронической сердечной недостаточностью СС, СТ и ТТ генотипов полиморфизма rs1143634 гена IL-1β.
С целью выявления возможной ассоциации полиморфизма rs1143634 гена IL-1β с течением хронической сердечной недостаточности собрана информация о событиях в течение 5 лет с момента включения. Сведения о достижении конечных точек были получены от 313 пациентов с хронической сердечной недостаточностью. В течение 5 лет умерли от любой причины 28,1%, несмертельное событие перенесли 25,6% пациентов, комбинированная конечная точка зарегистрирована у 47,6% пациентов. Ведущей причиной смерти была декомпенсация сердечной недостаточности (67%), с равной частотой – мозговой инсульт и инфаркт миокарда (9%), тромбозы (2,3%). Среди внесердечных причин смерти были онкологические заболевания (8%) и другие причины, в том числе инфекция COVID-19 (4,5%).
Распределение аллелей и генотипов полиморфизма rs1143634 гена IL-1β включенных в исследование пациентов и когорты с известным прогнозом в течение 5 лет не различалось (табл. 1).
Таблица 1. Частота встречаемости аллелей и генотипов полиморфизма rs1143634 гена IL-1β у пациентов с хронической сердечной недостаточностью в начале исследования и через 5 лет наблюдения Table 1. Frequency of occurrence of alleles and genotypes of the rs1143634 polymorphism of the IL-1β gene in patients with chronic heart failure at the beginning of the study and after 5 years of follow-up
|
Ген |
Генотип |
Исходно |
Через 5 лет |
χ2 |
p |
||
|
n |
% |
n |
% |
||||
|
IL-1β rs1143634 С/T |
CC |
261 |
58,7 |
164 |
60,1 |
0,31 |
0,85 |
|
CT |
161 |
36,2 |
97 |
35,5 |
|||
|
TT |
23 |
5,2 |
12 |
4,4 |
|||
|
С |
683 |
76,7 |
425 |
78 |
0,27 |
0,59 |
|
|
Т |
207 |
23,3 |
121 |
22 |
|||
У пациентов, достигших комбинированной конечной точки, генотип ТТ полиморфизма rs1143634 гена IL-1β встречался чаще в сравнении с пациентами с благоприятным течением заболевания (83,3 и 16,7% соответственно, χ2 = 6,02; p = 0,027), таблица 2.
У пациентов с хронической сердечной недостаточностью ТТ генотипа полиморфизма rs1143634 гена IL-1β риск смерти от всех причин в течение 5 лет составил (ОР = 2,85; 95% ДИ: 1,2– 6,76; р = 0,018), риск достижения комбинированной конечной точки – (ОР = 3,3; 95% ДИ: 1,62–6,71; р < 0,001). Риск смертельного исхода по причине мозгового инсульта у носителей ТТ генотипа полиморфизма rs1143634 гена IL-1β был выше в 17,11 раза в сравнении с СС генотипом (OШ = 17,11; 95% ДИ: 2,619–112,7; р = 0,008) и в 14,99 раза в сравнении с СТ генотипом (OШ = 14,99; 95% ДИ: 1,999–140; р = 0,018), таблица 3.
Таблица 2. Распределение частот встречаемости генотипов полиморфизма rs1143634 гена IL-1β у пациентов с хронической сердечной недостаточностью с различным прогнозом в течение 5 лет
Table 2. Distribution of genotypes of the rs1143634 polymorphism of the IL-1β gene in patients with CHF with different prognosis over 5 years
|
Генотип |
ККТ+ |
ККТ- |
χ2 |
p |
Смерть+ |
Смерть– |
χ2 |
p |
||||
|
n |
% |
n |
% |
n |
% |
n |
% |
|||||
|
CC |
76 |
46,3 |
88 |
55,7 |
0,92 |
0,33 |
45 |
27,4 |
119 |
72,6 |
0,032 |
0,857 |
|
CT |
47 |
48,5 |
50 |
51,5 |
0,004 |
0,95 |
25 |
25,8 |
72 |
74,2 |
0,32 |
0,572 |
|
TT |
10 |
83,3 |
2 |
16,7 |
6,02 |
0,027 |
6 |
50 |
6 |
50 |
3,06 |
0,079 |
Примечание: ККТ – комбинированная конечная точка.
Таблица 3. Достижение конечных точек пациентами с хронической сердечной недостаточностью в течение 5 лет с учетом полиморфизма rs1143634 гена IL-1β
Table 3. Achievement of end points by patients with CHF over 5 years, taking into account the rs1143634 polymorphism of the IL-1β gene
|
Конечные точки |
Генотип IL-1β |
p |
|||||
|
CC, n = 164 |
CT, n = 97 |
TT, n = 12 |
|||||
|
Абс. |
% |
Абс. |
% |
Абс. |
% |
||
|
Смертность от всех причин: |
45 |
27,4 |
25 |
25,8 |
6 |
50 |
0,207 |
|
Сердечно-сосудистая смертность, в т. ч. от: |
42 |
25,6 |
20 |
20,6 |
5 |
41,7 |
0,246 |
|
– декомпенсации хронической сердечной недостаточности |
32 |
19,5 |
15 |
15,5 |
2 |
16,7 |
0,7 |
|
– инфаркта миокарда |
2 |
1,2 |
2 |
2,1 |
0 |
– |
0,95 |
|
– мозгового инсульта |
3 |
1,8 |
2 |
2,1 |
3 |
25 |
0,00002 |
|
Несмертельные события, всего |
45 |
27,4 |
31 |
32 |
5 |
41,7 |
0,48 |
|
Несмертельные сердечно-сосудистые события: |
33 |
20,1 |
27 |
27,8 |
5 |
41,7 |
0,122 |
|
– инфаркт миокарда |
7 |
4,3 |
7 |
7,2 |
0 |
– |
0,31 |
|
– мозговой инсульт |
2 |
1,2 |
3 |
3,1 |
0 |
– |
0,53 |
|
– коронарное вмешательство |
6 |
3,7 |
2 |
2,1 |
1 |
8,3 |
0,475 |
|
– госпитализация по поводу декомпенсации хронической сердечной недостаточности |
17 |
10,4 |
12 |
12,4 |
4 |
33,3 |
0,06 |
|
– Комбинированная конечная точка |
76 |
46,3 |
47 |
48,5 |
10 |
83,3 |
0,047 |
Проведена визуализация достижения в течение 5 лет комбинированной конечной точки пациентами с хронической сердечной недостаточностью в зависимости от генотипа полиморфизма rs1143634 гена IL-1β (рис. 1).
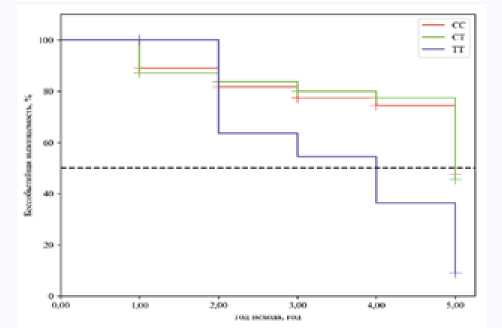
Рис. 1. Кривая достижения комбинированной конечной точки в зависимости от генотипа полиморфизма rs1143634 гена IL-1β
Fig. 1. Curve of achievement of the combined endpoint depending on the genotype of the rs1143634 polymorphism of the IL-1β gene
Бессобытийная выживаемость (недостижение комбинированной конечной точки) наблюдалась достоверно чаще у пациентов СС и СТ генотипов, чем у носителей ТТ генотипа полиморфизма rs1143634 гена IL-1β ( p log-rank = 0,024).
Учитывая возможные межгенные и генно-средовые взаимодействия, проявляющиеся в контексте коморбид- ности, проведен субанализ распределения генотипов и исходов пациентов с хронической сердечной недостаточностью, с сопутствующими хронической болезнью почек, хронической обструктивной болезнью легких и сахарным диабетом в течение 5 лет.
Распределение генотипов полиморфизма rs1143634 гена IL-1β у пациентов с хронической сердечной недостаточностью и в группе генетического контроля не различалось при наличии хронической болезни почек (СС – 57,8 и 61%, СТ – 36,4 и 34,7%, ТТ – 5,9 и 4,2%, χ2 = 0,55; р = 0,75); хронической обструктивной болезни легких (СС – 57 и 61%, СТ – 38,7 и 34,7%, ТТ – 4,3 и 4,2%, χ2 = 0,36; р = 0,83); сахарного диабета (СС – 54,1 и 61%, СТ – 41,8 и 34,7%, ТТ – 4,1 и 4,2%, χ2 = 1,16; р = 0,56).
У пациентов с хронической сердечной недостаточностью в коморбидности с хронической болезнью почек сохранялась тенденция к большей частоте смертельного исхода у носителей ТТ генотипа полиморфизма rs1143634 гена IL-1β (табл. 4). Смертельный мозговой инсульт регистрировался у каждого второго пациента с хронической сердечной недостаточностью в коморбидности с хронической болезнью почек ТТ генотипа полиморфизма rs1143634 гена IL-1β, превышая таковой СС генотип (50 и 2,8%, χ2 = 16,47; OШ = 29,33; 95% ДИ: 1,48–642,6; р = 0,025) и СТ генотип (50 и 2,6%, χ2 = 11,95; OШ = 29,12; 95% ДИ: 1,13–2235; р = 0,04).
Частота достижения конечных точек в течение 5 лет с учетом генотипа полиморфизма rs1143634 гена IL-1β значимо не различалась у пациентов с хронической сердечной недостаточностью в коморбидности с хронической обструктивной болезнью легких.
Таблица 4 . Достижение конечных точек пациентами с хронической сердечной недостаточностью и хронической болезнью почек в течение 5 лет с учетом полиморфизма rs1143634 гена IL-1β
Table 4 . Achievement of end points by patients with CHF and chronic kidney disease over 5 years, taking into account the rs1143634 polymorphism of the
IL-1β gene
|
Конечные точки |
Генотип IL-1β |
p |
|||||
|
CC, n = 71 |
CT, n = 38 |
TT, n = 4 |
|||||
|
Абс. |
% |
Абс. |
% |
Абс. |
% |
||
|
Смертность от всех причин: |
19 |
26,8 |
8 |
21,1 |
3 |
75 |
0,067 |
|
Сердечно-сосудистая смертность, в т. ч. от: |
18 |
25,4 |
7 |
18,4 |
2 |
50 |
0,332 |
|
– декомпенсации хронической сердечной недостаточности |
15 |
21,1 |
4 |
10,5 |
0 |
– |
0,258 |
|
– мозгового инсульта |
2 |
2,8 |
1 |
2,6 |
2 |
50 |
0,00004 |
|
Несмертельные события, всего |
24 |
33,8 |
11 |
28,9 |
0 |
0 |
0,605 |
|
Несмертельные сердечно-сосудистые события, в т. ч.: |
18 |
25,4 |
8 |
21,1 |
0 |
0 |
0,615 |
|
– инфаркт миокарда |
4 |
5,6 |
3 |
7,9 |
– |
– |
0,646 |
|
– коронарное вмешательство |
5 |
7 |
1 |
2,6 |
– |
– |
0,63 |
|
– госпитализация по поводу декомпенсации хронической сердечной недостаточности |
9 |
12,6 |
3 |
7,9 |
– |
– |
0,678 |
|
Комбинированная конечная точка |
36 |
50,7 |
15 |
39,5 |
2 |
50 |
0,53 |
В течение 5 летнего наблюдения все пациенты с хронической сердечной недостаточностью ТТ генотипа полиморфизма rs1143634 гена IL-1β в сочетании с сахарным диабетом были госпитализированы по причине декомпенсации сердечной деятельности, что превышало частоту госпитализаций пациентов СС и СТ генотипов (15,6 и 10,3%, χ2 = 6,33; р = 0,042).
Следующим этапом работы было оценить закономерности достижения конечных точек пациентами с сердечной недостаточностью при сопутствующих неинфекционных заболеваниях в зависимости от диапазона величины фракции выброса левого желудочка. Пациенты с СНсФВ ТТ генотипа полиморфизма rs1143634 гена IL-1β при наличии хронической болезни почек чаще достигали конечной точки смерть от всех причин (75% vs. СС: 20%, vs. СТ: 22,2%, р = 0,043); при наличии хронической обструктивной болезни легких – кардиоваскулярной смерти (100% vs. СС: 42,9% и vs. СТ: 21,4%, р = 0,037). При СНсФВ в сочетании с сахарным диабетом различий в достижении конечных точек с позиции полиморфизма rs1143634 гена IL-1β не наблюдалось.
Исходы пациентов с СНу/сФВ и СНнФВ при наличии хронической болезни почек, хронической обструктивной болезни легких, сахарного диабета значимо не различались в изучаемых генотипах полиморфизма rs1143634 гена IL-1β .
Обсуждение
Генетические исследования интегрируют концепции молекулярной генетики для познания этиологии, патогенетических механизмов клинического многообразия сердечно-сосудистых заболеваний. Однако на современном этапе развития кардиологии остается разрыв между научными достижениями в области молекулярной биологии и генетики с реальной клинической практикой. В то же время большинство исследователей считают целесообразным изучение генетического фона в комплексе с традиционными факторами сердечно-сосудистого риска, влияющими на клиническое течение и исход заболевания. Перспективность генотипирования обусловлена возможностью идентификации групп генетического риска до появления клинических проявлений, а также прогнозирования осложнений сердечно-сосудистых заболеваний, персонифицированного подхода к модификации образа жизни и фармакотерапии.
Проведенное исследование свидетельствует о функциональной значимости аллеля Т полиморфизма rs1143634 гена IL-1β в прогнозировании исходов в течение 5 лет пациентов с хронической сердечной недостаточностью ишемической этиологии. Встречаемость генотипов полиморфизма rs1143634 гена IL-1β у пациентов с хронической сердечной недостаточностью, в том числе при наличии хронической болезни почек, хронической обструктивной болезни легких, сахарного диабета, и группы генетического контроля значимо не различалась. В то же время в единственной работе по изучению данного полиморфизма у пациентов с хронической сердечной недостаточностью сообщается, что аллель С и генотип СС полиморфизма rs1143634 гена IL-1β признаются факторами генетического риска развития хронической сердечной недостаточности (OШ = 3,79; 95% ДИ: 1,06–13,61; χ2 = 4,72; p = 0,03) [14, 15].
U. Zeybek и соавт. (2011), сообщают о повышенном риске инфаркта миокарда в турецкой популяции при наличии аллеля Т полиморфизма rs1143634 гена IL-1β ( χ2 = 4,63; р = 0,03) и о протективном эффекте в отношении инфаркта миокарда при носительстве СС генотипа ( χ2 = 3,97; р = 0,046) [17]. В настоящей работе не было выявлено ассоциации с большим риском развития инфаркта миокарда, однако определен меньший возраст дебюта инфаркта миокарда у пациентов ТТ генотипа полиморфизма rs1143634 гена IL-1β в сравнении с СТ генотипом. В то же время А. Coker и соавт. (2011) не подтвердили ассоциации полиморфизма rs1143634 гена IL-1β с риском инфаркта миокарда ( р = 0,442), а также с возрастом дебюта инфаркта миокарда (< 40 или > 40 лет) ( р = 0,978) в турецкой популяции [18].
Выявлены существенные градиенты в достижении в течение 5 лет конечных точек пациентами с хронической сердечной недостаточностью ТТ генотипа полиморфизма rs1143634 гена IL-1β, что свидетельствует о большем риске смерти от всех причин (ОР = 2,85; 95% ДИ: 1,2–6,76; р = 0,018) и риске достижения комбинированной конечной точки – (ОР = 3,3; 95% ДИ: 1,62–6,71; р < 0,001). Смерть по причине мозгового инсульта чаще фиксировалась у носителей ТТ генотипа полиморфизма rs1143634 гена IL-1β в сравнении с СС (25 и 1,8%, χ2 = 18,23; OШ = 17,11; 95% ДИ: 2,62–112,7; р = 0,008) и СТ генотипом (25 и 2,1%, χ2 = 12,84; OШ = 14,99; 95% ДИ: 1,99–140; р = 0,018).
Результаты настоящей работы не согласуются с данными ранее проведенных исследований, где факторами неблагоприятного течения хронической сердечной недостаточности были аллель С и генотип СС полиморфизма rs1143634 гена IL-1β (OШ = 4,35; 95% ДИ: 2,22–8,49; χ2 = 20,68; p = 5,42 × 10–6 и OШ = 11,83; 95% ДИ: 1,62– 25,52; χ2 = 5,02; p = 0,025),тогда как аллель Т (OШ = 0,23; 95% ДИ: 0,12–0,45; χ2 = 20,68; p = 5,421 × 10–6), СТ и ТТ генотипы (OШ = 0,19; 95% ДИ: 0,09–0,41; χ2 = 20,29; p = 6,65 × 10–6 и OШ = 0,09; 95% ДИ: 0,004–1,61; χ2 = 5,02; p = 0,025) являются протективными факторами [14, 15].
К предполагаемым причинам несогласованности полученных ассоциаций полиморфизма rs1143634 гена IL-1β с исходами пациентов с хронической сердечной недостаточностью с ранее опубликованными работами можно отнести гетерогенность исследуемых популяций по этническим, половозрастным признакам, а также меньшую длительность наблюдения (12 мес.). Так, выборка сравниваемого исследования состояла из 165 пациентов, 121 из которых мужчины в возрасте 56,7 ± 5,3 года. Наблюдаемая в настоящем исследовании ассоциация аллеля Т с неблагоприятным течением хронической сердечной недостаточности обусловлена большей генетически детерминированной выраженностью воспаления (по уровню высокочувствительного С-реактивного белка).
Приоритетным направлением дальнейших исследований можно считать изучение остаточного воспалительного и липидного риска у пациентов с хронической сердечной недостаточностью ишемического генеза для оптимизации терапевтических тактик. Кроме того, учитывая мультифакторность хронической сердечной недостаточности, предполагающую тесное переплетение генетического профиля пациента и глубоких функциональных и структурных изменений организма вследствие внешних факторов, можно предположить разнонаправленность протекции в зависимости от средовых факторов, форми-
Список литературы Отдаленный прогноз неблагоприятных сердечнососудистых событий у пациентов с хронической сердечной недостаточностью в зависимости от полиморфизма RS1143634 гена интерлейкина-1
- Yndestad A., Damas J.K., Oie E., Ueland T., Gullestad L., Aukrust P. Role of inflammation in the progression of heart failure. Curr. Cardiol. Rep. 2007;9(3):236-241. https://doi.org/10.1007/bf02938356.
- Тепляков А.Т., Шилов С.Н., Попова А.А., Березикова Е.Н., Гракова Е.В., Неупокоева М.Н. и др. Роль провоспалительных цитокинов в развитии антрациклин-индуцированной сердечной недостаточности. Сибирский журнал клинической и экспериментальной медицины. 2020;35(2):66-74. https://doi.org/10.29001/2073-8552-2020-35-2-66-74.
- Fang Y., Xie H., Lin Z. Association between IL-1β + 3954C/T polymorphism and myocardial infarction risk: A meta-analysis. Medicine (Baltimore). 2018;97(30):e11645. https://doi.org/10.1097/MD.0000000000011645.
- Tabata N., Sueta D., Akasaka T., Arima Y., Sakamoto K., Yamamoto E. et al. Helicobacter pylori seropositivity in patients with interleukin-1 polymorphism is significantly associated with ST-segment elevation myocardial infarction. PLoS One. 2016;11(11):e0166240. https://doi.org/10.1371/journal.pone.0166240.
- Chen Q., Wang W., Huang Zh., Huang D.L., Li T., Wang F. et al. Correlation of rs1122608 SNP with acute myocardial infarction susceptibility and clinical characteristics in a Chinese Han population: A case control study. The Anatolian Journal of Cardiology. 2018;19(4):249-258. https://doi.org/10.14744/anatoljcardiol.2018.35002.
- Serafin M., Kalinka J. The role of chosen polymorphism of gens coding cytokines IL-1ß, IL1ra, IL-6 and TNFalpha in the pathogenesis of the preterm delivery. Ginekol i Poloznictwo.2014;33(3):9-23.
- Pociot F., Molvig J., Wogensen L., Worsaae H., Nerup J. A TaqI polymorphism in the human interleukin-1 beta (IL-1 beta) gene correlates with IL-1 beta secretion in vitro. Eur. J. Clin. Invest. 1992;22:396-402. https://doi.org/10.1111/j.1365-2362.
- Latkovskis G., Licis N., Kalnins U. C-reactive protein levels and common polymorphisms of the interleukin-1 gene cluster and interleukin-6 gene in patients with coronary heart disease. Eur. J. Immunogenet. 2004;31(5):207-213. https://doi.org/10.1111/j.1365-2370.2004.00476.x.
- rs1143634. Ensembl is a genome browser. URL: http://www.ensembl.org/Homo_sapiens/Variation/Population?db=core;r=2:112832313-112833313;v=rs1143634;vdb=variation;vf=182624122 (08.10.2024).
- Fadl M.A., Noor Аlgalil S.S. IL1 𝛽 exon 395 C/ Polymorphism potential genetic risk factor of heart diseases’ predisposition in Sudanese patients. Sudan Journal of Medical Sciences. 2020;15(4):399-407. https://doi.org/10.18502/sjms.v15i4.8162.
- Pan Q., Hui D., Hu C. A variant of IL1B is associated with the risk and blood lipid levels of myocardial infarction in Eastern Chinese individuals. Immunol. Invest. 2022;51(5):1162-1169. https://doi.org/10.1080/08820139.2021.1914081.
- Захарьян Е.А., Грицкевич О.Ю. Влияние однонуклеотидных полиморфизмов генов IL1β, EDN1 и NOS3 на индивидуальный генетический профиль пациентов с ишемической болезнью сердца в Республике Крым. Вестник современной клинической медицины. 2023;16(6):31-36. https://doi.org/10.20969/VSKM.2023.16(6).31-36.
- Топчиева Л.В., Курбатова И.В., Малышева И.Е., Корнева В.А., Топчиева А.В. Аллельный полиморфизм генов, вовлеченных в продук цию IL-1β, и предрасположенность людей к развитию артериальной гипертензии. Научные результаты биомедицинских исследований. 2023;9(1):53-70.
- Маянская С.Д., Яковлева Н.Ф., Яковлев А.В., Филипенко М.Л., Воронина Е.П., Березикова Е.Н. и др. Полиморфизм генов интерлейкина-1β и рецепторного антагониста интерлейкина-1 у больных хронической сердечной недостаточностью. Журнал сердечная недостаточность. 2008;9(2):60-63.
- Тепляков А.Т., Шилов С.Н., Березикова Е.Н., Яковлева Н.Ф., Торим Ю.Ю., Кистенева И.В. и др. Клинико-генетические детерминанты генов ФНО-ОС, ИЛ-1/3 И ИЛ-1РА в инициации и развитии хронической сердечной недостаточности у больных ишемической болезнью сердца. Сибирский медицинский журнал (Томск). 2009;24(1):40-48.
- Kramer F., Voss S., Roessig L., Igl B.W., Butler J., Lam C.S.P. et al. Evaluation of high-sensitivity C-reactive protein and uric acid in vericiguat-treated patients with heart failure with reduced ejection fraction. Eur. J. Heart Fail. 2020;22(9):1675-1683. https://doi.org/10.1002/ejhf.1787.
- Zeybek U., Toptas B., Karaali Z.E., Kendir M., Cakmakoglu B. Effect of TNF-α and IL-1β genetic variants on the development of myocardial infarction in Turkish population. Mol. Biol. Rep. 2011;38(8):5453-5457. https://doi.org/10.1007/s11033-011-0701-x.
- Coker A., Arman A., Soylu O., Tezel T., Yildirim A. Lack of association between IL-1 and IL-6 gene polymorphisms and myocardial infarction in Turkish population. Int. J. Immunogenet. 2011;38(3):2018. https://doi.org/10.1111/j.1744-313X.2010.00988.x.


