Открытое рандомизированное сравнительное исследование эффективности терапии мужчин с хроническим простатитом категорий II и IIIa левофлоксацином и тамсулозином в комбинации с препаратом ИндигалПлюс
Автор: Коган М.И., Кульчавеня Е.В., Каприн А.Д., Новиков А.И., Крупин В.Н., Ибишев Х.С., Родыгин Л.М., Киселев В.И., Друх В.М.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Андрология
Статья в выпуске: 3, 2016 года.
Бесплатный доступ
Введение. В статье представлены результаты сравнительного исследования по оценке эффективности и безопасности комбинации левофлоксацина и тамсулозина с препаратом ИндигалПлюс в терапии хронического простатита (ХП). Материалы и методы. Пациенты с диагнозом ХП II и IIIA категорий (n=12) были рандомизированы в 4 параллельные группы с равным количеством пациентов: больные I группы (ХП категории II) получали левофлоксацин 500 мг/сут 1 месяц и ИндигалПлюс по 2 капсулы 2 раза в сутки 3 месяца; во II группе (ХП категории II) больные получали левофлоксацин 500 мг/сут 1 месяц; в III группе (ХП категории IIIA) - получали тамсулозин 400 мг/сут и ИндигалПлюс по 2 капсулы 2 раза в сутки 3 месяца; в группа IV (ХП категории IIIA) больные получали тамсулозин по 400 мг/сут 3 месяца. Эффективность терапии оценивали по следующим показателям: изменений данных уродинамики, объема предстательной железы, сроки наступления и полнота бактериологической санации, сравнение качества жизни, состояния сексуальной функции и интенсивности обструктивной и ирритативной симп томатики (по данным опросников IPSS, NIH-CPSI и IIEF). Результаты. Прирост максимальной скорости мочеиспускания Qmax и средней скорости потока мочи Qave по данным урофлоуметрии через 6 месяцев исследования значимо возрастали более чем на 20% в группах I и III, пациенты которых применяли левофлоксацин и тамсулозин в комбинации с препаратом ИндигалПлюс. Также показано, что 3-месячный курс совместной терапии ИндигалПлюс и левофлоксацина приводит к значимому снижению содержания лейкоцитов в секрете предстательной железы, бактериальной обсемененности, а также степени выраженности нарушений мочеиспускания, оцениваемых с помощью суммарного балла IPSS, по сравнению с терапией только левофлоксацином. В ходе исследования зарегистрировано 4 нежелательных явления (НЯ) во всех группах. Значимых отличий в частоте НЯ между группами не было. Выводы. Препарат ИндигалПлюс является эффективным средством для лечения ХП и хорошо переносится пациентами. Отсутствие серьезных НЯ, отклонений биохимических показателей, изменений в анализах крови и мочи подтвердили безопасность проводимой терапии.
Хронический простатит, хроническая тазовая боль, лечение, левофлоксацин, тамсулозин, индигалплюс
Короткий адрес: https://sciup.org/142188137
IDR: 142188137
An open randomized study of the effectiveness of treatment of males with chronic prostatitis (categories II and IIIa) applying levofloxacin and tamsulosin combined with IndigalPlus
Introduction. The article presents the results of a comparative study of the evaluation of the effectiveness and safety of a combination of Levofloxacin and Tamsulosin with IndigalPlus. Materials and methods. Patients diagnosed with chronic prostatitis, CP (n=121, stages II and IIIA) were randomized into four parallel groups containing 30 patients. Patients from the first group (CP stage II) had been receiving Levofloxacin (500 mg per day) for one month and IndigalPlus (2 capsules twice a day) for three months. Patients from the second group (CP stage II) had been receiving Levofloxacin (500 mg per day) for one month. Patients from the third group (CP stage IIIA) had been receiving Tam-suloin (400 mg per day) and IndigalPlus (2 capsules twice a day) for three months. Patients from the fourth group (CP stage IIIA) had been receiving Tamsuloin (400 mg per day) for three months. The effectiveness of the therapy was evaluated by the following parameters: urodynamics, changes in prostate volume, timing and completeness of biological debridement, and also comparison of life quality, sexual function and the intensity of obstructive and irritative symptom scores, according to IPSS, NIH-CPSI and IIEF questionnaires. Results. According to the data collected from urofluorimetry after 6 months of the study, an increase in the peak urinary flow rate (Qmax) and average urinary flow rate (Qave) has significantly grown by more than 20% in the first and in the third groups. Patients from there groups had been taking Levofloxacin and Tamsuloin in combination with IndigalPlus. It was also shown that in comparison with Levofloxacin only therapy course, three-months course of IndigalPlus and Levofloxacin combination therapy leads to a significant decrease in leukocyte content of prostate secretions, bacterial contamination, and also in the severity of urination disorders, which were evaluated by the IPSS total score. During the study, four unwanted events (UE) were registered in all groups. No significant differences in the frequency of the UE were found. Results. Drug IndigalPlus is effective for the treatment of chronic prostatitis and is well tolerated by patients.’tte absence of serious UE, biochemical deviations, and deviations in blood and urine tests have proven the safety of the therapy administered.
Текст научной статьи Открытое рандомизированное сравнительное исследование эффективности терапии мужчин с хроническим простатитом категорий II и IIIa левофлоксацином и тамсулозином в комбинации с препаратом ИндигалПлюс
экспериментальная и клиническая урология №3 2 0 16 фективность левофлоксацина продемонстрирована в мультицентровом рандомизированном двойном слепом исследовании при лечении бактериального ХП [9].
экспериментальная и клиническая урология №3 20 1 6
По окончании исследования проводилась оценка главного критерия эффективности – доля пациентов с ростом Q max или Q ave не менее чем на 20% к 3-ему месяцу лечения. Для этого проводилось сравнение показателей уродинамики (Q max , Q ave , V res ) у пациентов с хроническим простатитом категорий II и IIIA, получающих тамсулозин и левофлоксацин в комбинации с ИндигалПлюс (группы I и III), в сравнении с применением тамсулозина и левофлоксацина (группы II и IV).
Данные о результатах лечения (прирост Q max или Q ave более чем на 20%) представлены в таблице 1.
Таким образом, статистически значимый эффект клинически значимого улучшения уродинамических показателей присутствует в группах I и III – у пациентов с ХП категории II, принимавших ИндигалПлюс в дополнение к антибиотикотерапии.
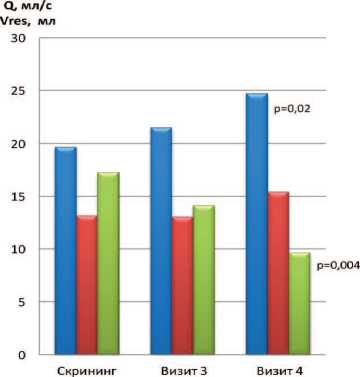
Дополнительно были проанализированы отличия в показателях уродинамики внутри групп (динамика между визитами). В группе I (прием «ИндигалПлюс и левофлоксацин» в страте ХП категории II) Q max значимо увеличилась с 19,83±10,52 мл/с на этапе скрининга до 24,71±10,86 мл/с ( p =0,02) к моменту окончания исследования. Значимые отличия также выявлены в группе «ИндигалПлюс и левофлоксацин» по среднему показателю V res : объем остаточной мочи уменьшился с 17,83±12,90 мл до 9,66±10,36 мл ( p =0,004) (рис. 1).
Также значимые отличия выявлены между Визитом скрининга и Визитом 4 у пациентов III группы
Таблица 1. Количество больных с изменением результатов урофлоуметрии на визите 4
|
Группа |
Число пациентов с положительным уродинамическим ответом на лечение |
Число пациентов с отрицательным уродинамическим ответом на лечение |
Значимость отличий р (по критерию χ 2 ) |
|
Группы I, III («ИндигалПлюс и левофлоксацин/тамсулозин») |
33 |
25 |
0,009 |
|
Группы II, IV («левофлоксацин /тамсулозин») |
19 |
39 |
|
|
Группа I («ИндигалПлюс и левофлоксацин») |
20 |
9 |
0,003 |
|
Группа II («левофлоксацин») |
9 |
21 |
|
|
Группа III («ИндигалПлюс и тамсулозин») |
13 |
16 |
0,483 |
|
Группа IV («тамсулозин») |
10 |
18 |
и Qmax u Qave U Vres
Рис. 1. Динамика уродинамических показателей Q max и Q ave (мл/с) и объема остаточной мочи V res (мл) у пациентов I группы («ИндигалПлюс и левофлоксацин») в страте ХП категории II (показаны значимые отличия от значений на скрининге)
(«ИндигалПлюс и левофлоксацин») в страте ХП категории IIIA по средним показателям Q ave и V res . Средняя скорость потока мочи Q ave увеличилась с 13,52±5,24 мл/с до 16,56±3,37 мл/с (p=0,005), а объем остаточной мочи уменьшился с 15,52±14,24 мл до 4,55±8,55 мл ( p =0,001) (рис. 2).
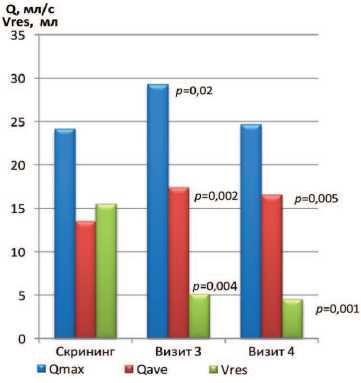
Рис. 2. Динамика уродинамических показателей Q max и Q ave (мл/с) и объема остаточной мочи V res (мл) у пациентов I группы («ИндигалПлюс и тамсуло-зин») в страте ХП категории IIIA (показаны значимые отличия от значений на скрининге)
Значимых отличий по средним показателям Q max , Q ave и V res не наблюдалось в группах, получавших только стандартную терапию.
Оценка противовоспалительного эффекта терапии проводилась на основании данных о межгрупповых отличиях по количеству лейкоцитов в секрете ПЖ и бактериологическим показателям. Сравнение по данным показателям на Визитах 1–4 проводилось у пациентов с ХП категории II, получающих левофлоксацин в комбинации с ИндигалПлюс (группа I), и получающих только левофлоксацин (группа II) (рис. 3). Значимые отличия были обнаружены в уровне числа лейкоцитов и бактериальной обсемененности в се- крете ПЖ на Визите 3 (p=0,047 и
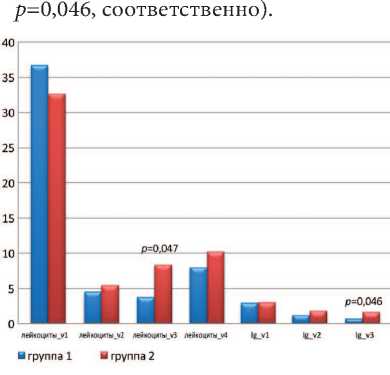
Рис. 3. Число лейкоцитов в секрете ПЖ (штук в поле зрения) на Визитах 1-4 и уровень бактериальной обсемененности (lg(КОЕ/мл)) секрета ПЖ
В ходе исследования проводилось также сравнение сроков наступления и полноты бактериологической санации секрета ПЖ в группах 1 и 2 у пациентов с ХП категории II, получающих левофлоксацин в комбинации с ИндигалПлюс и только левофлоксацин.
По данным бактериологического исследования секрета ПЖ эра-дикация возбудителя была достигнута в 96,7% случаев в группе I и в 80,6% в группе II, при этом в группе I приема «ИндигалПлюс и левофлоксацин» эрадикация первоначального возбудителя происходила значимо чаще ( p =0,049). Инфекция новым возбудителем в группе «Ин-дигалПлюс и левофлоксацин» В
Таблица 2. Частота эрадикации первоначального возбудителя и инфекции новым возбудителем и значимость их отличий в группах 1 и 2 (критерий χ 2 )
|
Группа |
Эрадикация (кол-во пациентов) |
Нет эффекта (кол-во пациентов) |
р (группа I /группа II) |
Нет инфекции новым возбудителем (кол-во пациентов) |
Инфекция новым возбудителем (кол-во пациентов) |
p (группа I /группа II) |
|
Группа I (ИндигалПлюс и левофлоксацин) (n=30) |
29 |
1 |
0,049 |
19 |
11 |
0,029 |
|
Группа II (левофлоксацин) (n=31) |
25 |
6 |
– |
11 |
20 |
– |
Таблица 3. Данные индексов IPSS, QoL, NIH-CPSI и IIEF пациентов первой и второй страт на Визите 1 и Визите 4
По результатам исследования также проведено сравнение качества жизни, состояния сексуальной функции и интенсивности обструктивной и ирритативной симптоматики (по данным опросников IPSS, NIH-CPSI и IIEF) с целью объективизации жалоб больных у пациентов с ХП категорий II и IIIA, получающих тамсулозин и левофлоксацин в комбинации с Инди-галПлюс в сравнении с применением тамсулозина и левофлоксацина.
Данные индексов IPSS, QoL, NIH-CPSI и IIEF пациентов первой и второй страт на первом и последнем визите представлены в таблице 3.
Значимые отличия в показателях обнаружены были в страте ХП категории II через 90 дней после начала лечения (Визит 3) в величине индекса IPSS и NIH-CPSI (в целом и по доменам «боль» и «качество жизни»). Тенденция сохранилась и к окончанию отдаленного периода наблюдения (Визит 4) – в индексах IPSS, QoL, NIH-CPSI (в целом и по доменам «боль» и «качество жизни») и IIEF (табл. 3).
Полученные данные позволяют отметить эффективное влияние совместной терапии Индигал-Плюс и левофлоксацина на качество жизни пациентов.
В страте ХП категории IIIA значимые отличия обнаружены
были на Визите 2 в величине индекса NIH-CPSI (в целом и по всем доменам), на Визите 3 – в величине индекса QoL и NIH-CPSI (в целом и по доменам «боль» и «качество жизни»), IIEF (в целом и по домену «эректильная функция»), а на Визите 4 – во всех указанных индексах и их доменах.
Наконец было проведено сравнение изменения объема предстательной железы у пациентов с ХП категорий II и IIIA, получающих тамсулозин и левофлоксацин в комбинации с ИндигалПлюс в сравнении с применением тамсуло-зина и левофлоксацина (рис. 4-5).
Достоверных различий размеров ПЖ до и после лечения выявлено не было, несмотря на некоторую тенденцию к уменьшению размеров ПЖ после лечения. Вероятно, для получения более выраженных положительных изменений необходима более продолжительная терапия комбинацией препаратов.
Необходимо также отметить
Изменение
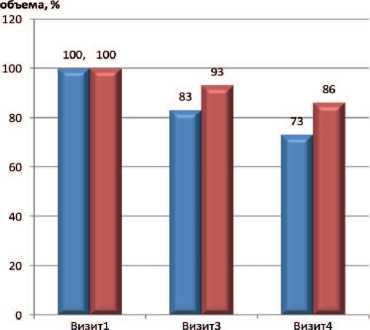
■ группа 1 ■группа 2
Рис. 4. Динамика объема предстательной железы в страте ХП категории II (исходный объем принят за 100%)
Изменение объема, %
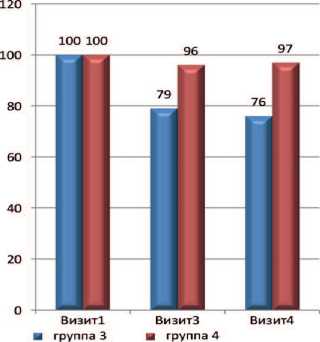
Рис. 5. Динамика объема ПЖ в страте ХП категории IIIA (исходный объем принят за 100%)
Таблица 4. Нежелательные явления
|
Группа |
Страта |
Описание |
Тяжесть |
Нежелательное явление разрешилось в период участия пациента в исследования? |
|
1 |
ХП категории II |
травма уздечки полового члена |
легкая |
да |
|
3 |
ХП категории IIIA |
эритроцитурия из-за солевого диатеза |
легкая |
да |
|
4 |
ХП категории IIIA |
боли в промежности. дискомфорт при мочеиспускании |
умеренная |
нет |
|
4 |
ХП категории IIIA |
обострение ХП: боль в промежности, мошонке, внизу живота. дискомфорт при мочеиспускании |
тяжелая |
да |
экспериментальная и клиническая урология №3 20 16 хорошую переносимость препарата ИндигалПлюс больными. В ходе исследования было зарегистрировано 4 нежелательных явления (НЯ) в обеих стратах (табл. 4) – два в группах I и III, получающих Ин-дигалПлюс, (частота 3,39%, 95% ДИ 0,41%-11,7%) и два в группах II и IV, получающих только левофлокса-цин/тамсулозин (частота 3,33%, 95% ДИ 0,41%-11,5%). Значимых отличий в частоте НЯ между группами не было (p=0,98). Серьезных НЯ зарегистрировано не было. Тяжесть НЯ охарактеризована исследователями в двух случаях как легкая, в одном – как умеренная, и в одном – как тяжелая. Связь НЯ с приемом исследуемых препаратов, по мнению исследователей, отсутствовала во всех случаях. Таким образом, в группе терапии препаратом ИндигалПлюс не отмечалось большее количество НЯ по сравнению с группой, получавшей только стандартную терапию.
ОБСУЖДЕНИЕ
Наше исследование показало, что терапия препаратом Инди-галПлюс была более эффективна в страте 1 при ХП II категории. К концу исследования в группе I (совместная терапия ИндигалПлюс и левофлоксацин) у пациентов наблюдались наименьшие значения индексов IPSS и NIH-CPSI, лучшие показатели уродинамики и наименьшее количество остаточной мочи. Улучшение субъективной симптоматики и качества жизни, а также значимая клиническая эффективность сохранялись не только на протяжении всего 3-хмесяч-ного курса терапии, но и спустя три месяца после его окончания.
Кроме того, терапия комбинацией препаратов ИндигалПлюс и левофлоксацин снижает бактериальную обсемененность и содержание лейкоцитов в секрете ПЖ, что, вероятно, обусловлено действием
активных субстанций препарата ИндигалПлюс, повышающих чувствительности бактерий к антибиотикам, а также снимающих воспаление предстательной железы.
Монотерапия пациентов с ХП II тамсулозином и левофлоксацином носила в основном симптоматический характер, так как, возможно, не устраняла причину морфологических и микроциркулятор-ных изменений ПЖ.
ВЫВОДЫ
Резюме:
Введение. В статье представлены результаты сравнительного исследования по оценке эффективности и безопасности комбинации левофлоксацина и тамсулозина с препаратом ИндигалПлюс в терапии хронического простатита (ХП).
Материалы и методы. Пациенты с диагнозом ХП II и IIIA категорий (n=12) были рандомизированы в 4 параллельные группы с равным количеством пациентов: больные I группы (ХП категории II) получали левофлоксацин 500 мг/сут 1 месяц и ИндигалПлюс по 2 капсулы 2 раза в сутки 3 месяца; во II группе (ХП категории II) больные получали левофлоксацин 500 мг/сут 1 месяц; в III группе (ХП категории IIIA) – получали тамсулозин 400 мг/сут и Инди-галПлюс по 2 капсулы 2 раза в сутки 3 месяца; в группа IV (ХП категории IIIA) больные получали тамсулозин по 400 мг/сут 3 месяца. Эффективность терапии оценивали по следующим показателям: изменений данных уродинамики, объема предстательной железы, сроки наступления и полнота бактериологической санации, сравнение качества жизни, состояния сексуальной функции и интенсивности обструктивной и ирритативной симп-
Список литературы Открытое рандомизированное сравнительное исследование эффективности терапии мужчин с хроническим простатитом категорий II и IIIa левофлоксацином и тамсулозином в комбинации с препаратом ИндигалПлюс
- McRae SN, Dairiki Shortlliffe. Bacterial Infections of the Genitourinary Tract. In: Smith’s General Urology. (eds. Tanago E.A., McAninch J.W.) 15th edition. Lange Medical Book, San Francisco: 2000.
- Dainel A, Shoskes G. Use of antibiotics in chronic prostatitis syndromes. Canadian J Urol 2001;8(1):24-28.
- Jeannette M, Potts F. ’ftie four categories of prostatitis: Practical approach to treatment. Clev Clin J Med 2001;61:389-397.
- Krieger JN, Nyberg L, Nickel JC NIH consensus definition and classification of prostatitis. JAMA 1999; 282 (3):236-237.
- Gurunadha Rao Tunuguntla HS, Evans CP. Management of prostatitis. Prostate Cancer Prostatic Dis. 2002;5(3):172-179.
- Weidner W, Diemer T, Huwe P, Rainer H, Ludwig M. ’ftie role of Chlamydia trachomatis in prostatitis. Int J Antimicrob Agents 2002;19:466-470.
- Mander R, Raukas E, Turk S, Korrovits P, Punab M. Mycoplasmas in semen of chronic prostatistis patients. Scand J Urol Nephrol 2005;39(6):479-482.
- Weidner W, Anderson RU. Evaluation of acute and chronic bacterial prostatitis and diagnostic management of chronic prostatitis/chronic pelvic pain syndrome with special reference to infection/inflammation. Int J Antimicrob Agents 2008;31(Suppl 1):91-95.
- Richard G, DeAbate C, Ruoff G. et.al. Short-course levofloxacin (250 mg qd) vs ofloxacin (200 mg bid) in uncomplicated UTI: a double-blind, randomized trial. 6th Int. Symp. on new Quinolones. Denver (Nov 1998) In: Abstracts, 1998: abs 126.
- Chen XS, Ye ZQ, Zeng XY. Tamsulosin for the treatment of chronic abacterial prostatitis. Zhonghua Nan Ke Xue 2002;8(1):51-53.
- Narayan P, Evans CP, Moon T. Long-term safety and efficacy of Tamsulosin for the treatment of lower urinary tract symptoms associated with benign prostatic hyperplasia. J Urol 2003;170:498-502.
- Горпинченко И.И., Гурженко Ю.Н. Исследование клинической эффективности альфа1-адреноблокатора тамсулозина у мужчин при хроническом абактериальном простатите/синдроме хронической тазовой боли. Здоровье мужчины 2013;(2):43-48
- Дьяков В.В., Говоров А.В. Опыт длительного применения тамсулозина (омник) у больных хроническим простатитом. Урология 2002;(5):1-4
- De Marzo AM, Platz EA, Sutcliffe S, Xu J, Grönberg H, Drake CG, et al. Inflammation in prostate carcinogenesis. Nat Rev Cancer 2007;7(4):256-269.
- Parameswaran N, Patial S. Tumor necrosis factor-а signaling in macrophages.
- Kundu JK, Na HK., Chun KS, Kim YK, Lee SJ, Lee SS, et al. Inhibition of phorbol ester-induced COX-2 expression by epigallocatechin gallate in mouse skin and cultured human mammary epithelial cells. J Nutr 2003;133(11Supl.1):3805-3810.
- Wheeler DS, Catravas JD, Odoms K, Denenberg A, Malhotra V, Wong HR. Epigallocate-chin-3-gallate, a green tea-derived polyphenol, inhibits IL-1-betadependent proinflammatory signal transduction in cultured respiratory epithelial cells J Nutr 2004;134(5):1039-1044.
- Singh BN, Shankar S, Srivastava RK. Green tea catechin, epigallocatechin-3-gallate (EGCG): mechanisms, perspectives and clinical applications. Biochemical pharmacology 2011;82(12):1807-1821.
- Vayalil PK, Katiyar SK. Treatment of epigallocatechin-3-gallate inhibits matrix metallo-proteinases-2 and -9 via inhibition of activation of mitogen-activated protein kinases, c-jun and NFkappaB in human Prostate carcinoma DU-145 cells. Prostate 2004;59(1):33-42.
- Aggarwal BB, Ichikawa H. Molecular targets and anticancer potential of indole-3-carbinol and its derivatives. Cell Cycle 2005;4(9):1201-1215.
- Takada Y, Andreeff M, Aggarwal BB. Indole-3-carbinol suppresses NF-kB and InBa kinase activation, causing inhibition of expression of NF-KB-regulated antiapoptotic and metastatic gene products and enhancement of apoptosis in myeloid and leukemia cells. Blood 2005;106(2):641-649.
- Jeong WS, Kim IW, Hu R, Kong AN. Modulatory properties of various natural chemopreventive agents on the activation of NF-kappaB signaling pathway. Pharm Res 2004;21(4):661-670.
- Sirab N, Robert G, Fasolo V, Descazeaud A, Vacherot F, de la Taille A, et al. Lipidosterolic extract of serenoa repens modulates the expression of inflammation related-genes in benign prostatic hyperplasia epithelial and stromal cells. Int J Mol Sci 2013;14(7):14301-14320.
- Sung WS, Lee DG. In vitro antimicrobial activity and the mode of action of indole-3-carbinol against human pathogenic microorganisms. Biol Pharm Bull 2007;30(10):1865-1869.
- Steinmann J, Buer J, Pietschmann T, Steinmann E. Anti-infective properties of epigallo-catechin-3-gallate (EGCG), a component of green tea. Br J Pharmacol 2013;168(5):1059-1073.
- Zhao WH, Hu ZQ, Okubo S, Hara Y, Shimamura T. Mechanism of synergy between epigallocatechin gallate and beta-lactams against methicillin-resistant Staphylococcus aureus. Antimicrob Agents Chemother 2001;45(6):1737-42.
- Sung WS, Lee DG. Mechanism of decreased susceptibility for Gram-negative bacteria and synergistic effect with ampicillin of indole-3-carbinol. Biol Pharm Bull 2008;31(9):1798-1801.


