Параметры эритропоэза и цитоархитектоника циркулирующих эритроцитов крыс с асцитной опухолью яичников
Автор: Генинг Т.П., Федотова А.Ю., Долгова Д.Р., Абакумова Т.В.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Физиология
Статья в выпуске: 1, 2019 года.
Бесплатный доступ
Развивающаяся неоплазма может влиять на эритропоэз организма-опухоленосителя. Установлено, что степень и характер этого влияния зависят от биологических характеристик опухоли. Цель работы - изучить морфометрические показатели эритроцитов и изменение эритропоэза у животных-опухоленосителей при развитии неопластического процесса. Материалы и методы. В качестве материала для исследования использовалась периферическая кровь экспериментального животного. Забор крови осуществлялся в стационарную (n=64) и терминальную (n=64) фазы роста опухоли. Контрольную группу составляли здоровые половозрелые крысы (n=62). Для оценки эритропоэза определялось содержание эритроцитов, уровень гемоглобина, количество ретикулоцитов и концентрация эритропоэтина в периферической крови животных-опухоленосителей. Методом атомно-силовой микроскопии изучалась цитоархитектоника. Результаты. Установлено значимое по сравнению с контролем снижение количества эритроцитов, а также понижение уровня гемоглобина...
Эритроциты, эритропоэтин, асцитная опухоль яичников
Короткий адрес: https://sciup.org/14116352
IDR: 14116352 | УДК: 612.111.3 | DOI: 10.34014/2227-1848-2019-1-119-125
Parameters of erythropoiesis and cytoarchitectonics of circulating erythrocytes in rat with ascites ovarian tumor
Developing neoplasm can affect the erythropoiesis of the tumor-bearer. It is found out that the degree and nature of such effect depend on tumor biological characteristics. The purpose of the study is to examine erythrocyte morphometric parameters and erythropoiesis change in tumor-bearing animals under neoplastic process development. Materials and Methods. Peripheral blood of experimental animals was used as trial material. Blood sampling was carried out during stationary (n=64) and terminal (n=64) tumor growth phases. Healthy adult rats (n=62) composed the control group. To assess erythropoiesis, the authors determined erythrocyte content, hemoglobin level, reticulocyte count, and erythropoietin concentration in the peripheral blood of tumor-bearing animals. Cytoarchitectonics was studied using atomic force microscopy. Results. Significant reduction in the number of red blood cells and decrease in hemoglobin level was established. The erythropoietin level in blood plasma increased during the stationary phase as well as the number of reticulocytes in blood during all periods of tumor growth...
Текст научной статьи Параметры эритропоэза и цитоархитектоника циркулирующих эритроцитов крыс с асцитной опухолью яичников
Введение. Исследование эритроцитов в патогенезе опухолевого роста привлекает внимание потому, что клетки красной крови - носители информации о процессах, протекающих в организме. Рост опухоли может привести к нарушению метаболизма эритроцитов, в результате чего возможно снижение их жизнеспособности и изменение их эластических свойств [1–5]. Накопление в мембранах эритроцитов высокотоксичных метаболитов за счет активации перекисного окисления липидов и аутокаталитического возрастания количества его продуктов способствует ухудшению физических параметров мембран, снижению способности красных клеток крови к деформации в микроциркуляторном русле [6].
Основная роль в регулировании производства эритроцитов в костном мозге принадлежит эритропоэтину. На сегодня известно, что при канцерогенезе отсутствует адекватное увеличение уровня эритропоэтина [7]. Состояние гипоксии выступает как стимулятор синтеза эритропоэтина, но увеличение уровня гормона при канцерогенезе недостаточно для предотвращения анемии. Таким образом, анемия у онкологических больных возникает в результате нарушения гемопоэза [8].
Атомно-силовая микроскопия (АСМ) -уникальный метод исследования биологических объектов без фиксации. Благодаря большому пространственному разрешению АСМ на сегодняшний день является основным ин- струментом для изучения рельефа биологического объекта. Характерная форма эритроцитов и их относительно небольшая толщина позволяют получить прочный препарат на стекле и изучить стереометрическую характеристику этих форменных элементов [9].
Поскольку эритроциты достаточно быстро изменяют морфофункциональные характеристики при воздействии патологических факторов, очевидно, что изучение состояния их мембран при экспериментальном канцерогенезе может дать ценную информацию о функциональной неполноценности эритроцитов.
Цель исследования. Изучить морфометрические показатели эритроцитов и изменение эритропоэза у животных-опухоленосите-лей при развитии неопластического процесса.
Материалы и методы. Экспериментальные исследования проведены на белых беспородных крысах массой 180–200 г с перевиваемой асцитной опухолью яичников (АОЯ, штамм РЯ, РОНЦ им. Н.Н. Блохина, г. Москва). Прогрессирование данного типа опухоли проходит в 3 фазы: логарифмическая (с 4-х сут после перевивки), стационарная (с 8-х сут после перевивки), терминальная (с 13-х сут после перевивки). В качестве материала для исследования использовали периферическую кровь экспериментального животного. Забор крови осуществляли в стационарную (n=64) и терминальную (n=64) фазы роста опухоли. Контрольную группу составили здоровые половозрелые крысы (n=62). Гематологические показатели крови оценивали с помощью анализатора Mindray BC 3600. Уровень эритропоэтина оценивали в плазме крови иммуноферментным методом (Mouse/Rat Epo Immunoassay, США). Подсчёт ретикулоцитов производили на 1000 клеток. Оценку осуществляли с помощью светового микроскопа Nikon Eclipse E200. Исследование морфометрических показателей эритроцитов проводили на свежевысушенных мазках крови методом АСМ (Solver Pro, NT-MDT, г. Зеленоград, Россия) в полуконтактном режиме. Использовали фирменные кремниевые зонды с жесткостью 0,2 N/m, радиус закругления кончика зонда составлял 10 нм.
Все животные содержались в стандартных условиях вивария при естественном освещении и свободном доступе к воде и корму. Были соблюдены «Правила проведения работ и использования экспериментальных животных», утверждённые Приказом МЗ СССР № 755 от 12 августа 1977 г., положения Хельсинкской декларации Всемирной медицинской ассоциации от 1964 г., дополненной в 1975, 1983 и 1989 гг., а также требования этического комитета ИМЭиФК Ульяновского государственного университета (№ 10 от 15.06.2014).
Результаты и обсуждение. В результате проведенных исследований нами установлено прогрессирующее снижение показателей гематокрита как в стационарную, так в терминальную фазы роста опухоли. Средний объем эритроцита (МСV) на всех сроках роста опухоли статистически значимо не отличался от показателей группы контроля. Показатель среднего содержания гемоглобина в отдельном эритроците (MCH) статистически значимо снижался в стационарную и повышался в терминальную фазу, не достигая однако контрольных значений. Как в стационарную, так и в терминальную фазы отмечалось статистически значимое повышение коэффициента вариации размеров эритроцитов (RDW-CV) и ширины распределения эритроцитов по объему (RDW-SD) относительно контроля, что предполагает возникновение пойкилоцитоза и анизоцитоза (табл. 1).
Данные, представленные в табл. 2, свидетельствуют о статистически значимом повышении высоты эритроцита как в стационарную, так в терминальную фазы роста опухоли, статистически значимом изменении глубины впадины в стационарную фазу роста АОЯ (в терминальную фазу углубление впадины не отмечается). Также установлено достоверное повышение среднего диаметра эритроцита и изменение длины эритроцитов во всех изученных фазах роста экспериментальной неоплазмы. Площадь поверхности эритроцита увеличивалась при прогрессировании опухоли, что соответствует изменению формы от нормоцита к сфероциту.
Таблица 1
|
Показатели |
Контроль, n=62 |
Стационарная фаза, n=64 |
Терминальная фаза, n=64 |
|
Ht, % |
38,1±0,5 |
34,3±0,5* |
31,3±0,3* |
|
MCV, фл |
52,8±0,8 |
53,3±0,7 |
53,0±0,5 |
|
MCH, пг/мл |
21,30±2,01 |
15,8±1,6* |
17,2±1,3 |
|
MCHС, г/л |
401±38 |
295,7±31,3* |
318,5±28,1* |
|
RDW-CV |
0,166±0,002* |
0,185±0,002* |
0,2±0,001* |
|
RDW-SD |
32,1±0,2 |
33,1±0,2* |
34±0,2* |
Примечание. * - статистически значимые различия с показателями контроля (р<0,05).
Морфофункциональные показатели крови крыс с АОЯ
Таблица 2
Морфометрические параметры эритроцитов у животных-опухоленосителей
|
Показатели |
Контроль, n=62 |
Стационарная фаза, n=64 |
Терминальная фаза, n=64 |
|
Высота эритроцита, мкм |
0,453±0,010 |
0,505±0,020* |
0,364±0,010* |
|
Глубина впадины, мкм |
0,374±0,013 |
0,163±0,020* |
Без впадины |
|
Средний диаметр эритроцита, нм |
6,03±0,17 |
6,78±0,12* |
7,17±0,14 |
|
Длина, нм |
7,603±0,118 |
8,350±0,246* |
9,090±0,185* |
|
Площадь, мкм2 |
45,50±1,42 |
55,25±3,08* |
65,27±3,01* |
Примечание. * - статистически значимые различия с показателями контроля (р<0,05).
При сканировании образцов эритроцитов крыс контрольной группы методом АСМ в основном (98 %) обнаруживались нормоциты с типичной дисковидной формой (рис. 1). В стационарную фазу цитоархитектоника эритроцитов менялась. Основную массу (52 %) эритроцитов составляли обратимо деформированные формы (рис. 2). В терминальную фазу роста опухоли 50,8 % эритроцитов представляли собой сфероциты (рис. 3).
Таким образом, в процессе экспериментального канцерогенеза наблюдается рост количества дегенеративных форм.
Для оценки эритропоэза определяли объем эритроцитов, уровень гемоглобина, количество ретикулоцитов и концентрацию эритропоэтина в периферической крови живот-ных-опухоленосителей (табл. 3).
Из представленных данных (табл. 3) следует, что количество эритроцитов в периферической крови как в стационарную, так в терминальную фазы роста АОЯ снижается по сравнению с контролем. Одновременно значимо уменьшается количество гемоглобина, что ведёт к нарушению дыхательной функции крови (табл. 3). Подобные изменения зарегистрированы у больных с колоректальным раком, раком шейки матки и раком легкого [10–12]. В эксперименте у крыс «Вистар» при развитии карциносаркомы также зафиксировано токсическое влияние опухоли на систему кроветворения [13]. В то же время показано снижение количества эритроцитов в циркулирующей крови у животных-опухоле-носителей с АОЯ на 4-е и 8-е сут роста опухоли [14].
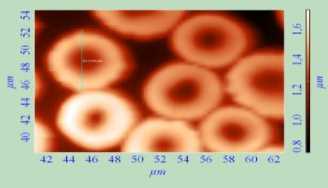
Рис. 1. Топология (а), боковое сечение профиля (б) и 3 D-изображение (в) интактных эритроцитов
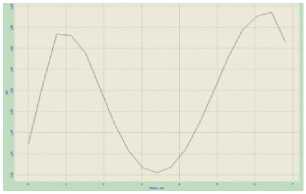
б
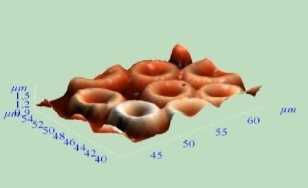
а
в
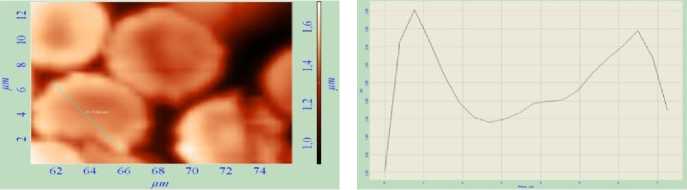
а б
Рис. 2. Топология (а), боковое сечение профиля (б) и 3D-изображение (в) эритроцитов в стационарную фазу
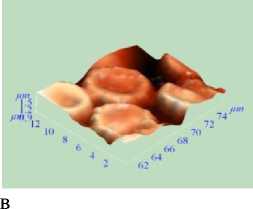
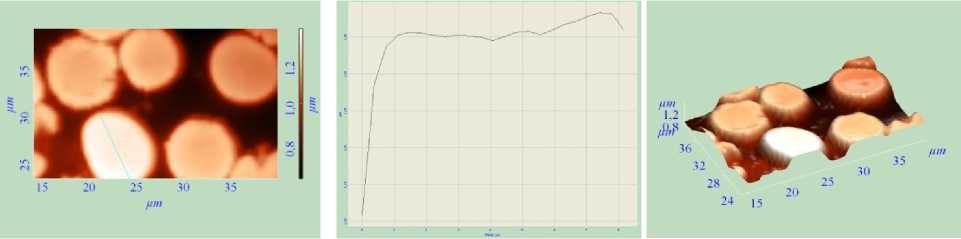
а б в
Рис. 3. Топология (а), боковое сечение профиля (б) и 3D-изображение (в) эритроцитов в терминальную фазу
Таблица 3
Показатели эритропоэза в организме-опухоленосителе при развитии АОЯ
|
Показатели |
Контроль, n=62 |
Стационарная фаза, n=64 |
Терминальная фаза, n=64 |
|
Эритроциты, млн/л |
7,20±0,05 |
6,40±0,08* |
6,00±0,04* |
|
Гемоглобин, г/л |
156,70±9,66 |
112,23±7,87* |
102,67±7,01* |
|
Ретикулоциты, % |
10,5±1,0 |
11,50±1,31 |
13,2±1,0* |
|
ЭПО, пкг/мл |
23,70±0,34 |
74,20±8,82* |
48,10±6,45* |
Примечание. * - статистически значимые различия с показателями контроля (р<0,05).
Регулирование производства эритроцитов в костном мозге осуществляет эритропоэтин. Нами было установлено статистически значимое повышение уровня эритропоэтина в плазме крови, наиболее выраженное в стационарную фазу роста опухоли (табл. 3). Одновременно увеличивается доля ретикулоцитов в крови, что также свидетельствует о стимуляции эритропоэза (табл. 3).
При экспериментальной карциносаркоме у крыс «Вистар» отмечается также повышение концентрации эритропоэтина. Авторы предполагают, что повышение эритропоэтина может являться отражением количественных, а не качественных перестроек механизмов контроля кроветворения при экспериментальном канцерогенезе [13].
Заключение. У крыс с экспериментальной АОЯ в динамике развития неоплазмы на фоне напряжённого эритропоэза снижается количество эритроцитов в периферической крови, количество гемоглобина, а также изменяется их цитоархитектоника, что может свидетельствовать о токсическом влиянии опухоли на систему кроветворения.
Список литературы Параметры эритропоэза и цитоархитектоника циркулирующих эритроцитов крыс с асцитной опухолью яичников
- Сладкова Е.А., Скоркина М.Ю., Забиняков Н.А. Морфофункциональные особенности клеток крови в условиях опухолевого роста. Биомедицина. 2013; 3: 63-67.
- Луговская С.А., Морозова В.Т., Почтарь М.Е. Лабораторная гематология. М.: ЮНИМЕД-пресс; 2002. 120.
- Боровская М.К., Кузнецова Э.Э., Горохова В.Г. Структурно-функциональная характеристика мембраны эритроцита и ее изменения при патологиях разного генеза. Бюллетень Восточно-Сибирского научного центра СО РАМН. 2010; 3 (73): 334-354.
- Крыжановский Г.Н. Дизрегуляционная патология. М.: Медицина; 2002. 632.
- Новицкий В.В., Степовая Е.А., Гольдберг В.Е. Эритроциты и злокачественные новообразования. Томск; 2000. 288.
- Диккер В.Е., Галенок В.А. Диабетическая микроангиопатия и нарушение транспорта кислорода. Обзор литературы и собственные данные. Терапевтический архив. 1986; 6: 106-110.
- Павлов А.Д., Морщакова Е.Ф. Лечение и профилактика анемии при злокачественных новообразованиях. Вопросы гематологии, онкологии и иммунопатологии в педиатрии. 2004; 3 (1): 56-63.
- Блиндарь В.Н., Зубрихина Г.Н. Диагностическая значимость определения уровня эритропоэтина в клинической практике (обзор литературы). Вестник РОНЦ им. Н.Н. Блохина РАМН. 2007; 18 (1): 10-16.
- Плескова С.Н. Атомно-силовая микроскопия в биологических и медицинских исследованиях. Долгопрудный; 2011. 184.
- Пумпур А.С. Роль оценки показателей общего анализа крови, биохимического анализа крови и гемостэзиограммы пациентов с колоректальным раком. Материалы Всероссийской научнопрактической конференции с международным участием «Актуальные вопросы колопроктологии». Воронеж; 2017; 3 (61): 64.
- Стуклов Н.И., Сушинская Т.В. Оценка эритроцитарных показателей периферической крови и активности гемостаза у больных раком шейки матки. Исследования и практика в медицине. 2016; 3 (1): 17-23.
- Даулетпаева Ж.О., Демина Е.В., Паньшина С.С. Состояние параметров красной периферической крови при наличии опухолей легкого. Science Time. 2016; 5 (29): 159-160.
- Тулеутаев М.Е., Узаков О.Ж., Ефремов А.В., Сафронов И.Д., Зубахин А.А., Самсонова Е.Н. Анализ клеток крови, костного мозга и медиаторов гемопоэза у крыс «Вистар» в динамике развития карциносаркомы Walker 256. Медицина Кыргызстана. 2016; 1 (3): 35-38.
- Трашков А.П., Панченко А.В., Васильев А.Г. Особенности роста экспериментальной АОЯ крыс и изменение гематологических показателей у животных-опухоленосителей под действием гемцитабина. Вестник Российской военно-медицинской академии. 2012; 2 (38): 90-96.


