Параметры острой токсичности и кожно-раздражающего потенциала кормовой композиции с метапробиотическими свойствами
Автор: Латыпов Г.Л., Мухаммадиева А.С., Валиуллин Л.Р., Гибадуллин Р.З., Мухаммадиев риШ.С., Мухаммадиев риН.С., Глинушкин А.П.
Статья в выпуске: 1 т.253, 2023 года.
Бесплатный доступ
В данной статье приведены результаты оценки параметров острой токсичности и кожно-раздражающего потенциала композиции на основе пробиотических штаммов L. acidophilus IV138, P. acidilactici PA-12, B. subtilis GA24 и их биологически активных метаболитов на теплокровных животных. Установлено, что изучаемая композиция не обладает острой токсичностью при пероральном введении белым мышам линии BALB/c, сенсибилизирующими свойствами при накожной аппликации беспородным морским свинкам. По результатам экспериментальных исследований разрабатываемая кормовая добавка с метапробиотическими свойствами отнесена к малоопасным средствам.
Острая токсичность, сенсибилизирующие свойства, метапробиотик, птицеводство
Короткий адрес: https://sciup.org/142237100
IDR: 142237100 | УДК: 619:615.9: | DOI: 10.31588/2413_4201_1883_1_253_174
Parameters of acute toxicity and skin irritant effect of feed composition with metaprobiotic properties
The paper presents the results of a study of the parameters of acute toxicity and skin-irritating potential of a composition based on probiotic strains L. acidophilus IV138, P. acidilactici PA-12, B. subtilis GA24 and their metabolites on BALB/c mice and outbred guinea pigs. It has been established that the studied composition does not have acute toxicity when administered orally to warm-blooded animals, sensitizing properties when applied to the skin. According to the results of experimental studies, the developed feed additive with metaprobiotic properties is classified as a low-hazard means.
Текст научной статьи Параметры острой токсичности и кожно-раздражающего потенциала кормовой композиции с метапробиотическими свойствами
В условиях интенсивного промышленного животноводства на ограниченных по площади производственных помещениях с высокой плотностью поголовья животных, применение в рационах кормов, содержащих антибиотики, привело к появлению резистентных к средствам данной группы условно-патогенных и патогенных микроорганизмов [1, 2]. С целью получения качественной продукции, прежде всего с точки зрения ее экологической безопасности, с 1 января 2006 г. в животноводстве стран Европейского союза запретили использование стимуляторов роста на основе антибиотиков при выращивании сельскохозяйственных животных [3]. По этой причине во всем мире, включая и Российскую Федерацию, ведутся работы, посвященные разработкам, внедрению нового поколения безопасных и эффективных кормовых добавок, в качестве альтернативы антибиотическим препаратам.
В настоящее время добавки с пробиотическими свойствами широко применяются в кормах для сельскохозяйственных животных, прежде всего свиней и птицы [3, 4]. Согласно определению, которое сформулировано членами группы экспертов ФАО и ВОЗ, «пробиотики» представляют собой «живые активные штаммы различных микроорганизмов, приносящих пользу здоровью организма хозяина при их использовании в необходимых количествах» [4, 5].
В последние несколько лет особое внимание начали привлекать метапробиотические добавки, которые состоят из различных активных штаммов и их метаболитов, и обладают комплексным действием [6]. Так, в научнопроизводственной компании «БИОТРОФ» разработана добавка под названием «Пробиоцид-Ультра» - комбинация штаммов бацилл и органических кислот (фумаровая и лимонная) микробного происхождения, способных ингибировать развитие условно-патогенных и патогенных бактерий, стимулировать рост и метаболическую активность кишечной нормофлоры цыплят-бройлеров [6]. В настоящее время Всероссийским научноисследовательским институтом фитопатологии (ФГБНУ ВНИИФ) создан опытный образец метапробиотического препарата для птицеводства. Добавка содержит в себе штаммы L. acidophilus
IV138, P. acidilactici PA-12, B. subtilis GA24 и их биологически активные метаболиты (антибиотики, экзополисахариды), обладающие антимикробными свойствами в отношении возбудителей кишечных инфекций и микотоксикозов цыплят-бройлеров, а также внеклеточные ферменты (целлюлазы, ксиланазы, амилазы, пектиназы, фитазы, протеазы и липазы) с различной субстратной специфичностью, способных к гидролизу различающихся по составу компонентов кормов сельскохозяйственных птиц.
Одним из основных требований, которые предъявляются к разрабатываемым кормовым добавкам, является доклинические исследования их безопасности [7, 8]. Общепринятым считается разделение токсикологических исследований на оценку общетоксических свойств и установление специфических видов токсичности.
Цель исследований – оценка параметров острой токсичности и кожнораздражающих свойств кормовой композиции на основе L. acidophilus IV138, P. acidilactici PA-12, B. subtilis GA24 и их биологически активных метаболитов.
Материал методы исследований. В работе применяли изготовленный ФГБНУ ВНИИФ опытный образец кормовой добавки, который состоит из пробиотических штаммов бактерий L. acidophilus IV138, P. acidilactici PA-12, B. subtilis GA24 и их биологически активных метаболитов.
Все процедуры с лабораторными животными, включая условия содержания и кормления, осуществляли по общепринятым этическим нормам обращения с животными, которые приняты Европейской Конвенцией по защите позвоночных животных, применяемых для экспериментальных и иных научных целей (Страсбург, 1986) и Международным рекомендациям Европейской Конвенции по защите используемых для экспериментальных исследований животных (1997), а также требованиям Директивы 2010/63/EU Европейского Парламента и Совета Европейского Союза от 22 сентября 2010 г.
Перед началом исследований прошедшие карантин лабораторные животные распределяли на группы, формирование которых проводили в соответствии с принципом аналогов, учитывая их возраст, живую массу и пол. Отклонение от среднего значения параметра массы тела в одной группе животных составляло не более 10%. Наблюдение за физиологическим состоянием, поведением и сохранностью животных в период карантина осуществляли ежедневно.
Класс острой токсичности опытного образца кормовой добавки с метапробиотическими свойствами устанавливали в соответствии с основополагающим документом OECD Test № 423 «Острая пероральная токсичность – метод определения класса острой токсичности» («Acute Oral Toxicity -Acute Toxic Class Method», 2001), позволяющей осуществить классификацию исследуемого препарата и определить его опасность по классификационной системе GHS [9].
Экспериментальное исследование проводили на белых мышах линии BALB/c, массой от 19 до 21 г обоего пола, в количестве 20 особей. Животные разделяли на две равные группы:
Контрольная группа – животные, которым вводили основу исследуемой кормовой композиции (n = 10).
Опытная группа – животные, которым вводили образец кормовой добавки, содержащей бактериальные штаммы с суммарным титром (1,0±0,3)*109 КОЕ/мл и их биологически активные метаболиты (n = 10).
При оценке острой токсичности тестируемый образец кормовой добавки вводили крысам однократно интрагастрально (атравматическим металлическим зондом) в вышеуказанных дозах. Объем вводимых образцов рассчитывали индивидуально с учетом массы каждого животного – 0,1 мл на 10 г живого веса.
После введения исследуемой кормовой композиции за животными устанавливали наблюдение для определения смертности и токсического действия: в 1-ые сутки в течение 12 часов, затем ежедневно 2 раза в день (утром и вечером) - клинический осмотр. В процессе экспериментального исследования оценивали физиологическое состояние организма животных – изменение состояния шерстного (волосяного) покрова, слизистых оболочек, подвижности, реакции на тактильные, болевые и звуковые раздражители, потребление воды и корма, интенсивность роста; определяли негативное воздействие на неврологический статус, включая наличие тремора (дрожания), судорожного расстройства, изменение подвижности и двигательной активности, признаков стереотипного поведения; заболеваемость и сохранность. По окончании экспериментального исследования (на 15 сутки) животных контрольной и опытной групп подвергали эвтаназии и проводили патологоанатомическое их вскрытие для макроскопического анализа внутренних органов.
Оценку раздражающего потенциала опытного образца кормовой добавки с метапробиотическими свойствами проводили способом накожных аппликаций [10]. Экспериментальное исследование осуществляли на беспородных морских свинках, массой тела от 380 до 400 г, в количестве 20 особей. Лабораторные животные разделяли на две равные группы:
Контрольная группа – животным, которым наносили основу исследуемой кормовой композиции (n = 10).
Опытная группа – животные, которым наносили тестируемый образец кормовой добавки, содержащей пробиотические штаммы с суммарным титром (1,0±0,3) ⋅ 109 КОЕ/мл и их биологически активные метаболиты (n = 10).
Однократную и многократные аппликации (20 повторности) изучаемой композиции проводили на предварительно эпилированные и обезжиренные участки кожи боковой поверхности туловища (площадь 4 см2) животных по 5 раз в неделю на протяжении 14 суток. Реакцию кожи на воздействие исследуемой композиции судили визуальным ее осмотром и оценивали в баллах по шкале оценки кожных проб. Определение наличия отека осуществляли количественным методом - измерением толщины складок кожи в мм с применением микрометра. Изучение кожно-раздражающих свойств кормовой добавки также проводили путем ежедневного наблюдения за клиническим состоянием подопытных животных в период эксперимента.
Результат исследований.
Исследование острой токсичности кормовой композиции, содержащей штаммы L. acidophilus IV138, P. acidilactici PA-12, B. subtilis GA24 и их биологически активные метаболиты, показало, что однократное внутрижелудочное ее применение не вызывает гибели белых мышей линии BALB/c в течение экспериментального периода (Таблица 1).
Таблица 1 – Результаты гибели мышей линии BALB/c после введения опытного образца кормовой добавки интрагастрально
|
Показатель |
Количество животных в группе |
Количество погибших животных, гол. |
|||
|
самцы |
самки |
||||
|
1 сутки |
14 сутки |
1 сутки |
14 сутки |
||
|
Контрольная группа |
10 |
0 |
0 |
0 |
0 |
|
Опытная группа |
10 |
0 |
0 |
0 |
0 |
Изменения поведенческих реакций и основные параметры жизнедеятельности животных опытной группы находились в пределах физиологической нормы и не отличались от контрольных значений.
Патологоанатомический анализ внутренних органов мышей контрольной и опытной групп показал отсутствие видимых морфологических изменений на поверхности их легких, сердца, почек, селезенки, печени, желудка и кишечника, а также различий их анатомического рисунка на 15 сутки после введения кормовой композиции в исследуемой дозе (Рисунок 1).
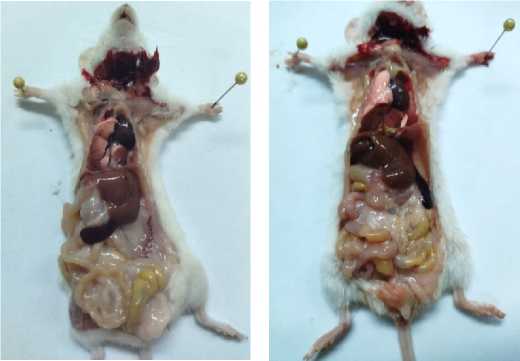
Рисунок 1 – Определение состояния внутренних органов мышей линии BALB/c: 1 – контрольная группа животных, 2 – группа животных после интрагастрального введения метапробиотической композиции
Экспериментальное исследование раздражающего эффекта разрабатываемой кормовой добавки на лабораторных животных показало, что композиция, содержащая пробиотические штаммы и их метаболиты, при однократном и многократном нанесении на кожные покровы морских свинок не приводила к возникновению эритемы или отеков (Рисунок 2).
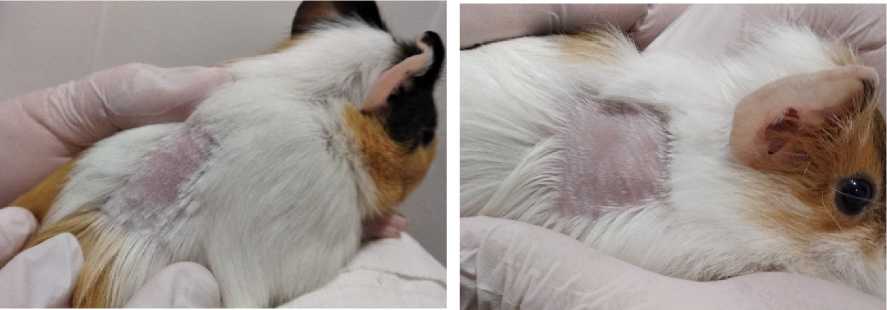
Рисунок 2 – Состояние кожных покровов беспородных морских свинок: 1 – контрольная группа животных, 2 – группа животных после нанесения метапробиотической композиции
На протяжении всего периода эксперимента за подопытными морскими свинками видимых патологических изменений, таких как инфильтрация, изъязвления (некроз), геморрагия в области воздействия выявлено не было. Не было установлено и изменение местной температуры животных. Суммарный балл на появление реакции кожи в соответствии со шкалой оценки кожных проб составил 0 баллов, что указывает на отсутствие опасности сенсибилизации организма животных (Таблица 2).
Статистически значимых различий в толщине кожной складки при аппликации проб в контрольной и опытной группах животных в течение наблюдения не установлено (результаты не показаны).
После накожного нанесения морским свинкам изучаемой кормовой композиции поведенческие реакции и основные параметры их жизнедеятельности находились в пределах физиологической нормы и не отличались от контрольных значений. По массе тела животных достоверных отклонений не выявлено. Выстриженные участки кожи боковой поверхности туловища опытных животных быстро зарастали молодой шерстью и не отличались по густоте с контрольной группой.
Таблица 2 – Результаты раздражающего потенциала опытного образца кормовой добавки при аппликации на кожные покровы беспородных морских свинок
|
Группа |
Количество животных в группе |
Оценка в баллах |
Раздражающий эффект |
||
|
самцы |
самки |
самцы |
самки |
||
|
Контрольная группа |
10 |
0 |
0 |
Отсутствует |
Отсутствует |
|
Опытная группа |
10 |
0 |
0 |
Отсутствует |
Отсутствует |
Заключение. Оценка параметров острой токсичности и раздражающего действия композиции на основе L. acidophilus IV138, P. acidilactici PA-12, B. subtilis GA24 и их биологически активных метаболитов показала, что кормовая добавка не обладает острой токсичностью при пероральном введении теплокровным животным, сенсибилизирующими свойствами при накожной аппликации. По результатам экспериментальных исследований разрабатываемая кормовая добавка с метапробиотическими свойствами отнесена к малоопасным средствам.
Работа выполнена за счет финансовых средств, выделенных в рамках государственной поддержки Всероссийского научноисследовательского института фитопатологии для повышения его конкурентоспособности среди научных центров Российской Федерации и зарубежья, а также поддержки гранта Президента РФ № МК-2439.2022.5 (соглашение № 075-15-2022-414 от «12» мая 2022 г).
Резюме
В данной статье приведены результаты оценки параметров острой токсичности и кожно-раздражающего потенциала композиции на основе пробиотических штаммов L.
acidophilus IV138, P. acidilactici PA-12, B. subtilis GA24 и их биологически активных метаболитов на теплокровных животных. Установлено, что изучаемая композиция не обладает острой токсичностью при пероральном введении белым мышам линии BALB/c, сенсибилизирующими свойствами при накожной аппликации беспородным морским свинкам. По результатам экспериментальных исследований разрабатываемая кормовая добавка с метапробиотическими свойствами отнесена к малоопасным средствам.
Список литературы Параметры острой токсичности и кожно-раздражающего потенциала кормовой композиции с метапробиотическими свойствами
- Валиуллин, Л. Р. Бактерии -антагонисты возбудителей кишечных инфекций и продуценты комплекса целлюлаз как основа для создания добавок, объединяющих функции пробиотика и кормового фермента / Л. Р. Валиуллин, Риш. С. Мухаммадиев, Рин. С. Мухаммадиев [и др.] // Достижения науки и техники АПК. - 2021. - Т. 35. - № 9. - С. 60-66.
- Еганян, Е. С. Оценка острой токсичности и местнораздражающего действия кормовой добавки Абиопептид-плюс / Е. С. Еганян // Сборник научных трудов Краснодарского научного центра по зоотехнии и ветеринарии. - 2021. - Т. 10. -№ 1. - С. 341-344.
- Йылдырым, Е. А. Метапробиотики вместо антибиотиков / Е. А. Йылдырым, Л. А. Ильина, Д. Г. Тюрина [и др.] // Птицеводство. -2020. - № 11. - С. 33-39.
- Миронов А. Н. Руководство по проведению доклинических исследований лекарственных средств / А. Н. Миронов. -М.: Гриф и К., 2012. - 944 с.
- Мухаммадиев, Р. С. Исследование общетоксических свойств пробиотического препарата на основе молочнокислых и пропионовокислых микроорганизмов in vivo / Р. С. Мухаммадиев, А. М. Тремасова [и др.] // Бутлеровские сообщения. - 2020. -Т. 64. - № 12. - С. 11-17.
- Руководящий документ OECD Test № 423 "Acute Oral Toxicity - Acute Toxic Class Method". -14 с. -.
- Феоктистова, Н. В. Биопрепараты микробного происхождения в птицеводстве / Н. В. Феоктистова, А. М. Марданова, М. Т. Лутфуллин [и др.] // Учен. зап. Казан. ун-та. Сер. Естеств. науки. - 2018. - Т. 160 - С. 395-418.
- Хадиева, Г. Ф. Влияние пробиотиков Bacillus subtilis GM2 и GM5 на рост и усвояемость кормов у цыплят-бройлеров / Г. Ф. Хадиева, М. Т. Лутфуллин, А. А. Николаева [и др.] // Учен. зап. Казан. ун-та. Сер. Естеств. науки. - 2019. - Т. 161, кн. 3. - С. 472-489.
- Bajagai S. FAO. 2016. Probiotics in animal nutrition - Production, impact and regulation by Yadav / S. Bajagai, Athol V. Klieve, Peter J. Dart and Wayne L. Bryden // FAO Animal Production and Health Paper №179. - Rome. - 2017. - Available at: http://www.fao.org/3/a-i5933e.pdf. Accessed October 31, 2017.
- FAO. Guidelines for the Evaluation of Probiotics in Food. Report of a Joint FAO/WHO Working Group on Drafting Guidelines for the Evaluation of Probiotics in Food. - London, Ontario, Canada. - 2002. - 11 p.


