Патогенетические аспекты лечения и профилактики хронической рецидивирующей герпес-вирусной инфекции
Автор: Коростелев А.А., Гаврилкина И.А., Ко- Строва Т.О., Мартыненко И.В.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 4 т.22, 2007 года.
Бесплатный доступ
Представлены обобщенные данные литературы, ка- сающиеся клинико-эпидемиологических аспектов за- болеваний, вызываемых вирусами семейства герпеса, их взаимосвязи с иммунодефицитными состояниями, факторов риска возникновения и рецидивирования болезни. В настоящее время лечение герпес-вирусной ин- фекции остается до конца не решенным вопросом. Поиск новых средств терапии герпеса является актуальной задачей дермато-венерологии. Полученные данные позволяют сделать вывод о необходимости применения при лечении рецидиви- рующего герпеса препаратов не только с противогерпе- тической активностью, но и иммунокорригирующего действия, таких, как Ликопид и Имунофан. При раннем ежедневном назначении Ликопида и Имунофана реэпителизация наступала быстрее, а длительность рецидива сокращалась. Клиника течения рецидива на фоне приема пре- парата отличалась слабой выраженностью местных и общих симптомов. Количество рецидивов в ближайшем отдаленном периоде после курса терапии уменьшилось.
Вирус простого герпеса, простой герпес, инфицированность, заболеваемость, иммунодефицит, лечение, профилактика, ликопид, имунофан
Короткий адрес: https://sciup.org/14918777
IDR: 14918777 | УДК: 616.523-07:615.37
Pathogenetic aspects of chronic recurrent herpes-viral infection treatment and prophylaxis
Literature data concerning clinical-epidemiologic aspects of the disease which are due to herpes viruses, their interrelations with immune-deficient states, risk factors of occurrence and recurrence of the diseases are given in the article. The data obtained allow to come to the conclusion about necessity of using drugs having not only anti-herpetic activity but immune correcting ones such as Licopid and Immunofan.
Текст научной статьи Патогенетические аспекты лечения и профилактики хронической рецидивирующей герпес-вирусной инфекции
ПАТОГЕНЕТИЧЕСКИЕ АСПЕКТЫ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ХРОНИЧЕСКОЙ РЕЦИДИВИРУЮЩЕЙ ГЕРПЕС-ВИРУСНОЙ ИНФЕКЦИИ
ГОУ ВПО «Кемеровская государственная медицинская академия»
Инфекционные заболевания, вызываемые вирусами семейства герпеса, являются одними из наиболее распространенных и обусловливают развитие чрезвычайно широкого спектра клинических проявлений. Это определяет не только медицинскую, но и огромную социальную значимость проблемы. Несмотря на многочисленные исследования в области клинической вирусологии, проблемы герпес-вирусных инфекций, и прежде всего вируса простого герпеса (ВПГ), не теряют актуальности, приобретая со временем новое звучание [2].
Лечение больных с герпетической инфекцией вызывает определенные трудности. В первую очередь это связано со склонностью ВПГ к пожизненному персистированию в организме хозяина и частотой рециди-вированию, а также высокой частотой латентных форм [15, 19]. На выбор терапии влияют частота и степень тяжести рецидива, а также нарушения иммунного и интерферонового (ИФН) статуса.
Герпетическую инфекцию в последнее время относят к болезням иммунной системы [9], поскольку частота и тяжесть заболевания более выражены у иммунокомпрометированных лиц (с первичным или вторичным иммунодефицитом), а также у новорожденных в связи с незрелостью их иммунной системы [16, 20]. Обладая тропизмом к иммунокомпетентным клеткам ВПГ способствует снижению сопротивляемости организма другим инфекционным заболеваниям.
Различным компонентам иммунной системы принадлежит разная роль в элиминации внеклеточных (пиогенных) и внутриклеточных микроорганизмов [10, 11, 17]. В элиминации первых (стафилококки, стрептококки, клебсиеллы и др.) главную функцию выполняет триада: нейтрофилы, иммуноглобулины, комплемент, причем гибель микроорганизма происходит в основном в нейтрофиле, а комплемент и иммуноглобулины (опсонины) усиливают этот процесс. В элиминаци внутриклеточных микроорганизмов (микобактерии, вирусы, простейшие и др.) главная роль принадлежит другой триаде: Т-лимфоциты, натуральные киллеры (НК), макрофаги, причем все 3 компонента обладают способностью синтезировать цитокины: у-интерферон (у-ИНФ), интерлейкин (ИЛ)-1, ИЛ-2, фактор некроза опухоли, резко усиливающие их функциональные свойства.
Регуляторные Т-клетки играют ключевую роль в регуляции антителообразующих В-клеток и эффекторных Т-клеток.
Рецидивы герпетической инфекции находятся под иммунным контролем, состояние иммунодефицита ведет к увеличению их частоты, более длительным периодам распространения вируса и пролонгированию симптомов [9].
Таким образом, учитывая полученные данные наиболее рациональным представляется использование в лечении хронического рецидивирующего герпеса иммунотропных препаратов, реализующих свой эффект через клетки моноцитарно-фагоцитирующей системы и влияющих на восстановление популяции и функции Т-хелперов, цитотоксических клеток, а также нормализующих синтез цитокинов и иммуноглобулинов.
Целью исследования явилось изучение роли нарушений иммунной системы в патогенезе хронической рецидивирующей герпес-вирусной инфекции и разработка методов их коррекции, а также профилактики заболевания.
Обследованы 67 пациентов (35 мужчин и 32 женщины в возрасте от 18 до 45 лет) с хронической рецидивирующей герпес-вирусной инфекцией (ХРГВИ) в период клинического обострения (44 больных) и ремиссии заболевания (23 пациента). Верификацию диагноза проводили на основании данных клиникоэпидемиологического и серологического (с помощью иммуноферментного анализа определяли антигерпе-тические IgM- и IgG-антитела серотипов 1 и 2).
Критерием исключения из исследования являлось наличие инфекционных и воспалительных процессов иной этиологии. Все пациенты были обследованы до начала проведения лечения.
Контрольную группу (без проведения иммунокоррекции) составили 23 пациента, которым иммунокоррекция и иммунопрофилактика не проводилась по причине отказа от приёма иммунотропных препаратов.
В контрольную (здоровую) группу были включены 25 здоровых доноров с аналогичными характеристиками по полу и возрасту, не страдавших инфекционными заболеваниями и не предъявлявших на момент обследования жалоб соматического профиля.
Общий анализ крови проводили с использованием гематологического анализатора «HEMATOLUKS».
Оценку системного иммунитета осуществляли путем определения в крови абсолютного и относительного количества лейкоцитов и лимфоцитов.
Субпопуляционный состав лимфоцитов (CD3+, CD4+, CD8+, CD16,56+, СД19,22+, лимфоцитов, несущих рецептор CD25+ и СД 95+ ( Fas – антиген, рецептор апоптоза), оценивали с использованием прямомеченных моноклональных антител («Caltag»), методом проточной цитофлюорометрии на лазерном проточном цитофлюориметре FACScan производства фирмы «Becton Dickinson».
Цитометричский анализ образцов проводился в программе Cellquest.
Определение концентрации цитокинов проводили с использованием наборов ЗАО «Вектор Бест» на основе «sandwich» метода твердофазного иммунофер-ментного анализа.
Для иммунотерапии и иммунопрофилактики хронического рецидивирующего герпеса нами были применены препараты Ликопид и Имунофан отечественного производства.
Ликопид. Действующее начало ликопида глюкозаминилмурамил-дипептид (ГМДП), представляет собой универсальный минимальный компонент бактериальной стенки и является естественным стимулятором иммунной системы человека [3, 7].
Имунофан. Синтетический регуляторный гексапептид, являющийся иммуноактивным производным фрагментом молекулы тимопоэтина [4, 5, 6].
Анализ данных проводили с использованием статистического пакета программ Statistica 6.O. Вычислялись среднее арифметическое значение (М), выборочное стандартное отклонение (STD) и ошибка средней арифметической величины (m). Данные в таблицах представлены в виде М±m. Все получен-
в иммунном статусе 75% изменений
25 %
Рис. 1. Структура пациентов по иммунному статусу
Проведенное клинико-лабораторное и иммунологическое обследование 67 пациентов с хронической рецидивирующей герпес-вирусной инфекцией (ХРГВИ) выявило две группы больных: у 50 (75%) больных имелись как клинические признаки ХРГВИ, так и иммунологические изменения, а у 17 (25%) больных при наличии клинической картины ХРГВИ, отклонения в иммунном статусе отсутствовали (рис. 1).
Основные изменения в иммунном статусе пациентов с ХРГВИ в процентном отношении представлены на рис. 2.
В группе пациентов с измененными параметрами иммунной системы были обнаружены следующие отклонения: снижение абсолютного количества лимфоцитов отмечалось у 16 пациентов (32%), количества СД3+ лимфоцитов – у 13 пациентов (16%), СД4+ лимфоцитов – у 27 пациентов (54%), СД8+ лимфоцитов – у 9 пациентов (18%), СД16,56+ лимфоцитов – у 11 пациентов (22%), СД19,22+ лимфоцитов – у 7 пациентов (14%), снижение иммуно-регуляторного индекса (ИРИ) наблюдалось у 32 пациентов (64%).
Более детально изменения в иммунном статусе у пациентов с ХРГВИ представлены в табл. 1.
В ходе анализа иммунограмм у пациентов, имеющих изменения в параметрах иммунной системы на фоне снижения абсолютного содержания лимфоцитов в крови до 27,6%, обнаружено снижение количества Т-лимфоцитов до 62,5% (р<0,05), Т-хелперов до 31,2% (р<0,05) , NK-клеток до 6,5%, снижение показателя ИРИ до 1,1 (р<0,05).
ные результаты проверяли на нормальность распределения с помощью критерия Колмогорова-Смирнова. В случае когда закон распределения измеряемых величин можно было считать нормальным, был использован t-критерий Стьюдента. Для признаков, не отвечающих требованиям нормального распределения, использовали непараметрический тест Манна-Уитни (U-тест) для независимых совокупностей и Т-тест Вилкоксона для попарно связанных выборок.
Критический уровень значимости (р) при проверке статистических гипотез принимался равным 0,05.
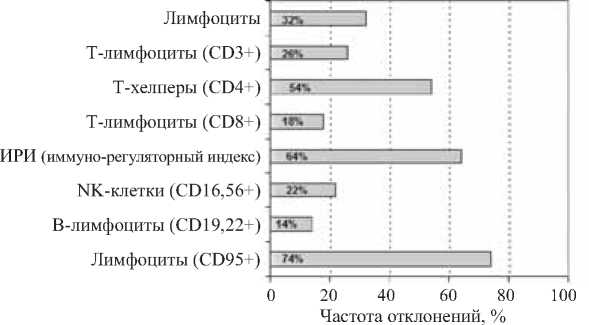
Рис. 2. Частота отклонений в параметрах иммунного статуса у пациентов с хронической рецидивирующей герпес-вирусной инфекцией
Таблица 1
Содержание лимфоцитов и их субпопуляций в крови у пациентов с ХРГВИ
|
Показатели |
Пациенты с ХРГВИ n = 67 |
Здоровые доноры n = 25 |
|
Лимфоциты % |
27,6 ± 4,5 |
35,7± 2,5 |
|
абс. (109/л) |
1,7 ± 0,4 |
2,35±0,7 |
|
Т-лимфоциты |
62,5 ± 1,8* |
71,2±2,3 |
|
(СD3+)% абс. (109/л) |
1,2 ± 0,2 |
1,7 ±0,15 |
|
Т – хелперы |
31,2± 1,3* |
37,2±1,7 |
|
(СD4+) % абс. (109/л) |
0,5 ± 0,1 |
0,85 ±0,15 |
|
Лимфоциты |
21,1 ± 2,2 |
24,3 ± 3,1 |
|
(СD8+) % абс. (109/л) |
0,56 ± 0,05 |
0,75 ±0,1 |
|
ИРИ (иммуно-регуляторный индекс) |
1,1 ±0,2* |
1,8 ±0,3 |
|
NK-клетки |
6,5 ± 3,3 |
12 ±2,7 |
|
(СD16,56+) % абс. (109/л) |
0,17 ± 0,02 |
0,25 ±0,03 |
|
В-лимфоциты |
9,4 ± 2,1 |
16 ±1,8 |
|
(СD19,22+)% абс. (109/л) |
0,25 ± 0, 0 4 |
0,4 ±0,02 |
Примечание: *– р< 0,05 по сравнению со здоровыми донорами.
Проведенное исследование выявило увеличение экспрессии Fas- антигена на лимфоцитах пациентов при рецидиве герпетической инфекции (табл. 2).
Таким образом, для хронического рецидивирующего герпеса характерно повышение экспрессии Fas-антигена при обострении заболевания и его снижение в период ремиссии, что может быть использовано для иммунологического мониторинга и прогнозирования рецидива заболевания.
Для оптимального иммунного ответа при обострении герпеса важно нормальное содержание СD4+ -клеток, которые после стимуляции вирусом продуцируют интерфероны (ИФН) и другие лимфокины, активи-
Таблица 2
Экспрессия СД95+ на лимфоцитах пациентов с ХРГВИ
|
Лимфоциты |
Здоровые доноры n=25 |
Пациенты с ХРГВИ |
|
|
Стадия обострения n=44 |
Стадия ремиссии n=23 |
||
|
Количество CD95+ -лимфоцитов, % |
11,2± 1,5 |
23,4±2,7* |
14,2±2,3 |
Примечание: * – р< 0,05 по сравнению со здоровыми донорами.
рующие макрофаги, стимулирующие рост и созревание клеток-предшественников и антителообразующих клеток, а также пролиферацию антигенспецифических цитотоксических Т-лимфоцитов [9].
Наиболее частый тип нарушения интерферонового статуса в острой стадии различных заболеваний увеличение титров циркулирующего ИФ и одновременно глубокое подавление ИФН - продуцирующей способности иммуноцитов [9].
Имеются данные [18], показывающие, что для адекватной оценки состояния иммунной системы у пациентов с часто рецидивирующей герпетической инфекцией (более 10 раз в год) необходимо подробно исследовать систему ИФН-у.
Учитывая вышеизложенное, нами было проведено исследование содержания сывороточного ИНФ-у у пациентов с хроническим рецидивирующим герпесом в стадии обострения и ремиссии заболевания. Результаты исследования приведены в табл. 3.
Таблица 3
Содержание сывороточного интерферона-у у пациентов с ХРГВИ
|
Концентрация в сыворотке пг/мл |
Здоровые доноры n=25 |
Пациенты с ХРГВИ |
|
|
Стадия обострения n=44 |
Стадия ремиссии n=23 |
||
|
ИФН-у |
17,2±3,6 |
81,5±15,3* |
26,7±7,2 |
Примечание: * – р< 0,05 по сравнению со здоровыми донорами.
В стадии обострения герпетической инфекции выявлено увеличение содержания сывороточного ИНФ-у, что может быть использовано для прогнозирования рецидива заболевания.
Иммунотерапия является наиболее естественным методом лечения герпетической инфекции, поскольку имеются предпосылки к управлению иммунным ответом.
Главной мишенью применения иммуномодулирующих препаратов служат вторичные иммунодефициты, которые проявляются частыми, рецидивирующими, трудно поддающимися лечению инфекционно-воспалительными процессами разной локализации. В основе любого хронического инфекционно-воспалительного процесса лежат те или иные изменения в иммунной системе, которые и являются одной из причин этого процесса. Изучение параметров иммунной системы не всегда выявляет эти изменения.
В связи с этим при наличии хронического инфекционно-воспалительного процесса больному можно назначить иммуномодулирующие препараты даже в том случае, если иммунодиагностическое исследование не выявило существенных отклонений в иммунном статусе [13, 14].
В работе использовалась следующая схема проведения иммунокоррекции при хроническом рецидивирующем герпесе:
-
- Ликопид - 1 мг, под язык, утром до завтрака, один раз в день, курс 10 дней;
-
- Имунофан - 1 мл (0,005%), внутримышечно, один раз в три дня, курс 30 дней.
На фоне проводимой иммунокоррекции у большинства пациентов в стадии обострения ХРГВИ длительность течения рецидива и период реэпителизации сократились в среднем с 7 до 3,5 дней.
При приеме ликопида и имунофана отмечались положительные изменения гематологических и иммунологических показателей – увеличение исходно сниженного общего числа лейкоцитов и нейтрофилов, повышение числа лимфоцитов и Т–лимфоцитов (СД3+, СД4+), (р<0,05), нормализация значений иммуно-регуляторного индекса (ИРИ) (р<0,05), а также естественных киллеров (табл. 4).
Таблица 4
Содержание лимфоцитов и их субпопуляций в крови у пациентов с ХРГВИ до и после проведения иммунокоррекции
|
До коррекции |
После коррекции |
|
|
Лимфоциты % |
27,6±4,5 |
34,7±5,2 |
|
абс. (109/л) |
1,7±0,4 |
1,9±0,5 |
|
Т-лимфоциты |
62,5±1,8 |
68,3±2,2 |
|
(СD3) % абс. (109/л) |
1,2±0,2 |
1,5±0,3 |
|
Т-хелперы |
31,2±1,3 |
36,2±1,5* |
|
(СD4) % абс. (109/л) |
0,5±0,1 |
0,75±0,15 |
|
Т- лимфоциты |
21,1±2,2 |
22,5±4,3 |
|
(СD-8) % абс. (109/л) |
0,56±0,05 |
0,42±0,12 |
|
ИРИ (иммуно-регуляторный индекс) |
1,1±0,2 |
1,7±0,2* |
|
NK-клетки |
6,5±3,3 |
9,7±3,5 |
|
(СD16,56) % абс. (109/л) |
0,17±0,02 |
0,25±0,03 |
|
В-лимфоц. |
9,4±2,1 |
11,7±2,6 |
|
(СD19,22) % абс. (109/л) |
0,25±0, 0 4 |
0,35±0,02 |
Примечание: * – р< 0,05 по сравнению с пациентами до коррекции.
Таким образом, установлено, что развитие клинического эффекта при использовании иммунотропных препаратов сопровождается и нормализацией показателей иммунного статуса.
Для проведения иммунопрофилактики была сформирована группа из 67 пациентов с хроническим рецидивирующим герпесом (из них 32 – с клиническими проявлениями герпетической инфекции и 35 – вне стадии обострения герпеса).
Иммунопрофилактику хронического рецидивирующего герпеса проводили по единой схеме (табл. 5).
Таблица 5
Схема иммунокоррекции и иммунопрофилактики ХРГВИ
|
Иммунокоррекция |
Первый этап иммунопрофилактики через 2 месяца |
Второй этап иммунопрофилактики через 4 месяца |
|
Ликопид |
Ликопид: |
Ликопид |
|
Курс – 10 дней |
Курс – 10 дней |
Курс – 10 дней |
|
Имунофан |
Имунофан: |
Имунофан |
|
Курс – 30 дней |
Курс – 30 дней |
Курс – 30 дней |
-
- Ликопид - 1 мг, под язык, утром до завтрака, один раз в день, курс лечения 10 дней;
-
- Имунофан - 1 мл (0,005%), внутримышечно, один раз в три дня, курс лечения 30 дней;
Периодичность приема ликопида и имунофана обусловлена их фармакокинетикой [3, 4, 5, 6, 7].
Выявлена зависимость эффективности иммунопрофилактики от двух факторов: во-первых, от времени проведения иммунопрофилактики в различные стадии заболевания; во-вторых, от наличия или отсутствия изменений в иммунном статусе больных.
Так, при проведении курса иммунопрофилактики в группе больных в стадии обострения заболевания частота рецидивов снизилась до 52,4% (у 14 из 32 пациентов), а в группе больных в стадии ремиссии ХРГВИ – до 31,7% (у 11из 35 пациентов).
Результаты иммунопрофилактики считали положительными у тех больных, у которых рецидивы заболевания по окончании терапии отсутствовали в течение 3 месяцев.
При проведении курса иммунопрофилактики, в группе больных ХРГВИ с наличием изменений в иммунограмме частота рецидивов снизилась до 47,3% (рецидивы наблюдались у 23 из 48 пациентов), а в группе больных с отсутствием изменений в иммунограмме до - 32,4% (у 6 из 19 пациентов).
Таким образом, основными нарушениями в иммунном статусе пациентов с хроническим рецидивирующим герпесом является снижение Т-лимфоцитов, Т- хелперов, ИРИ (иммуно-регуляторного индекса). При этом повышается содержание в сыворотке крови интерферона-у и экспрессия рецептора апоптоза CD95+ (Fas-антигена) на поверхности лимфоцитов.
Применение иммунокорригирующей терапии при хроническом рецидивирующем герпесе отечественными препаратами Ликопид и Имунофан способствует нормализации показателей иммунной системы - увеличивается число Т-лимфоцитов (CD3+), Т-хелперов (CD4+), натуральных киллеров (CD16+), нормализу- ется ИРИ (иммуно-регуляторный индекс). Клинически это проявляется в сокращении сроков лечения и уменьшении числа рецидивов заболевания.
Лучшим вариантом иммунопрофилактики хронической рецидивирующей герпес-вирусной инфекции является проведение иммунокоррекции во время ремиссии заболевания и у пациентов с исходно нормальными показателями иммунограммы.
Снижение возникновения рецидивов у пациентов с хронической рецидивирующей герпес-вирусной инфекцией почти в два раза по сравнению с пациентами контрольной группы убедительно доказывает необходимость проведения иммунопрофилактики в комплексном лечении ХРГВИ.
-
1. Андронова, Т.М. Ликопид (ГМПД) – современный отечественный, высокоэффективный иммуномодулятор / Т.М. Андронова, Б.В. Пинегин. – М., 1995. – 30 с.
-
2. Баскакова Д.В., Халдин А.А., Брико Н.И. // Российский журнал кожных и венерических болезней. Приложение «Герпес». -2006.- № 2.- С. 26-30.
-
3. Иммунотерапевтические возможности применения Ли-копида у больных с вторичными иммунодефицитнымим состояниями: Метод. рекомендации № 96/181/ Мин. здравоохранения РФ. - М., 1996.
-
4. Иммунофан - регуляторный пептид в терапии инфекционных и неинфекционных болезней / В.В. Лебедев, Т.М. Шелепова, О. Г. Степанов и др. - М., 1998. – 119 с.
-
5. Лебедев, В.В. Имунофан – регуляторный пептид в терапии инфекционых и неинфекционных болезней / В.В. Лебедев, Т.М. Шелепова, О.Г. Степанова; под ред. В.И. Покровского. – М., 1998. – 118 с.
-
6. Лебедев, В.В. Имунофан - синтетический пептидный препарат нового поколения: иммунологические и патогенетические аспекты клинического применения/В.В. Лебедев // Иммунология.- 1999. - № 1. - С. 25-30.
-
7. Ликопид (глюкозаминилмурамилдипептид) - новый отечественный высокоэффективный иммуномодулятор для лечения и профилактики заболеваний, связанных со вторичной иммунологической недостаточностью/ В.Т. Иванов, Р.М. Хаитов, Т.М. Андронова и др. // Иммунология. - 1996. - № 2. - С. 4-6.
-
8. Марченко Л. А. Генитальная герпетическая инфекция у женщин (клиника, диагностика, лечение): Дис....д-ра мед. наук. - М., 1997.
-
9. Мирзоян Ж.В. // Акушерство и гинекология. -2000.-№ 4.- С. 15-17.
-
10. Петров Р. В., Хаитов Р. М., Пинегин Б. В. // Иммунология. - 1994. - № 6. - С. 6-9.
-
11. Петров Р. В., Хаитов Р. М., Пинегин Б. В. // Иммунология. - 1997. - № 4. - С. 4-7.
-
12. Пинегин, Б.В. Ликопид. Современный подход к профилактике и лечению иммунодефицитных состояний / Б.В. Пи-негин, Т.М. Андронова, М.Ю. Швецов. – М., 2004. – 82 с.
-
13. Хаитов Р. М., Пинегин Б. В. // Иммунология. - 2000. -№ 5. - 4 с.
-
14. Хаитов Р. М., Пинегин Б. В. // Иммунология. - 2003. -№ 4. - С. 196-203.
-
15. Скрипкин Ю. К., Машкиллейсон А. Л., Шарапова Г. Я. Кожные и венерические болезни. - М., 1995. - С. 197-203.
-
16. Сухих Г. Т., Ванько Л. В., Кулаков В. И. Иммунитет и генитальный герпес. - М., 1997.
-
17. Хаитов Р. М., Пинегин Б. В. // Медикал маркет. — 1999. № 31. - С. 6-9.
-
18. Черноусов А.Д., Пичугина Л.В., Гомберг М.А., Голубкова О.В., Пинегин Б.В., Георгий Голдава // Российский журнал кожных и венерических болезней. Приложение «Герпес». -2006.- № 2.- С. 30-33.
-
19. De Clercg Е. // Clin. Microb. Rev. - 1997. - Vol. 136. -P. 674-693.
-
20. Safrin S., Crumpacker C., Chatis P. et al. // N. Engl. J. Med. - 1991. -Vol. 325. - P. 551.
PATHOGENETIC ASPECTS OF CHRONIC RECURRENT HERPES-VIRAL INFECTION TREATMENT AND PROPHYLAXIS
A.A. Korostelev, I.A. Gavrilkina, T.O. Kostrova,I.V. Martynenko
Список литературы Патогенетические аспекты лечения и профилактики хронической рецидивирующей герпес-вирусной инфекции
- Андронова, Т.М. Ликопид (ГМПД) -современный отечественный, высокоэффективный иммуномодулятор/Т.М. Андронова, Б.В. Пинегин. -М., 1995. -30 с.
- Баскакова Д.В., Халдин А.А., Брико Н.И.//Российский журнал кожных и венерических болезней. Приложение «Герпес». -2006.-№ 2.-С. 26-30.
- Иммунотерапевтические возможности применения Ликопида у больных с вторичными иммунодефицитнымим состояниями: Метод. рекомендации № 96/181/Мин. здравоохранения РФ. -М., 1996.
- Иммунофан -регуляторный пептид в терапии инфекционных и неинфекционных болезней/В.В. Лебедев,Т.М. Шелепова, О. Г. Степанов и др. -М., 1998. -119 с.
- Лебедев, В.В. Имунофан -регуляторный пептид в терапии инфекционых и неинфекционных болезней/В.В. Лебедев, Т.М. Шелепова, О.Г. Степанова; под ред.В.И. Покровского. -М., 1998. -118 с.
- Лебедев, В.В. Имунофан -синтетический пептидный препарат нового поколения: иммунологические и патогенетические аспекты клинического применения/В.В. Лебедев//Иммунология.-1999. -№ 1. -С. 25-30.
- Ликопид (глюкозаминилмурамилдипептид) -новый отечественный высокоэффективный иммуномодулятор для лечения и профилактики заболеваний, связанных со вторичной иммунологической недостаточностью/В.Т. Иванов, Р.М. Хаитов, Т.М. Андронова и др.//Иммунология. -1996. -№ 2. -С. 4-6.
- Марченко Л. А. Генитальная герпетическая инфекция у женщин (клиника, диагностика, лечение): Дис.... д-ра мед. наук. -М., 1997.
- Мирзоян Ж.В.//Акушерство и гинекология. -2000.-№ 4.-С. 15-17.
- Петров Р. В., Хаитов Р. М., Пинегин Б. В.//Иммунология. -1994. -№ 6. -С. 6-9.
- Петров Р. В., Хаитов Р. М., Пинегин Б. В.//Иммунология. -1997. -№ 4. -С. 4-7.
- Пинегин, Б.В. Ликопид. Современный подход к профилактике и лечению иммунодефицитных состояний/Б.В. Пи-негин, Т.М. Андронова, М.Ю. Швецов. -М., 2004. -82 с.
- Хаитов Р. М., Пинегин Б. В.//Иммунология. -2000. -№ 5. -4 с.
- Хаитов Р. М., Пинегин Б. В.//Иммунология. -2003. -№ 4. -С. 196-203.
- Скрипкин Ю. К., Машкиллейсон А. Л., Шарапова Г. Я. Кожные и венерические болезни. -М., 1995. -С. 197-203.
- Сухих Г. Т., Ванько Л. В., Кулаков В. И. Иммунитет и генитальный герпес. -М., 1997.
- Хаитов Р. М., Пинегин Б. В.//Медикал маркет. -1999. № 31. -С. 6-9.
- Черноусов А.Д., Пичугина Л.В., Гомберг М.А., Голубко-ва О.В., Пинегин Б.В., Георгий Голдава//Российский журнал кожных и венерических болезней. Приложение «Герпес». -2006.-№ 2.-С. 30-33.
- De Clercg Е.//Clin. Microb. Rev. -1997. -Vol. 136. -P. 674-693.
- Safrin S., Crumpacker C., Chatis P. et al.//N. Engl. J. Med. -1991. -Vol. 325. -P. 551.


