Патогенетические закономерности каскадного механизма развития хронических гастродуоденальных заболеваний у детей, обусловленных потреблением питьевой воды ненадлежащего качества по содержанию продуктов гиперхлорирования и марганца
Автор: Устинова О.Ю., Лужецкий К.П., Маклакова О.А., Землянова М.А., Долгих О.В., Уланова Т.С.
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Медико-биологические аспекты оценки воздействия факторов риска
Статья в выпуске: 3 (7), 2014 года.
Бесплатный доступ
Исследованы патогенетические механизмы развития у детей хронических гастродуоденальных заболеваний, обусловленных потреблением питьевой воды ненадлежащего качества по содержанию продуктов гиперхлорирования (хлороформ) и марганца. Установлено, что клиническая манифестация патологического процесса у детей с повышенным содержанием марганца и хлороформа в крови сопряжена с развитием вегетативных дисфункций по парасимпатическому типу, реактивных изменений ткани печени, билиарной дисфункции по гипомоторному типу, нарушения моторики желудка и двенадцатиперстной кишки по гиперкинетическому варианту. Патогенетические закономерности развития у детей хронических гастродуоденальных заболеваний [Hp -], ассоциированных с воздействием продуктов гиперхлорирования (хлороформ) и марганца, предопределяют патоморфоз патологического процесса с развитием атрофических/субатрофических измененений слизистой верхних отделов желудочно-кишечного тракта.
Хроническая гастродуоденальная патология, дети, качество питьевой воды, продукты гиперхлорирования, марганец
Короткий адрес: https://sciup.org/14237879
IDR: 14237879 | УДК: 616-008
Pathogenic patterns in cascade mechanism of gastroduodenitis diseases' progress in children associated with drinking low quality water due to hyperchlorination and manganese content
We have studied the pathogenic mechanisms of chronic gastroduodenitis diseases in children consuming low quality drinking water with high content of chlorine and manganese. It was established, that clinic manifestation of pathogenic process is coupled with parasympathetic vegetative dysfunctions reactive changes of hepatic tissues, biliary (hypokinetic) dysfunction, gastric and duodenum motor activity (hyperkinetic) disorder. Pathogenic patterns of chronic gastroduodenal diseases [Hp -] in children, associated with products of hypochlorination (chloroform) and manganese exposure, predefine pathomorphism of pathologic process followed by atrophic/preatrophic changes of upper gastrointestinal mucosa.
Текст научной статьи Патогенетические закономерности каскадного механизма развития хронических гастродуоденальных заболеваний у детей, обусловленных потреблением питьевой воды ненадлежащего качества по содержанию продуктов гиперхлорирования и марганца
развития хронической гастродуоденальной патологии, ассоциированной с воздействием химических веществ техногенного происхождения, требуют дальнейшего изучения. Присутствие в питьевой воде остаточных продуктов гиперхлорирования и тяжелых металлов обусловливает возникновение дополнительных случаев гастродуоденальных заболеваний на уровне 18 ‰ в год, способствует увеличению частоты встречаемости тяжелых и осложненных форм с рецидивирующим течением и устойчивостью к консервативной терапии [1, 4, 9].
Целью исследования являлось изучение особенностей патогенеза хронических гастродуоденальных заболеваний [Hp-] у детей, обусловленных потреблением питьевой воды ненадлежащего качества по содержанию продуктов гиперхлорирования и марганца.
Материалы и методы. Оценка качества питьевой воды и атмосферного воздуха на территориях проживания детей проводилась на основании данных мониторинговых исследований ФИФ СГМ (согласно Постановлению правительства РФ № 60 от 02.02.2006 г. «Положение о проведении социально-гигиенического мониторинга» с изменениями от 04.09.2012 г.).
Оценка риска для здоровья населения, обусловленного потреблением питьевой воды ненадлежащего качества по содержанию продуктов гиперхлорирования и марганца, осуществлялась по стандартизованной методике в соответствии с «Руководством по оценке риска для здоровья населения при воздействии химических веществ, загрязняющих окружающую среду» (Р 2.1.10.1920-04) [8].
Медико-биологические исследования проводились с соблюдением этических принципов, изложенных в Хельсинкской декларации (1975 г., с дополнениями 1983 г.) и в соответствии с Национальным стандартом РФ ГОСТ-Р 52379-2005 «Надлежащая клиническая практика» (ICH E6 GCP) (утвержденным 27.09.2005 г.).
Группу наблюдения составили 116 детей в возрасте 7–10 лет (8,6±1,2 г.) с хрони- ческой гастродуоденальной патологией [Hp-] (МКБ-10: К29.3-29,9), проживавших на территории с неудовлетворительным качеством питьевой воды по санитарнохимическим показателям (продукты гиперхлорирования, марганец). В группу сравнения вошли 56 детей аналогичного возраста (8,4±1,4 г., р ≥ 0,05) с хронической гастродуоденальной патологией [Hp-] (МКБ-10: К29.3-29,9), проживавших на территории, где качество питьевой воды соответствовало гигиеническим нормативам. Группы были сопоставимы по гендерному параметру.
Лабораторное обследование включало: оценку состояние окислительно-антиоксидантных процессов (общая антиоксидантная активность сыворотки крови, содержание малонового диальдегида, Сu/Zn-супероксид-дисмутазы, глутатионпероксидазы, глутати-он-S-трансферазы, гидроперекисей липидов), факторов неспецифической резистентности (абсолютный фагоцитоз, процент фагоцитоза, индекс фагоцитоза, фагоцитарное число), иммунологического статуса (абсолютное и относительное содержание CD4+, CD25+, CD95+-лимфоцитов), неспецифической сенсибилизации (JgE общ ), гормонального статуса (уровень серотонина, дофамина, кортизола), нейромедиаторов, регулирующих процессы возбуждения и торможения (уровень глутамата и гамма-аминомасляной кислоты), содержания в крови пепсиногена 1 и пепсиногена 2, щелочной фосфатазы, аланиновой и аспарагиновой аминотрансфераз. Исследования выполнялись по традиционным методикам с использованием микроскопа Micros MC-200 (Австрия), автоматического биохимического анализатора Kone-lab (Финляндия), иммуноферментного анализатора EL×808 и стандартных тест-наборов. Методами иммуногенетического исследования (ПЦР-диагностика в режиме реального времени) определялась распространенность патологических аллелей генов СРОХ, CYP1A1 и частота полиморфизма гена сульфотрансферазы.
Полученная информация анализировалась статистическими методами (Statistica
-
6.0) и с помощью специальных программных продуктов, сопряженных с приложениями MS-Office. Сопоставление качественных бинарных признаков проводили методами непараметрической статистики с построением и анализом двумерных таблиц сопряженности с использованием критерия хи-квадрат (χ2). Для сравнения групп по количественным признакам использовали двухвыборочный критерий Стьюдента. Оценку зависимостей между признаками осуществляли методом однофакторного дисперсионного анализа (для качественных признаков) и методом корреляционнорегрессионного анализа (для количественных переменных).
Результаты и их обсуждение. Анализ санитарно-гигиенической ситуации по данным мониторинговых исследований показал, что на территории проживания детей группы наблюдения имело место превышение гигиенических нормативов качества питьевой воды по хлороформу – до 2,70 ПДК; хлору остаточному свободному – до 2,20 ПДК; хлору остаточному связанному – до 1,25 ПДК; дихлорметану – до 8,0 ПДК, марганцу – до 3,3 ПДК. На территории сравнения гигиенические нормативы качества питьевой воды по исследуемым ингредиентам не были превышены.
Оценка опасности возникновения нарушений здоровья населения, обусловленных потреблением питьевой воды ненадлежащего качества по содержанию продуктов гиперхлорирования и марганца, выявила наличие неприемлемого риска ( HI = 1,75–2,18) развития патологии нервной системы и гепатобилиарного тракта.
В ходе анамнестического обследования установлено, что дети, включенные в группы исследования, рождены от 1–3-й беременности, не имели врожденной патологии желудочно-кишечного тракта, были доношенными (95 % – группа наблюдения и 94,1 % – группа сравнения; p = 0,34), имели близкие при рождении весоростовые показатели (3241,3±154,6 г и 51,2±0,6 см – группа наблюдения; 3132,4±162,4 г и 50,37±1,56 см – группа сравнения; p = 0,43–0,48) и оценку по шкале Апгар (8,12±0,20 против 8,58±0,10 усл. ед. соответственно; p = 0,20). Частота регистрации в анамнезе острых кишечных инфекций в сравниваемых группах не имела различий (10,3 и 12,5 % соответственно, р = 0,67). В группе наблюдения в 41,7 % случаев ежемесячный доход на одного члена семьи составлял от 4001 до 7000 рублей (в группе сравнения - у 34,5 %, р = 0,42), менее 4000 рублей - в 42 % (52,4 % в группе сравнения, р = 0,08), более 7000 рублей - в 16,3 % (13,1 % в группе сравнения, р = 0,08). Большая часть детей (79,3 и 73,2 % соответственно, р = 0,37) проживали в благоустроенном жилье и использовали водопроводную воду без дополнительной очистки (95,0 и 87,5 % соответственно, р = 0,24). Нарушения режима питания отмечали 32,8 % родителей детей группы наблюдения и 25,0 % - группы сравнения (р = 0,29). Длительность заболевания в исследуемых группах составляла 2,1±1,1 г. и 1,9±1,2 г. соответственно (р = 0,72).
Результаты химико-аналитического исследования показали, что содержание марганца в крови у детей группы наблюдения достигало 0,0283±0,0042 мкг/см3 (референтная концентрация - 0,011 мкг/см3, р < 0,01), а хлороформа - 0,019891±0,006675 мкг/см3 (референтная концентрация - 0,0 мкг/см3, р < 0,01). В группе сравнения уровень марганца не превышал 0,0110±0,0004 мкг/см3 ( р = 0,78 к референтному), а хлороформа -0,001801±0,000001 мкг/см3 (р = 0,89 к референтному). В целом содержание марганца в крови детей группы наблюдения в 2,6 раза превышало показатель группы сравнения (р < 0,01), а хлороформа - в 10 раз (р < 0,001).
Сравнительный анализ частоты жалоб гастроинтестинального характера выявил, что дети группы наблюдения чаще отмечали снижение аппетита (91,4 и 61,0 % соответственно, р = 0,04), отрыжку воздухом (45,5 против 25,4 %, р = 0,03), боли в животе (58,6 против 37,2 %, р = 0,03), локализующиеся в эпигастрии (58,2 против 23,2 %, р < 0,001) или правом подреберье (61,2 против 32,1 %, р < 0,001), нарушение стула (78,5 против 57,1 %; р = 0,004). Среди жалоб астеновеге-тативного характера наиболее часто отмеча- лись: потливость (37,1 против 10,9 %, р = 0,02), быстрая утомляемость (16,4 и 8,6 % соответственно, р = 0,04), непереносимость транспорта (6,9 и 5,4 %, р = 0,82). У детей группы наблюдения признаки гепатобилиарной дисфункции регистрировались в 1,4 раза чаще, чем в группе сравнения (87,9 и 64,3 % соответственно, р = 0,001). Установлена достоверная причинно-следственная связь вероятности развития заболеваний желчевыводящих путей с повышенным содержанием в крови хлороформа (R2 = 0,293-0,448; F = 15,348 - 36,392; р = 0,001) и болезней нервной системы функционального характера - с увеличенным содержанием марганца и хлороформа (R2 = 0,50 - 0,77; F = 93,67 -109,62; р = 0,01-0,001).
Преобладающим типом исходного вегетативного тонуса у детей группы наблюдения являлась эйтония (в 50 % случаев), однако у 37,5 % установлен ваготонический вариант, что в 1,9 раза превышало аналогичные данные группы сравнения (20 %, р = 0,02). В группе наблюдения симпатико-тонический тип вегетативной реактивности отмечался лишь в 25 %, что в 1,2 раза реже, чем в группе сравнения (30 %, ОШ = 1,2; ДИ =1,1 -1,7), преобладающим же типом являлся ги-персимпатико-тонический (62,5 %); в группе сравнения этот вариант встречался в 1,5 раза реже - 43,3 % (ОШ = 1,45; ДИ = 1,16 - 3,11). Установлены прямые достоверные связи «повышенное содержание в крови марганца - развитие исходной ваготонии и гипер-симпатико-тонического типа вегетативной реактивности» ( R 2 = 0,37 - 0,42; F = 87,54 -- 118,12; р = 0,01).
При ультразвуковом сканировании гепатобилиарной области реактивные изменения печени в группе наблюдения регистрировались в 7 раз чаще (31,7 против 4,5 %, p = 0,01), кроме того, в 1,6-1,7 раза чаще определялась билиарная дисфункция по гипо-моторному типу (80,2 против 50,0 %, р = 0,001) и увеличение линейных размеров печени (12,2 и 7,0 % соответственно, ОШ = 1,74; ДИ = 1,32-3,76). Установлена достоверная связь между повышенным содержанием в крови детей хлороформа и раз- витием реактивных изменений печени (R2 = 0,39; F = 76,83; р = 0,01); увеличенным содержанием в крови марганца и наличием билиарной дисфункции по гипомоторному типу (R2= 0,41; F = 99,23; р = 0,01).
В ходе электроэнцефалографического исследования установлено, что измененный тип параметров биоритмики головного мозга у детей группы наблюдения регистрировался в 2 раза чаще (55,5 %), чем в группе сравнения (27,3 %; OR = 2,03; DI = 1,64 – 3,85), и имел преимущественно общемозговой, функциональный характер.
При исследовании биохимических показателей у детей группы наблюдения выявлены признаки оксидативного стресса: уровень гидроперекиси липидов в сыворотке крови составил 325,44±23,72 мкмоль/дм3, а МДА – 3,54±0,117 мкмоль/см3, что в 1,5–1,7 раза выше показателей группы сравнения
(р = 0,000 – 0,001); частота регистрации проб с повышенным уровнем гидроперекиси липидов составила 28 %, при отсутствии таковых в группе сравнения, МДА – 52 %, что в 5 раз выше аналогичных данных в группе сравнения. Установлена связь повышенного содержания гидроперекиси липидов и МДА – с концентрацией марганца в крови (OR = = 3,1 – 4,2; DI = 2,5 – 4,8; р = 0,001). Выявленный оксидативный стресс обусловлен истощением ресурсов антиоксидантной защиты от субклеточного до системного уровня: активность глутатионпероксидазы в сыворотке крови составила 30,95±3,31 нг/см3, Сu/Zn-супероксиддисмутазы – 36,45±2,16 нг/см3, что в 1,2–1,6 раза ниже таковых в группе сравнения (р = 0,001 – 0,0001); кроме того, в 1,2–1,4 раза была снижена активность глутатионпероксидазы, глутатион-S-трансферазы (р = 0,001). В целом частота регистрации пониженных уровней данных ферментов (51– 55 % случаев) была в 3,8–4,2 раза выше показателей группы сравнения (р = 0,001). Общий антиоксидантный статус, как интегральный показатель, у более чем 50 % детей группы наблюдения отражал выраженное снижение активности процессов антиоксидантной защиты (125,64±8,38 мкмоль/дм3, что в 2,2 раза ниже показателя группы сравнения, р = = 0,000). Установлена связь угнетения антиоксидантных процессов с концентрацией марганца и хлороформа в крови (OR = 2,6 – – 5,1; DI = 2,0 – 6,1; р = 0,000). Вклад марганца и хлороформа в развитие дисбаланса окислительно-антиоксидантных процессов составил 41–68 %, (F = 16,19 – 425,05; р = 0,000 – 0,040). В ходе лабораторного исследования у детей группы наблюдения установлен дисбаланс нейромедиаторов, регулирующих процессы возбуждения и торможения: повышенный в 1,5 раза относительно группы сравнения уровень глутамата (148,87±16,76 мкмоль/дм3, р = 0,001) и сниженный в 2 раза уровень гамма-аминомасляной кислоты в сыворотке крови (0,046±0,013 мкмоль/дм3, р = 0,000); частота регистрации измененных показателей была в 4,3–5,0 раза выше таковой в группе сравнения. Установлена связь повышения уровня глутамата и снижения гамма-аминомасляной кислоты с концентрацией марганца в крови (OR = 3,4 – 6,1; DI = 2,2 – 10,5; р = 0,000); вклад марганца в развитие дисбаланса нейромедиаторов составляет 64–79 % (F = = 145,06 – 287,55, р = 0,000). Кроме того, у детей группы наблюдения установлено нарушение синтеза гормонов гипофизарнонадпочечниковой оси (снижение содержания дофамина и кортизола – в 1,3 раза, серотонина – в 2,0 раза относительно таковых группы сравнения), имеющее достоверную связь с повышенным уровнем в крови марганца и хлороформа (R2 = 0,36 – 0,77; F = 28,74 – 94,62; р = 0,01). Результаты иммунологического обследования свидетельствуют о развитии у детей группы наблюдения транзи-торного иммунодефицита (снижение в 1,3– 1,6 раза показателей фагоцитоза, сывороточного IgА, активности Т-лимфоцитарного звена иммунного ответа, содержания IgА в слюне и повышение в 1,3 раза сывороточного IgEобщ относительно аналогичных сведений группы сравнения), достоверно связанного с повышенным содержанием в крови марганца и хлороформа (R2 = 0,33 – 0,63; F = 57,41 – 183,11; р = 0,01 – 0,001). Кроме того, у детей группы наблюдения в 1,3–1,6 раза чаще выявлялось повышение содержания щелочной фосфатазы, активности аспарагиновой аминотрансферазы, пепсиногена 2 на фоне угнетения активности пепсиногена 1, достоверно связанных с повышенным содержанием в крови марганца и хлороформа (R2 = 0,39 – 0,52; F = 33,67 – 121,76; р = 0,01 – 0,001). В ходе иммуногенетического обследования у 10,3 % детей группы наблюдения выявлен полиморфизм гена сульфотрансферазы, отвечающего за детоксикацию органических соединений; у 13,8 % – наличие патологического аллеля CYP1A1 (ген цитохрома), отвечающего за 1-ю фазу детоксикации органических токсикантов; у 14,7 % – патологического аллеля CPOX (копропорфириногено-ксидазы), отвечающего за конъюгацию ме-таллопротеинов. Следует подчеркнуть, что у детей, имеющих полиморфизм гена сульфотрансферазы и/или патологические аллели CPOX и CYP1A1, содержание марганца и хлороформа в крови на 15–25 % превышало среднегрупповые показатели.
Результаты проведенного исследования свидетельствуют о том, что на территориях с ненадлежащим качеством питьевого водоснабжения (превышение гигиенических нормативов по содержанию продуктов гиперхлорирования и марганца до 2,7–3,3 ПДК) риск развития у населения патологии нервной системы и гепатобилиарного тракта ( HI ) составляет 1,75–2,18. В крови детей, потребляющих воду с повышенным содержанием марганца и продуктов гиперхлорирования, обнаруживается хлороформ, а содержание марганца в 2,7 раза превышает референтный уровень (маркеры: содержание марганца и хлороформа в крови).
У детей с наследственной предрасположенностью (10–15 % популяции) (маркеры: патологические аллели СРОХ, CYP1A1, по-лиморфность гена сульфотрансферазы, регулирующих процессы детоксикации хлорор-ганических соединений и металлов) содержание марганца и хлороформа в крови на 15– 25 % выше, чем таковое у детей без генетических дефектов.
Повышенное содержание марганца и хлороформа оказывает негативное влияние на центральную и вегетативную нервную системы, что проявляется дисбалансом гомеостаза нейротрансмиттеров и нейромедиаторов (маркеры: снижение уровня серотонина, дофамина, кортизола и гамма-аминомасляной кислоты; повышение содержания глутамата, обусловленное присутствием в крови повышенных концентраций марганца и хлороформа; R 2 = 0,36 – 0,79), с развитием в 2 раза чаще астеноневротиче-ских и вегетативных расстройств, преимущественно по парасимпатическому типу (маркеры: ваготонический тип исходного вегетативного тонуса с гиперсимпатико-тоническим вариантом вегетативной реактивности, нарушение биоритмики головного мозга по данным электроэнцефалографии, связанные с повышенным содержанием марганца; R 2 = 0,36 – 0,42) (рисунок). Вегетативные расстройства с преобладанием парасимпатических влияний у детей проявля-
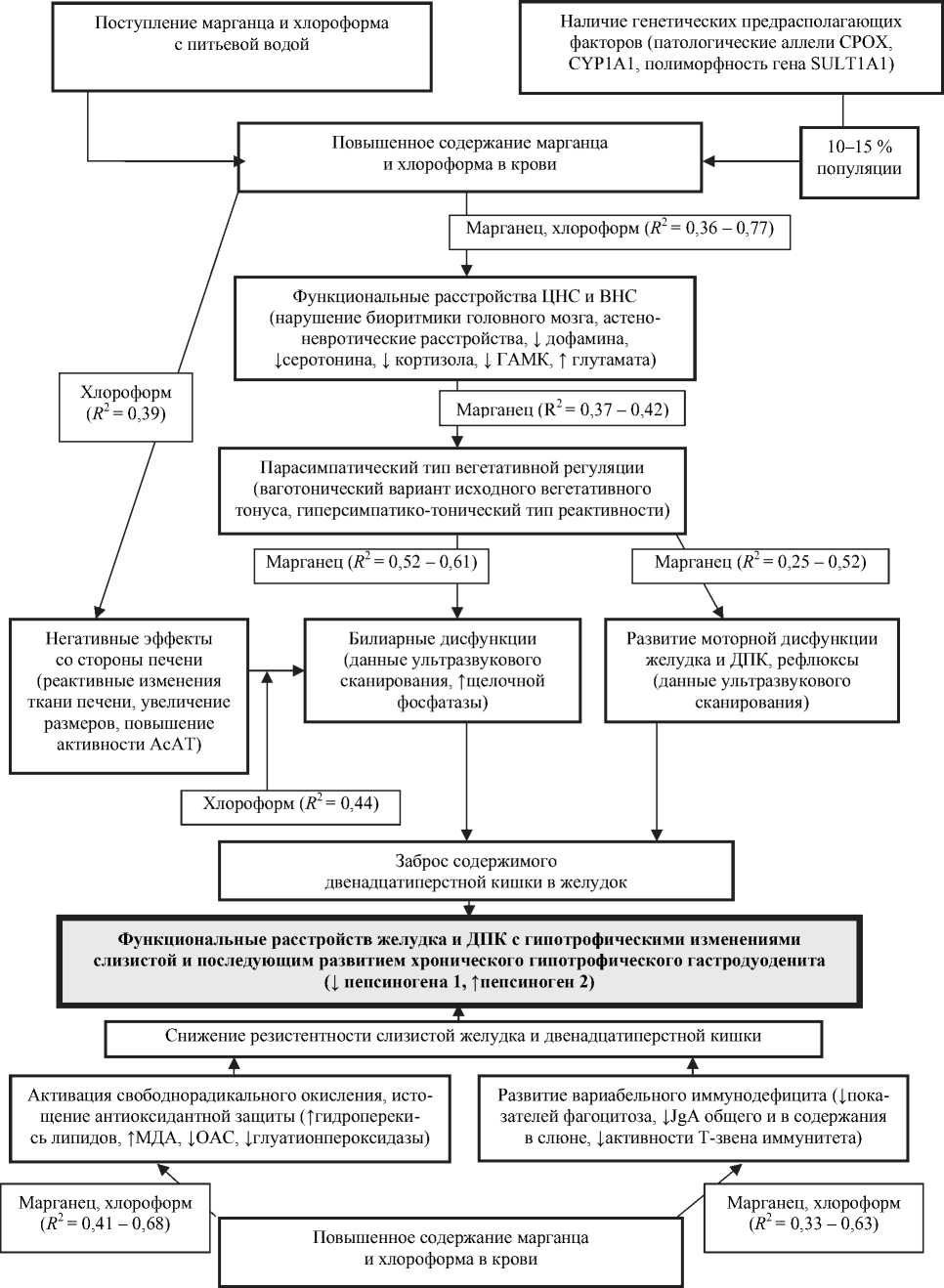
Рис. Патогенетические особенности каскадного механизма развития хронических гастродуоденальных заболеваний, обусловленных воздействием продуктов гиперхлорирования и марганца
Установленные патогенетические закономерности развития риск-ассоциирован-ной гастродуоденальной патологии следует учитывать при разработке программ превентивной и вторичной профилактики у детей, потребляющих питьевую воду ненадлежащего качества по содержанию продуктов гиперхлорирования и марганца.
Список литературы Патогенетические закономерности каскадного механизма развития хронических гастродуоденальных заболеваний у детей, обусловленных потреблением питьевой воды ненадлежащего качества по содержанию продуктов гиперхлорирования и марганца
- Алешко-Ожевский Ю.П. Сезонные колебания макро-и микроэлементов в крови больных с язвенной болезнью желудка и двенадцатиперстной кишки//Вопросы питания. -2005. -№ 2. -С. 9-14.
- Бабак О.А. Атрофический гастрит: прогнозы и перспективы//Здоровье Украины. -2006. -№ 21(1). -С. 1-3.
- Баранов А.А., Климанская Е.В., Римарчук Г.В. Детская гастроэнтерология. -М., 2002. -232 с.
- Баранов А.А., Щербаков П.Л. Актуальные вопросы детской гастроэнтерологии//Вопросы современной педиатрии. -2002. -№ 1. -С. 12-16.
- Зайцева Н.В., Май И.В., Шур П.З. Анализ риска здоровью населения на современном этапе//Здравоохранение Российской Федерации. -2013. -№ 2. -С. 20-24.
- Ивашкин В.Т., Трухманов А.С., Маев И.В. Физиологические основы моторно-эвакуаторной функции пищеварительного тракта//Российский журнал гастроэнтерологии, гепатологии, колопроктологии. -2007. -№ 5. -С. 4-10.
- О состоянии санитарно-эпидемиологического благополучия населения в Российской Федерации в 2012 году: Государственный доклад. -М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека, 2013. -176 с.
- Р 2.1.10.1920-04. Руководство по оценке риска для здоровья населения при воздействии химических веществ, загрязняющих окружающую среду. -М.: Федеральный центр Госсанэпиднадзора Минздрава России, 2004. -143 с.
- Рудаева Е.Г., Нейжмак З.Ф., Салманов Ф.Э. Особенности хронического гастродуоденита у подростков на современном этапе//Детская гастроэнтерология: материалы XV Международного конгресса детских гастроэнтерологов. -М., 2008. -С. 170-171.


