Патогистологические изменения скелетных мышц при хронической артериальной недостаточности нижних конечностей
Автор: Деев Роман Вадимович, Мжаванадзе Н.Д., Мавликеев М.О., Малахов А.А., Калинин Р.Е., Одинцова И.А., Матвеев С.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.10, 2015 года.
Бесплатный доступ
Цель исследования - выявить структурные изменения в тканях мышц различных сегментов нижних конечностей у пациентов с облитерирующими заболеваниями сосудов нижних конечностей при критической ишемии.Материалом послужили фрагменты тканей мышц трех сегментов - стопы, голени и бедра, полученные из ампутированных в связи с прогрессией заболевания конечностей (N=9). Препараты изучены при помощи гистологических, иммуногистохимических и морфометрических методов. Показано, что по оси стопа-бедро уменьшается доля соединительной ткани, увеличивается средний диаметр мышечных волокон, количество кровеносных сосудов; показано увеличение клеток-продуцентов эндотелиального сосудистого фактора роста и статистически одинаковое количество клеток, несущих рецептор к данному фактору.
Критическая ишемия нижних конечностей, скелетная мышечная ткань, эндотелиальный сосудистый фактор роста
Короткий адрес: https://sciup.org/140188417
IDR: 140188417 | УДК: 611.73+616.718:616.13-036.12-008.64-091.8
Histopathological changes in skeletal muscles in case of chronic limb ishemia
The aim of the research was to identify structural changes in the muscle tissue of various segments of the lower limbs in patients with critical ischemia in case of peripheral arterial disease. Muscle tissue of three segments - the foot, the leg and the thigh, derived from amputated due to disease progression limbs (N = 9) was examined. Histological, immunohistochemical and morphometric methods were used. It was shown that from foot to thigh the amount of connective tissuedecreases, the average diameter of muscle fibersand the number of blood vesselsincrease. Also, the increased number of cells, producing vascular endothelialgrowth factor and statistically equal amount of cells with the receptor to this factor, was found.
Текст научной статьи Патогистологические изменения скелетных мышц при хронической артериальной недостаточности нижних конечностей
Хроническая артериальная недостаточность нижних конечностей,связанная, как правило, с непрерывно прогрессирующим атеросклерозом, приводит к формированию морфофункциональных сдвигов как в региональных сосудах, так и в кровоснабжаемых ими мышцах. Показано, что количество сосудов микроциркуляторного русла в скелетной мышце обратно пропорционально стадии патологического процесса [4].Терминальное состояние ишемии – критическая ишемия нижних конечностей (КИНК), характеризуется глубокими структурными, биохимическими и функциональными изменениями в структуре мышц – соотношении различных тканей в ее составе, необратимыми изменениями мышечных волокон (некроз), признаками воспаления и др. Клинически это состояние характеризуется неблагоприятным прогнозом. Так, в течение первого года после диагностирования КИНК лишь у 45% пациентов удается сохранитьконечность. Остальные пациенты или погибнут, или им будет выполнена высокая ампутация [3]. Несмотря на угрожающую статистику, данная группа заболеваний не находится в фокусе внимания клиницистов, а реактивные изменения поперечнополосатой скелетной мышечной ткани и патогистологические изменения мышц при выраженной хронической ишемии только начинают изучаться как на экспериментальном, так и на клиническом материале [1, 2].
Цель исследования – выявить структурные изменения в тканях мышц различных сегментов нижних конечностей у пациентов с облитерирующими заболеваниями сосудов нижних конечностей при критической ишемии.
Материал и методы исследования
Материалом исследования послужили фрагменты тканей мышц трех сегментов – стопы (разгибатели пальцев), голени (икроножные) и бедра (двуглавая мышца), полученные из ампутированных в связи с прогрессией заболевания конечностей (N = 9) (ЛПУ г. Рязань). Фиксированный тканевый материал подвергался стандартной гистологической обработке. Изготавливались препараты для световой микроскопии, их окрашивали гематоксилином и эозином, по Голднеру. Регистрировали следующие морфометрические параметры: доля соединительной ткани в поле зрения при стандартном увеличении (х800, %), средний диаметр мышечных волокон (мкм), соотношение количества кровеносных сосудов к количеству мышечных волокон в поле зрения при увеличении х200.

Иммуногистохимическое исследование выполняли с антитителами к гладкомышечному актину (выявление миофибробластов, гладких миоцитов; морфометрически оценивали количество сосудов в стандартном поле зрения, х800), а также к эндотелиальному сосудистому фактору роста (vascularendothelialgrowthfactor)и его рецептору-2. Количество клеток с положительным цитоплазматическим окрашиванием оценивали полуколичественно при увеличении х800.
Результаты и обсуждение
Выраженность патоморфологических изменений закономерно уменьшается по направлению от стопы к бедру. Скелетная мышечная ткань мышц стопы на момент ампутации находилась в состоянии глубоких необратимых изменений. Значительная часть мышечных волокон погибла и подвергается резорбции фагоцитами. Мышца инфильтрирована полиморфно-ядерными лейкоцитами (рис. 1). Просветы кровеносных сосудов частично или полностью заполнены тромбами. Существенные объемы погибшей скелетной мышечной ткани замещены реактивно измененной соединительной тканью –7,6 ± 1,5%.
Часть мышечных волокон характеризуется нарушением тинкториальных свойств, извитым ходом, исчезновением поперечной исчерченности.
Длительно существующая хроническая ишемия приводит к структурной перестройке капиллярного русла. Существенно снижается количество капилляров, окружающих мышечные волокна, что выражается в уменьшении числа капилляров, приходящихся на одно мышечное волокно (таблица 1). В связи с массированным некрозом, пропитыванием тканевого дебриса фибрином и компонентами крови при ИГХ-анализе продуценты VEGF выявлены в незначительном количестве. Преимущественно это клетки, которые можно морфологически идентифицировать как макрофаги/гистиоциты, мигрировавшие из кровеносного русла (рис. 2). Тканевые структуры, несущие рецепторы к данному фактору достоверно выявлены не были, что связано с массированным неспецифическим связыванием хромагента с тканевым дебрисом.
В мышцах голени наблюдаются признаки некроза, пролиферации клеток фибробластического дифферона, выработка волокнистого соединительнотканного матрикса (рис. 1). В отдельных участках определяются скопления мелких мышечных волокон, различных размеров и очертаний на поперечном срезе. Как правило, они разобщены большими полями рыхлой соединительной ткани. Среди них в малом количестве могут быть идентифицированы мышечные трубочки – структуры с центрально расположенными ядрами, свидетельствующие о протекающей реактивной регенерации скелетной мышечной ткани. В совокупности данные признаки свидетельствуют о том, что несмотря на глубокое гипоксическое повреждение на тканевом иерархическом уровне реализуется механизм репаративного рабдомиогистогенеза, который, однако, остается незавершенным. Доля соединительной ткани в мышцах этого сегмента составила 6,4 ± 1,8%.
Помимо участков гибели и регенерации имеются обширные зоны мышечных волокон, частично или
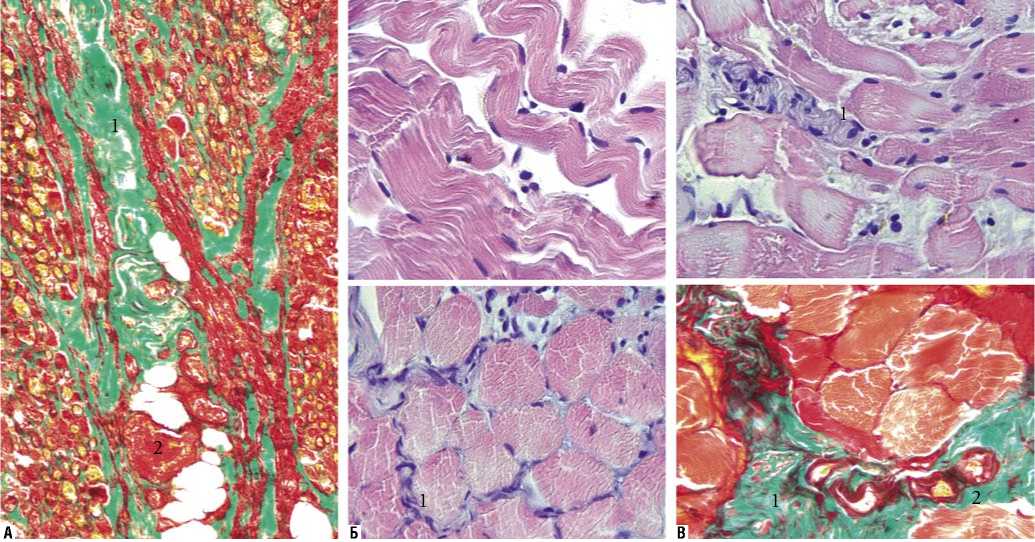
Рис. 1. Скелетная мышечная ткань стопы (А), голени (Б), бедра (В) конечностей, ампутированных по поводу критической ишемии: 1 – волокнистая соединительная ткань; 2 - кровеносные сосуды. Окраска: по Голднеру и гематоксилином и эозином. Ув.: А х 200, Б, В х 400
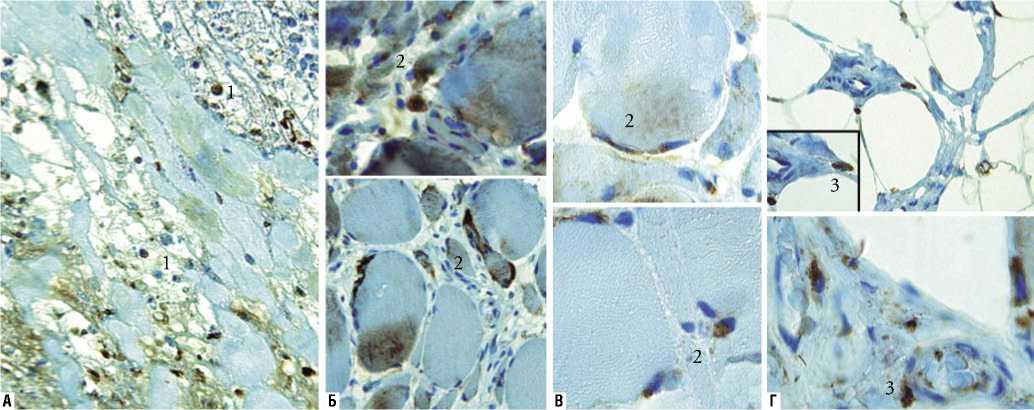
Рис. 2. Скелетная мышечная ткань стопы (А), голени (Б, В), бедра (Г) конечностей, ампутированных по поводу критической ишемии. ИГХ-реакция с антителами к VEGF: 1 – VEGF+клетки экссудата; 2 – VEGF+клетки, ассоциированные с мышечными волокнами; 3 – VEGF+клетки, ассоциированные с рыхлой соединительной тканью. Докраска гематоксилином. Ув.: А х 200, Б х 400, В х 800, Г х 400, х 800
полностью сохранивших поперечную исчерченность. Встречаются извитые мышечные волокна, иногда распадающиеся на отдельные фрагменты. Средний диаметр мышечных волокон в икроножных мышцах превышает этот показатель в стопе и составляет 2,5 ± 0,6 мкм (см. таблицу 1). Количество сосудов, приходящихся на одно мышечное волокно, колеблется от 0 до 4.
Наиболее удаленные от периферического сосудистого русла мышцы – мышцы бедра – в целом характеризуются выраженными изменениями, которые, однако, не столь фатальны как в дистальных сегментах. На этом уровне также обнаружены мозаичные участки некроза, области, заполненные хорошо развитой волокнистой соединительной тканью, однако ее доля не столь велика – 1,8 ± 0,7%. Мышечные волокна имеют существенно больший диаметр, равный 4,2 ± 1,1 мкм. Количество сосудов, приходящееся на одно волокно – от 2 до 8. Имеются мышечные волокна с центрально расположенными ядрами, что свидетельствует о регенераторных процессах в органе; но количество таких симплатов невелико. Изменения тинкториальных свойств ткани незначительные.
Полученные в ходе исследования результаты свидетельствуют о том, что патоморфологические изменения в скелетной мышце нарастают от периферии конечности к центру, что связано с центростремительным угнетением микроциркуляции, несмотря на центробежное распространение атеросклероза в сосудистом русле. По-видимо-му, этой же тенденции соответствует и глубина тканевой гипоксии, нарастающая к периферии. Доля волокнистой соединительной ткани, замещающей некротизированные мышечные волокна, снижается в направлении от стопы к бедру с 7,6 ± 1,5 % до 1,8 ± 0,7 (различия– 50–70%). При этом, несмотря на клинически определяемые показания к ампутации на уровне проксимального сегмента, со-
Табл. 1. Морфометрические показатели скелетных мышц нижних конечностей при КИНК (Х ± х)
|
Показатель |
Стопа |
Голень |
Бедро |
|
Доля соединительной ткани,% |
7,6 ± 1,5 |
6,4 ± 1,8 |
1,8 ± 0,7 |
|
Средний диаметр мышечных волокон, мкм |
1,5 ± 0,7 |
2,5 ± 0,6 |
4,2 ± 1,1 |
|
Количество сосудов на одно мышечное волокно, шт. |
0–4 |
0–4 |
2–8 |
Табл. 2. Количество клеток, вырабатывающих –VEGF, и содержащих его рецептор 2 типа (Х ± х)
Средний диаметр мышечных волокон, косвенно свидетельствующий о функциональном состоянии сократительного аппарата, уменьшен в дистальных сегментах и на уровне бедра сохраняется до средних величин (4,2 ± 1,1 мкм). Некоторые авторы справедливо считают это явление сочетанной атрофией мышечных волокон и сопровождающих их капилляров [4].
Данные о количественной характеристике микрососудов сочетаются с результатами подсчета числа клеток-продуцентов (представители гистиоцитарного и фибробластического рядов) основного ангиогенного

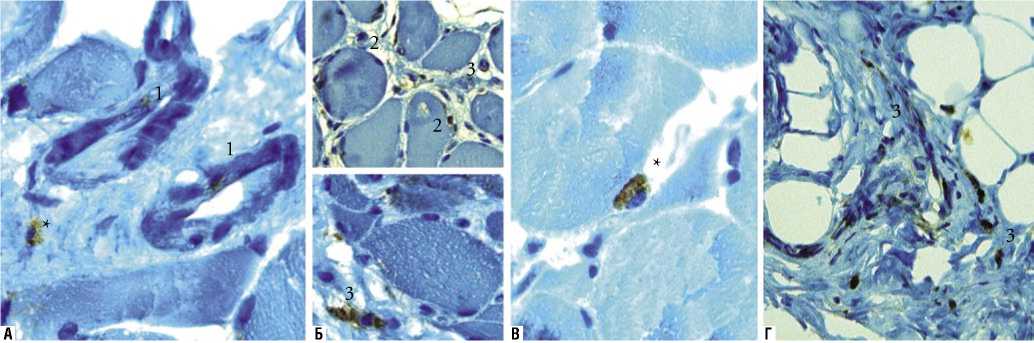
Рис. 3. Скелетные мышцы голени (А-В), бедра (Г) конечностей, ампутированных по поводу критической ишемии. ИГХ-реакция с антителами к рецептору VEGF 2 типа: 1 – VEGFR2+клетки в составе сосудистой стенки (единичные эндотелиоциты) и находящаяся отдельно гистиоцито- или фибробластоподобная клетка (*); 2 – VEGFR2+клетки, тесно связанные с мышечными волокнами; 3 – VEGFR2+клетки, находящиеся в рыхлой соединительной тканью. Докраска гематоксилином. Ув.: А х 400, Б х 200, В х 1000, Г х 200
фактора – VEGF. Обнаружена обратная зависимость между этими двумя показателями, что может объясняться компенсаторным характером данного состояния – в ответ на выраженную тканевую гипоксию происходит активная выработка ангиогенного фактора. «Рецепторное поле» для него характеризуется стабильностью, вне зависимости от того или иного сегмента конечности, и представлены как уплощенными клетками, находящимися в тесной связи с мышечными волокнами, так и клетками рыхлой соединительной ткани, что позволяет предположить наличие среди них клеток-предшественниц эндотелиоцитов (рис. 3). Полученные данные носят предварительный характер и согласуются с показанной ранее динамикой концентрации VEGF в периферической венозной крови при хронической артериальной недостаточности. По данным С.А. Теплякова (2011), концентрация этого ангиогенного фактора нарастала у пациентов с терапевтическими стадиями болезни и IIб-III стадией. При IV стадии заболевания автор наблюдал уменьшение количества VEGF, свидетельствующее о снижении компенсаторных синтетических возможностей [4].
Заключение
Таким образом, во всех сегментах нижней конечности обнаружены выраженные морфологические преобразования как обратимого, так и необратимого характера. Некротизированные ткани по механизму субституции замещаются брадитрофной волокнистой соединительной тканью. Несмотря на тканевую гипоксию, в скелетной мышечной ткани происходят явления регенерационного рабдомиогистогенеза, которые, однако, не приводят к полному восстановлению органа. Количество клеток-продуцентов VEGF снижается по направлению от стопы к бедру, в то время, как количество клеток, несущих рецепторы к данному фактору, остается неизменным.
Список литературы Патогистологические изменения скелетных мышц при хронической артериальной недостаточности нижних конечностей
- Мавликеев М.О., Плотников М.В., Максимов А.В. и др. Патогистологическая оценка состояния скелетной мышцы после прямой генной терапии VEGF165 пациентов с хроническими облитерирующими заболеваниями артерий нижних конечностей//Гены и Клетки, 2014, т. IX, №3. -С. 56-64.
- Мжаванадзе Н.Д. Геннотерапевтическая индукция неоангиогенеза в комплексном лечении пациентов с хронической ишемией нижних конечностей атеросклеротической этиологии. Автореферат дисс. канд. мед. наук. М., 2013. -29 с.
- Национальные рекомендации по ведению пациентов с патологией артерий нижних конечностей//Ангиология и сосудистая хирургия, 2013, т. 19, №2, приложение. -70 с.
- Тепляков С.А. Особенности морфо-функциональных изменений мышц при хронической артериальной недостаточности нижних конечностей. Автореферат дисс. канд. мед. наук. М., 2011. -29 с.


