Патоморфологическая оценка эффективности внутрисуставного применения растворимых факторов тромбоцитов для лечения экспериментального остеоартрита
Автор: Третьяков А.А., Зиновкин Д.А., Карпенко Ф.Н., Потапнев М.П., Николаев В.И., Пранджол М.З.И.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.30, 2024 года.
Бесплатный доступ
Введение. Основная цель нехирургического лечения остеоартрита - это стабилизация дегенеративно-воспалительных процессов в суставе, что будет способствовать продлению сроков работоспособности сустава и отдалению сроков выполнения тотальной артропластики.Цель работы - патоморфологически обосновать доклиническую эффективность применения разработанного ПОРФТ/PRP при ОА на основе сравнительного анализа с истощенной плазмой и сывороткой крови.Материалы и методы. Эксперимент проведен на 120 крысах линии Вистар, разделенных на 4 группы. Предварительное моделирование остеоартрита производили по оригинальной методике. Через 2 недели после моделирования остеоартрита, под ингаляционным наркозом после рассечения кожи под визуальным контролем в коленные суставы животных 1 группы вводили 0,05 мл ПОРФТ/PRP, 2 группы - 0,05 мл плазмы, 3 группы - 0,05 мл сыворотки крови. Крысам контрольной группы вводили такой же объём физиологического раствора. Инъекции проводили троекратно с промежутками в две недели. Животных выводили из эксперимента по 10 особей через две недели после каждой инъекции.Результаты. На шестой неделе эксперимента медиана по MANKIN score в группе 1 составила 2,0 (1,0; 2,0) балла, в группе 2 - 6,0 (5,0; 7,0) баллов, в группе 3 - 7,0 (6,0; 7,0) баллов. В контрольной группе медиана баллов была 7,5 (7,0; 8,0). При сравнении групп определяли (р function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Остеоартрит, экспериментальная модель, лабораторные крысы, суставной хрящ, суставная капсула, субхондральная кость, лечение остеоартрита, обогащенная факторами тромбоцитов плазма, prp, сыворотка крови
Короткий адрес: https://sciup.org/142240813
IDR: 142240813 | УДК: [616.72-007.248-08:615.38]-092.9 | DOI: 10.18019/1028-4427-2024-30-1-90-98
Pathomorphologic evaluation of intra-articular injections of soluble platelet-rich plasma for treatment of experimental osteoarthritis
Introduction Non-surgical treatment of osteoarthritis is aimed at managing joint degeneration and inflammation to prolong the life of the original joint and delay total joint replacement. The objective was to pathomorphologically substantiate preclinical effectiveness of PRP in OA using comparative analysis of depleted plasma and serum.Material and methods The experiment was performed in 120 Wistar rats, divided into 4 groups. Osteoarthritis was simulated using an original method. Knee joint injection given to the animals after skin dissection under inhalation anesthesia and visual control two weeks later contained 0.05 ml PRP in group 1, 0.05 ml plasma in groups 2 and 0.05 ml blood serum in groups 3. The same volume of physiological saline solution was used for the injections produced for control animals. Injections were administered three times at 2-week intervals. Animals were sacrificed in groups of 10 at 2 weeks of each injection.Results The median MANKIN value scored 2.0 (1.0; 2.0) in group 1, 6.0 (5.0; 7.0) in group 2 and 7.0 (6.0; 7.0) in group 3 at 6 weeks. The median MANKIN value scored 7.5 (7.0, 8.0) in the control group. Statistically significant differences were determined between the groups at p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Патоморфологическая оценка эффективности внутрисуставного применения растворимых факторов тромбоцитов для лечения экспериментального остеоартрита
В последние десятилетия ортобиологический подход, как один из принципов регенеративной медицины, приобретает все больший интерес среди специалистов, разрабатывающих технологию получения новых или оптимизированных биологических материалов для локального лечения ОА, и среди ортопедов-травматологов при стабилизации дегенеративных изменений суставного хряща [1-3]. При этом интерес вызывает использование производных крови, включающих аутологичную кондиционированную сыворотку крови (СК) или плазму, обогащенную тромбоцитами (ПОРФТ/PRP) [4-12].
Литературные данные по доклинической оценке эффективности PRP-терапии на биологических моделях ОА достаточно неоднозначны. Наиболее вероятно, это связано с различными способами моделирования ОА, технологиями получения экспериментальных PRP-продуктов, а также кратностью их внутрисуставного введения и интервалами между инъекциями [13, 14, 15].
Во многих исследованиях индуцирование экспериментального ОА осуществляется путем внутрисуставного введения монойодацетата или суспензии талька, однако воздействие химических веществ на гиалиновый хрящ сустава, по нашему мнению, вызывает достаточно распространенное его химическое повреждение, что может сказываться на результатах оценки результатов терапии [15, 16]. Поэтому в нашем исследовании использован оригинальный малотравматичный функциональный способ моделирования ОА коленного сустава у крыс, который воспроизводил основные патогенетические механизмы развития ОА [14, 17].
Кратность введения экспериментальных PRP-продуктов варьирует у различных авторов от одной до трех внутрисуставных инъекций. Патоморфологическая и иммунологическая оценка эффективности PRP-терапии зависит от увеличения толщины суставного хряща, улучшения показателей тинкто-риальных свойств матрикса суставного хряща, появления фиброзно-гиалинового хряща до анальгетического противовоспалительного эффекта [18-24].
Основная цель нехирургического лечения ОА – это стабилизация дегенеративно-воспалительных процессов в суставе, что будет способствовать продлению сроков работоспособности сустава и отдалению сроков выполнения тотальной артропластики. В Республиканском научно-практическом центре трансфузиологии и медицинских биотехнологий (Республика Беларусь, Минск) разработаны оригинальные технологии получения биологически стандартизированных аутологичных и донорской ПОРФТ/PRP.
Для оптимизации малоинвазивного интраартикулярного введения препаратов производных крови мы проводили оценку эффективности их применения при моделировании ОА у экспериментальных животных.
Цель работы – патоморфологически обосновать доклиническую эффективность применения разработанного ПОРФТ/PRP при ОА на основе сравнительного анализа с истощенной плазмой и СК.
МАТЕРИАЛЫ И МЕТОДЫ
Лабораторные животные
В эксперименте участвовали 120 крыс (60 самок и 60 самцов) линии Wistar. Животные содержались в виварии Гомельского государственного медицинского университета в клетках по три особи, с контролем влажности и температуры. Воду и пищу предоставляли ad libitum. Цикл день/ночь составлял 12 часов. Перед проведением экспериментов животные акклиматизировались в течение 14 дней. Содержание и уход за животными проводили согласно рекомендациям Надлежащей лабораторной практики Министерства здравоохранения Республики Беларусь (ТПК 125-2008 (02040)). При выведении животных из эксперимента соблюдали требования биоэтики Хельсинской декларации гуманного обращения с лабораторными животными в редакции 2013 года [18]. Экспериментальные исследования с животными одобрены комитетом по этике Гомельского государственного медицинского университета (протокол заседания комитета № 4 от 23.12.2020).
При проведении экспериментальных исследований животные были рандомизированы с использованием конвертов/генератора случайных чисел и разделены на четыре равные группы (по 30 животных каждая). В группу 1 (группу исследования) включены крысы, получавшие аллогенную плазму, обогащенную растворимыми факторами тромбоцитов (ПОРФТ/PRP), в группу 2 (группа сравнения 1) – крысы, которым вводили плазму крови крыс, в группу 3 (группа сравнения 2) – сыворотку крови крыс, группа 4 (группа контроля) являлась контрольной.
Приготовление плазмы, сыворотки, ПОРФТ/PRP
Протокол получения ПОРФТ/PRP включал несколько строго определенных стадий. Отбор крови осуществляли шприцом кардиально у крыс под общим наркозом 2,5 % тиопентала натрия, введенного внутрибрюшинно в дозе 45 мг/кг веса. Данный способ позволяет взять примерно 10 мл крови. Со- держимое шприца переносили в пробирки с 3,8 % цитратом натрия (в соотношении 9:1) и центрифугировали при комнатной температуре при 1000 об/мин. в течение 20 мин. С помощью пастеровской пипетки отбирали плазму и лейкотромбоцитарный слой и центрифугировали при 1500 об/мин. в течение 20 мин. Образовавшийся верхний слой отбирали и использовали в качестве плазмы, освобожденной от элементов крови, – обедненная плазма. Контроль содержания тромбоцитов как в обедненном, так и в обогащённом слое проводили на гематологическом анализаторе Sysmex XP-300 (Sysmex Europe GmbH, Германия). Нижний слой, обогащённый тромбоцитами, доводили обедненной плазмой до концентрации тромбоцитов 2,0 × 1012/мл. Для оценки чистоты ПОРФT/PRP проводили подсчет лейкоцитов, число которых было меньше 0,1 × 103/мкл. Полученные фракции плазмы подвергали замораживанию при -70 °C. Через 1-3 дня обогащенную плазму размораживали и центрифугировали при 3000 об/мин. в течение 15 мин. Супернатант отбирали, фильтровали с помощью стерильных фильтров с диаметром пор 0,2 мкм, расфасовывали по 0,25 мл в пробирки Эппендорф и хранили при 70 °C до использования [19].
Получение сыворотки проводили по общепринятой методике. Полученную кровь в объеме от 5 до 10 мл отстаивали при температуре 4 °C в течение часа. Свернувшуюся кровь центрифугировали в течение 20 мин. при 2000 об/мин. Надосадочную жидкость – сыворотку без признаков гемолиза – переносили в пробирки типа Эппендорф и хранили при -70 °C до использования.
Хирургическое моделирование остеоартрита и протокол дозирования
Моделирование остеоартрита коленного сустава у крыс проводили по оригинальной методике [25]. Оно включало несколько этапов: рассекали кожу и фасции коленного сустава крысы под ингаляционным наркозом в асептических условиях, затем в полость сустава вводили стерильную инъекционную иглу и механически наносили травму хрящевым структурам наружных мыщелков бедренных и большеберцовых костей режущей частью среза иглы. При этом диаметр иглы соответствовал суммарной толщине хрящевого слоя суставных поверхностей, на рассеченные ткани накладывали швы. Со второго дня послеоперационного периода крыс заставляли ходить в колесе, что создавало статодинамическую нагрузку на травмированные суставы и воспроизводило основные патогенетические механизмы развития остеоартрита. Через две недели после моделирования ОА под ингаляционным наркозом после рассечения кожи под визуальным контролем в коленные суставы животных группы 1 производили введение 0,05 мл ПОРФТ/PRP, группы 2 – 0,05 мл плазмы, группы 3 – 0,05 мл сыворотки крови. Крысам контрольной группы вводили такой же объём физиологического раствора. Инъекции проводили троекратно с промежутками в две недели. Животных выводили из эксперимента по 10 особей через две недели после каждой инъекции. Основные этапы эксперимента представлены на рисунке 1.
1 день 2 недели 4 недели 6 недель
|
_____ Группа 1__ * (п=30) f - |
0,05 мл ___ ПОРФТ |
,0,05 мл , 0,05 мл _ |
(n=W) |
|
|
ПОРФТ ПОРФТ * |
||||
|
1 1 |
||||
|
Группа 2 |
0,05 мл __► |
(п=10) (п=10) 0,05 мл ___0,05 мл ___► |
||
|
* (п=30) |
плазмы |
плазмы плазмы |
||
|
— |
_ Группа 3 |
0,05 мл __* |
1 1 (п=10) (п=10) 0,05 мл ___0,05 мл ___ |
(n=W) |
|
* (п=30) |
сыворотки |
сыворотки сыворотки |
||
|
е±^> , Контроль |
0,05 мл ___ |
(n=W) (п=10) 0,05 мл ___, 0,05 мл ___ |
(n=10) |
|
|
* (п=30) |
0,9% NaCI |
” 0,9% NaCI 0,9% NaCI |
||
|
1. |
(n=W) |
(п=10) (п=10)
Рис. 1. Схема эксперимента с терапией индуцированного остеоартрита коленного сустава у крыс
Приготовление гистологических препаратов
Сразу после вывода животного из эксперимента производили выделение сустава и помещение его в декальцинирующую жидкость Histodecalc (Sigma, Италия) на 48-72 ч. После этого сустав разрезали в сагиттальном направлении, все кусочки тканей фиксировали в 10 % нейтральном забуференном по Лилли формалине в течение 24-48 часов. Гистологическую проводку производили по методике в гистопроцессоре STP-120 (ThermoScientific, Германия), после чего ткани заливали в парафиновые блоки. Из парафиновых блоков на микротоме ThermoScientificMicrom HM 450 (ThermoScientific, Германия) готовили серии срезов толщиной 4 мкм. После депарафинирования проводили окрашивание сафранином O согласно R. Asjid et al. [21].
Морфометрический анализ
Микроскопию и морфометрический анализ проводили с использованием светового микроскопа NikonEclipse 50i (Nikon, Япония). Морфометрическую оценку гиалинового хряща вокруг места его повреждения проводили в трех неперекрывающихся полях зрения. Для оценки патологоанатомических изменений хряща коленного сустава использовали модифицированную F.M.D. Henson et al. балльную шкалу MANKIN [21] (табл. 1).
Таблица 1 Модифицированная шкала MANKIN
|
Структура |
Клеточность |
Целостность матрикса |
Целостность пограничной линии |
Баллы |
|
Гладкая поверхность / норма |
Нормальное расположение |
Нормальное окрашивание |
Нормальная и не нарушена |
0 |
|
Шероховатая поверхность / одиночная трещина или область расслоения хряща |
Кластеры клеток в поверхностном слое или потеря до 10 % клеток |
Слабая потеря окраски |
Нарушена |
1 |
|
Множественные трещины / умеренное расслоение хряща |
Дезорганизация или потеря до 25 % клеток |
Умеренная потеря окраски |
2 |
|
|
Фрагментация или сильное расслоение хряща |
Ряды клеток отсутствуют или потеря клеток составляет до 50 % |
Выраженная потеря окраски |
3 |
|
|
Утрата фрагментов хряща |
Единичные клетки |
Отсутствие окраски |
4 |
|
|
Эрозирование не доходит до пограничной линии |
5 |
|||
|
Эрозирование глубже пограничной линии |
6 |
Статистическая обработка полученных результатов
При проведении анализа Шапиро – Уилка не было выявлено нормального распределения, в связи с чем, все значения показателей в нашем исследовании были представлены медианой, 25-м и 75-м процентилями. Межгрупповые сравнения проводили с использованием теста Краскела – Уоллиса. При проведении теста post-hoc использовали критерий Данна. Статистически значимыми считали результаты при р < 0,05. Для статистического анализа и графического представления данных использовали пакет программ GraphPadPrism v. 7.04 (GraphPadSoftware inc., США).
РЕЗУЛЬТАТЫ
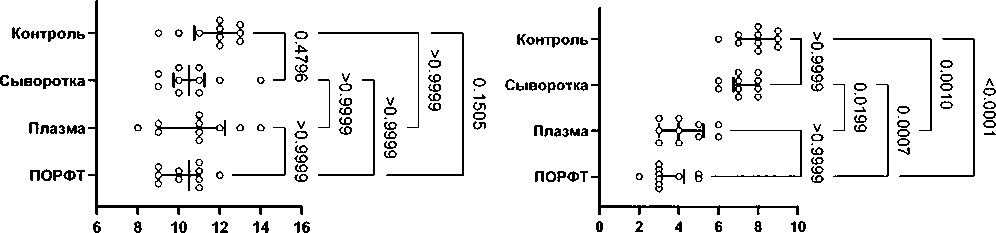
Все животные хорошо перенесли хирургические манипуляции на коленных суставах, проводимые под наркозом, и оставались живыми до вывода из эксперимента. Через две недели после первого введения у животных всех групп определяли гистологические признаки выраженного остеоартрита. Отмечали разрушение гиалинового хряща с утратой его фрагментов, определяли участки потери клеток и окрашивания, пограничная линия имела участки прерывистости. Медиана по MANKIN в группе 1 составила 10,50 (9,0; 11,0) баллов, в группе 2 – 11,0 (9,0; 12,3) баллов, в группе 3 – 10,5 (9,8; 11,6) баллов. В контрольной группе медиана баллов была 12,0 (10,8; 13,0). При сравнении групп не определялись ( p = 0,326) статистически значимые различия (рис. 2, а).
Через четыре недели после первой инъекции препаратов производных крови при микроскопии гистологических препаратов гиалиновых хрящей суставов животных группы 1 отмечали участки растрескивания и фрагментации хряща, определяли участки увеличения клональности хондроцитов, имелись области потери окраски и разрывы пограничной линии. В группе 2 у животных наблюдали участки разрушения и потери фрагментов хряща, потерю его клеточности и окраски на единичных участках. У крыс группы 3 имелись участки потери фрагментов хряща, на месте которых определяли незрелую соединительную ткань, пограничная линия была прерывиста. У животных группы контро- ля отмечали образование незрелой соединительной ткани на месте дефекта хряща, потерю клеточ-ности и прерывистость пограничной линии. Медиана баллов по MANKIN через четыре недели эксперимента у животных группы 1 составила 3,00 (3,0; 4,3) балла, в группе 2 – 4,0 (3,0; 5,3) балла, в группе 3 – 7,0 (6,8; 8,0) баллов. В контрольной группе крыс медиана баллов по MANKIN была 8,0 (7,0; 9,0). При сравнении групп определяли (p < 0,001) статистически значимые различия. Межгрупповые различия представлены на рисунке 2, б.
б
а
MANKIN (баллы)
в
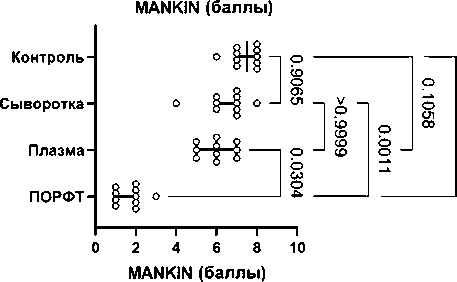
Рис. 2. Патоморфологическая характеристика
регенерации тканей коленного сустава под действием вводимых препаратов производных крови в группах крыс в разные сроки лечения остеоартрита: а – через 2 недели; б – через 4 недели; в – через 6 недель
Через шесть недель после начала эксперимента у животных группы 1 отмечали единичную шероховатость поверхности гиалинового хряща и небольшие участки потери окраски его матриксом. В группе 2 имелись участки шероховатости поверхности хряща, отмечали небольшие очаги замещения хряща соединительной тканью. В группе 3 наблюдали участки замещения соединительной тканью гиалинового хряща с уменьшением его клеточности и окраски матрикса. В контрольной группе крыс визуализировали участки полного замещения соединительной тканью хряща на всю глубину со значительным уменьшением клеточности в данных участках. Наиболее показательные микрофотографии представлены на рисунке 3.
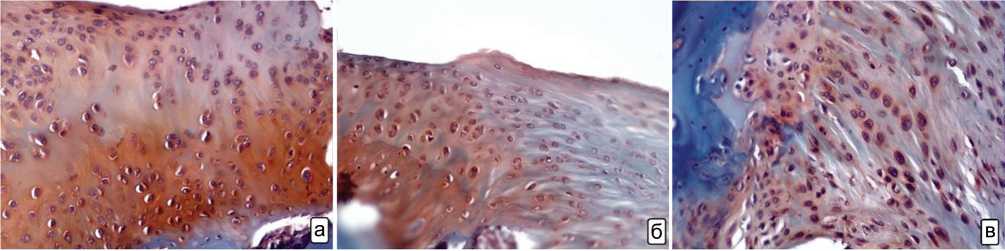
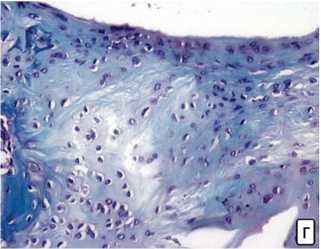
Рис. 3. Патоморфологическая картина хряща коленного сустава крыс, пролеченных в течение 6 недель с использованием: а – ПОРФТ/PRP; б – плазмы; в – сыворотки; г – физраствора. Окраска: сафранин О. Увеличение ×200
Медиана по MANKIN в группе 1 составила 2,0 (1,0; 2,0) балла. в группе 2 – 6,0 (5,0; 7,0) баллов, в группе 3 – 7,0 (6,0; 7,0) баллов. В контрольной группе медиана баллов была 7,5 (7,0; 8,0). При сравнении групп определяли ( p < 0,001) статистически значимые различия. Межгрупповые различия представлены на рисунке 2, в.
ОБСУЖДЕНИЕ
В нашем исследовании получены патоморфологические данные, указывающие на увеличение кле-точности, снижение шероховатости поверхности и накопление протеогликанов в сохранившемся гиалиновом хряще, при этом участок глубокого дефекта хряща заполнялся соединительной тканью [26]. Полученные данные совпадают с данными систематического обзора A. Boffa et al., в котором указаны похожие изменения у малых лабораторных животных в 28 исследованиях. Во всех представленных в систематическом обзоре исследованиях группу животных, получавших PRP-терапию, сравнивали с животными контрольной группы, которые получали физиологический раствор (saline solution) [20]. В нашем исследовании был показан статистически значимый эффект ПОРФТ/PRPв сравнении с контролем и сывороткой [27-28], который мы связываем с выраженным регенеративным потенциалом ПОРФТ/PRP по сравнению с плазмой крови, не содержащей тромбоциты и растворимые факторы тромбоцитов, и сывороткой крови, содержащей естественный (в 3-5 раза ниже) уровень растворимых факторов тромбоцитов. В работах авторов с использованием других экспериментальных исследований были получены аналогичные данные [26, 29].
ЗАКЛЮЧЕНИЕ
Данное исследование показало, что внутрисуставное введение модифицированного ПОРФТ/PRP приводило к выраженному терапевтическому эффекту, проявлявшемуся улучшением морфофункционального состояния гиалинового хряща (MANKIN score – 2 балла) на шестые сутки, в сравнении с плазмой и сывороткой.
Список литературы Патоморфологическая оценка эффективности внутрисуставного применения растворимых факторов тромбоцитов для лечения экспериментального остеоартрита
- Wu PI, Diaz R, Borg-Stein J. Platelet-Rich Plasma. Phys Med Rehabil Clin N Am. 2016;27(4):825-853. doi: 10.1016/j. pmr.2016.06.002
- Cole BJ, Karas V, Hussey K, et al. Hyaluronic Acid Versus Platelet-Rich Plasma: A Prospective, Double-Blind Randomized Controlled Trial Comparing Clinical Outcomes and Effects on Intra-articular Biology for the Treatment of Knee Osteoarthritis. Am J Sports Med. 2017;45(2):339-346. doi: 10.1177/0363546516665809
- Эйсмонт О.Л. Ортобиологические технологии в лечении остеоартрита суставов. Медицинские новости. 2020;8(311):45-48.
- Laver L, Marom N, Dnyanesh L, et al. PRP for Degenerative Cartilage Disease: A Systematic Review of Clinical Studies. Cartilage. 2017;8(4):341-364. doi: 10.1177/1947603516670709
- Joshi Jubert N, Rodriguez L, Reverte-Vinaixa MM, Navarro A. Platelet-Rich Plasma Injections for Advanced Knee Osteoarthritis: A Prospective, Randomized, Double-Blinded Clinical Trial. Orthop J Sports Med. 2017;5(2):2325967116689386. doi: 10.1177/2325967116689386
- Fox BA, Stephens MM. Treatment of knee osteoarthritis with Orthokine-derived autologous conditioned serum. Expert Rev Clin Immunol. 2010;6(3):335-345. doi: 10.1586/eci.10.17
- Frisbie DD, Kawcak CE, Werpy NM, et al. Clinical, biochemical, and histologic effects of intra-articular administration of autologous conditioned serum in horses with experimentally induced osteoarthritis. Am J Vet Res. 2007;68(3):290-296. doi: 10.2460/ajvr.68.3.290
- Osterdahl J. Evaluation of autologous conditioned serum. Swed Uni Agricultural Sci. 2008;(3):1-5.
- Marx RE, Carlson ER, Eichstaedt RM, et al. Platelet-rich plasma: Growth factor enhancement for bone grafts. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 1998;85(6):638-646. doi: 10.1016/s1079-2104(98)90029-4
- Котлубаева Э.Ю., Белашов Н.В., Лапынин А.И. К вопросу об истории применения и эффективности PRP-терапии. Научный альманах. 2020;(1-2(63)):69-72. Доступно по: https://ukonf.com/doc/na.2020.01.02.pdf. Ссылка активна на 25.10.2024.
- Потапнев М.П., Загородный Г.М., Кривенко С.И., и др. Современные аспекты применения плазмы, обогащенной растворимыми факторами тромбоцитов, в лечении травм и заболеваний опорно-двигательного аппарата. Спортивная медицина: наука и практика. 2019;9(4):33-45. doi: 10.17238/ISSN2223-2524.2019.4.33
- Yamaguchi R, Terashima H, Yoneyama S, et al. Effects of platelet-rich plasma on intestinal anastomotic healing in rats: PRP concentration is a key factor. J Surg Res. 2012;173(2):258-66. doi: 10.1016/j.jss.2010.10.001
- Николаев В.И., Петкевич О.В., Третьяков А.А. и др. Способ экспериментального моделирования остеоартроза коленного сустава у крысы. Патент Респ. Беларусь № 23186. 30.06.2010. Доступно по: https://elib.gsmu.by/handle/ GomSMU/3486. Ссылка активна на 25.10.2023.
- Park YG, Han SB, Song SJ, et fl. Platelet-rich plasma therapy for knee joint problems: review of the literature, current practice and legal perspectives in Korea. Knee SurgRelat Res. 2012;24(2):70-8. doi: 10.5792/ksrr.2012.24.2.70
- Троянов А.А., Потапнев М.П., Кондратенко Г.Г., и др. Биологические эффекты и ранозаживляющее действие плазмы, обогащенной растворимыми факторами тромбоцитов, в условиях экспериментальной гипергликемии. Медицинский журнал. 2018;(2):107-112.
- Hanafy AS, El-Ganainy SO. Thermoresponsive Hyalomer intra-articular hydrogels improve monoiodoacetate-induced osteoarthritis in rats. Int JPharm. 2020;573:118859. doi: 10.1016/j.ijpharm.2019.118859
- Bansal H, Leon J, Pont JL, et al. Platelet-rich plasma (PRP) in osteoarthritis (OA) knee: Correct dose critical for long term clinical efficacy. SciRep. 2021;11(1):3971. doi: 10.1038/s41598-021-83025-2
- Magalon J, Chateau AL, Bertrand B, et al. DEPA classification: a proposal for standardising PRP use and a retrospective application of available devices. BMJ Open Sport Exerc Med. 2016;2(1):e000060. doi: 10.1136/bmjsem-2015-000060
- Потапнев М.П., Кривенко С.И., Богдан В.Г., и др. Плазма крови, обогащенная растворимыми факторами тромбоцитов: получение, стандартизация, медицинское применение. Здравоохранение. 2018;10(859): 38-44.
- Boffa A, Salerno M, Merli G, et al. Platelet-rich plasma injections induce disease-modifying effects in the treatment of osteoarthritis in animal models. Knee Surg Sports Traumatol Arthrosc. 2021;29(12):4100-4121. doi: 10.1007/s00167-021-06659-9
- Asjid R, Faisal T, Oamar K, et al. Effect of Platelet-rich Plasma on Mankin Scoring in Chemically-induced Animal Model of Osteoarthritis./ Coll Physicians Surg Pak. 2019;29(11):1067-1071. doi: 10.29271/jcpsp.2019.11.1067
- Papalia R, Diaz Balzani L, Torre G, et al. Intraoperative application Platelet rich fibrin, postoperative injections OF PRP or microfracture only for osteochondral lesions of the knee: a five-year retrospective evaluation. J Biol Regul Homeost Agents. 2016;30(4 Suppl 1):41-49.
- Маланин Д.А., Трегубов А.С., Демещенко М.В., Черезов Л.Л. PRP-терапия при остеоартрите крупных суставов. Волгоград: Издательство ВолгГМУ; 2018:49. Доступно по: http://www.prplab.ru/docs/PRP-terapiya-pri-osteoartrite-krupnyh-sustavov.pdf. Ссылка активна на 25.10.2023.
- Glynn LG, Mustafa A, Casey M, et al. Platelet-rich plasma (PRP) therapy for knee arthritis: a feasibility study in primary care. Pilot Feasibility Stud. 2018;4:93. doi: 10.1186/s40814-018-0288-2
- Третьяков А.А., Николаев В.И., Зиновкин Д.А., Сердюченко Н.С. Экспериментальная модель остеоартрита коленного сустава у крыс. Новости медико-биологических наук. 2020;20(4):90-97.
- Huang GS, Peng YJ, Hwang DW, et al. Assessment of the efficacy of intra-articular platelet rich plasma treatment in an ACLT experimental model by dynamic contrast enhancement MRI of knee subchondral bone marrow and MRI T2* measurement of articular cartilage. Osteoarthritis Cartilage. 2021;29(5):718-727. doi: 10.1016/j.joca.2021.02.001
- Azizi S, Kheirandish R, Farsinejad A, Rasouli N. The effect of intraarticular serum rich in growth factors (SRGF) on knee osteoarthritis in the rat model. Transfus Apher Sci. 2017;56(3):371-375. doi: 10.1016/j.transci.2017.02.006
- Araya N, Miyatake K, Tsuji K, et al. Intra-articular Injection of Pure Platelet-Rich Plasma Is the Most Effective Treatment for Joint Pain by Modulating Synovial Inflammation and Calcitonin Gene-Related Peptide Expression in a Rat Arthritis Model. Am J Sports Med. 2020;48(8):2004-2012. doi: 10.1177/0363546520924011
- Суббот А.М., Труфанов С.В., Шазбазян Н.П. Сравнительный анализ регенеративного потенциала производных крови на клеточной модели повреждения эпителия роговицы. Гены и клетки. 2021;16(1):64-68. doi: 10.23868/202104010


