Патоморфологические особенности слизистой желудка в условиях желудочно-кишечного кровотечения на фоне COVID-ассоциированной пневмонии
Автор: Хоробрых Т.В., Проценко Д.Д., Каммаев К.А., Петровская А.А., Крылова М.Ю., Сентюрина А.М., Саакян А.К.
Журнал: Хирургическая практика @spractice
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.10, 2025 года.
Бесплатный доступ
Цель. Анализ доступных морфологических изменений слизистой оболочки желудочно-кишечного тракта, развившихся на фоне COVID-19-ассоциированной пневмонии, и приводящих к кровотечениям. Материал и методы. В исследование было включено 72 случая обнаружения эрозивно-язвенного гастродуоденального кровотечения на фоне осложненной Covid-пневмонии. Пациенты находились на лечении в Университетской Клинической Больнице №4 Первого Московского Государственного Медицинского Университета (ПМГМУ) им. И.М. Сеченова (Сеченовского Университета) с апреля 2020 года по март 2022 года. Результаты. При морфологическом исследовании биоптатов из желудочно-кишечного тракта были получены доказательства как прямого, так и опосредованного воздействия вируса SARS-CoV2 на клетки слизистой желудочно-кишечного тракта. Проводимая антикоагулянтная и противовоспалительная терапия помогает в разрешении «тромбовоспалительного синдрома». Однако, нарастающая кислородная задолженность тканей в сочетании с внешними неблагоприятными факторами, влияющими на микроциркуляцию в стенке желудка (терапия антикоагулянтами и НПВС), могут совместно приводить к интерстициальному отеку и нарастанию ишемии. Ухудшение кровоснабжения слизистой оболочки желудка и снижение регенераторной активности эпителиальных клеток приводит к формированию прогрессирующей язвенной деструкции у всех пациентов. У 53 пациентов изменения слизистой оболочки возникли на фоне ослабления факторов защиты, где первичное обеднение кровотока являлось возможной первопричиной язвообразования. Кровотечениями чаще осложнялись острые язвы у пациентов без язвенного анамнеза 55,5% против 40,6%, хотя у пациентов с язвенным анамнезом язвы были достоверно глубже 75% против 25%. Заключение. Слизистая желудка у больных COVID-19 подвергается воздействию вируса, что приводит к эрозивно-язвенным ее изменениям, приводящим к кровотечению. Этому одновременно способствует антикоагулянтная и противовоспалительная терапия, проводящаяся таким больным. Указанные осложнения необходимо предвидеть и своевременно предотвращать.
Желудочно-кишечные кровотечения, патоморфологический субстрат осложнений Covid-19, ишемия слизистой оболочки желудка, язвы желудка, рецепторы АПФ2
Короткий адрес: https://sciup.org/142244163
IDR: 142244163 | УДК: 617-089.844 | DOI: 10.5922/2223-2427-2025-10-1-2
COVID-associated pathomorphological changes in the gastric mucosa during gastrointestinal bleeding
Aim. Analysis of morphological changes in the mucous membrane of the gastrointestinal tract that developed against the background of COVID-19-associated pneumonia, accompanied by bleeding. Methods. The study included 72 cases of erosive and ulcerative gastroduodenal bleeding with complicated Covid-pneumonia. The patients were treated at the University Clinical Hospital No. 4 of Sechenov Moscow State Medical University (Sechenov University) from April 2020 to March 2022. Results. Morphological examination of biopsies from the gastrointestinal tract has provided irrefutable evidence of both direct and indirect effects of the SARS-CoV2 virus on cells of the gastrointestinal mucosa. Conclusion. The gastric mucosa in COVID-19 patients is exposed to the virus, which leads to erosive and ulcerative changes in it, leading to bleeding. This is simultaneously facilitated by anticoagulant and anti-inflammatory therapy given to such patients. These complications must be anticipated and prevented in a timely manner.
Текст научной статьи Патоморфологические особенности слизистой желудка в условиях желудочно-кишечного кровотечения на фоне COVID-ассоциированной пневмонии
В литературе все чаще появляются данные свидетельствующие о том, что желудочно-кишечный тракт, в клетках слизистой которого выявляется нуклеокапсидный белок SARS-CoV-2 , является основным местом проникновения для вируса [1; 2]. Способность SARS-CoV-2 инфицировать широкий спектр тканей объясняется диффузной тканевой экспрессией клеточного рецептора ангиотен-зин-превращающего фермента 2 (АПФ2). АПФ2 регулирует артериальное давление, водный и электролитный баланс, системное сосудистое сопротивление [1; 3-6]. В клетках нижних дыхательных путей имеется большое количество рецепторов АПФ2, которые в меньшей степени эспрессированы в желудочно-кишечном тракте, с чем связано преобладание легочных симптомов, и системность проявлений [1; 5-7]. Развивающиеся на этом фоне нарушения гемостаза у больных COVID-19 приводят к протромботическому состоянию и возникновению микротромбозов в мелких сосудах. Прокоагулянтное состояние является важным прогностическим критерием, влияющим в желудочно-кишечном тракте пациентов с COVID-19 на изменения слизистой оболочки в виде эрозивно-язвенного повреждения [7- 9].
Согласно временным методическим рекомендациям, каждому госпитализированному пациенту с COVID-19 индифидуально подбирают дозы препаратов и проводят антикоагулянтную, антибактериальную, противовоспалительную и симптоматическую терапию [10]. Однако, сочетанное применение антикоагулянтной терапии и нестероидных противовоспалительных препаратов приводит к повышенному риску появления на слизистой желудочно-кишечного тракта эрозивно-язвенных повреждений и развитию кровотечений [10-15].
Целью данной работы является анализ доступных морфологических изменений слизистой оболочки желудочно-кишечного тракта, развившихся на фоне COVID-19-ассоциированной пневмонии, и приводящих к кровотечениям.
Материал и методы
В исследование было включено 72 пациента с эрозивно-язвенным гастродуоденальным кровотечением на фоне осложненной Covid-пневмонии. Все они находились с апреля 2020 года по март 2022 года на лечении в Университетской Клинической Больнице №4 ПМГМУ им. И.М. Сеченова.
В нашем исследовании мы подсчитали количество клинико-лабораторно верифицированного инфицирования вирусом SARS-CoV-2 у каждого пациента. Так же, мы провели подробный подсчет количества язв и источников кровотечения у каждого пациента. Язвы охарактеризовали по их форме, величине и глубине проникновения в стенку органа.
Биопсию производили по методике Л.К. Соколова (1972) специальными щипцами фирмы “Olympus” тип ФБ-433Д; брали 5 фрагментов при первом и контрольном осмотрах. Биоптат фиксировали в 10% растворе забуференного формалина, затем заливали парафином с последующим окрашиванием срезов гематоксилином и эозином. Всего было изготовлено и проанализировано 4 препарата.
Результаты
Количество клинико-лабораторно подтвержденых инфицированиий вирусом SARS-CoV-2 у 72 пациентов с эрозивно-язвенным гастродуоденальным кровотечением приведены в таблице 1.
Таблица 1. Количество перенесенных Covid-инфекций.
Table 1. The number of Covid infections suffered.
|
Состояние |
Удовлетворительное |
СреднеТяжелое |
Тяжелое |
Крайне тяжелое |
|
|
Количество перенесенных Covid-инфекций |
1 |
58,3% |
|||
|
2 |
6,9% |
12,5% |
6,9% |
6,9% |
|
|
3 |
- |
- |
- |
8,3% |
|
Инфицированных в первый раз было 42 пациента (58,3%), во второй раз - 24 пациента (33,3%), в третий раз - 6 пациентов (8,3%). Среди инфицированных вирусом Sars-Cov-2 в третий раз, все пациенты к концу госпитализации были в крайне тяжелом состоянии, тогда как среди инфицированных в первый раз, все пациенты были в удовлетворительном состоянии. К концу госпитализации, среди инфицированных во второй раз состояние пациентов было: крайне тяжелое у 5 пациентов (6,9%), тяжелое у 5 пациентов (6,9%), средней степени тяжести у 9 пациентов (12,5%), и удовлетворительное у 5 пациентов (6,9%).
Количество язв отображено в таблице 2.
Таблица 2. Количество язв и источников кровотечения.
Table 2. The number of ulcers and sources of bleeding.
|
Язвы |
Острые язвы |
Хроническая язвенная болезнь |
||
|
Пациенты |
Источники кровотечения |
Пациенты |
||
|
1 |
3 |
17 |
9 |
1 |
|
2 |
9 (18) |
4 (8) |
5 (10) |
4 (8) |
|
3 |
15 (45) |
6 (18) |
10 (30) |
7 (21) |
|
4 |
2 (8) |
13 (52) |
1 (4) |
6 (24) |
|
5 |
3 (15) |
3 (15) |
1 (5) |
1 (5) |
|
6 |
1 (6) |
1 (6) |
1 (6) |
1 (6) |
|
7 |
- |
- |
1 (7) |
1 (7) |
|
8 |
5 (40) |
- |
- |
- |
|
10 |
3 (30) |
1 (10) |
||
|
11 |
- |
- |
- |
1 (11) |
|
13 |
2 (26) |
- |
- |
1 (13) |
|
14 |
1 (14) |
|||
|
17 |
- |
- |
- |
1 (17) |
|
18 |
1 (18) |
- |
- |
1 (18) |
|
20 |
■ |
1 (20) |
||
|
Итого |
209 (54,4%) |
116 (55,5%) |
71 (40,6%) |
175 (45,6%) |
У 72 пациентов выявлено 384 язвы и 187 источников кровотечения. У 28 пациентов с хронической язвенной болезнью визуализировано 175 язв (45,6%), в то время как у 44 пациентов с острыми язвами визуализировано 209 язв (54,4%). Среднее количество язв на 1 человека у пациентов без язвенного анамнеза равно 4,75, в то время как у пациентов с хронической язвенной болезнью - 6,25. У 28 пациентов с хронической язвенной болезнью был зафиксирован 71 источник кровотечения (40,6%), в то время как у 44 пациентов с острыми язвами было зафиксировано 116 источников кровотечения (55,5%).
Характеристика язвенных дефектов по форме, величине и глубине проникновения в стенку представлены на рисунках 1 и 2, и в таблице 3.
|
—и,ии /0 |
. а —♦—Пациенты с |
|
DD,UU /0 QA АПОЛ _ |
\ язвенным |
|
0« плол _ |
\ / \ анамнезом \ / \______ / п=28 |
|
ZDjUU/O он ллол _ |
|
|
ZU,UU70 |
|
|
丄。, UU /0 |
/ \\ без |
|
1U,UU /0 « л пол _ |
/ язвенного |
|
А ПАОЛ _ |
4 \ анмнеза / |
|
U,UU /0 и |
1 1 1 1 1 丄丄 1 мм 2 мм 3 мм 4 мм 5 мм |
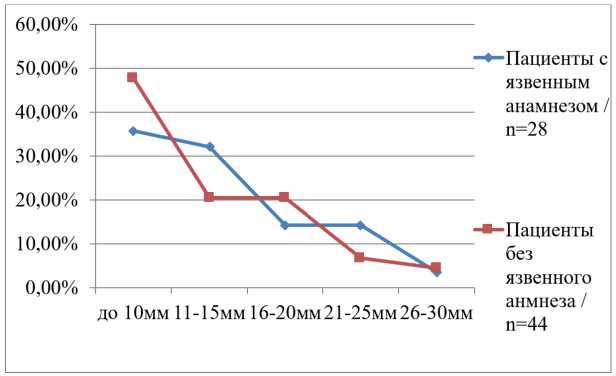
Рис.2. Диаметр или длина язв.
Fig.2. The diameter or length of the ulcers.
Форму круга или овала имели острые язвы 27 пациентов (61,4%), линейной формы были острые язвы 17 пациентов (38,6%). С хронической язвенной болезнью было 28 пациентов (100%), у которых язвы имели только форму круга или овала. Глубину до 2мм имели острые язвы 23 пациентов (52,3%) и более 2мм была у 21 пациента (47,7%). У пациентов с хронической язвенной болезнью глубина язв менее 2мм была у 7 пациентов (25%) и более 2мм у 21 пациента (75%). Острые язвы с диаметром или длиной до 10мм были у 21 пациента (47,7%) и более 10мм были у 23 пациентов (52,3%). У пациентов с хронической язвенной болезнью диаметр или длина до 10мм были у 10 пациентов (35,7%), и более 10мм у 18 пациентов (64,3%).
Таблица 3. Размеры язв.
Table 3. The size of the ulcers.
|
Глубина |
Острые язвы |
Хроническая язвенная болезнь |
|
Все язвы (линейной формы)/n=44 |
28 (100%) / n=28 |
|
|
1 мм |
16 (6) / 36,4% |
1 / 3,6% |
|
2 мм |
7 (5) / 15,9% |
6 / 21,4% |
|
3 мм |
10 (4) / 22,7% |
10 / 35,7% |
|
4 мм |
10 (2) / 22,7% |
9 / 32,1% |
|
5 мм |
1 / 2,3% |
2 / 7,2% |
|
Диаметр (или длина) язв |
||
|
До 10 мм |
21 (8) / 47,7% |
10 / 35,7% |
|
11-15 мм |
9 (5) / 20,5% |
9 / 32,1% |
|
16-20 мм |
9 (3) / 20,5% |
4 / 14,3% |
|
21-25 мм |
3 (1) / 6,8% |
4 / 14,3% |
|
26-30 мм |
2 (0) / 4,5% |
1 / 3,6% |
При эзофагогастродуоденоскопии у 72 пациентов с ковид-ассоциированной пневмонией, слизистая оболочка чаще была бледной и анемичной, в силу особенностей COVID-19 (табл. 4).
|
Характер изменений слизистой |
Анемичная, бледная Сосудистый рис. скудный Края язв чаще сглажены |
Гиперемирована, отечна Сосудистый рис. обеднен. Края язв отечные/каллезные |
|
Количество пациентов |
53 |
19 |
|
Язвенный анамнез |
-+ 44 9 |
+ |
У 53 пациентов, среди которых 44 пациента без язвенного анамнеза, при гастроскопии выявлены стойкие изменения в кровеносном русле вокруг язвы. Кровотечение возникало на фоне анемичной или атрофичной слизистой оболочки (рис. 3, 4).
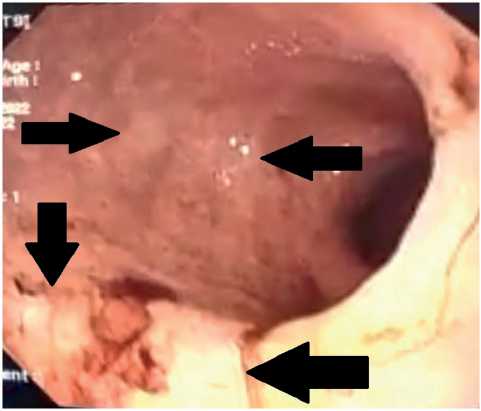
Рис. 3. Кровотечение на фоне анемичной слизистой.
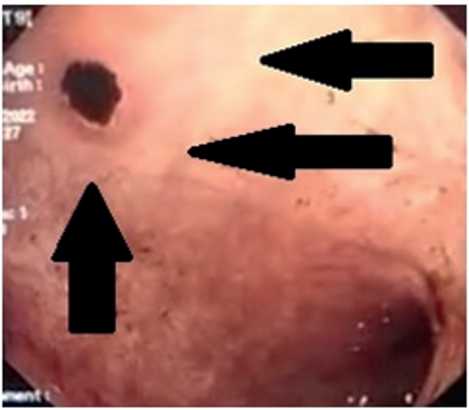
Рис. 4. Язвенная деструкция на фоне анемичной слизистой.
Fig. 3. Bleeding on the background of anemic mucosa.
Fig. 4. Ulcerative destruction on the background of anemic mucous.
У 19 из 28 пациентов, с хронической язвенной болезнью в анамнезе, при гастроскопии слизистая оболочка отечна, гиперемирована, складки утолщены и плохо расправляются воздухом, перистальтика усилена. В острую стадию края язв с четкими границами, гиперемированы, отечны. часть язв с подрытыми, каллёзными краями (рис. 5). Дно язв представлено фибрином и/или вкраплениями солянокислого гематита, так же в дне могут визуализироваться сосуды (рис. 6, 7). У 12 пациентов отмечались эрозии, которые часто сливались между собой (рис. 8).
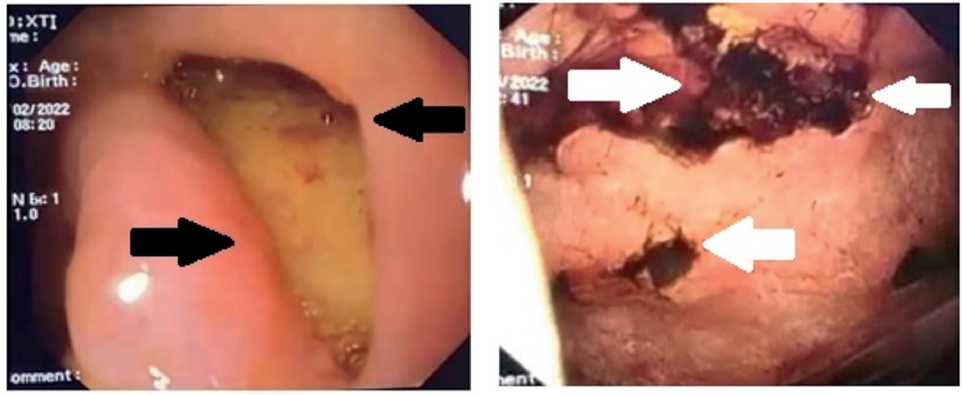
Рис. 5. Края язвы подрытые, каллезные.
Слизистая вокруг гперемирована, отечная.
Fig. 5. The The edges of the ulcer are covered, callous. The mucosa around the area is eremated, edematous.
Fig. 6. Erosions of the stomach body merge with each other, against the background of uneven hyperemia around.
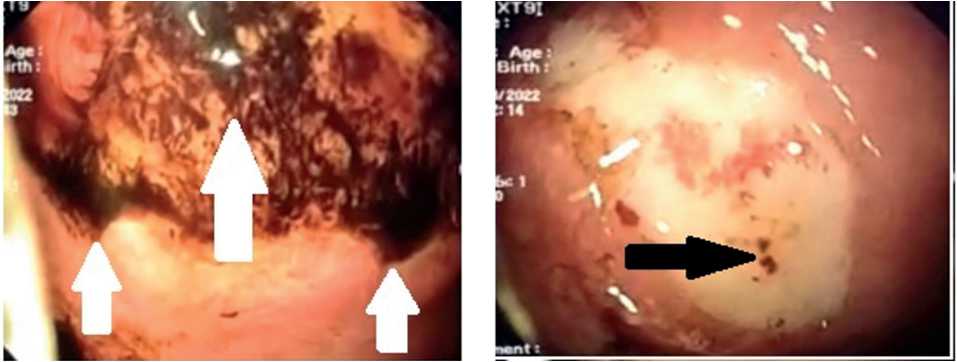
Рис. 8. Тромбированный сосуд.
Рис.7. Солянокислый гематин.
-
Fig. 7. Hematin hydrochloric acid.
-
Fig. 8. The vessel is thrombosed.
В стадию заживления, воспалительные изменения слизистой оболочки в периульцерозной зоне стихали, градиент между дном и краем язвы сглаживался. Иногда наблюдалась конвергенция складок слизистой оболочки к краям язвы. Фибрин в дне язвы постепенно замещался грануляционной тканью (рис. 9).
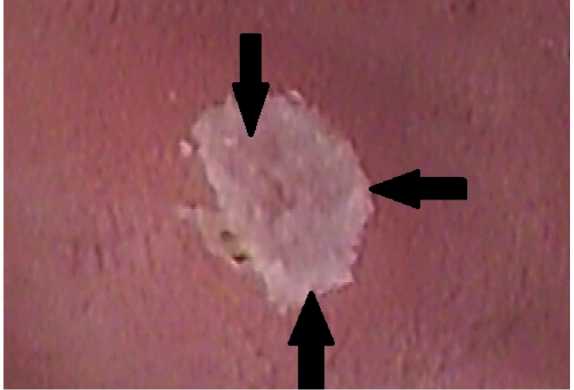
Рис. 9. Язва в стадию заживления.
Fig. 9. The ulcer is in the healing stage.
При ЭГДС контроле язв в динамике, у пациентов, в стадию заживления воспалительные изменения слизистой оболочки и в периульцерозной зоне стихали, градиент между дном и краем язвы сглаживался. Фибрин в дне язвы постепенно замещался грануляционной тканью. Иногда наблюдалась конвергенция складок слизистой оболочки к краям язвенного дефекта, различные нарушения рельефа слизистой оболочки: рубцы, деформации (рис. 10а, 10б).
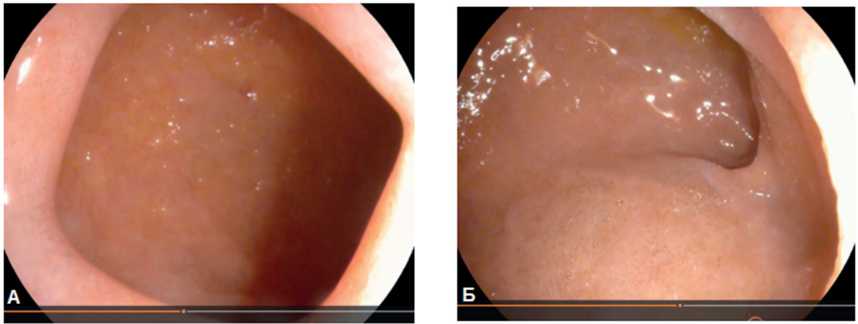
Рис. 10. а,б. Рубцовая деформация луковицы двенадцатиперстной кишки.
Fig. 10. a,b. Scarring of the duodenal bulb.
В стадии рубцевания язвы в виде гиперемированного участка слизистой оболочки, за счет большого количества сосудов, с линейным или звездчатым втяжением стенки (стадия «красного» рубца). Вокруг язв небольшая инфильтрация и гиперемия (рис. 11). Зрелые рубцы приобретали белесоватый вид, вследствие замещения грануляционной ткани соединительной тканью и отсутствия активного воспаления (стадия «белого» рубца) (рис. 12).
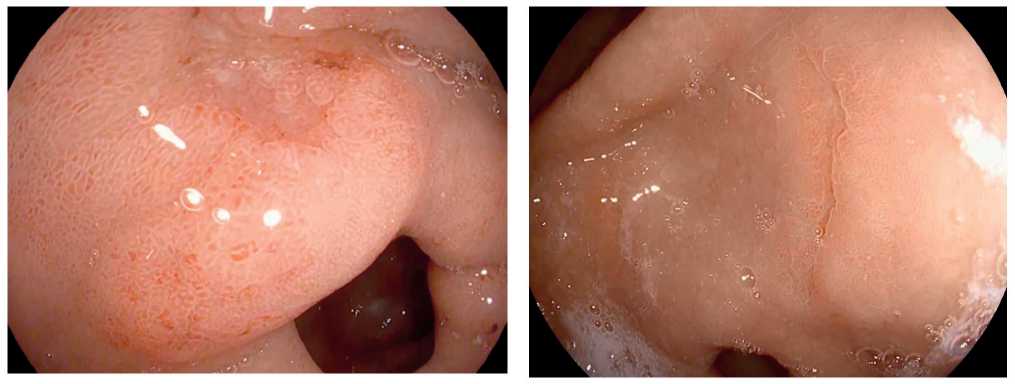
Рис. 11. Стадия «красного рубца».
Рис. 12. Стадия «белого рубца».
Fig. 11. The stage of the “red scar”.
Fig. 12. The stage of the “white scar”.
Гистологическое исследование
Случай 1.
Описание препаратов. Диффузное резко выраженное венозно-капиллярное полнокровие с элементами эритростазов, диапедезными кровоизлияниями, краевым стоянием полиморфно-нуклеарных лейкоцитов, единичными микротромбами (рис. 13). Слизистая оболочка атрофична, фокально аутолизирована, с участками некротических изменений и мелкими кровоизлияниями. Собственная пластинка слизистой с признаками отека и разволокнения, умеренно выраженной инфильтрацией полиморфно-нуклеарными лейкоцитами и немногочисленными лимфоцитами. Подслизистая основа и мышечная оболочка с участками отека и разволокнения. Серозная оболочка и мышечный слой интактны (рис. 14).
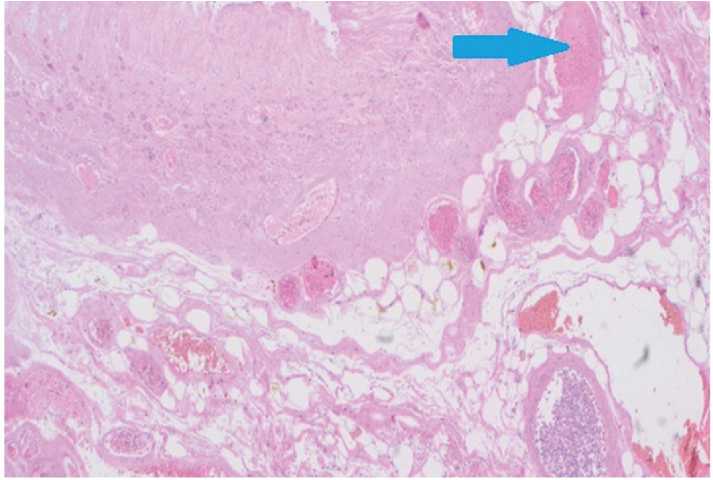
Рис. 13. Случай 1. Микротромбы в периульцерозной зоне (стрелка). Окраска гематоксилином и эозином, х200.
-
Fig. 13. Case 1. Microthrombi in the periulcerous zone (arrow). Staining with hematoxylin and eosin, x200.
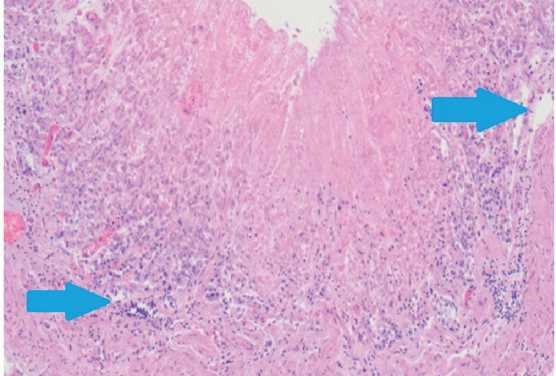
Рис. 14. Случай 1. Участки отека и разволокнения подслизистой основы и мышечной оболочки (стрелки). Окраска гематоксилином и эозином, х100.
-
Fig. 14. Case 1. Areas of swelling and fibrillation of the submucosal base and muscle membrane (arrows).
Staining with hematoxylin and eosin, x 100.
Случай 2.
Описание препаратов. Слизистая оболочка фокально аутолизирована, отмечаются колонии микроорганизмов (рис. 15). Фокусы некроза слизистой, окруженные слабовыраженным нейтрофильным инфильтратом с примесью единичных лимфоцитов. Подслизистая основа отечна. Сосуды резко полнокровны, отмечаются скопления лейкоцитов с феноменом краевого стояния, просветы отдельных содержат тромботические массы. Мелкие кровоизлияния (рис. 16).
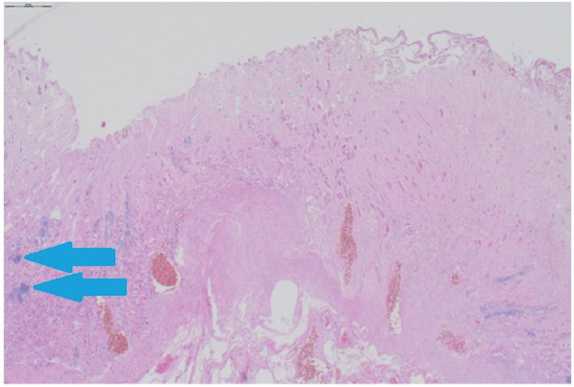
Рис. 15. Случай 2. Колонии микроорганизмов (стрелки). Окраска гематоксилином и эозином, х200.
Fig. 15. Case 2. Colonies of microorganisms (arrows). Staining with hematoxylin and eosin, x200.
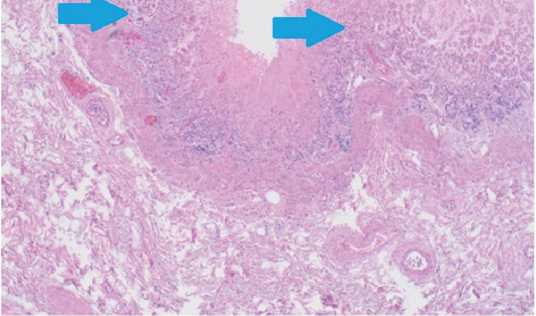
Окраска гематоксилином и эозином, х100.
Fig. 16. Case 2. Foci of necrosis of the gastric mucosa surrounded by neutrophil infiltrate with an admixture of single lymphocytes (arrows). Staining with hematoxylin and eosin, x 100.
Обсуждение
Обнаруженные нами данные подтверждают сведения о том, что эрозивно-язвенные кровотечения в гастродуоденальный зоне, как напрямую, так и опосредованно могут быту связаны с SARS-CoV-2 . Вирус, инфицируя широкий спектр тканей, способствует нарушениям гемостаза, приводя к протромботическому состоянию и возникновению микротромбозов в мелких сосудах [16-20].
Проводимая антикоагулянтная и противовоспалительная терапия способствует улучшению эффективности лечения, но также может приводить к появлению на слизистой желудочно-кишечного тракта эрозивно-язвенных повреждений и развитию кровотечений [21; 22].
Нами так же отмечено, что на эффективность лечения может влиять количество инфицирований вирусом SARS-CoV-2 . Таким образом, все пациенты инфицированные вирусом в первый раз, были выписаны в удовлетворительном состоянии, тогда как все пациенты инфицированные вирусом в третий раз, были в тяжелом или крайне тяжелом состоянии.
Нами получены противоречивые данные в плане выраженности язвенной деструкции и источников кровотечения. Количество язв на 1 пациента, у пациентов с хронической язвенной болезнью превалировало над таковым у пациентов без язвенного анамнеза на 31,6%. Тогда как кровотечениями чаще осложнялись острые язвы у пациентов без язвенного анамнеза 55,5% против 40,6%, хотя у пациентов с язвенным анамнезом язвы были достоверно глубже 75% против 25%.
Ведущую роль ишемической теории образования язвы поддерживают и стойкие изменения в кровеносном русле вокруг язвы и рубца в стадии обострения и ремиссии.
Нами отмечено, что количество инфицирований вирусом SARS-CoV-2 могло влиять на прогнозы лечения, что в свою очередь, при выполнении эндогемостаза, требовало стимуляции местной репарации тканей.
Нами получены противоречивые данные. На фоне прогрессирующей кислородной задолженности тканей, обусловленной тромбоассоциированными нарушениями микроциркуляции в сочетании с неблагоприятными факторами, язвенная деструкция больше прогрессировала у пациентов с пред-существующей язвенной компрометацией, но источников кровотечения было больше у пациентов без язвенного анамнеза.
Указанные осложнения необходимо предвидеть, ввиду того что кислородная задолженность растет во всех тканях и органах человека. Своевременное предотвращение прогрессирующей язвенной деструкции, с помощью стимуляторов местной репарации тканей, не только позволяет избежать рецидива кровотечения, но и помогает организму сохранить внутренний резерв для иных нужд. Ввиду чего необходимы альтернативные варианты купирования прогрессирующей язвенной деструкции опосредованной нарастающей ишемией в зоне повреждения.


