Патоморфология трофической язвы венозной этиологии в эксперименте при аутотрансплантации жировой ткани
Автор: Гуликян Г.Н., Карапетян Г.Э., Кириченко А.К., Винник Ю.С., Пахомова Р.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 2 (54), 2017 года.
Бесплатный доступ
В статье представлена модель для получения трофической язвы венозной этиологии, а так же морфологические изменения в трофических язвах данной этиологии при аутотранспалнтации жировой ткани в зону патологического очага. За счет авторского добавления в патент РФ № 2510083 от 2014 г. были смоделированы трофические язвы именно венозной этиологии. В ходе морфологического исследования выявлено, что в группе кроли- ков, где была выполнена аутотранспалнтации жировой ткани в область трофической язвы отмечается усиление и ускорение процессов репарации. Результаты проведенного экспериментального исследования позволяют судить об эффективности предложенного метода лечения на морфологиче- ском уровне.
Трофическая язва, липофиллинг, аутотрансплантация жировой ткани
Короткий адрес: https://sciup.org/142211310
IDR: 142211310 | УДК: 616-001.4-039.22
Текст научной статьи Патоморфология трофической язвы венозной этиологии в эксперименте при аутотрансплантации жировой ткани
Актуальность
Несмотря на достижения и успехи современной медицины, проблема лечения трофических язв не теряет свою актуальность на протяжении многих десятилетий [1]. Данная патология диагностируется у 1-2% трудоспособного населения развитых стран [2]. Большая распространенность трофических язв и недостаточная эффективность существующих консервативных методов лечения приводит к значительному экономическому ущербу.
Отсутствие стойкого эффекта от применения традиционной терапии заставляет искать альтернативные методы лечения. Одним из перспективных направлений в лечении данной патологии, является аутотрансплантация жировой ткани, содержащей большое количество стволовых клеток [3]. Многочисленные клинические и фундаментальные исследования показывают эффективность трансплантации стволовых клеток при лечении трофических язв через разностороннее воздействие на факторы регенерации, такие как клеточная пролиферация, выработка факторов роста, неоваскуляризация. Кроме того, стволовые клетки могут сами дифференцироваться в клетки кожи или сосудов. Стимуляция ангиогенеза является ключевым аспектом в заживлении трофических язв, в основе патогенеза которых лежат нарушения микроциркуляции. Поэтому клеточная терапия в сочетании с этиотропным лечением рассматривается в качестве эффективной современной альтернативы традиционным методам лечения данной патологии [4, 5].
Цель исследования: изучить морфологические изменения в трофических язвах венозной этиологии в условиях эксперимента при применении аутотрансплантации жировой ткани.
Задачи исследования:
-
1. Получить модель трофической язвы венозной этиологии в эксперименте.
-
2. Оценить морфологическую картину при аутотрансплантации жировой ткани в лечении трофических язв в эксперименте.
Материалы и методы
Объекты исследования: в виварии выполнена серия экспериментов, на 20 кроликах линии Шиншилла, старше 4-х месячного возраста обоего пола с массой тела от 3,0 килограмм.
Проведенные процедуры: всем кроликам обеих групп, изначально моделировалась трофическая язва по патенту РФ № 2510083 от 2014 г., с авторским добавлением, для получения трофической язвы именно венозной этиоло- гии, которая включала в себя дополнительную перевязку v. femoralis (бедренной вены). Далее после получения трофической язвы венозной этиологии, очищения и появления вялой грануляции, кролики были разделены на две группы. В контрольной группе из 10 кроликов применялась системная лекарственная терапия, включающая в себя ежедневные перевязки с обработкой трофической язвы раствором антисептика – диоксидина, и наложением асептической повязки с мазью левомеколь. Основной группе кроликов, состоящей из 10 кроликов, на фоне аналогичной системной лекарственной терапии, была проведена аутотрансплантация жировой ткани в область трофической язвы.
Экспериментальным животным в обеих группах, после очищения трофической язвы, проводилось морфологическое исследование на 9-е, 18-е и 27-е сутки после аутотрансплантации жировой ткани. Биопсионный материал брался из края язвы с захватом нормальной ткани и дна трофической язвы, которое иссекалось на всю толщу до фасции. Материал подвергался фиксации в забуференном 10% нейтральном формалине, затем по стандартным методикам обезвоживали в спиртах, пропитывали парафином, заливали в парафиновые блоки, изготавливали гистологические срезы толщиной 5 мкм на микротоме. Полученные препараты окрашивали гематоксилином и эозином. Все гистологические препараты в дальнейшем подвергали обзорной микроскопии.
Результаты и обсуждение
Моделирование трофической язвы проводили следующим способом:
-
1. За 15 минут до операции с целью премедикации экспериментальным животным вводили атропина сульфат в дозе 0,05 мг/кг подкожно.
-
2. После предварительной обработки кожи в асептических условиях, под наркозом (с помощью препарата золетил 100 - 15 мг/кг в/м), на выбритом от шерсти участке кожи, на внутренней поверхности бедра, проводился оперативный доступ к бедренной вене с последующим прошиванием через центр сосуда проленом 7/0 и перевязкой ½ вены, что приводило к сужению просвета в 2 раза. Производили далее контроль на гемостаз. Послеоперационную рану послойно ушивали. Накладывали асептическую повязку.
-
3. Далее на той же конечности, ниже уровня перевязки, после предварительной обработки кожи и гидропрепаровки раствором лидокаина 2% - 5 мл, в асептических условиях, на выбритом от шерсти участке кожи, выполняли иссечение кожи по задненаружной поверхности нижней трети бедра кролика, до поверхностной фасции в виде окружности, диаметром около 40 мм.
-
4. На поверхности дна образованной раны производили рассечение поверхностной фасции поперечными и продольными, взаимоперпендикулярными разрезами.
-
5. По краям раны накладывали кисетный шов для создания картины нарушения микроциркуляции, стягивали, доводя рану в диаметре до 20 мм.
-
6. В целях удержания краев раны и предотвращения их сближения накладывали кожно-фасциальные узловые швы. Далее выполняли контроль на гемостаз. Накладывали асептическую повязку.
-
7. Смену асептической повязки проводили через день.
Полученная модель позволила через 2 недели сформировать трофическую язву венозной этиологии в эксперименте со всеми характерными для нее признаками: отек нижней конечности, где была перевязана бедренная вена; имеется рана со скудным фибринозно-гнойным отделяемым, дно раны покрыто участками фибрина, вялыми грануляциями. Кожа вокруг раны отечна, несколько гиперемирована (рис. 1).
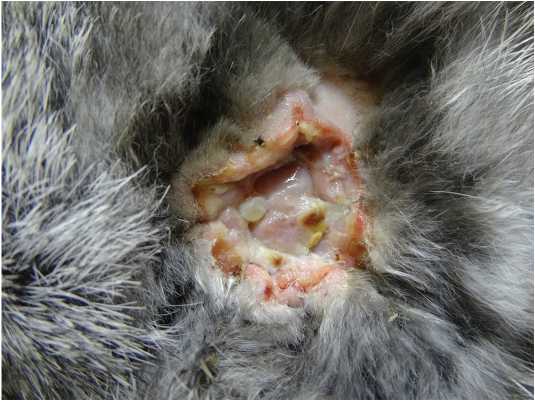
Рис. 1. Трофическая язва венозной этиологии полученная в эксперименте
Далее, после получения трофической язвы с элементами нагноения, проводилась специфическая консервативная терапия, направленная на очищение раны, которая включала в себя ежедневные перевязки с обработкой 3% перекисью водорода и раствором антисептика (диоксидин 1%). После очищения трофической язвы, кролики были разделены на 2 группы.
Контрольная группа из 10 кроликов получала консервативную терапию, которая включала в себя ежедневную обработку трофической язвы 1% раствором диоксидина и наложением асептической повязки с мазью левомеколь.
Основной группе из 10 кроликов, на фоне аналогичной консервативной терапии, была проведена аутотрансплантация жировой ткани (рис. 2).
Морфологические изменения в трофических язвах на 9-е сутки эксперимента идентичны в обеих группах. Регистрируются начальные проявления краевой эпителизации в виде пролиферации эпидермиса с его акантозом и распространением с краев раны на ее поверхность. Раневой дефект покрыт некротическими массами, под которыми определяется неравномерной толщины слой грануляционной ткани, отграниченный от умеренно отечной подкожной клетчатки
нешироким лейкоцитарным валом. В подлежащих и окружающих рану тканях визуализируются различного калибра сосуды, в том числе капилляры, которые паретически расширены, полнокровны. В краях язвы определяются в умеренном количестве макрофаги, отдельные фибробласты и немногочисленные плазматические клетки (рис. 3).
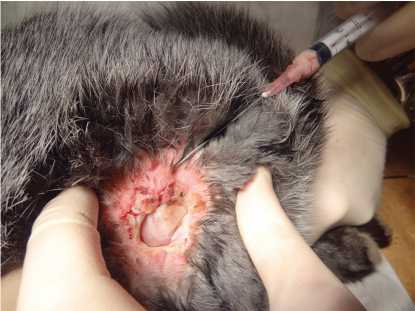
Рис. 2. Аутотрансплантация жировой ткани в эксперименте
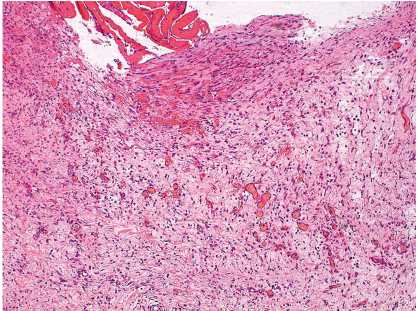
Рис. 3. Рана на 9-е сутки эксперимента. Грануляционная ткань в дне раневого дефекта содержит воспалительную инфильтрацию, составляющие ее кровеносные сосуды расположены хаотично, волокнистые структуры представлены слабо развитой нежнопетлистой сетью. ×200. Окраска гематоксилином и эозином
В наблюдениях основной группы визуализируются участки, представленные пересаженными адипоцитами, имеющие вид долек, отделенных друг от друга перегородками из рыхлой соединительной ткани с многочисленными фибробластами (рис. 4). Воспалительная инфильтрация равномерно выражена в краях и дне раны. В ее составе преобладают сегментоядерные лейкоциты, макрофаги, лимфоциты.
Дно язвенного дефекта содержит слой грануляционной ткани, состоящей из многочисленных новообразованных тонкостенных сосудов, нежных волокнистых структур, между которыми расположены полиморфно-ядерные лейкоциты, макрофаги, лимфоидные элементы, небольшое количество фибробластов.
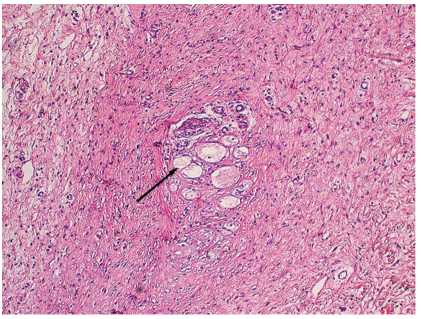
Рис. 4. Рана животного основной группы на 9-е сутки эксперимента. Пересаженные адипоциты, расположенные в глубине края раны, разграниченные перегородками из волокнистой соединительной ткани ( ↑ ). ×200. Окраска гематоксилином и эозином
На 18-е сутки во всех случаях контрольной группы имеет место неравномерное венозное полнокровие, очаговый, умеренный отек дермы и воспалительная инфильтрация. Дно раны содержит грануляционную ткань, слой которой имеет неравномерную толщину, но более внушительную, чем на 9-х сутках эксперимента. Кровеносные сосуды, составляющие основу грануляций, расположены разнона-правлено, с различной ширины просветами, клеточная инфильтрация сохраняет прежнюю выраженность, волокнистые структуры более отчетливы, но по-прежнему с небольшим количеством фибробластов. Эпителизация ограничена пределами краев раны (рис. 5). В основной группе на данном этапе эпидермис в краях раневого дефекта активно пролиферирует, обладает большей степенью дифференцировки (рис. 6). В центре раны сохраняется клеточная инфильтрация воспалительного характера, интенсивность которой заметно ниже, чем в наблюдениях группы контроля. Дно язвенного дефекта на всех участках содержит внушительной толщины слой зрелой грануляционной ткани, отличающейся упорядоченным расположением сосудов, лучшим развитием волокнистых структур и большим количеством фибробластов.
На 27-е сутки у животных контрольной группы сохраняются слабо выраженный отек дермы, перифокальная венозная гиперемия и воспалительная инфильтрация. Грануляционная ткань в дне язвенного дефекта имеет более зрелое, чем на предшествующем сроке эксперимента, строение, ее клеточная инфильтрация выглядит менее густой, наряду с фибробластами содержит немногочисленные фиброциты, лучше выражен волокнистый компонент. Пролиферация эпидермиса в краях ран имеет более активный, чем ранее характер, но несмотря на это большая часть поверхности трофической язвы лишена эпителия, эпидер-мизация ограничена пределами краевой зоны (рис. 7). В ос-
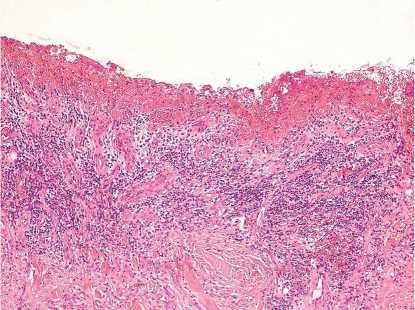
Рис. 5. Рана животного контрольной группы на 18-е сутки эксперимента. Дно дефекта не покрыто эпидермисом, содержит грануляционную ткань с разнонаправлено расположенными сосудами и воспалительную инфильтрацию. х200. Окраска гематоксилином и эозином
новной группе к 27 суткам большая часть раневого дефекта представлена хорошо развитой рыхлой, местами компактной волокнистой соединительной тканью, покрыта относительно дифференцированным эпидермисом с явными признаками ороговения. Под эпидермисом определяются небольшие участки зрелой грануляционной ткани, окруженные рыхлой волокнистой соединительной с небольшими фокусами полиморфноклеточной воспалительной инфильтрации (рис. 8).
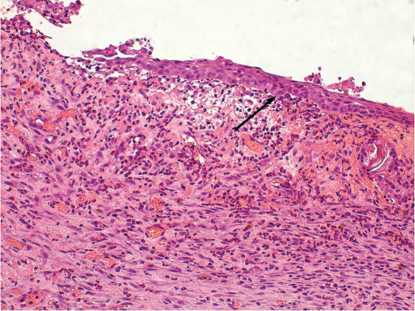
Рис. 6. Рана животного основной группы на 18-е сутки эксперимента. Эпителизация в крае раны путем «наползания» на дефект тонкого слоя эпидермиса ( ↑ ). х200. Окраска гематоксилином и эозином
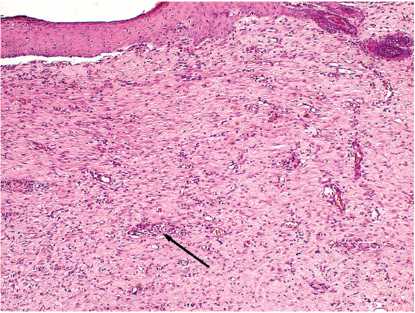
Рис. 8. Рана животного основной группы на 27-е сутки эксперимента. Дефект покрыт хорошо дифференцированным эпидермисом, под которым расположена волокнистая соединительная ткань с небольшими очаговыми воспалительными инфильтратами ( ↑ ). х200.
Окраска гематоксилином и эозином
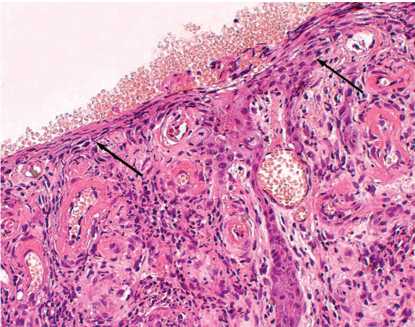
Рис. 7. Рана животного контрольной группы на 27-е сутки эксперимента. Поверхность трофической язвы в краевой зоне покрыта вновь образованным тонким, без проявлений ороговения эпителием ( ↑ ). х200. Окраска гематоксилином и эозином
Заключение
Полученная модель трофической язвы в эксперименте, позволяет ее отнести к венозной этиологии, что в дальнейшем может служить для этиопатогенетического выяснения закономерностей репаративной регенерации при различных способах лечения именно при данном патологии. Морфологическая картина позволяет судить о том, что в основной группе животных, где была применена предложенная методика, заживление происходило значительно быстрее.
Список литературы Патоморфология трофической язвы венозной этиологии в эксперименте при аутотрансплантации жировой ткани
- Лечение больных с трофическими язвами/Карапетян Г.Э., Якимов С.В., Микитин И.Л., Кочетова Л.В., Пахомова Р.А.//Вестник хирургии им. И.И. Грекова.-2014.-№3.-С.72-76.
- Савельев, В.С. Трофические язвы/В.С. Савельев, А.И. Кириенко//Клиническая хирургия: национальное руководство. -М.: ГЭОТАР-Медиа, 2008. -Т. 1. -С. 619-654.
- Миланов, Н.О. Перспективы клинического применения стволовых клеток жировой ткани в пластической хирургии и регенеративной медицине/Н.О. Миланов, О.И. Старцева, А.Л. Истранов, Д.В. Мельников, А.С. Захаренко//Хирургия. -2014. -№ 4. -С. 70-76.
- Stem Cells Therapy of Lower Extremity Ulcers/T. Tuganbekov //Journal of clinical medicine of Kazakhstan. -2013. -Vol. 4, N 30. -P. 14-20.
- Q. L. Zhong, F. R. Liu, D. W. Liu, et al., "Expression of β-catenin and cyclin D1 in epidermal stem cells of diabetic rats," Molecular Medicine Reports, vol. 4, no. 2, pp. 377-381, 2011.


