ПЦР в реальном времени для диагностики парагриппа-3 крупного рогатого скота
Автор: Гериш Ашуак , Галиуллин А.К., Гумеров В.Г., Шаева А.Ю., Парамонов А.С.
Статья в выпуске: 1 т.241, 2020 года.
Бесплатный доступ
Целью работы было определение эффективности метода ПЦР в диагностике парагриппа-3 (111 -3) крупного рогатого скота. Для исследований использовали референтный штамм «SF-4», вакцинный штамм «ПТК-45/86» и изолят «ЛД-9» вируса парагриппа-3. В результате проведенных исследований установлена эффективность и высокая скорость постановки ПЦР-РВ с флуоресцентной детекцией в диагностике парагриппа-3 крупного рогатого скота. Все исследованные штаммы вируса ПГ-3 показали положительную амплификацию.
Вирус парагриппа-3 крупного рогатого скота, пцр-рв с флуоресцентной детекцией, лабораторная диагностика
Короткий адрес: https://sciup.org/142224199
IDR: 142224199 | УДК: 619:616078:616.98:578/579:636.2 | DOI: 10.31588/2413-4201-1883-241-1-62-66
Real-time PCR for diagnosis of bovine parainfluenza-3
The aim of the work was to determine the effectiveness of the PCR method in the diagnosis of bovine parainfluenza-3 (BPI-3). For research, we used the reference strain SF-4, the vaccine strain PTK-45/86 and the isolate LD-9 of the parainfluenza virus 3. As a result of the studies, the effectiveness and high execution speed of RT-PCR with fluorescence detection for the diagnosis of bovine parainfluenza type 3 were established. All studied strains of BPIV-3 showed positive amplification.
Текст научной статьи ПЦР в реальном времени для диагностики парагриппа-3 крупного рогатого скота
Респираторные заболевания молодняка крупного рогатого скота, вызываемые вирусами парагриппа-3, диареи, инфекционного ринотрахеита и респираторносинцитиальной болезни, представляют собой серьезную проблему для здоровья крупного рогатого скота во всем мире, в том числе и в России. [1, 5]. Наиболее тяжелые последствия среди этих инфекций вызывает вирус ПГ-3.
Вирус парагриппа- 3 (ПГ-3) крупного рогатого скота относится к семейству Paramyxoviridae [9]. Геном вируса представлен однонитевой нефрагментирован-ной РНК негативной полярности, размером порядка 15500 оснований. Белки возбудителя, взаимодействуя с геномной РНК, образуют вирусный нуклеокапсид [3].
Парагрипп-3 крупного рогатого скота (инфекционный бронхит, бронхопневмония, острый катар верхних дыхательных путей, транспортная лихорадка, параинфлуэнца-3) – острое контагиозное заболевание крупного рогатого скота (преимущественно молодняка до 6-месячного возраста), характеризующееся катаральногнойным поражением органов дыхания, лихорадкой, общим угнетением, приступами сухого, болезненного кашля, катаральным конъюнктивитом [2, 4]. Кроме того, у взрослых животных парагрипп-3
может проявляться в виде абортов [8]. Сложность диагностики увеличивается из-за постоянного смешанного течения болезни (осложнение сальмонеллезом, ста-филококкозом, пастереллёзом) [6].
Лабораторная диагностика возбудителя болезни парагриппа-3 крупного рогатого скота обычно выполняется путем выделения вируса в культуре клеток (золотой стандарт), вирус вызывает типичный ци-топатический эффект с образованием синцития и цитоплазматических включений [11]. Молекулярным методом, используемым для диагностики ПГ-3, является ПЦР с предварительной обратной транскрипцией [10, 7].
Целью исследования было определение эффективности полимеразной цепной реакции в реальном времени (ПЦР-РВ) с применением тест-системы «ПЦР-парагрипп-3 КРС-фактор» в диагностике парагриппа-3 крупного рогатого скота.
Материал и методы исследований. В работе использовались следующие вирусные штаммы:
-
- «SF-4» – референтный штамм вируса ПГ-3, инфекционная активность на перевиваемых линиях культуры клеток легкого эмбриона коровы (ЛЭК) - 7,25 кг ТЦД 50 / мл.
-
- «ПТК-45/86» – вакцинный штамм вируса ПГ-3, инфекционная активность на
перевиваемой линии культуры клеток ЛЭК - 6,75 лг ТЦД 50 / мл.
-
- «ЛД-9» – вирусный изолят, выделенный из патологического материала, взятого от больного респираторным заболеванием теленка, инфекционная активность на перевиваемой линии культуры клеток ЛЭК - 6,25 кг ТЦД 50 / мл.
ПЦР проводили с использованием набора «ПЦР-парагрипп-3 КРС-фактор», согласно инструкции производителя (ООО «ВЕТ ФАКТОР», Москва-Троицк) на ам-плификаторе ДТ-96 («ДНК-технология», Россия).
Выделение РНК возбудителя из биологического материала осуществляли с применением набора «ДНК / РНК-с- фактор» (ООО «ВЕТ ФАКТОР», Москва-Троицк).
Для экстракции РНК использовали 50 мкл биологического материала. Для процесса амплификации использовали по 10 мкл выделенной РНК при общем объёме реакционной смеси 25 мкл.
Для постановки ПЦР-РВ с флуоресцентной детекцией необходима двухцепочечная ДНК, поэтому амплификации фрагментов генетического материала вируса прагриппа-3 предшествовало преобразование молекулы РНК возбудителя в ДНК путём обратной транскрипции.
Обратная транскрипция и амплификация осуществлялись по режиму, описанному в таблице 1.
Таблица 1 – Температурно-временной режим амплификации на ДТ-96.
|
№ п/п |
Температурно-временной режим |
Число циклов |
|
1 |
55оС-15минут (обратная транскрипция) |
1 |
|
2 |
95оС-5мин |
1 |
|
3 |
95оС-20сек |
45 |
|
58оС-30с, детекция НЕХ, Су5 |
||
|
72оС-20сек |
Результаты исследований. Результаты кривых накоплений флуоресцентного сигнала анализировали с помощью программного обеспечения используемого прибора для проведения ПЦР в соответствии с инструкцией к прибору .
Учет результатов ПЦР-РВ проводили по наличию или отсутствию пересечения кривой флуоресценции с установлен- ной на соответствующем уровне пороговой линии. На рисунках 1, 2, 3 представлены полученные нами графики амплификации.
В соответствии с вышеизложенным, все использованные нами пробы, как и предполагалось, оказались положительными, т.е показали присутствие вируса парагриппа-3 крупного рогатого скота
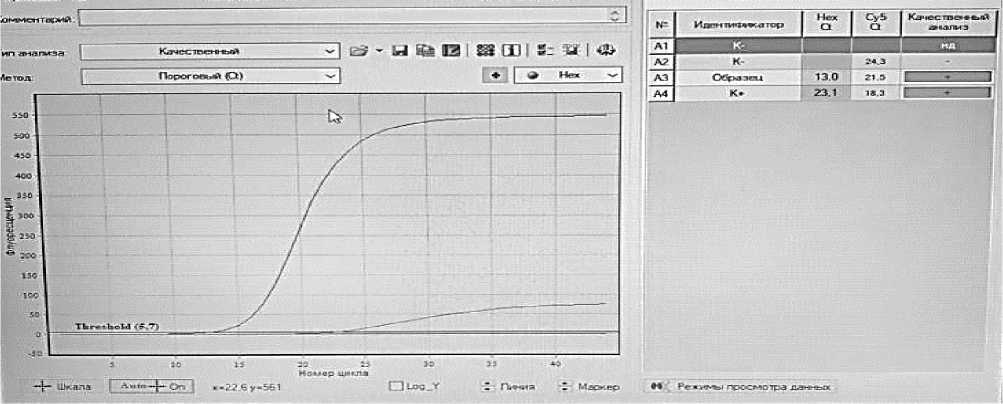
Рисунок 1 – График амплификации по флуорофору НЕХ изолята «ЛД-9» вируса парагриппа-3 крупного рогатого скота
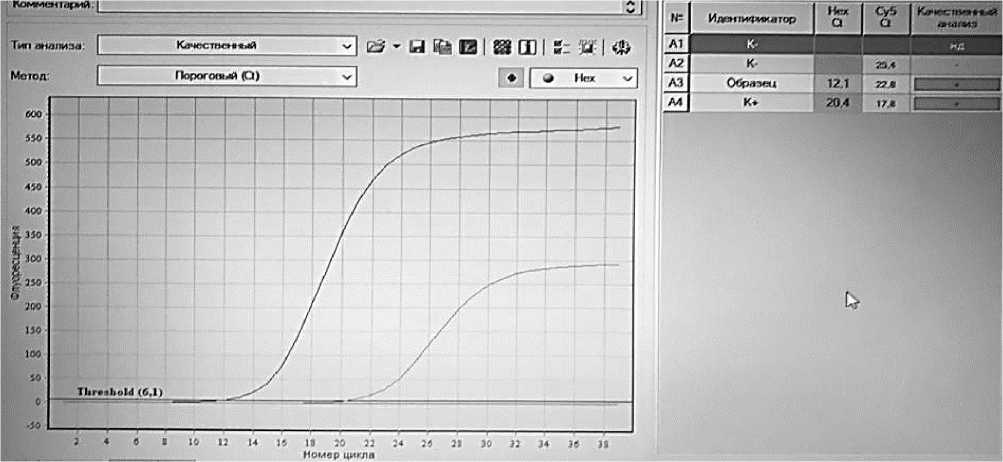
Рисунок 2 – График амплификации по флуорофору НЕХ вакцинного штамма «ПТК 45/86»
вируса парагриппа-3 крупного рогатого скота
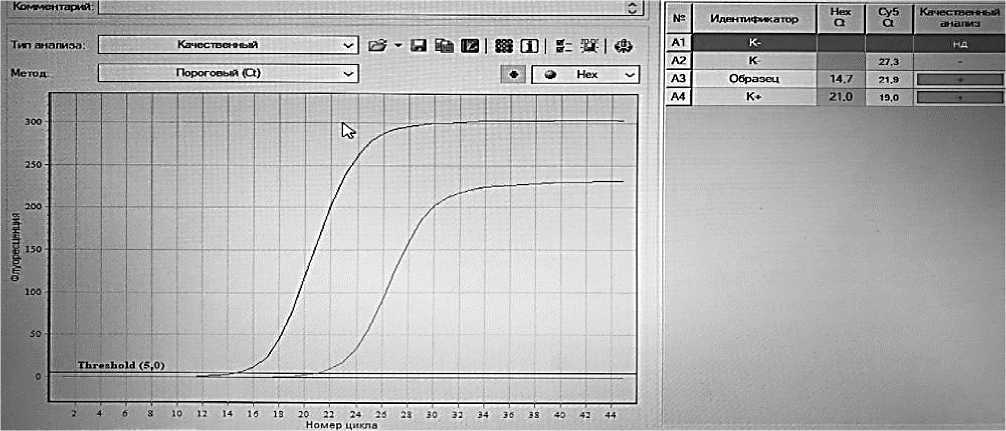
Рисунок 3 – График амплификации по флуорофору НЕХ референтного штамма «SF-4» вируса парагриппа-3 крупного рогатого скота
Таблица 2 - Анализ по номеру цикла по видам штамма
|
№ п/п |
Штамм |
Идентификатор |
СТ |
Качественный анализ |
|
1 |
Вирусный изолят «ЛД-9» |
К- |
- |
- |
|
Образец |
13,0 |
+ |
||
|
К+ |
23,1 |
+ |
||
|
2 |
Вакцинный штамм «ПТК 45/86» |
К- |
- |
- |
|
Образец |
12,1 |
+ |
||
|
К+ |
20,4 |
+ |
||
|
3 |
Референтный штамм «SF-4» |
К- |
- |
- |
|
Образец |
14,7 |
+ |
||
|
К+ |
21,0 |
+ |
Примечание: К- – отрицательный контроль; К+ – положительный контроль; СТ – номер цикла
На рисунках 1, 2 и 3 показаны графики накопления флуоресценции при постановке ПЦР-РВ со штаммами вируса ПГ-3. Сигналы флуоресценции исследуемых образцов во всех трёх случаях появляются значительно раньше, чем в положительных контролях, что указывает на изначально более высокую концентрацию вируса парагриппа-3 крупного рогатого скота в пробах. Расшифровка графиков с указанием номеров циклов начала сигнала флуоресценции представлена в таблице 2.
Результаты показали, что значения СТ контрольных образцов находятся в пределах нормы (СТ<31), значит наблюдается экспоненциальный рост сигнала по НЕХ, образец считается положительным, РНК вирус парагриппа-3 крупного рогатого скота присутствует.
Заключение. Результаты исследований методом полимеразной цепной реакции с флуоресцентной детекцией в режиме реального времени (ПЦР-РВ) известных штаммов (референтный «SF-4», вакцинный «ПТК45/86» и вирусный изолят «ЛД-9») вируса парагриппа-3 крупного рогатого скота, как и предполагалось, оказались положительными, так как РНК вируса ПГ-3 крупного рогатого скота присутствует во всех образцах.
При отрицательных контролях амплификации активности не зарегистрировано. Это говорит о высокой достоверности метода ПЦР-РВ при диагностике ПГ-3 КРС.
Кроме того, система ПЦР в реальном времени обеспечивает дополнительную возможность определить начальное количество целевой ДНК или РНК, присутствующей в образце.
Исходя из вышеизложенного, следует заключить, что полимеразная цепная реакция в реальном времени, основанная на обнаружении генетического материала возбудителя, является надежным, точным и быстрым методом диагностики парагриппа-3 и при этом не требует выделения и культивирования самого вируса.
Резюме
Целью работы было определение эффективности метода ПЦР в диагностике парагриппа-3 (ПГ-3) крупного рогатого скота. Для исследований использовали референтный штамм «SF-4», вакцинный штамм «ПТК-45/86» и изолят «ЛД-9» вируса парагриппа-3. В результате проведенных исследований установлена эффективность и высокая скорость постановки ПЦР-РВ с флуоресцентной детекцией в диагностике парагриппа-3 крупного рогатого скота.
Все исследованные штаммы вируса ПГ-3 показали положительную амплификацию.
Summarу
The aim of the work was to determine the effectiveness of the PCR method in the diagnosis of bovine parainfluenza-3 (BPI-3). For research, we used the reference strain SF-4, the vaccine strain PTK-45/86 and the isolate LD-9 of the parainfluenza virus 3. As a result of the studies, the effectiveness and high execution speed of RT-PCR with fluorescence detection for the diagnosis of bovine parainfluenza type 3 were established.
All studied strains of BPIV-3 showed positive amplification.
Список литературы ПЦР в реальном времени для диагностики парагриппа-3 крупного рогатого скота
- Гумеров, В.Г. Эпизоотологический и серологический мониторинг смешанных респираторно-кишечных инфекций крупного рогатого скота / В.Г. Гумеров [и др.] // Ученые записки Казанской государственной академии ветеринарной медицины им. Н.Э. Баумана - 2019. - № 237(1). - С. 56-60.
- Лисицын, В.В. Проблемы респираторных болезней молодняка крупного рогатого скота и пути их решения / В.В. Лисицын // Ветеринария с/х животных. -2010. - № 5. - С. 12-16.
- Allan, E.M. Some characteristics of a natural infection by parainfluenza-3 virus in a group of calves / E.M. Allan [et al.] // Research in Veterinary Science. - 1978. - V. 24(3). - P. 339-346.
- Ellis, J.A. The immunology of the bovine respiratory disease complex / J.A. Ellis // Veterinary Clinic of North America Food Animal Practice. - 2001. - Vol. 17. - P. 535-550.
- Galiullin, A.K. Inactivated Liposomal Vaccine Against Bovine Infectious Rhinotracheitis And Parainfluenza-3 / A.K. Galiullin [et al.] / Research Journal of Pharmaceutical, Biological and Chemical Sciences. -2019. - V. 10(1). - P. 1766-1771.
- Henrickson, K.J. Parainfluenza Viruses / K.J. Henrickson // Clin. Microbiol. Rev. - 2003. - V. 16(2). - P. 242-264.
- Horwood, P.F. Identification of two distinct bovine parainfluenza virus type 3 genotypes // P.F. Horwood, J.L. Gravel, T.J. Mahony // Journal of General Virology. -2008. - V. 89(7). - P. 1643-1648
- Kirkbride, C.A. Viral agents and associated lesions detected in a 10-year study of bovine abortions and stillbirths / C.A. Kirkbride // J. Vet. Diag. Invest. - 1992. - V. 4(4). - P. 374-379.
- Maidana, S. Isolation and characterization of bovine parainfluenza virus type 3 from water buffaloes (Bubalus bubalis) in Argentina / S. Maidana [et al.] // BMC Veterinary Research. - 2012. - 8:83. - P. 1-9.
- Murphy, F. Paramyxoviridae / F. Murphy [et al.] // Veterinary Virology. Third Edition. - 1999. - P. 411-428.
- Vaucher, R.A. RT-PCR for detection of bovine parainfluenza virus type 3 (BPIV-3) / R.A. Vaucher, A.B. Simonetti, P.M. Roehe // Acta Scientiae Veterinariae. - 2008. - V. 36(3). - P. 215-220.


