Переэтерификация 3-аминопропилтриэтоксисилана трифенилсиланолом
Автор: Владимир Викторович Семёнов
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 4 т.17, 2025 года.
Бесплатный доступ
Показано, что трифенилсиланол способен заместить одну или две этоксигруппы в 3-аминопропилтриэтоксисилане. 3 Аминопропил(трифенилсилокси)(диэтокси)силан (Ph3SiO)(EtO)2Si-CH2CH2CH2-NH2 и 3 аминопропилбис(трифенилсилокси)(этокси)силан (Ph3SiO)2(EtO)Si-CH2CH2CH2-NH2 получены с выходами 56 и 27 %. 3 Аминопропил(трифенилсилокси)(диэтокси)силан не подвергается гидролизу водой в диоксане. Добавление катализатора Bu4NF приводит к образованию 3 аминопропил(трифенилсилокси)(дигидрокси)силана (Ph3SiO)(HO)2SiCH2CH2CH2NH2 и продукта его конденсации до полимера HO[(Ph3SiO)Si(CH2CH2CH2NH2)O]nH. Соединения охарактеризованы методами элементного анализа, ИК и ЯМР спектроскопии.
3-аминопропилтриэтоксисилан, трифенилсиланол, реакции замещения
Короткий адрес: https://sciup.org/147252518
IDR: 147252518 | УДК: 547.245 | DOI: 10.14529/chem250406
Transesterification of 3-aminopropyltriethoxysilane with triphenylsilanol
It has been shown that triphenylsilanol is capable of replacing one or two ethoxy groups in 3-aminopropyltriethoxysilane. 3-Aminopropyl(triphenylsiloxy)(diethoxy)silane (Ph3SiO)(EtO)2Si-CH2CH2CH2-NH2 and 3-aminopropylbis(triphenylsiloxy)(ethoxy)silane (Ph3SiO) 2(EtO)Si-CH2CH2CH2-NH2 have been obtained, yielding 56% and 27%. 3-Aminopropyl(triphenylsiloxy)(diethoxy)silane is not subject to hydrolysis by water in dioxane. Addition of the Bu4NF catalyst results in formation of 3-aminopropyl(triphenylsiloxy)(dihydroxy)silane (Ph3SiO)(HO)2SiCH2CH2CH2NH2 and its condensation product to polymeric HO[(Ph3SiO)Si(CH2CH2CH2NH2)O]nH. The compounds are characterized by elemental analysis, IR and NMR spectroscopy.
Текст научной статьи Переэтерификация 3-аминопропилтриэтоксисилана трифенилсиланолом
Введение
3-Аминопропилтриэтоксисилан (АПТЭС) представляет собой один из наиболее важных и доступных мономеров для золь-гель процессов [1–5]. Многие приложения требуют негидро-лизующихся мономеров. Так, с целью допирования органических и силиконовых полимеров флуоресцирующими ингредиентами в работе [6] были получены координационные соединения европия(III) и эрбия(III), содержащие в лиганде трис (триметилсилокси)силильную группу. Синтез лиганда производили взаимодействием ацетилацетона с
3-аминопропил трис (триметилсилокси)силаном (Me3SiO)3Si-CH2CH2CH2-NH2. Получающаяся смесь изомеров 4-(3/- трис (триметилсилокси)силилпропилимин)пент-2-ен-2-ола (Me 3 SiO) 3 Si-
CH 2 CH 2 CH 2 -N=C(Me)CH=C(Me)OH (90 %) и 4-(3/- трис (триметилсилокси)силилпропиламин)пент-3-ен-2-она (Me 3 SiO) 3 Si-CH 2 CH 2 CH 2 -NН-C(Me)=CH-C(О)Me (10 %) взаимодействовала с безводными изопропилатами Eu(OPri)3 и Er(OPri)3, давая трис [4-(3/- трис (триметилсилокси)силил-пропилимин)пент-2-ен-2-оляты] европия(III) и эрбия(III), которые представляли собой устойчивые на воздухе перегоняющиеся в вакууме прозрачные жидкости, обладающие растворимостью в полимеризующихся под действием света полиорганосилоксановых каучуках и олигоэфируретан-акрилатах. Переэтерификация АПТЭС триметилсиланолом изучалась ранее в работе [7]. В настоящем исследовании представлены сведения о переэтерификации АПТЭС трифенилсиланолом. В отличие от триметилсиланолятных трифенилсиланолятные производные кремнийорганическо-го амина способны эффективно поглощать в УФ области спектра и передавать полученную световую энергию на лиганд и люминесцирующий катион редкоземельного металла.
Экспериментальная часть
ИК-спектры соединений в виде жидкой пленки между пластинами KBr, CaF2 регистрировали на ИК-Фурье спектрометре ФСМ 1201. Cпектры ЯМР 1Н в растворе CDCl 3 регистрировали на приборе Bruker Avance DPX-200 (200 МГц) при 25 ºС, внутренний стандарт Me 4 Si.
3-Аминопропил(трифенилсилокси)(диэтокси)силан ( I ). Раствор 2,73 г (9,88 ‧ 10–3 моль) Ph3SiOH и 2,86 г (1,29 ‧ 10–2 моль) АПТЭС в 25 мл толуола нагревали при кипении 20 ч, толуол отгоняли при атмосферном давлении, избыточный АПТЭС – в вакууме. В остатке получили вязкую жидкость, из которой через 12 ч выпало 0,24 г кристаллов гексафенилдисилоксана. Остаток разбавили гексаном, отфильтровали, фильтрат упарили и перегнали в условиях молекулярной дистилляции. Получили 2,34 г (5,52 ‧ 10–3 моль, 56 %) соединения I в виде бесцветной вязкой жидкости, n D 20 1,4980. Найдено, %: C 66,42; Н 7,69; Si 12,05. C 25 H 33 NO 3 Si 2 . Вычислено, %: C 66,47; Н 7,36; Si 12,44. ИК-спектр, см–1: 3380 сл N-H), 3070, 3065, 3020 (C-H фенил), 2980, 2930, 2895 (С-Н алкил), 1965, 1900, 1830, 1600, 1830, 1600, 1490, 1440, 1395, 1300, 1190, 1165, 1130, 1080, 1030, 1000, 965, 870, 800, 750, 720, 520. Cпектр ЯМР 1H, δ, м. д.: 0,52; 0,56; 0,57; 0,60 (кв., 2H, CH 2 -Si); 0,96 (c., 2H, NH 2 ); 1,08; 1,11; 1,15 (т., 6H, CH 3 -CH 2 O); 1,35; 1,40; 1,42; 1,44; 1,47 (п., 2H, CH 2 ); 2,48; 2,51; 2,55 (т., 2H, CH 2 N); 3,67; 3,70; 3,74; 3,77 (кв., 2H, CH 3 - CH 2 -O); 7,26–7,65 (м., 15H, C 6 H 5 ).
3-Аминопропилбис(трифенилсилокси)(этокси)силан ( II ) получали аналогично. Выход 27 %. Найдено, %: C 72,10; Н 6,37; Si 11,92. C 41 H 43 NO 3 Si 3 . Вычислено, %: C 72,20; Н 6,36; Si 12,35. ИК-спектр, см–1: 3370, 3290 (NH), 3070, 3065, 3020 (CH фенил), 2980, 2930, 2890 (CH алкил), 1965, 1890, 1835, 1600 (Ph), 1500, 1440 (SiPh), 1395, 1200, 1160 (SiOEt), 1140 (SiPh), 1090 (SiOSi), 1010, 970 (SiOEt) 870, 800, 750 (SiOEt), 730, 540. Cпектр ЯМР 1H, δ, м. д.: 0,57 (м., 2H, CH 2 Si); 0,88 (м., 2H, NH 2 ); 1,00; 1,15; 1,23 (т., 3H, CH 3 CH 2 O); 1,43 (м., 2H, CH 2 ); 2,34; 2,50; 2,67 (т., 2H, CH 2 N); 3,61; 3,76; 3,78; 3,89 (кв., 2H. CH 3 CH 2 O); 7,37; 7,65 (м., 30H, C 6 H 5 ).
Гидролиз 3-аминопропил(трифенилсилокси)(диэтокси)силана ( I ). Соединение I 1,45 г (3,42 ‧ 10–3 моль) растворили в 20 мл диоксана, добавили 0,50 г (2,78 ‧ 10–2 моль) Н 2 О. Через 5 суток диоксан и воду удалили в вакууме. Получили прозрачную бесцветную жидкость, ИК-спектр которой оказался полностью идентичным спектру исходного соединения I. Соединение снова растворили в 20 мл диоксана, добавили 0,50 г Н 2 О и 0,01 г Bu 4 NF. Через 1 ч из раствора начал выпадать белый осадок. Через 4 суток раствор сдекантировали с осадка и упарили в вакууме. Получили 0,98 г полимера IV в виде белой смолы, которая при последующем вакуумировании превратилась в твердое вещество, плотно прилипшее к стенкам колбы и нерастворимое в эфире, хлороформе, ацетонитриле, плохо растворимое в бензоле и толуоле. ИК-спектр, см-1: 3380, 3290 (NH), 3130, 3065, 3030, 3010 (CH фенил), 1665, 1590, 1510, 1445 (SiPh), 1125, 1100 (SiPh), 1050 (SiOSi), 1000, 750, 725 (SiPh), 710, 525, 475, 440. Осадок промыли эфиром, высушили в вакууме, получили 0,14 г (3,5 ‧ 10–4 моль, 10 %) 3-аминопропил(трифенилсилокси)(дигидрокси)силана (Ph 3 SiO)(HO) 2 SiCH 2 CH 2 CH 2 NH 2 ( III ). ИК-спектр, см-1: 3740 (OH), 3370, 3300 (NH), 3270 (c., ушир., SiOH), 3075, 3065, 3020 (CH, фенил), 1660, 1600, 1435 (SiPh), 1310, 1265, 1230, 1190, 1130 (SiPh), 1035 (SiO), 935, 765, 725 (SiPh), 465. Найдено, %: C 63,51; Н 6,20; Si 14,81. C 41 H 43 NO 3 Si 3 . Вычислено, %: C 63,76; Н 6,37; Si 14,20.
Обсуждение результатов
Реакция АПТЭС с небольшим избытком трифенилсиланола в кипящем толуоле привела к образованию 3-аминопропил(трифенилсилокси)бис(триэтокси)силана с выходом 56 %. Длительным нагреванием раствора в толуоле (20 ч) 3 молей трифенилсиланола с 1 молем АПТЭС удалось заместить только 2 диэтоксигруппы у атома кремния. И в том, и в другом случае наблюдалась побочная реакция конденсации трифенилсиланола до гексафенилдисилоксана, который выделялся в виде белого кристаллического осадка из реакционной смеси после удаления толуола.
Ph 3 SiOH + (EtO) 3 SiCH 2 CH 2 CH 2 NH 2 → (Ph 3 SiO)(EtO) 2 SiCH 2 CH 2 CH 2 NH 2
I
2 Ph 3 SiOH + (EtO) 3 SiCH 2 CH 2 CH 2 NH 2 → (Ph 3 SiO) 2 (EtO)SiCH 2 CH 2 CH 2 NH 2
II
2 Ph 3 SiOH → Ph 3 SiOSiPh 3 + H 2 O
Соединение I представляло собой бесцветную прозрачную жидкость, соединение II по внешнему виду напоминало вазелин. Они были очищены от примесей молекулярной дистилляцией. Оба соединения устойчивы на воздухе. Диэтоксипроизводное I не подвергалось гидролизу избытком воды в растворе диоксана. Добавление в качестве катализатора фтористого тетрабути-ламмония привело к образованию 3-аминопропил(трифенилсилокси)(дигидрокси)силана ( III ) и продукта его конденсации до полимера ( IV ).
(Ph3SiO)(EtO)2SiCH2CH2CH2NH2 + 2 Н2О → (Ph3SiO)(HO)2SiCH2CH2CH2NH2 + 2EtOH I III n (Ph3SiO)(HO)2SiCH2CH2CH2NH2 → HO[(Ph3SiO)Si(CH2CH2CH2NH2)O]nH + (n-1) H2O III IV
В ИК-спектрах соединений I–IV присутствовали две малоинтенсивных полосы поглощения аминной группы в области 3300 см–1, серия полос, относящихся к колебаниям связи С-Н фенильного радикала 3070–3020 см–1. Полосы 1440 и 1130 см–1 характеризовали фрагмент SiPh. Группа EtO- представлена 4 полосами 1160, 965, 800 и 470 см–1, силоксановая связь – интенсивной полосой 1080–1030 см-1. Увеличение количества фенильных групп при переходе от соединения I к соединению II наглядно проявилось в возрастании интенсивности полос поглощения связей С-Н фенильных групп. В спектре силандиола III присутствовала широкая интенсивная полоса поглощения с центром при 3270 см–1, принадлежащая валентным колебаниям связи О-Н в гидроксильных группах у атома кремния. Гидроксильные группы связаны водородными связями. Острая полоса поглощения свободных ОН групп при 3740 см–1 имела малую интенсивность. Аминная группировка проявилась в виде двух пиков 3370 и 3300 см–1, наложенных на широкую полосу связей О-Н. В полимере IV содержание гидроксильных группировок во много раз меньше, поэтому соответствующая полоса поглощения имела малую интенсивность.
В спектре ПМР соединения I (см. рисунок) резонансы протонов группы СН 2 , располагающейся у атома кремния, представлены квадруплетом 0,52; 0,56; 0,57; 0,60 м. д, протоны аминной группы – синглетом 0,96 м. д. Интенсивный триплет 1,08; 1,11; 1,15 м.д. соответствует шести протонам этоксизаместителя CH3 -CH2O-. Располагающийся справа в более слабом поле пентет 1,35; 1,40; 1,42; 1,44; 1,47 м.д. принадлежит срединной метиленовой группе 3-аминопропильного фрагмента.
CH 2 CH 2 CH 2 NH 2 . Триплет 2,48; 2,51; 2,55 м.д. соответствует группировке CH 2 N, а квадруплет 3,67; 3,70; 3,74; 3,77 м.д. метиленовой группе у атома кислорода этоксизаместителя CH 3 - CH 2 -O). Интенсивный мультиплет 7,26–7,65 м.д. характеризует 15 протонов 3 фенильных заместителей.
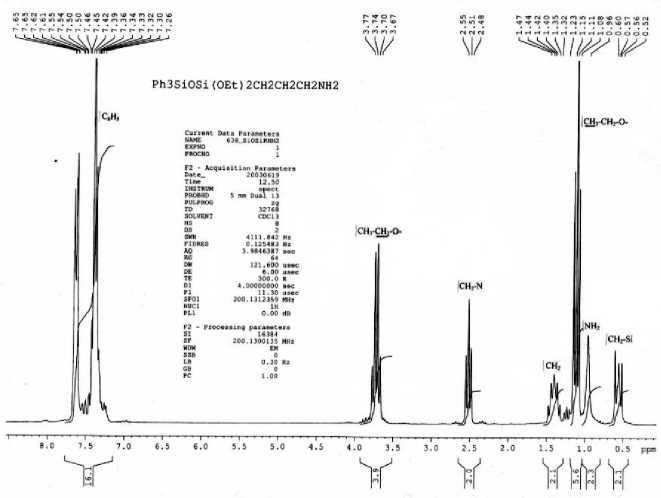
Спектр 1Н-ЯМР 3-аминопропил(трифенилсилокси)(диэтокси)силана (Ph 3 SiO)(EtO) 2 Si-CH 2 CH 2 CH 2 -NH 2 (I)
Таким образом, в результате проведенных исследований показана возможность замещения этокси групп в 3-аминопропилтриэтоксисилане на один или два объемистых трифенилсилокси заместителя. Монозамещенное производное стабилизировано и не гидролизуется водой в растворе диоксана без добавления катализатора. Несмотря на большую молекулярную массу дизаме-щенное производное не проявляет склонности к кристаллизации.


