Периферическая блокада как компонент анестезии и послеоперационного обезболивания при эндопротезировании коленного сустава
Автор: Жирова Т.А., Мокиенко А.П., Комкин В.А., Смышляев М.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.9, 2014 года.
Бесплатный доступ
Актуальность. Регионарная анестезия традиционно используется для обеспечения ортопедических операций. В последнее время наибольшее распространение получили блокады периферических нервов, как для анестезии, так и для послеоперационного обезболивания. Цель. Оценить возможности различных вариантов периферической блокады как компонента анестезии и послеоперационного обезболивания при эндопротезировании коленного сустава. Материал и методы. Ретроспективный анализ 66 пациентов, оперированных в условиях общей или сочетанной анестезии. Все пациенты получили тотальную внутривенную анестезию пропофолом, кетамином и фентанилом, из них: 12 - только общую анестезию, 17 - в сочетании с продленной илиофасциальной блокадой, 18 - в сочетании с продленной блокадой бедренного нерва и 19 - в сочетании с однократной блокадой бедренного нерва. Результаты. Общий расход пропофола был меньше в группах с сочетанной анестезией по сравнению с пациентами, у которых использовали общую анестезию. Применение продленных методик периферической блокады связано с меньшим расходом тримепередина для послеоперационного обезболивания. Гипертензия наблюдалась только в группе общей анестезии у 42% пациентов, в то время как гипотония отмечена в 9% случаев при использовании периферической блокады. Заключение. Блокада периферических нервов является эффективным и безопасным компонентом анестезиологической защиты при эндопротезировании коленного сустава. Продленные периферические блокады наиболее эффективны для послеоперационного обезболивания по сравнению с однократной блокадой нервов.
Эндопротезирование коленного сустава, блокада периферических нервов, общая анестезия, послеоперационная анальгезия
Короткий адрес: https://sciup.org/140188339
IDR: 140188339 | УДК: 616.728.3-089,844-089.5
Peripheral nerve block as the component of anesthesia and postoperative analgesia for total knee arthroplasty
Background: Regional anesthesia is most often used for orthopedic surgery. Nowadays peripheral nerve blocks are the most widespread techniques for anesthesia as well as for postoperative pain relief. Purpose: To evaluate the possibility of different peripheral nerve blocks as the component of anesthesia and postoperative analgesia in total knee arthroplasty. Methods: Retrospective analysis of 66 cases of total knee replacement under general anesthesia or in combination with peripheral nerve block. Total intravenous anesthesia with propofol, ketamine and fentanyl was performed for all patients. Patients received either alone general anesthesia (12 patients) or general anesthesia with continuous fascia iliaca compartment block (17 patients) or general anesthesia with continuous femoral nerve block (18 patients) or general anesthesia with single femoral nerve block (19 patients). Results: The total consumption of propofol was less in groups of patients under general anesthesia combined with different peripheral nerve block compared to alone general anesthesia group. Application of continuous peripheral nerve block techniques was associated with a lower consumption of trimeperidine for postoperative analgesia. Hypertension was observed only in the general anesthesia group, while hypotension was detected in the patients who received the peripheral nerve block (42% and 9% respectively). Conclusion: Peripheral nerve block is an effective and safe component of anesthesia for total knee arthroplasty. Continuous peripheral nerve blocks are more effective than a single block alone for postoperative pain relief.
Текст научной статьи Периферическая блокада как компонент анестезии и послеоперационного обезболивания при эндопротезировании коленного сустава
Традиционно для обеспечения ортопедических операций широко используются регионарные методы анестезии. В течение последних десятилетий доля регионарных видов обезболивания в ортопедической практике уверенно растет наряду с прогрессивным снижением числа наркозов [7]. Согласно обзору ортопедической практики GLORY [9] на их долю приходится от 50% до 70% всех выполняемых анестезий при эндопротезировании тазобедренного и коленного сустава. Преобладающим методом анестезии по данным регистра является нейроаксиальная блокада, а основой послеоперационного обезболивания – продленная эпидуральная анальгезия. Однако в начале нового тысячелетия структура регионарной анестезии и анальгезии претерпела существенные изменения. Так, на рубеже XX–XXI веков различные виды нейроаксиальной блокады все чаще уступают место изолированной анестезии нервных стволов и сплетений, а в течение последних 5–7 лет предпочтения специалистов фокусируются на сочетании различных периферических блоков с общей анестезией [6, 3].
Представленные тенденции определяются рядом факторов. Несмотря на отсутствие доказательных данных о преимуществах общей или регионарной анестезии в отношении эффективности и безопасности [7, 8], некоторые возможности регионарных методик позволяют обеспечить большую удовлетворенность и степень комфорта пациента, а также улучшить результаты лечения и дальнейшее качество жизни. Так в ближайшем послеоперационном периоде отсутствует постнаркозная седация, тошнота и рвота. Использование продленных блокад позволяет последовательно обеспечить адекватную анальгезию на всех этапах послеоперационного периода, облегчить реабилитацию и сократить сроки лечения. Регионарная анальгезия ассоциирует со снижением потребности в системных опиоидных анальгетиках

и сводит к минимуму нежелательные эффекты от их применения [4, 2, 1].
Наряду с этим блокада нервных стволов по сравнению с различными видами нейроаксиальной блокады минимизирует риск гемодинамических расстройств, не вызывает задержку мочеиспускания и исключает развитие такого грозного осложнения как эпидуральная/спи-нальная гематома, что существенно улучшает профиль безопасности медикаментозной профилактики тромбо-осложнений у ортопедических пациентов [1, 5].
Цель настоящего исследования – оценить возможности различных вариантов периферической блокады как компонента анестезии и послеоперационного обезболивания при эндопротезировании коленного сустава.
Материал и методы
Объектом исследования стали взрослые пациенты с дегенеративно-дистрофическими заболеваниями коленного сустава, которым была выполнена операция тотального эндопротезирования. Структура исследования представлена в таблице 1.
Задачи исследования:
-
1. Оценить эффективность и безопасность различных вариантов периферической блокады как компонента общей анестезии.
-
2. Определить потенциал различных видов периферической блокады в структуре послеоперационной анальгезии.
Пациенты отбирались методом сплошной нестра-тифицированной выборки по следующим критериям соответствия:
-
1. Вид анестезии:
-
а. Тотальная внутривенная анестезия с искусственной вентиляцией легких (ТВА с ИВЛ).
-
б. Сочетанная анестезия (ТВА с ИВЛ + периферический блок).
-
2. Пол: мужчины и небеременные, не кормящие грудью женщины.
-
3. Отсутствие декомпенсированной органной дисфункции.
-
4. Отсутствие онкологических заболеваний.
За указанный период (6 мес.) было отобрано 66 пригодных к извлечению данных историй болезни и
Табл. 1. Структура исследования
Во всех группах была выполнена тотальная сбалансированная внутривенная анестезия с ИВЛ: индукция осуществлялась диазепамом и фентанилом в сочетании с кетамином и (или) пропофолом; поддержание анестезии фентанилом и пропофолом с добавлением, при необходимости, анальгетических доз кетамина.
Периферические блокады выполняли до индукции под местной анестезией 2% раствором лидокаина. Во второй группе илиофасциальная блокада выполнялась иглой Туохи 18G (Portex®, Великобритания) по методике «double pop». После идентификации пространства одномоментно вводили болюс, для чего использовали ропивакаин 0,5% или 0,75% (Наропин®, Astra Zeneca, Швеция). Затем через иглу устанавливали катетер и начинали постоянную инфузию ропивакаина 0,2% (Наропин®, Astra Zeneca, Швеция) со скоростью 10 мл/час. Суммарная (болюс + инфузия) интраоперационная доза ропивакаина варьировалась в пределах от 150 до 300 мг со средним значением (СО) – 237,5 (75) мг. После операции инфузию 0,2% ропи-вакаина продолжали со скоростью 8–12 мл/час.
В третьей группе выполняли продленную блокаду бедренного нерва набором для продленной периферической блокады «StimuLong Sono» (Pajunk, Германия). Месторасположение нервных стволов определяли методом ответа на элктрический импульс с иглы и катетера с помощью нейростимулятора «MultiStim Switch» (Pajunk, Германия). После локации ветвей бедренного нерва (сокращение четырехглавой мышцы бедра и подъем коленной чашечки) вводили болюсно ропивакаин 0,5% или 0,75%, доза которого колебалась в диапазоне от 30 до 350 мг со средним значением (СО) – 212 (80) мг. В послеоперационном периоде сразу после окончания операции начинали продленную инфузию 0,2% ропивакаином 3 – 12 мл/час. Перед пере-
Жирова Т.А., Мокиенко А.П., Комкин В.А., Смышляев М.В.
ПЕРИФЕРИЧЕСКАЯ БЛОКАДА КАК КОМПОНЕНТ АНЕСТЕЗИИ И ПОСЛЕОПЕРАЦИОННОГО ОБЕЗБОЛИВАНИЯ ПРИ ЭНДОПРОТЕЗИРОВАНИИ КОЛЕННОГО СУСТАВА
водом больных 2-ой и 3-ей групп в отделение к катетерам присоединяли эластомерную помпу с 0,2% раствором ропивакаина и продолжали введение местного анестетика в течение 1 суток после операции со скоростью 5 мл/час. Катетер удаляли на 2 сутки после операции утром.
У пациентов 4-ой группы выполняли интраоперационную однократную блокаду бедренного нерва с помощью нейростимулятора «Stimuplex» (BBraun, Германия). Вводили ропивакаин 0,5% или 0,75% от 75 до 225 мг, средняя доза (СО) составила 179 (49) мг. По общей дозе интраоперационно введенного наропина пациенты в группах с периферическим блоком статистически значимо не отличались (p > 0,05).
В послеоперационном периоде пациентам всех исследуемых групп с целью обезболивания были назначены нестероидные противовоспалительные препараты: кетопрофен 100 мг или кеторолак 30 мг – от 2 до 3 раз в сутки в/м и тримеперидин (промедол) 20 мг в/м по требованию.
Оценку извлеченных данных проводили по следующим критериям: расход анестетиков, потребность в опиоидных анальгетиках, частота осложнений в интраоперационном и ближайшем послеоперационном периоде.
Статистический анализ осуществляли с использованием программы BIOSTAT для IBM PC (Glantz S.A., перевод на русский язык – М: «Практика», 1999). Все выборочные данные соответствовали нормальному распределению. Параметры распределения количественных признаков описывали с помощью среднего и стандартного отклонения. Для сравнения групп применяли однофакторный дисперсионный анализ, в случае сравнения двух групп, его частный случай – критерий Стъюдента. Множественные сравнения проводили, используя критерий Ньюмена-Кейлса. При сравнении долей использовали критерий χ2. Во всех случаях уровень значимости α, при котором отвергалась нулевая гипотеза, был принят равным 0,05.
Результаты и их обсуждение
Расход анестетиков
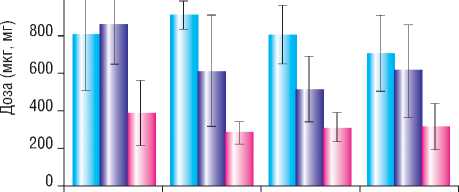
Потребность в пропофоле была статистически значимо меньше в группах с сочетанной анестезией по сравнению с пациентами, у которых операция была проведена в условиях общей анестезии (р < 0,05). Средний расход (СО) пропофола составил: в группе GA 850 (207) мг, в группе cFICB 607 (290) мг, у пациентов с cFNB 507 (171) мг и у больных с sFNB – 605 (246) мг. Статистически значимых отличий по расходу пропофола среди пациентов с различными видами сочетанной анестезии найдено не было (р > 0,05).
Потребность в кетамине возникла у всех пациентов с общей анестезией, у 14 из 17 (82%) в группе cFICB, у 13 из 18 (72%), в группе cFNB и у 16 из 19 (84%) больных в группе sFNB (p < 0,05). Статистически значимых отличий в расходе кетамина среди пациентов исследуемых групп найдено не было (р > 0,05). В группе общей анестезии количество введенного кетамина колебалось в пределах от 100 до 700 мг со средним значением (СО) – 383 (170) мг.
При использовании сочетанной анестезии расход кетамина находился в диапазоне от 100 до 500 мг, среднее значение (СО) определено в группах: cFICB –279 (58) мг, cFNB – 308 (76) мг и sFNB – 313 (120) мг.
Несмотря на отсутствие межгрупповых статистически значимых отличий клиническое значение имеет факт меньшей потребности и меньшего расхода анестетика в группах, где использовалась сочетанная анестезия. Отсутствие статистической разницы вероятно обусловлено двумя причинами: низкой статистической мощностью исследования и субъективным фактором, связанным с определенным консерватизмом в проведении рутинных анестезий на этапе внедрения новых методик. Тем не менее, увеличив чувствительность критерия путем преобразования групп (группа общая анестезия – 12 человек и группа сочетанная анестезия – 54 пациента) становится очевидным, что расход кетамина в случаях, когда компонентом анестезии был периферический блок, статистически значимо меньше (р < 0,05). Среднее значение (СО) дозы кетамина составил в группе общей анестезии – 383 (170 мг), в группе сочетанной анестезии – 300 (90) мг.
Интраоперационный расход анальгетиков статистически значимо не отличался в исследуемых группах (р > 0,05), количество введенного фентанила находилось в пределах от 300 до 1700 мкг со следующими средними значениями (СО) в группах: GA – 800 (300) мкг, cFICB – 900 (70) мкг, cFNB – 800 (150) мкг и sFNB – 700 (200) мкг. Данные по общему расходу анестетиков представлены на рисунке 1.
1000,
GA cFICB
I ■ Фентанил (мкг)
I ■ Пропофол (мг)
I ■ Кетамин (мг)
cFNB sFNB
Вид анестезии
Рис. 1. Расход анестетиков
Потребность в опиоидных анальгетиках
В послеоперационном периоде потребность в тримепередине статистически значимо не отличалась в исследуемых группах (р = 0,104), однако клиническое значение имеет четкая тенденция к снижению его расхода во 2-ой и 3-ей группах, где использовались продленные методики периферических блокад. Общая доза введенного за операционные сутки тримепередина варьировала в
пределах от 20 до 100 мг; среднее значение (СО) в группах сравнения составила: GA – 75 (23) мг, cFICB – 60 (26) мг, cFNB – 57 (29) мг и sFNB – 73 (20) мг. Следует отметить, что на фоне продленной периферической блокады 2 из 17 (12%) пациентам в группе cFICB и 1 из 19 (5%) в группе cFNB обезболивание опиоидными анальгетиками не потребовалось (р > 0,05).
Увеличив чувствительность критерия посредством преобразования данных (группа GA+sFNB – 31 человек и группа cFICB+cFNB – 32 пациента), можно подтвердить статистическую значимость различий в изучаемых исходах. Так потребность в тримепередине среди пациентов, у которых компонентом анестезии был продленный периферический блок, была ниже по сравнению с больными, прооперированными в условиях наркоза или сочетанной анестезии с однократной блокадой бедренного нерва. Среднее значение (СО) в группе GA+sFNB составило 74 (21) мг, а в группе cFICB+cFNB – 58 (27) мг (р < 0,05). Данные по потребности в опиоидных анальгетиках представлены на рисунке 2.
1000 _
“ 800 .

GA cFICB cFNB sFNB
Вид анестезии
Рис. 2. Потребность в опиоидных анальгетиках
Анализ осложнений
Критических осложнений в популяции выбранных пациентов отмечено не было. Однако обращают на себя внимание гемодинамические сдвиги, зарегистрированные у части больных во время операции и в ближайшем послеоперационном периоде. Примечательно, что гипертензия во время операции была зарегистрирована только в группе общей анестезии (у 5 из 12 больных; 42%), в то время как гипотония только в группе сочетанной анестезии (у 5 из 54 пациентов; 9%). Вероятно, что гипотензия во время сочетанной анестезии была связана с избыточным введением анестетиков на фоне эффективного периферического блока и обусловлена умеренной вазоплегией и кардиодепрессией. Во всех случаях, в/в введение небольших доз вазопрессоров (фенилэфрина 100–500 мкг или эфедрина от 10 до 30 мг) позволило быстро купировать нежелательные явления.
В послеоперационном периоде гипертензия наблюдалась у 2 из 12 пациентов в группе общей анестезии (17%) и 3 из 19 больных в группе, где была выполнена однократная блокада бедренного нерва (16%), в то время как у пациентов с продленной методикой периферической блокады ни одного случая гипертензии зарегистрировано не было. Полученные в ходе анализа данные можно интерпретировать как преимущество продленного метода послеоперационного обезболивания над методикой однократной блокады, которая, вероятно мало чем отличается от общей анестезии в отношении контроля над болью после операции.
Заключение
Таким образом, результаты ретроспективного анализа свидетельствуют о том, что периферическая блокада является эффективным и безопасным компонентом анестезиологической защиты при эндопротезировании коленного сустава. Сочетанная анестезия, обеспечивая многоуровневую блокаду ноцицептивной импульсации, позволяет сократить расход анестетиков во время операции и снизить риск гемодинамических осложнений.
В послеоперационном периоде более предпочтительными являются продленные методики периферической блокады, которые обеспечивают адекватное обезболивание и снижают потребность в опиоидных анальгетиках, уменьшая потенциальный риск побочных эффектов от их применения.
Список литературы Периферическая блокада как компонент анестезии и послеоперационного обезболивания при эндопротезировании коленного сустава
- Alan J.R., Macfarlane M. et al. Does regional anesthesia improve outcome after total knee arthroplasty?//Clin. Orthop. Relat. Res. -2009. -Vol. 467. -P. 2379-2402. (8)
- Bonnet F., Marret E. Influence of anaesthetic and analgesic techniques on outcome after surgery//Brit. J. Anaesth. -2005. -Vol. 95(1). -P. 52-58. (7)
- Bouaziz H., Bohdàr A., Jochum D. et al. Regional anaesthesia practice for total knee arthroplasty: French national survey/Pain and Regional Anaesthesia Committee of the French Anaesthesia and Intensive Care Societe (Sfar)//Ann. Fr. Anesth. Reanim. -2010. -Jun. -Vol. 29(6). -P. 440-451. (2)
- Choi P., Bhandari M., Scott J. et al. Epidural analgesia for pain relief following hip or knee replacement//Cochrane Database Syst.Rev. -2003. -Vol. 3. CD 003071. (6)
- Fowler S.J. Epidural analgesia compared with peripheral nerve blockade after major knee surgery: a systematic review and meta-analysis of randomized trials//Brit. J. Anaesth. -2008. -Vol. 100(2). -P. 154-164. (9)
- Fuser R., Cuvillon P., Delcourt J. et al. Peripheral nerve block in orthopaedic surgery: multicenter evaluation of practicing professionals and impact on the activity of the recovery room//Ann. Fr. Anesth. Reanim. -2007. -Sep. -Vol. 26(9). -P. 761-768. (1)
- O’Hara D., Duff A., Berlin J. et al. The effect of anestehetic technique on postoperative outcomes in hip fracture repair//Anesthesiology. -2000. -Vol. 92(4). -Apr. -P. 947-957. (3)
- Poldermans D., Bax J.J., Boersma E. et al. Guidelines for pre-operative cardiac risk assessment and perioperative cardiac management in non-cardiac surgery: The Task Force for Preoperative Cardiac Risk Assessment and Perioperative Cardiac Management in Non-cardiac Surgery of the European Society of Cardiology (ESC) and endorsed by the European Society of Anaesthesiology (ESA)//Eur. J. Anaesth. -2010. -February. -Vol. 27. -Issue 2. -P. 92-137. (5)
- Waddell J., Jonson K., Hein W. et al. Orthopedic practice in total hip arthroplasty and total knee arthroplasty: results from the global orthopedic registry (GLORY)//Am. J. Orthop. -2010. -Vol. 39. -9 Suppl. -P. 5-13. (4)


