Периферическая эмболия и микроциркуляция при реваскуляризации поверхностной бедренной артерии нативными баллонами и баллонами с лекарственным покрытием на периоде наблюдения один год
Автор: Гостев А. А., Осипова О. С., Клинкова A. С., Каменская О. В., Карпенко А. А.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 4 т.38, 2023 года.
Бесплатный доступ
Обоснование. Эмболический эффект лекарственного покрытия баллонов был продемонстрирован только в доклинических исследованиях.Цель: выявить интраоперационную дистальную эмболию при использовании лекарственных баллонов при реваскуляризации поверхностной бедренной артерии; оценить влияние лекарственной эмболии на микроциркуляцию нижних конечностей в течение 12 мес. после лечения.Материал и методы. Проспективное рандомизированное пилотное одноцентровое исследование. Были включены 20 пациентов с атеросклеротическим поражением поверхностной бедренной артерии выше щели коленного сустава с хронической ишемией нижних конечностей категории 3-6 по Rutherford. 1-й группе пациентов выполнялась чрескожная транслюминальная ангиопластика с использованием баллона с лекарственным покрытием (БСЛП), 2-й группе - с использованием баллона без лекарственного покрытия (ББЛП).Результаты. При интраоперационной детекции эмболов дистальная микроэмболия зарегистрирована у 10 пациентов (100%) в группе БСЛП (медиана количества эмболов = 200) и у 8 пациентов (80%) в группе ББЛП (медиана количества эмболов = 135), р = 0,47. Первичная проходимость в группе БСЛП составила 100%, в группе ББЛП 60% (рлог-ранг = 0,02).Через 12 мес. увеличение ТсрО2 на голени в группе БСЛП составило 12,2% (р = 0,42), в группе ББЛП 37,1% (р = 0,001).При этом по результатам ТсрО2 на голени в группе БСЛП отмечается сначала снижение показателей по сравнениюс дооперационным уровнем на 6% (р = 0,64) с последующим увеличением на 12,2% через 12 мес. (р = 0,22). В группе БСЛП сумма баллов по опроснику SF-36 увеличилась на 22,7% (р = 0,017), а в группе ББЛП на 25,3% по сравнению с исходными показателями (р = 0,04).Заключение. При использовании БСЛП отмечается тенденция к большей частоте интраоперационной дистальной эмболии и количеству эмболов по сравнению с ББЛП. По результатам исследования микроциркуляции можно предположить наличие дистальной эмболии лекарственным покрытием в группе БСЛП.
Атеросклероз артерий нижних конечностей, эндоваскулярное лечение, чрескожная транслюминальная ангиопластика, баллоны с лекарственным покрытием, микроэмболия, микроциркуляция
Короткий адрес: https://sciup.org/149144429
IDR: 149144429 | УДК: 616.137.83-004.6-089.844-06-005.7 | DOI: 10.29001/2073-8552-2023-38-4-202-212
Peripheral embolism and microcirculation during revascularization of the superficial femoral artery with native and drug-coated balloons over a one-year follow-up period
Relevance. The embolic effect of drug-coated balloons has only been demonstrated in preclinical studies.Aim: To identify intraoperative distal embolism when using drug-coated balloons during revascularization of the superficial femoral artery. To evaluate the effect of drug embolism on microcirculation of the lower extremities within 12 months after treatment.Material and Methods. Prospective, randomized, single-center pilot study. Twenty patients with symptomatic atherosclerotic femoro-popliteal above the knee lesions were included in the study. The first group underwent percutaneous transluminal angioplasty (PTA) using a drug-coated balloon (DCB), the second group - using a non-drug-coated conventional balloon (CB).Results. During intraoperative detection of emboli, distal microembolism was recorded in 10 patients (100%) in the DCB group (median number of emboli = 200) and in 8 patients (80%) in the CB group (median number of emboli = 135), p = 0.47. Primary patency in the DCB group was 100%, in the CB group 60% (p log-rank = 0.02). In the shin there was increase in TcPO2 by 12.2% in the DCB group (p = 0.42), and by 37.1% in the CB group (p = 0.001). At the same time, according to the results of TcPO2 on the shin in the DCB group, there was first a slight decrease in indicators compared to the preoperative level by 6% (p = 0.64), followed by an increase of 12.2% after 12 months of observation (p = 0.22). In the DCB group, the sum of SF-36 questionnaire points increased by 22.7% (p = 0.017), and by 25.3% in the CB group, compared to baseline values respectively (p = 0.04).Conclusion. When using DCB, there is a tendency towards a higher incidence of intraoperative distal embolism and the number of emboli compared with CB. The results of microcirculation studies suggest the presence of distal drug-coated embolism in DCB group.
Текст научной статьи Периферическая эмболия и микроциркуляция при реваскуляризации поверхностной бедренной артерии нативными баллонами и баллонами с лекарственным покрытием на периоде наблюдения один год
Гостев А.А., Осипова О.С., Клинкова А.С., Каменская О.В., Карпенко А.А.. Периферическая эмболия и микроциркуляция при реваскуляризации поверхностной бедренной артерии нативными баллонами и баллонами с лекарственным покрытием на периоде наблюдения один год. Сибирский журнал клинической и экспериментальной медицины. 2023;38(4):202–212.
Gostev A.A., Osipova O.S., Klinkova A.S., Kamenskaya O.V., Karpenko A.A. Peripheral embolism and microcirculation during revascularization of the superficial femoral artery with native and drug-coated balloons over a one-year follow-up period. The Siberian Journal of Clinical and Experimental Medicine. 2023;38(4):202–212.
В актуальных Российских и Европейских рекомендациях по лечению заболеваний периферических артерий в настоящее время предлагают первичную эндоваскулярную стратегию лечения для всех поражений короче 25 см [1]. Однако отдаленные результаты реваскуляризации остаются неудовлетворительными в связи с большим количеством рестенозов и реокклюзий артерий. Баллонная ангиопластика артерий баллонами с лекарственным покрытием (БСЛП) паклитакселем при коротких поражениях позволяет снизить частоту рестеноза таргетного поражения [2].
Однако проведенный метаанализ рандомизированных исследований для изучения долгосрочного риска обширной ампутации с использованием баллонов, покрытых паклитакселом, при заболевании периферических артерий (3 760 человек) показал, что существует повышенный риск обширной ампутации (HR 1,66 (95% ДИ 1,14–2,42; p = 0,008, одностадийная стратифицированная модель Кокса) [3]. Это может быть связано с дистальной эмболией элементами лекарственного покрытия, что приводит к ухудшению микроциркуляторного кровотока в нижней конечности. Феномен дистальной эмболизации изучен мало. Учитывая рост частоты использования этих устройств для реканализации периферических артерий нижних конечностей, необходимо проведение дополнительных рандомизированных проспективных исследований.
Цель исследования: выявить интраоперационную дистальную эмболию при использовании баллонов, покрытых цитостатиком, при реваскуляризации поверхностной бедренной артерии; оценить влияние лекарственной эмболии на микроциркуляцию нижних конечностей в течение 12 мес. после лечения.
Материал и методы
Дизайн исследования
Проспективное, рандомизированное, одноцентровое пилотное исследование было проведено в 2022 г. на базе ФГБУ «НМИЦ им. акад. Е.Н. Мешалкина» Минздрава России. После отбора пациентов по критериям включения / невключения выполнялась рандомизация методом конвертов. Это исследование было проведено в соответствии с принципами Хельсинкской декларации и рекомендациями по надлежащей клинической практике. Исследование одобрено локальным этическим комитетом.
Отбор пациентов
Критерии включения: возраст более 18 лет; симптом-ная хроническая ишемия нижних конечностей категории 3–6 по Rutherford; атеросклеротическое поражение артерий бедренно-подколенного сегмента выше щели коленного сустава, подтвержденное с помощью компьютерной томографии или артериографии; проходимая третья порция подколенной артерии и хотя бы одна артерия голени; поражение артерий бедренно-подколенного сегмента de novo ; наличие информированного согласия пациента.
Критерии невключения: возраст пациента менее 18 лет; опека или попечительство пациента; потенциальная беременность у женщин; асимптомное поражение; острая ишемия нижних конечностей или острый тромбоз; ранее проведенное лечение на пораженном сегменте; поражение, не связанное с атеросклерозом; нарушение гемостаза; тяжелая сопутствующая патология с ожида- емой продолжительностью жизни менее 2 лет; наличие противопоказаний к антитромбоцитарной терапии (двойная антитромбоцитарная терапия необходима в течение не менее 2 мес. после вмешательства); участие пациента в другом клиническом исследовании; сопутствующая патология или другие факторы, которые могут помешать проведению исследования, по мнению исследователя; наличие аневризмы рядом с пораженной артерией; невозможность наблюдения за пациентом; отказ пациента от участия в исследовании.
Обследования
До оперативного вмешательства выполнялось исследование транскутанной оксиметрии (ТсрО2) на тыле стопы и голени. ТсрО2 – неинвазивный метод оценки напряжения кислорода непосредственно в тканях нижних конечностей. Исследование отражает состояние микроциркуляции, реальное снабжение кислородом клеток кожи, что позволяет оценить степень ишемии и жизнеспособность тканей. Исследование выполнялось на транскутанном шестиканальном оксиметре ТСМ400 (Radiometer, Дания).
Также больным была проведена лазерная допплеровская флоуметрия (ЛДФ) на пораженной нижней конечности с использованием лазерно-допплеровского флоуметра фирмы «Transonic Systems Inc» (США) и поверхностных датчиков. Параметр микроциркуляторного кровотока (МЦК) характеризует поток эритроцитов в единицу времени через единицу объема ткани, измеряемый в перфузионных единицах (перф. ед.). Функциональное состояние МЦК оценивалось при проведении активной ортостатической пробы (ОП) (переход из положения лежа в положение стоя). ОП позволяет оценить веноартериолярную реакцию в микроциркуляторное русло, которая осуществляется за счет гемодинамического механизма, обусловленного собственной чувствительностью прекапиллярных сфинктеров. После проведенных обследований осуществлялось оперативное лечение.
Во время оперативного вмешательства выполнялась детекция эмболии в дистальное сосудистое русло нижней конечности с помощью допплерографии в непрерывном режиме. В ходе исследования использовался аппарат «Ангиодин-Универсал» с датчиком 2/2,66 (2,3) МГц. Мониторинг завершался после окончания операции. Во время мониторинга устройство настраивалось на подавление возможных помех (псевдоэмболии) и дифференциацию эмболов на 2 типа: газообразные и твердые.
После оперативного вмешательства на 2-е сут на госпитальном этапе выполнялись повторные измерения ТсрО2 и ЛДФ на оперированной нижней конечности и ультразвуковое дуплексное сканирование артерий нижней конечности (линейным датчиком на аппарате «General Electric Voluson e10»). После выписки пациенты проходили контрольный осмотр через 6 и 12 мес. после операции. На осмотре выполнялись ультразвуковое дуплексное сканирование артерий оперированной нижней конечности, измерение ТсрО2, ЛДФ и контрольный осмотр сосудистого хирурга.
Техника реваскуляризации
Чрескожная транслюминальная ангиопластика артерий нижних конечностей проводилась под местной анестезией. Осуществлялся стандартный эндоваскулярный доступ и визуализировался пораженный артериальный сегмент с последующей баллонной ангиопластикой. После контрольной ангиографии при наличии остаточ- ных стенозов или гемодинамически значимых диссекций интимы устанавливался стент на всем протяжении поражения. В группе БСЛП ангиопластика проводилась баллоном Lutonix™ (C. R. BARD, INC., США) с покрытием паклитакселом. В группе с использованием баллона без лекарственного покрытия (ББЛП) ангиопластика проводилась баллоном Armada™ (C. R. BARD, INC., США).
Медикаментозная терапия
Медикаментозная терапия включала назначение кло-пидогреля перед процедурой (300 мг однократно), ацетилсалициловой кислоты 75 мг/сут, начиная минимум за день, и введение гепарина во время процедуры (100 Ед/ кг веса тела внутривенно). После процедуры всем больным назначался аспирин (75 мг/сут) длительно и клопи-догрель (75 мг/сут) на 3 мес.
Определения
Технический успех был определен как остаточный стеноз менее 30%. Первичная проходимость определялась как отсутствие окклюзии или стеноза, ограничивающего кровоток (увеличение линейной скорости кровотока > 2,5, по данным дуплексной ультрасонографии, или уменьшение диаметра сосуда не менее чем на 50%, по данным цифровой субтракционной ангиографии или компьютерной томографической ангиографии целевого сегмента, включая 1 см проксимальнее и дистальнее). Вторичная проходимость определялась как отсутствие окклюзии или ограничивающего кровоток стеноза после хотя бы одного повторного вмешательства для восстановления проходимости вместе со всеми случаями первичной проходимости. Свобода от повторных операций была определена как отсутствие повторных процедур в области целевого поражения.
Частота первичного устойчивого клинического улучшения определялась как сдвиг вверх по классификации Рутерфорда на один уровень без необходимости повторной реваскуляризации у пациентов и без необходимости незапланированной ампутации. Вторичное устойчивое клиническое улучшение определялось как сдвиг вверх по классификации Рутерфорда на один уровень без необходимости незапланированной ампутации после повторной реваскуляризации.
Статистический анализ данных
Для накопления данных и их первичной сортировки использовали пакет Microsoft Excel 2010. Результаты исследований были обработаны с использованием пакета программ для статистической обработки STATISTICA 10 в среде Windows 7 (StatSoft Inc., США). Для проверки нормальности распределения количественных данных применяли W критерий Шапиро – Уилка. Нормально распределенные количественные данные представляли средним значением и стандартным отклонением, M ± SD , при отсутствии нормального распределения – медианой и интерквартильным промежутком, Me [ Q 1; Q 3]; категориальные признаки абсолютными (n) и относительными (в %) частотами встречаемости.
Статистическую значимость различий количественных показателей между двумя группами определяли с помощью U -критерия Манна – Уитни, а категориальных признаков – с помощью точного двустороннего критерия Фишера. Внутригрупповой анализ динамики количественных показателей на 4 этапах наблюдения проводили по критерию Фридмана. Парные сравнения количественных показателей на этапах выполняли по критерию Вилкоксо-на, а категориальных признаков – по критерию Мак-Не-мара. Для анализа динамики неблагоприятных исходов строили кривые Каплана Мейера и проводили их сравнение по лог-ранговому критерию. Пороговый уровень значимости при проверке гипотез составлял р = 0,05.
Результаты
Характеристика пациентов
Исходные характеристики пациентов представлены в таблице 1. Статистически значимых различий между двумя группами не наблюдалось.
Таблица 1. Исходные характеристики пациентов в группах Table 1. Patient’s baseline characteristics
|
Характеристики Characteristic |
Группа баллонов с лекарственным покрытием, n = 10 Drug coated balloons group, n = 10 |
Группа баллонов без лекарственного покрытия, n = 10 Conventional balloons group, n = 10 |
р |
|
Возраст, лет Age, years |
64,5 [63,0; 70,0] |
63,5 [57,0; 68,0] |
0,19 |
|
Пол, мужской, n (%) Sex, male, n (%) |
8 (80) |
9 (90) |
1,00 |
|
Тип поражения целевой артерии: Target lesion type: Гемодинамически значимый стеноз, n (%) Hemodynamically significant stenosis, n (%) Окклюзия, n (%) Occlusion, n (%) |
4 (40) 6 (60) |
4 (40) 6 (60) |
1,00 1,00 |
|
Степень ХИНК по Покровскому, n (%) Chronic limb ischemia stage by Pokrovsky 2Б, n (%)
|
7 (70) 2 (20) 1 (10) |
6 (60) 3 (30) 1 (10) |
0,67 1,00 1,00 |
|
Артериальная гипертензия, n (%) Arterial hypertension, n (%) |
10 (100) |
10 (100) |
1,00 |
|
Дислипидемия, n (%) Dyslipidemia, n (%) |
1 (10) |
4 (40) |
0,30 |
|
ХСН, n (%) Chronic heart failure, n (%) |
9 (90) |
10 (100) |
1,00 |
Окончание табл. 1
End of table 1
|
Характеристики Characteristic |
Группа баллонов с лекарственным покрытием, n = 10 Drug coated balloons group, n = 10 |
Группа баллонов без лекарственного покрытия, n = 10 Conventional balloons group, n = 10 |
р |
|
ИБС, n (%) Ischemic heart disease, n (%) |
9 (90) |
8 (80) |
1,00 |
|
Курение, n (%) Smoking, n (%) |
6 (60) |
6 (60) |
1,00 |
|
Сахарный диабет, n (%) Diabetes mellitus, n (%) |
1 (10) |
4 (40) |
0,30 |
|
АКШ в анамнезе, n (%) Coronary arteries bypass grafting in anamnesis, n (%) |
2 (20) |
2 (20) |
1,00 |
|
ЧТКА в анамнезе, n (%) Percutaneous transluminal coronary angioplasty in anamnesis, n (%) |
6 (60) |
4 (40) |
0,66 |
|
Вмешательство на контрлатеральной нижней конечности в анамнезе, n (%) Contralateral lesion revascularization in anamnesis, n (%) |
5 (50) |
3 (30) |
0,65 |
|
SF-36 физическое благополучие, баллы SF-36 physical component, points |
37,56 [33,10; 39,69] |
31,94 [27,12; 41,19] |
0,52 |
|
SF-36 психическое благополучие, баллы SF-36 psychical component, points |
38,36 [36,31; 54,77] |
37,80 [33,31; 57,93] |
0,77 |
|
SF-36 сумма баллов SF-36, common points |
78,07 [74,69; 87,67] |
72,98 [65,19; 86,65] |
0,27 |
Примечание: ХИНК – хроническая ишемия нижних конечностей, ХСН – хроническая сердечная недостаточность, ИБС – ишемическая болезнь сердца, АКШ – аортокоронарное шунтирование, ЧТКА – чрескожная транслюминальная коронарная ангиопластика.
Note: CLLI – chronic lower limb ischemia, CHF – chronic heart failure, IHD – ischemic heart disease, CABG – coronary arteries bypass grafting, PTCA – percutaneous transluminal coronary angioplasty.
Процедурные и ранние результаты
Интраоперационные характеристики исследуемой популяции представлены в таблице 2. Группы статистически значимо не различались по длине и диаметру используемых баллонов, а также по длине и диаметру установленных стентов в тех случаях, где это было необходимо.
Технический успех вмешательства был достигнут у всех пациентов в обеих группах. Интраоперационная детекция эмболов выявила факт дистальной эмболии у 10 пациентов (100%) в группе БСЛП (медиана количества эмболов = 200) и у 8 пациентов (80%) в группе ББЛП (медиана количества эмболов = 135) без статистических различий (р = 0,47). Для более подробного изучения про- цесса дистальной эмболизации оценивалось количество эмболов на следующих 4 основных этапах оперативного вмешательства: прохождение целевого поражения артерии проводником, предилатация целевого поражения с помощью баллона, имплантация стента, постдилатация стентированного сегмента. Следует отметить, что основная эмболизация происходила во время прохождения целевого артериального поражения с помощью проводника. На втором месте по частоте случаев эмболии оказалась предилатация целевого поражения с помощью баллона. При этом на всех этапах вмешательства не было выявлено статистически значимых отличий между группами (см. табл. 2).
Таблица 2. Интраоперационные характеристики пациентов в группах
Table 2. Intraoperative patient’s characteristics
|
Характеристики Characteristic |
Группа баллонов с лекарственным покрытием, n = 10 Drug coated balloons group, n = 10 |
Группа баллонов без лекарственного покрытия, n = 10 Conventional balloons group, n = 10 |
р |
|
Вид вмешательства Intervention type: ЧТА, n (%) Percutaneous transluminal angioplasty, n (%) ЧТА со стентированием Percutaneous transluminal angioplasty with stenting, n (%) |
2 (20) 8 (80) |
3 (30) 7 (70) |
1,00 |
|
Длина баллона, мм Balloon length, mm |
150,0 [150,0; 150,0] |
150,0 [120,0; 150,0] |
0,27 |
|
Диаметр баллона, мм Balloon diameter, mm |
5,5 [5,0; 6,0] |
5,0 [5,0; 6,0] |
0,88 |
|
Длина имплантированных стентов, мм Implanted stents length, mm |
144,5 [90,0; 165,0] |
120,0 [120,0; 150,0] |
0,86 |
|
Диаметр имплантированных стентов, мм Implanted stents diameter, mm |
6,00 [5,75; 7,00] |
6,00 [5,5; 6,5] |
0,68 |
Окончание табл. 2
End of table 2
|
Характеристики Characteristic |
Группа баллонов с лекарственным покрытием, n = 10 Drug coated balloons group, n = 10 |
Группа баллонов без лекарственного покрытия, n = 10 Conventional balloons group, n = 10 |
р |
|
Степень остаточного стеноза, % Residual stenosis range, % |
10,0 [5,0; 15,0] |
10,0 [10,0; 15,0] |
0,54 |
|
Интраоперационная эмболия в дистальное русло, n (%) Intraoperative distal emboli, n (%) |
10 (100) |
8 (80) |
0,47 |
|
Эмболия во время прохождения, n (%) поражения целевой артерии, n (%) Emboli via target lesion recanalization , n (%) |
9 (90) |
8 (80) |
1,00 |
|
Эмболия во время предилатации целевого поражения, n (%) Emboli via target lesion predilatation, n (%) |
6 (60) |
7 (70) |
0,67 |
|
Эмболия во время имплантации стента, n (%) Emboli via stent implantation, n (%) |
3 (30) |
5 (50) |
0,65 |
|
Эмболия во время постдилатации стентированного сегмента целевым баллоном, n (%) Emboli via implanted stent postdilatation, n (%) |
4 (40) |
6 (60) |
0,65 |
|
Количество материальных эмболов Number of material emboli |
200,0 [100,0; 200,0] |
135,0 [15,0; 320,0] |
0,70 |
|
Технический успех оперативного вмешательства, n (%) Technical success of intervention, n (%) |
10 (100) |
10 (100) |
1,00 |
Примечание: ЧТА – чреcкожная транслюминальная ангиопластика.
Note: PTA – percutaneous transluminal angioplasty.
В госпитальном периоде не было зафиксировано случаев тромбоза, значимых сердечно-сосудистых событий (инфаркт миокарда, острое нарушение мозгового кровообращения (ОНМК)), летальных исходов, а также каких-либо осложнений, связанных с эндоваскулярным доступом (гематомы, инфекция, нейропатия).
Среднесрочные результаты
Первичная проходимость в группе БСЛП составила 100%, в группе ББЛП 60% ( р лог-ранг = 0,02). В группе ББЛП было 3 случая рестеноза и 1 случай окклюзии. Через 12 мес. наблюдения показатели свободы от повторных операций на оперированном сегменте и вторичной проходимости были сопоставимы в обеих группах (табл. 3, рис. 1, 2).
Результаты сравнительного анализа ЛДФ, TcpO2 нижних конечностей до, после оперативного вмешательства в раннем послеоперационном периоде и через 6 и 12 мес. наблюдения представлены в таблице 4.
Оценка исследования МЦК нижних конечностей показала статистически значимое увеличение перфузионных единиц по результатам ЛДФ нижних конечностей на 428% в группе БСЛП ( р = 0,01) и на 117% в группе ББЛП ( р = 0,05) на 6-месячном периоде наблюдения с последующим снижением на 50% (378% от первоначального уровня) в группе БСЛП ( р = 0,02) и со снижением на 60% (до 57% от первоначального уровня) в группе ББЛП( р = 0,06)) на периоде наблюдения 12 мес. (рис. 3).
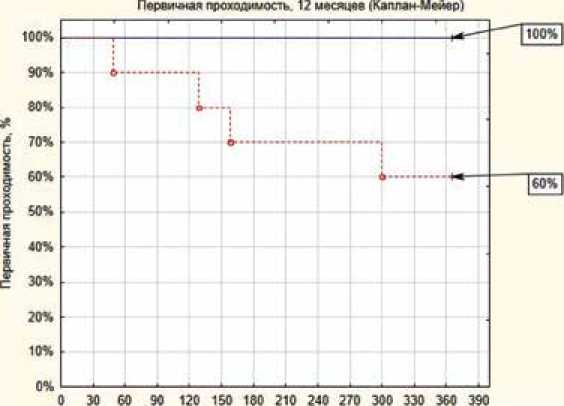
Рис. 1. Первичная проходимость в исследуемых группах на периоде наблюдения 12 месяцев Fig. 1. Primary patency at 12-months follow-up period
Время дни р(кй)«пк>*0.02
— Группа БСЛЛ • - ■ • Грута ББЛП
Свобода от повторил операций на оларирсеажсы сегмента (Каллаи-Мвйас1>
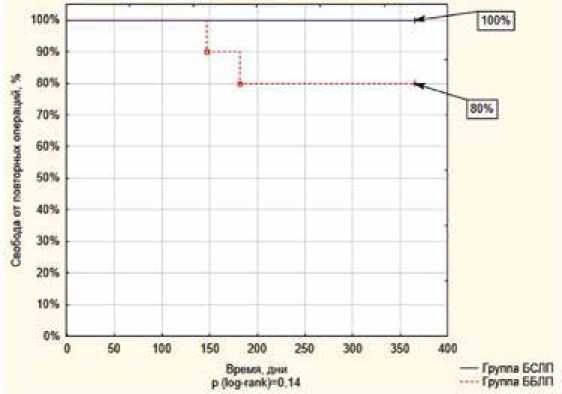
Рис. 2. Свобода от повторных операций на оперированном сегменте в исследуемых группах на периоде наблюдения 12 месяцев
Fig. 2. Freedom from target lesion revascularization at 12-months follow-up period
Таблица 3. Показатели проходимости и клинического статуса в исследуемых группах на 12-месячном периоде наблюдения Table 3. Patency and patients clinical characteristics at 12-months follow-up
|
Характеристики Characteristics |
Группа баллонов с лекарственным покрытием, n = 10 Drug coated balloons group, n = 10 |
Группа баллонов без лекарственного покрытия, n = 10 Conventional balloons group, n = 10 |
р |
|
Первичная проходимость, n (%) Primary patency, n (%) |
10 (100) |
6 (60) |
0,04 |
|
Свобода от повторных операций на оперированном сегменте, n (%) Freedom from target lesions revascularization, n (%) |
10 (100) |
8 (80) |
0,11 |
|
Вторичная проходимость, n (%) Secondary patency, n (%) |
10 (100) |
8 (80) |
0,11 |
|
Инфаркт миокарда, n (%) Myocardial infarction, n (%) |
1 (10) |
0 (0) |
1,00 |
|
ОНМК, n (%) Stroke, n (%) |
0 (0) |
0 (0) |
1,00 |
|
Летальные исходы, n (%) Deaths, n (%) |
0 (0) |
0 (0) |
1,00 |
|
Первичное устойчивое клиническое улучшение, n (%) Primary sustained clinical improvement, n (%) |
8 (80) |
6 (60) |
0,31 |
|
Вторичное устойчивое клиническое улучшение, n (%) Secondary sustained clinical improvement, n (%) |
8 (80) |
8 (80) |
1,00 |
|
SF-36 физическое благополучие, баллы SF-36 physical component, points |
46,00 [35,90; 60,00] |
45,50 [36,70; 55,00] |
0,94 |
|
SF-36 психическое благополучие, баллы SF-36 psychical component, points |
56,70 [45,10; 63,50] |
55,50 [40,00; 58,00] |
0,35 |
|
SF-36 суммарная оценка качества жизни, сумма баллов SF-36, common points |
95,80 [82,60; 102,70] |
91,45 [81,00; 110,00] |
0,94 |
Примечание: ОНМК – острое нарушение мозгового кровообращения.
Note: ACA – acute cerebrovascular accident.
Таблица 4. Результаты исследования периферической микроциркуляции
Table 4. Results of peripheral microcirculation investigation
|
Характеристики Characteristic |
Группа баллонов с лекарственным покрытием, n = 10 Drug coated balloons group, n = 10 |
р |
Группа баллонов без лекарственного покрытия, n = 10 Conventional balloons group n = 10 |
р |
||||||
|
Исходный уровень |
1 нед. |
6 мес. |
12 мес. |
Исходный уровень |
1 нед. |
6 мес. |
12 мес. |
|||
|
ЛДФ нижних конечностей, мл/ мин/100 г = перф. ед Laser Doppler Flow-metry, ml/min/100 g = perfusion units |
1,60 [1,02; 5,30] |
7,15 [2,7; 9,9] |
8,45 [3,00; 9,10] |
6,05 [4,00; 7,20] |
0,37 |
4,35 [1,30; 7,00] |
6,35 [4,60; 9,70] |
9,45 [1,90; 9,60] |
6,85 [5,00; 12,50] |
0,06 |
Окончание табл. 4
End of table 4
|
Характеристики Characteristic |
Группа баллонов с лекарственным покрытием, n = 10 Drug coated balloons group, n = 10 |
р |
Группа баллонов без лекарственного покрытия, n = 10 Conventional balloons group n = 10 |
р |
||||||
|
Исходный уровень |
1 нед. |
6 мес. |
12 мес. |
Исходный уровень |
1 нед. |
6 мес. |
12 мес. |
|||
|
TcPO2 тыл стопы, мм рт. ст. TcPO2 foot dorsum, mm Hg |
48,5 [28,0; 62,0] |
58,5 [43,0; 63,0] |
55,0 [45,0; 74,0] |
60,0 [46,0; 65,0] |
0,01 |
49,0 [44,0; 55,0] |
50,5 [40,0; 68,0] |
52,5 [40,0; 70,0] |
55,0 [42,0; 70,0] |
0,38 |
|
TcPO2 голень, мм рт. ст. TcPO2 shin, mm Hg |
45,0 [34,0; 68,0] |
42,5 [36,0; 59,0] |
57,5 [35,0; 76,0] |
50,5 [41,0; 59,0] |
0,42 |
40,5 [35,0; 59,0] |
60,0 [44,0; 61,0] |
59,0 [45,0; 64,0] |
55,5 [36,0; 60,0] |
0,001 |
Примечание: ЛДФ – лазерная допплеровская флоуметрия, TcPO2 – транскутанное напряжение кислорода.
Note: LDF – laser doppler flowmetry, TcPO2 – transcutaneous oxygen tension.
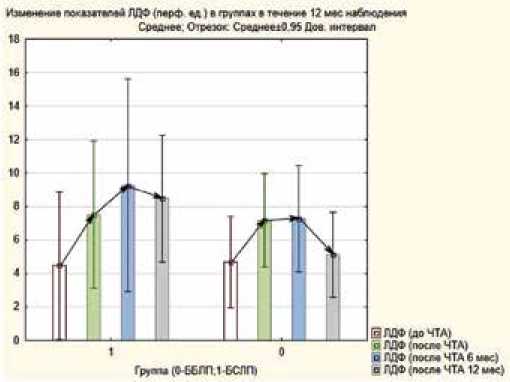
Рис. 3. Изменение показателей лазерной допплеровской флоу-метрии (перф. ед.) в группах в течение 12 месяцев наблюдения Fig. 3. Laser doppler flowmetry perfusion units changing via 12 months
Ч ерез 12 мес. наблюдалось статистически значимое увеличение ТсрО2 на тыле стопы (рис. 4) на 23% мм рт. ст. в группе БСЛП, р = 0,01, и статистически незначимое увеличение на 12,2% мм рт. ст. в группе ББЛП, р = 0,38.
Через 12 мес. на голени увеличение ТсрО2 (рис. 5) в группе БСЛП составило 12,2% ( р = 0,42), в группе ББЛП 37,1% ( р = 0,001).
В группах не было зафиксировано летальных исходов и ОНМК. Однако в группе БСЛП был зарегистрирован один случай инфаркта миокарда. В группе БСЛП сумма баллов по опроснику SF-36 увеличилась на 22,7% ( р = 0,017), а в группе ББЛП на 25,3% по сравнению с исходными показателями ( р = 0,04). Не отмечалось статистически значимых различий первичного и вторичного устойчивого клинического улучшения между группами (см. табл. 3).
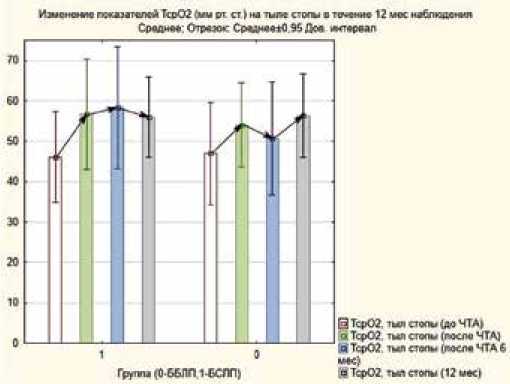
Рис. 4. Изменение показателей TcpO2 на тыле стопы (мм рт. ст.) в группах в течение 12 месяцев наблюдения
Fig. 4. TcpO2 units changing at foot dorsum via 12 months
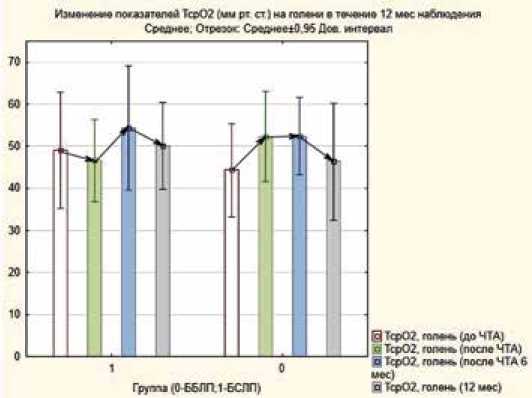
Рис. 5. Изменение показателей TcpO2 на голени
(мм рт. ст.) в группах в течение 12 месяцев наблюдения Fig. 5. TcpO2 units changing at shin via 12 months
Обсуждение
Феномен дистальной эмболизации при использования БСЛП мало изучен и описан в небольшом количестве доклинических исследований [4, 5]. Данные о количестве доставляемого лекарства к тканям-мишеням артериальной стенки, а также о количестве дистальных эмболов элементами лекарственного покрытия различны. Так, B. Kelsch и соавт. в своем доклиническом исследовании показывают, что примерно 25–35% паклитаксела было потеряно в периферический кровоток во время процедуры [6]. В других исследованиях было отмечено, что только 10% паклитакселя передается на обрабатываемую стенку при баллонной ангиопластике, а до 90% лекарства поступает в периферическое русло [7, 8]. Такая разнородная информация говорит об отсутствии достоверных данных о механизмах дистальной эмболизации лекарственного покрытия после запуска магистрального кровотока в артериях нижних конечностей.
Многофазная и нелинейная фармакокинетика паклитаксела приводит к длительному нахождению препарата в тканях с неизвестными долгосрочными биологическими эффектами на периферическое русло и окружающие ткани. Как заявляют исследователи, наиболее грозным осложнением использования БСЛП является увеличение риска отсроченной ампутации. В метаанализе 21 рандомизированного контролируемого исследования частота больших ампутаций в группе пациентов после реваскуляризации артерий нижних конечностей с БСЛП составила 4%, а в контрольной группе – 2,7%. Риск большой ампутации был значительно выше для баллонов, покрытых паклитакселем (ОР 1,66 (95% ДИ 1,14 и 2,42; p = 0,008) [9]. Интраоперационная дистальная эмболизация частицами носителя цитотоксического паклитаксела может быть фактором риска ампутации у пациентов после восстановления магистрального кровотока с использованием баллонных катетеров с лекарственным покрытием [4, 10]. Однако ни в одном исследовании не была доказана прямая причинно-следственная связь между эмболией частицами лекарственного покрытия и ампутацией.
Отсутствуют надежные клинические доказательства дистальной эмболизации лекарственным покрытием, так как это связано с трудностью в диагностике состояния микроциркуляторного русла [11]. Невозможно выявление микроэмболизации при контрольной ангиографии. Этот феномен можно диагностировать лишь по косвенным признакам, в том числе по нарушению периферической микроциркуляции, выявленному по результатам лазерной допплеровской флоуметрии, TcPO2, а также с помощью ультразвуковой микроэмболдетекции, которая не применяется рутинно.
В нашем исследовании мы использовали ультразвуковую эмболдетекцию для выявления случаев интраоперационной микроэмболии. Периферическая эмболизация была зарегистрирована у всех больных в группе БСЛП и у 80% пациентов в группе контроля. При этом абсолютное число микроэмболов было выше в группе БСЛП. Эти данные могут косвенно свидетельствовать о существовании дистальной эмболии частицами лекарственного покрытия периферического баллона. По результатам ТсрО2 на голени в группе БСЛП отмечается сначала незначительное снижение показателей на 6% по сравнению с дооперационным уровнем ( р = 0,64), а затем последующее увеличение на 12,2% через 12 мес. наблюдения (р = 0,22). В группе ББЛП данный феномен не наблюдается, а происходит значимое увеличение показателей на 48% сразу в раннем послеоперационном периоде по сравнению с дооперационным уровнем ( р = 0,001).
Последующие увеличение показателей к 12 мес., возможно, связано с растворением лекарственных эмболов или развитием коллатерального кровотока. Ухудшение периферической микроциркуляции в раннем послеоперационном периоде при использовании БСЛП не повлияло на первичную проходимость зоны реконструкции, что подтверждает локальное циторедуктивное действие паклитаксела.
В большинстве случаев эмболизация периферического русла в нашем исследовании оставалась бессимптомной. Отсутствовали местные проявления цитотоксичности паклитакселя: фибриноидный некроз, васкулит, панникулит, фокальный некроз скелетных мышц. Также мы проводили оценку клинического улучшения и качества жизни пациентов в динамике. В обеих группах произошло статистически значимое улучшение общего качества жизни, а также физического и психологического благополучия по результатам опросника SF-36. Частота первичного и вторичного устойчивого клинического улучшения не различалась между группами через 12 мес. наблюдения, несмотря на статистически значимо лучшую первичную проходимость в группе БСЛП.
Ограничения исследования
Данное исследование имеет ряд ограничений: оно являлось одноцентровым исследованием с малым объемом выборки. Также отсутствовала независимая оценки качества жизни больных. У многих пациентов кроме ангиопластики выполнялось стентирование таргетного поражения, что также могло оказать влияние на исход.
Заключение
При использовании БСЛП отмечается тенденция к большей частоте случаев интраоперационной дистальной эмболии и количеству эмболов по сравнению с ББЛП. На голени было выявлено изначальное снижение показателей в раннем послеоперационном периоде в группе БСЛП с последующим увеличением показателей в течение 12 мес. наблюдения в отличие от группы ББЛП, где уже в раннем послеоперационном периоде происходило значимое увеличение показателей ТсрО2 на голени.
Список литературы Периферическая эмболия и микроциркуляция при реваскуляризации поверхностной бедренной артерии нативными баллонами и баллонами с лекарственным покрытием на периоде наблюдения один год
- Aboyans V., Ricco J.B., Bartelink M.E.L., Björck M., Brodmann M., Cohnert T. et al. Editor’s Choice - 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the European Society for Vascular Surgery (ESVS). Eur. J. Vasc. Endovasc. Surg. 2018;55(3):305-368. https://doi.org/10.1016/j.ejvs.2017.07.018.
- Tepe G., Schnorr B., Albrecht T., Brechtel K., Claussen C.D., Scheller B. et al. Angioplasty of femoral-popliteal arteries with drug-coated balloons: 5-year follow-up of the THUNDER trial. JACC Cardiovasc. Interv. 2015;8(1 Pt. A):102-108. https://doi.org/10.1016/J.JCIN.2014.07.023.
- Katsanos K., Spiliopoulos S., Kitrou P., Krokidis M., Paraskevopoulos I., Karnabatidis D. Risk of death and amputation with use of paclitaxel-coated balloons in the infrapopliteal arteries for treatment of critical limb ischemia: A systematic review and meta-analysis of randomized controlled trials. J. Vasc. Intervent. Radiol. 2020;31(2):202-212. https://doi.org/10.1016/j.jvir.2019.11.015.
- Torii S., Jinnouchi H., Sakamoto A., Romero M.E., Kolodgie F.D., Virmani R., et al. Comparison of biologic effect and particulate embolization after femoral artery treatment with three drug-coated balloons in healthy swine model. J. Vasc. Interv. Radiol. 2019;30(1):103-109. https://doi.org/10.1016/J.JVIR.2018.07.025.
- Kolodgie F.D., Pacheco E., Yahagi K., Mori H., Ladich E., Virmani R. Comparison of particulate embolization after femoral artery treatment with IN.PACT Admiral versus Lutonix 035 Paclitaxel-coated balloons in healthy swine. J. Vasc. Interv. Radiol. 2016;27(11):1676-1685.e2. https://doi.org/10.1016/J.JVIR.2016.06.036.
- Kelsch B., Scheller B., Biedermann M., Clever Y.P., Schaffner S., Mahnkopf D. et al. Dose response to Paclitaxel-coated balloon catheters in the porcine coronary overstretch and stent implantation model. Invest. Radiol. 2011;46(4):255-263. https://doi.org/10.1097/RLI.0B013E31820577DF.
- Speck U., Cremers B., Kelsch B., Biedermann M., Clever Y.P., Schaffner S. et al. Do pharmacokinetics explain persistent restenosis inhibition by a single dose of paclitaxel? Circ. Cardiovasc. Interv. 2012;5(3):392-400. https://doi.org/10.1161/CIRCINTERVENTIONS.111.967794.
- Stolzenburg N., Breinl J., Bienek S., Jaguszewski M., Löchel M., Taupitz M. et al. Paclitaxel-coated balloons: Investigation of drug transfer in healthy and atherosclerotic arteries - first experimental results in rabbits at low inflation pressure. Cardiovasc. Drugs Ther. 2016;30(3):263- 270. https://doi.org/10.1007/S10557-016-6658-1.
- Katsanos K., Spiliopoulos S., Teichgräber U., Kitrou P., del Giudice C., Björkman P. et al. Editor’s choice - Risk of major amputation following application of paclitaxel coated balloons in the lower limb arteries: a systematic review and meta-analysis of randomised controlled trials. Eur. J. Vasc. Endovasc. Surg. 2022;63(1):60-71. https://doi.org/10.1016/j.ejvs.2021.05.027.
- Чебан А.В., Игнатенко П.В., Рабцун А.А., Саая Ш.Б., Гостев А.А., Бугуров С.В. и др. Современные подходы к реваскуляризации бедренно-подколенных поражений. Достижения и перспективы. Кардиоваскулярная терапия и профилактика. 2020;19(2):2274. https://doi.org/10.15829/1728-88002019-2274.
- Великанова Е.А., Матвеева В.Г., Сенокосова Е.А., Ханова М.Ю., Кривкина Е.О., Антонова Л.В. Анализ эффективности различных белковых покрытий для оптимизации эндотелизации полимерных матриксов. Сибирский журнал клинической и экспериментальной медицины. 2023;38(1):160-166. https://doi.org/10.29001/2073-8552-2023-38-1-160-166.


