Периоперационное ведение пациента с недостаточностью XII фактора (болезнь Хагемана)
Автор: Шулутко А.М., Крылов А.Ю., Просолов Н.В., Петровская А.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 4 (44), 2015 года.
Бесплатный доступ
В статье представлены данные пациентки, находившейся на стационарном лечении в ГКБ № 61 города Москвы с дефицитом фактора XII, которой было успешно выполнено оперативное лечение - лапароскопическая холецистэктомия.
Лапароскопичсекая холецистэктомия, система гемостаза, фактор xii, тромбоз
Короткий адрес: https://sciup.org/142211220
IDR: 142211220 | УДК: 617-089.844
Текст научной статьи Периоперационное ведение пациента с недостаточностью XII фактора (болезнь Хагемана)
Фактор XII (фактор Хагемана) – плазменный профермент, является одним из стимуляторов коагуляционного каскада, участвующий во внешнем пути гемостаза. Фактор XII активируется под действием калликреина и в присутствии отрицательно заряженного высокомолекулярного киногена, является естественным активатором как свертывающей, так и калликреин кининовой и фибринолитической систем. Структура молекулы фактора XII более схожа со строением молекулы плазминогена, что подтверждает более значимую роль фактора XII для процессов фибринолиза, а не коагуляционного ответа. Конверсия плазминогена в плазмин при активном факторе XII (XIIa) и ингибиция фибринолиза гораздо более важны для больного. У пациентов с дефицитом фактора XII отмечается значительное удлинение АЧТВ, однако геморрагические осложнения выявляются крайне редко. Поскольку в человеческом организме процессы коагуляции и фибринолиза находятся в постоянном равновесии, дефицит фактора XII потенциально увеличивает риск тромбоза. Риск венозных тромбозов при дефиците фактора XII возрастает приблизительно в 5 раз и развивается в среднем у 8% пациентов [1–3].
Встречаемость дефицита фактора XII не превышает 1 больного на 1000000 человек. У оперированного больного при этом, с одной стороны, возникают трудности мониторирования эффективности гепаринопрофилактики ВТЭО, с другой – повышается риск развития тромбозов в послеоперационном периоде, в связи с нарушенным фибринолизом [2].
Для оценки состояния гемостаза используют локальные и глобальные коагулогические тесты. Локальные тесты фиксируют изменения активности концентрации отдельных компонентов системы плазменного гемостаза, но при этом не могут охарактеризовать, насколько эти локальные изменения повлияли на общую способность плазмы больного к образованию сгустка. В их число входят ежедневно используемые тесты, такие как АЧТВ, ТВ, ФГ, ПВ, протромбиновый индекс, международное нормализованное отношение, D- димер, АТIII, ПС и другие. Основной же задачей глобальных тестов является оценка интегрального потенциала свертывающей системы крови пациента к образованию сгустка. К глобальным тестам относят тромбоэластографию как старейший из глобальных тестов гемостаза. Данный метод регистрирует изменение вязкоупругих свойств образца крови в процессе свертывания, графически отображая процесс полимеризации фибрина, а также последующий лизис сгустка. Главным достоинством ТЭГ является то, что сейчас это единственный доступный глобальный тест, рабо- тающий в цельной крови, кроме того тромбоэластография может использовать разнообразные активаторы свертывания и фибринолиза, позволяя изучать и диагностировать нарушения элементов системы свертывания. Еще одним глобальным тестом является тест генерации тромбина, который в большей степени относится к научным методам исследования системы гемостаза. Тромбин - главный фермент системы свертывания крови, который не только катализирует основную реакцию превращения фибриногена в фибрин, но и является ключевым регулятором системы, на которой замкнуты почти все петли обратных связей. Тест генерации тромбина определяет кинетику изменения концентрации тромбина в процессе свертывания крови. И, наконец, новый глобальный тест диагностики нарушений системы плазменного гемостаза - тест тромбодинамики. В отличие от остальных, применяемых в клинической практике методов оценки состояния плазменного гемостаза, в которых активация свертывания происходит одновременно во всем исследуемом объеме плазмы, в основу метода был положен принцип локального запуска свертывания на плоской поверхности с нанесенным на нее тромбопластином - активатором свертывания, содержащем ТФ и липиды, что имитирует повреждение стенки сосуда и начало формирования в этом месте тромба. Тест тромбодинамики позволяет оценить как качество функционирования отдельных блоков системы гемостаза, так и функционирование всей системы плазменного гемостаза в целом [4].
В данной статье представлен клинический опыт лечения больной с дефицитом фактора XII, перенесшей видеолапа-роскопическую холецистэктомию под эндотрахеальным наркозом. Для оценки системы гемостаза у представленной пациентки использовали ТЭГ и тест тромбодинамики.
Клинический пример
Больная П., 32 лет, рост 176 см, вес 100 кг, ИМТ 32,3, в течение 4-х лет страдала желчекаменной болезнью, которая периодически манифистировалась приступами болей в правом подреберье (желчная колика), тошнотой, вздутием живота, которые быстро купировались приемом спазмали-тиков. При УЗИ был выявлен крупный одиночный конкремент в теле желчного пузыря до 2 см в диаметре. Признаков желчной гипертензии не выявлено. В анамнезе у больной две беременности, двое родов, геморрагические явления (спонтанные и при бытовых травмах) отсутствовали. При амбулаторном обследовании было выявлено значительное удлинение АЧТВ до 160 секунд. Провели гематологическое обследование (таблица 1).
Коагулограмма пациентки за сутки до проведения хирургического вмешательства выглядела следующим образом (таблица 2).
При УЗАС артерий и вен нижних конечностей патологии не выявлено.
Таблица 1
Предоперационное гематологическое исследование больной П.
|
Показатель |
Результат |
Норма |
|
АЧТВ |
161 |
25–37 сек. |
|
ПТИ по Квику |
103% |
80–132% |
|
Фактор VIII |
128% |
5–150% |
|
Фактор IX |
91,7% |
85–150% |
|
Фактор XI |
110% |
70–120% |
|
Фактор XII |
5% |
70–150% |
Заключение: Дефицит фактора XII – 5% (Болезнь Хагемана). Данных за антифосфолипидный синдром нет.
Таблица 2
Показатели коагулограммы пациентки за сутки до операции
|
Показатель |
Результат |
Норма |
|
АЧТВ |
Не определяется |
25–37 сек, |
|
Протромбиновое время (индекс) |
11,3 сек (93,3%) |
9,8–12,0 сек (80–132%) |
|
Тромбиновое время |
17,7 сек, |
14–21 сек, |
|
Фибриноген |
2,8 г/л |
1,8–4,2 г/л |
Заключение: Выраженная гипокоагуляция по АЧТВ, по остальным параметрам – нормокоагуляция.
Поскольку при дефиците фактора XII нарушается активация ряда противосвертывающих механизмов, в частности фибринолитической системы, происходит компенсация гипокоагуляции. Эта недостаточность фибринолиза может вызвать тромботические осложнения – тромбоз глубоких вен нижних конечностей, ТЭЛА, инфаркт миокарда. Выявленная выраженная гипокоагуляция с одной стороны и умеренный риск развития ВТЭО с другой стороны, продиктовали необходимость дополнительной коррекции (переливание СЗП) и тщательного периоперационного контроля за системой гемостаза.
Произведено переливание 2-х доз СЗП из расчета – 10 мл/кг массы тела пациентки.
После переливания СЗП произошла частичная коррекция параметров коагулограммы (таблица 3).
Исследование тромбодинамики перед операцией выявило наличие умеренной гиперкоагуляции (таблица 4).
По данным таблицы 4, ряд показателей тромбодинамики (Vs, Vi, CS, D) перед операцией констатировали у больной состояние умеренной гиперкоагуляции.
Операция лапароскопическая холецистэктомия выполнена опытным хирургом под эндотрахеальным наркозом по традиционной методике. Уровень внутрибрюшного давления во время операции – 12 мм рт. ст., кровопотеря от-
Таблица 3
Показатели коагулограммы пациентки после переливания СЗП
|
Показатель |
Результат |
Норма |
|
АЧТВ |
50,9 сек, |
25–37 сек, |
|
Протромбиновое время (индекс) |
12,0 сек (83,6%) |
9,8–12,0 сек (80–132%) |
|
Тромбиновое время |
17,2 сек, |
14–21 сек, |
|
Фибриноген |
3,1 г/л |
1,8–4,2 г/л |
|
Тромбоциты |
191 х 109/л |
180–320 ∙ 109/л |
Заключение: Умеренная гипокоагуляция по АЧТВ.
Таблица 4
Показатели тромбодинамики до операции
Во время операции больной выполнена ТЭГ, выявившая нормокоагуляцию (рисунок).
1 Petrova Natalya - 000397 [choleclstectomia] Citrated native control Sample: 03.12.2014 11:42-
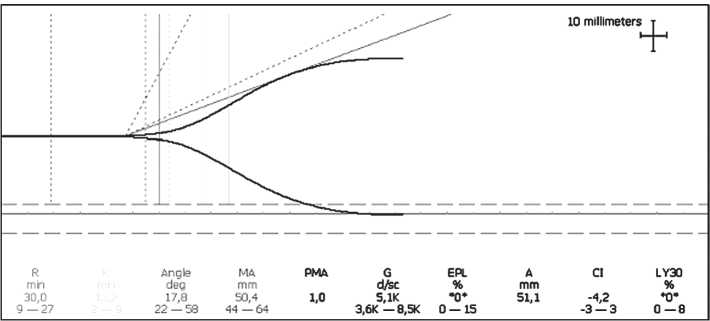
Интраоперационно профилактика ВТО осуществлялась за счет умеренной изоосмолярной гемодилюции и эластической компрессии нижних конечностей.
Исследование тромбодинамики в раннем послеоперационном периоде (через 6 часов от момента окончания операции) позволило регистрировать нормализацию показателей роста сгустка, кроме плотности сгустка (таблица 5).
Таблица 5
Показатели тромбодинамики через 6 часов после операции
|
Показатель |
Обозначение |
Результат |
Норма |
|
Стационарная скорость роста сгустка |
Vs |
25,3 мкм/мин |
20–29 мкм/мин |
|
Задержка роста сгустка |
Tlag |
1,4 мин |
0,6–1,5 мин |
|
Начальная скорость роста сгустка |
Vi |
49,5 мкм/мин |
38–56 мкм/мин |
|
Размер сгустка через 30 мин |
CS |
1044 мкм |
800–1200 мкм |
|
Плотность сгустка |
D |
34502 усл. ед. |
15000–32000 усл. ед. |
Течение послеоперационного периода без осложнений, профилактика ВТЭО – ранняя (в день операции) активизация больной, эластическая компрессия, оральное питание с первых суток после операции. Контрольное УЗАС на 3 сутки после операции – без патологии. Больная выписана в удовлетворительном состоянии на амбулаторное долечивание.
Контроль состояния больной по телефону через 3 месяца – состояние удовлетворительное, жалоб существенных не предъявляет, контроль УЗАС – без патологии (глубокие вены нижних конечностей проходимы).
Таким образом, болезнь Хагемана должна быть заподозрена в тех случаях, когда определяется значительное удлинение времени свертывания крови и АЧТВ при отсутствии каких-либо геморрагических осложнений и приема антикоагулянтов. При уровне фактора XII от 3 до 9% наблюдаются умеренные нарушения свертывания. Такой дефицит фактора XII не только не является препятствием для тромбообразования, но и может повышать риск развития ВТЭО. Выявленный у больного до операции дефицит фактора ХII требует повышенного внимания и при необходимости коррекции у него системы гемостаза в пери- и послеоперационном

периоде. В нашем наблюдении коррекция гемостаза посредством переливания СЗП результатировалась нормализацией АЧТВ и умеренной гиперкоагуляцией по результатам тромбодинамики, что, однако, не подтвердилось при выполнении ТЭГ.
Заключение
Глобальные коагулогические тесты у больной с дефицитом фактора XII и перенесшей хирургическое вмешательство позволили своевременно оценить и скорректировать у нее систему гемостаза, при этом по сравнению с ТЭГ тест тромбодинамики оказался более чувствительным к выявлению состояния гиперкоагуляции. Неспецифическая профилактика ВТЭО позволила безопасно провести до-, пери- и послеоперационный периоды у данной больной.
Список литературы Периоперационное ведение пациента с недостаточностью XII фактора (болезнь Хагемана)
- M. Cei, N. Mumoli, S. Giuntoli, O. Marino at al. Concomitant ST-elevation myocardial infarction and deep vein thrombosis in a patient with severe factor XII deficiency: case report and review of the literature.//Q J Med 2011; 104: 1083-1086.
- Przemystaw Rygal, Alicja Kuc Perioperative management of cardiac surgery patients with factor XII deficiency -two cases report. Anaesthesiology Intensive Therapy 2012, vol. 44, no 4, 217-220
- Макацария А.Д., воробьев А.в., Бицадзе в.О., Чабров А.М. Злокачественные новообразования, тромбофилия и тромбозы. М., Триада-Х, 2008, стр. 271-273.
- Атауллаханов Ф.И., Баландина А.Н., варданян Д.М. и др. Под ред. проф. А.М. Шулутко. Применение теста тромбодинамики для оценки состояния системы гемостаза. -Учебно-методические рекомендации, Москва, 2015, 72 с.


