Перспективы применения диетрессы, нового препарата на основе антител к каннабиноидному рецептору 1 типа, в лечении ожирения
Автор: Гурьянова Н.Н., Дугина Ю.Л., Жавберт Е.С., Эпштейн О.И.
Журнал: Вестник Международной академии наук (Русская секция) Электронный ресурс @vestnik-rsias-online
Рубрика: Медико-биологические науки, безопасность жизнедеятельности
Статья в выпуске: 1, 2012 года.
Бесплатный доступ
В настоящей статье представлен обзор результатов доклинических и клинических исследований эффективности и безопасности нового препарата сверхмалых доз антител к каннабиноидному рецептору 1 типа (диетрессы) в лечении избыточного веса и ожирения. Показано, что диетресса уменьшает прирост массы тела экспериментальных животных, находящихся на высококалорийной диете, по выраженности эффекта не уступая сибутрамину; а также снижает массу тела у пациентов с избыточным весом, I и II степенью ожирения. Безопасность применения препарата подтверждена в полном токсикологическом исследовании, а также в исследовании возможного наркогенного потенциала препарата. В клинических исследованиях нежелательных явлений, связанных с приемом диетрессы не было зарегистрировано.
Дистресс, каннабиноидные рецепторы, ожирение
Короткий адрес: https://sciup.org/14315498
IDR: 14315498
Текст научной статьи Перспективы применения диетрессы, нового препарата на основе антител к каннабиноидному рецептору 1 типа, в лечении ожирения
ПЕРСПЕКТИВЫ ПРИМЕНЕНИЯ ДИЕТРЕССЫ, НОВОГО ПРЕПАРАТА НА ОСНОВЕ АНТИТЕЛ К КАННАБИНОИДНОМУ РЕЦЕПТОРУ 1 ТИПА, В ЛЕЧЕНИИ ОЖИРЕНИЯ
Н. Н. Гурьянова, Ю. Л. Дугина, Е. С. Жавберт, О. И. Эпштейн
ООО «НПФ «Материа Медика Холдинг», Москва, Россия
Dietressa®, a Drug Based on Antibodies to CB1 Cannabinoid Receptor, is a Novel Option for the Treatment of Obesity
N. N. Gurianova, J. L. Dugina, E. S. Zhavbert, O. I. Epstein
ООО «NPF «Materia Medica Holding», Moscow, Russia
В настоящей статье представлен обзор результатов доклинических и клинических исследований эффективности и безопасности нового препарата сверхмалых доз антител к каннабиноидному рецептору 1 типа (диетрессы) в лечении избыточного веса и ожирения. Показано, что диетресса уменьшает прирост массы тела экспериментальных животных, находящихся на высококалорийной диете, по выраженности эффекта не уступая сибутрамину; а также снижает массу тела у пациентов с избыточным весом, I и II степенью ожирения. Безопасность применения препарата подтверждена в полном токсикологическом исследовании, а также в исследовании возможного наркогенного потенциала препарата. В клинических исследованиях нежелательных явлений, связанных с приемом диетрессы не было зарегистрировано. Ключевые слова: диетресса, каннабиноидные рецепторы, ожирение.
The preclinical and clinical trials of a novel drug containing ultra-low doses of antibodies to cannabioid receptor type 1 (Dietressa®) efficacy and safety in treating obesity are reviewed in the present paper. The effect of dietressa on the body weight gain in experimental animals on high-caloric diet comparable to that of sibutramine was shown. Dietressa also reduced the body mass of overweight patients and in patients with I and II stage obesity. Full toxicological and abuse potential study of dietressa revealed the safety of its use. No adverse events caused by dietressa were registered during the clinical studies. Key words: dietressa, cannabioid receptors, obesity.
Проблема массового набора лишнего веса возникла лишь несколько десятилетий назад, однако темпы распространения ожирения в развитых странах уже приобрели характер пандемии. Ожирение не только приводит к сокращению продолжительности и ухудшению качества жизни, но и увеличивает риск возникновения и тяжесть течения сопутствующих заболеваний, таких как сахарный диабет II типа, дислипидемия, артериальная гипертензия, ишемическая болезнь сердца и др. [7, 9].
Существующие лекарственные препараты против ожирения направлены на устранение отдельных проявлений заболевания. Известны лекарственные средства регулирующие аппетит (сибутрамин, фентермин, флуоксетин, диэтилпропион), уменьшающие всасывание жиров (орлистат) или увеличивающие расход энергии в организме (эфедрин, кофеин). Препараты, применяющиеся для лечения ожирения, часто имеют ряд побочных эффектов, в связи с чем их использование в лечебной практике ограничено. Для устранения исходных причин и нежелательных последствий данного заболевания необходим системный патогенетический подход, включающий как регуляцию аппетита, так и сокращение имеющихся в организме жировых отложений.
В патогенезе ожирения, регуляции пищевого поведения и накопления жира существенную роль играет эн-доканнабиноидная система [5, 6, 10]. Наиболее перспективной мишенью для лекарственных препаратов для лечения ожирения являются каннабиноидные рецепторы 1 типа. В гипоталамусе каннабиноидные рецепторы 1 типа и эндоканнабиноиды представляют собой единую систему, регулирующую аппетит и, как результат, потребление пищи. Потребление высококалорийной и богатой жирами пищи ведет к гиперактивации эндоканнабиноидной системы, увеличению аппетита и усилению липогенеза. Следует также отметить периферические метаболические эффекты эндоканнабиноидной системы, связанные с ее влиянием на адипоциты, гепатоциты, желудочно-кишечный тракт, скелетные мышцы и эндокринную ткань поджелудочной железы [11, 2]. Препарат Акомплия (Sanofi-Aventis, Франция), действующим веществом которого является римонабант, селективный ингибитор каннабиноидного рецептора 1 типа, успешно применялся для лечения ожирения в Европе с июля 2006 года, однако в январе 2009 года был запрещен к применению в клинической практике в связи с непредвиденным побочным действием
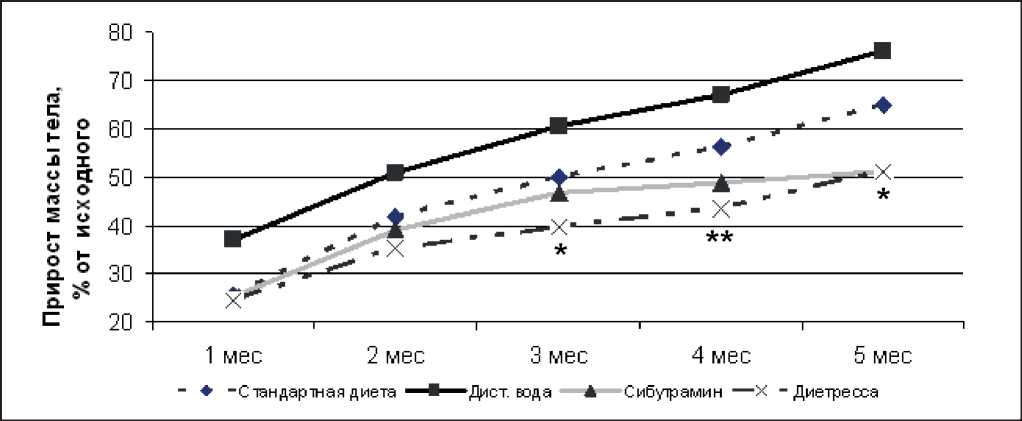
Рис. 1. Прирост массы тела мышей, получавших препараты на протяжении 5 месяцев введения. Примечание. * — p <0,05 от контроля; ** — p <0,01 от контроля, t -критерий Стьюдента).
на центральную нервную систему [12]. В настоящее время имеются данные о разработке препаратов на основе селективных ингибиторов каннабиноидного рецептора I типа нового поколения, лишенные данных побочных эффектов [8].
В 2010 году компанией ООО «НПФ «Материа Медика Холдинг» был зарегистрирован новый препарат ди-етресса (РУ № ЛСР-006933/10-210710), созданный на основе аффинно очищенных антител к каннабиноидному рецептору 1 типа. В доклинических исследованиях диетрессы была изучена способность препарата снижать прирост массы тела крыс, находящихся на высококалорийной диете [3].
В данном исследовании влияние диетрессы на динамику прироста массы и пищевое поведение изучали на 40 мышах-самцах линии C57Bl6 (возраст 2 мес., исходная масса 14,3—15,6 грамм), 10 из которых были интактными и получали стандартную диету (3611 ккал/кг), а 30 — стандартную диету с высокожировыми добавками (не менее 4400 ккал/кг). В течение 20 недель мышам на высококалорийной диете внутрижелудочно вводили дистиллированную воду ( n =10, контроль, 0,4 мл/мышь/сут), диетрессу ( n =10, 0,4 мл/мышь/сут) и препарат сравнения сибутрамин ( n =10, 10 мг/кг/сут). Каждые 4 недели у мышей измеряли массу тела, суточное потребление пищи и двигательную активность в тесте «открытое поле» [4].
Диетресса и препарат сравнения сибутрамин эффективно снижали прирост массы тела мышей в течение всего периода наблюдения (рис. 1).
Данный эффект был более выражен в группе диетрессы, достоверные отличия от контроля наблюдали уже к 12 неделе эксперимента, а в группе сибутрамина только к 20 неделе. Лишь на 20 неделе исследования эффективности препаратов в снижении массы тела практически сравнялись. Через 4 недели от начала введения препаратов прирост массы тела в группе сибутрамина был на 12,2%, а в группе диетрессы — на 12,7% ниже контроля; через 8 недель — на 12,1 и 16,2%; через 12 недель — на 13,6 и 20,7% ( p <0,05); через 16 недель — на 18,4 и 23,5% ( p <0,05); через 20 недель — на 24,3% ( p <0,01) и 24,7% ( p <0,01), соответственно.
Среднесуточное потребление пищи мышами на высококалорийной диете в среднем было больше, чем у мышей на стандартной диете (1,59 г/10 г массы тела vs 1,46 г/10 г массы тела, p <0,05). Сибутрамин снижал потребление пищи на всех сроках исследования, в то время как диетресса снижала потребление пищи только до 12 недели исследования, затем аппетит мышей этой группы возрастал.
В контрольной группе мышей на высококалорийной диете двигательная активность мышей в течение всего периода наблюдения была выше, чем у мышей на стандартной диете. Сибутрамин повышал двигательную активность экспериментальных животных в период с 12-ой по 16-ую неделю введения (на 32,6 и 63,9% vs контроль; p <0,05), затем этот эффект нивелировался. В группе диетрессы двигательная активность не отличалась от контроля, и лишь на 12 неделе была несколько ниже, чем в контроле (на 23%, p <0,05).
Таким образом, диетресса по эффективности снижения прироста массы тела у экспериментальных животных не уступала препарату сравнения сибутрамину. По-видимому, сибутрамин оказывал влияние на вес мышей за счет снижения пищевой и возрастания двигательной активности, а диетресса, напротив, проявляла менее выраженное анорексигенное действие и не влияла на двигательную активность. Предположительно, снижение прироста массы тела под действием диетрессы связано с ее воздействием на метаболические процесса организма.
В полном токсикологическом исследовании была показана безопасность диетрессы. В исследовании острой токсичности, а также при длительном (6 месяцев) введении диетрессы крысам и кроликам не было зарегистрировано токсических эффектов препарата. Диетресса не оказывала повреждающего действия на генеративную функцию крыс, не нарушала эмбриофетальное и постнатальное развитие крысят при введении беременным самкам, не обладала генотоксическими, иммунотоксическими и аллергизирующими свойствами в стандартных тестах.
В связи с влиянием препарата на эндоканнабиоидную систему, изучали также возможный наркогенный потенциал диетрессы, который оценивали с помощью реакции самостимуляции латерального гипоталамуса в модификации Воробьевой Т. М. у крыс [13]. В данном исследовании не было выявлено увеличения частоты реакции са-мостимуляции относительно контроля и исходных значений. После прекращения приема препарата не только не наблюдали синдром отмены, но и отмечали снижение частоты реакции самостимуляции на 15,0—35,2% по сравнению с исходными значениями ( p <0,05) и на 32,3—44,3% по сравнению с контролем ( p <0,05). Это свидетельствует о снижении у крыс потребности к самостимуляции (активации системы положительного эмоционального подкрепления). Таким образом, было показано отсутствие у препарата диетресса наркогенного потенциала.
В пилотном несравнительном клиническом исследовании, проведенном на базе кафедры терапии и семейной медицины ФУВ ГБОУ ВПО ВолгГМУ Минздравсоцразвития России, исследовали безопасность применения диетрес-сы и ее эффективность при избыточной массе тела и ожирении. В исследовании приняли участие 80 добровольцев в возрасте от 20 до 69 лет (средний возраст 40,2±1,26 года), 68,7% которых страдали избыточной массой тела или ожирением (I—III степени). В течение 1 месяца терапии пациенты наносили врачу 2 визита, во время которых оценивали наличие нежелательных явлений, измеряли массу тела, окружность талии и окружность бедер пациентов, определяли выраженность чувства голода по визуальной аналоговой шкале (ВАШ). Статистическая обработка данных проводилась с использованием параметрических и непараметрических методов вариационной статистики.
При оценке влияния диетрессы на изменение массы тела испытуемых было показано, что использование препарата привело к снижению массы тела у 56 (70%) пациентов. Назначение препарата в дозе 1 таблетка 2 раза в день в течение 1 месяца приводило к статистически достоверному снижению массы тела с 86,2±2,14 до 84,7±2,08 кг ( p <0,001), уменьшению окружности талии (с 96,3±1,97 до 94,1±2,07 см, p <0,001) и окружности бедер (с 110,8±1,52 до 107,8±1,69 см, p <0,001), а также способствовало снижению выраженности чувства голода у пациентов, в первую очередь в период его наибольшей интенсивности — в вечернее время (c 49,4±3,75 до 42,0±4,32 баллов по ВАШ, p <0,001). У 24 (30%) пациентов вес оставался неизменным или незначительно увеличивался, однако следует отметить, что среди указанных пациентов 14 (17,5%) исходно имели нормальную массу тела (индекс массы тела (ИМТ) <25 кг/м2). В течение всего периода наблюдения за пациентами отмечалась хорошая переносимость диетрессы, нежелательные явления, связанные с приемом препарата, отсутствовали.
Эффективность диетрессы также была протестирована в мультицентровом двойном слепом плацебоконт-ролируемом рандомизированном клиническом исследовании, включавшем 80 пациентов из 10 медицинских центров России [1]. В данном исследовании участвовали пациенты с диагностированным ожирением 1 степени ( n =37, ИМТ 30,0—34,9) и ожирением 2 степени ( n =43, ИМТ 35,0—39,9). Средний возраст участников исследования составил 44 года (минимальный возраст — 22 года, максимальный — 71 год), большую часть пациентов составляли женщины (88,75% женщин и 11,25% мужчин). Пациентов случайным образом разделяли на две группы: группу диетрессы (38 женщин/5мужчин) и группу плацебо (33 женщины/4 мужчины). Средний вес в группах составил 97,9 кг и 97,1 кг, соответственно. Группы были сопоставимы по возрастным и основным антропометрическим характеристикам. Более половины испытуемых страдали заболеваниями сердечно-сосудистой системы, 30% — заболеваниями опорно-двигательной системы, 20% — заболеваниями желудочно-кишечного тракта, 15% имели нарушенную толерантность к глюкозе или сахарный диабет II типа.
Препарат ( n =40) или плацебо ( n =40) применяли в дозе 1 таблетка 3 раза в день за 15—30 минут до приема пищи. В комплексе с препаратом/плацебо пациентам также назначали диету. Период приема препарата/пла-цебо составил 12 недель. В процессе лечения пациенты наносили 7 визитов врачу, в ходе которых измеряли вес пациента, окружность талии и бедер, оценивали степень выраженности голода и качество жизни (по самооценке пациента), а также осуществляли контроль назначенной и сопутствующей терапии, оценивали ее безопасность. Статистическую обработку проводили с использованием методов параметрической и непараметрической вариационной статистики.
Анализ динамики абсолютного и относительного снижения массы тела в течение 12 недель терапии показал, что вес пациентов снижался в обеих группах. Доля пациентов с ожирением 1-ой и 2-ой степени, которые принимали диетрессу и снизили свой вес на 5% и более, составила 35% против 19% в группе плацебо. Наиболее значимый эффект диетрессы в сравнении с группой плацебо был показан на пациентах с диагностированным ожирением I степени (рис. 2). Доля похудевших на 5% и более в этой подгруппе через 10 недель лечения составила 41%, а через 12 недель — 47% против 10% и 15% в группе плацебо, соответственно ( p <0,05, рис. 2). К концу третьего месяца введения среднее изменение массы тела в этой подгруппе составило –3,8±1,0 кг против –1,8±0,6 кг в группе плацебо ( p <0,05).
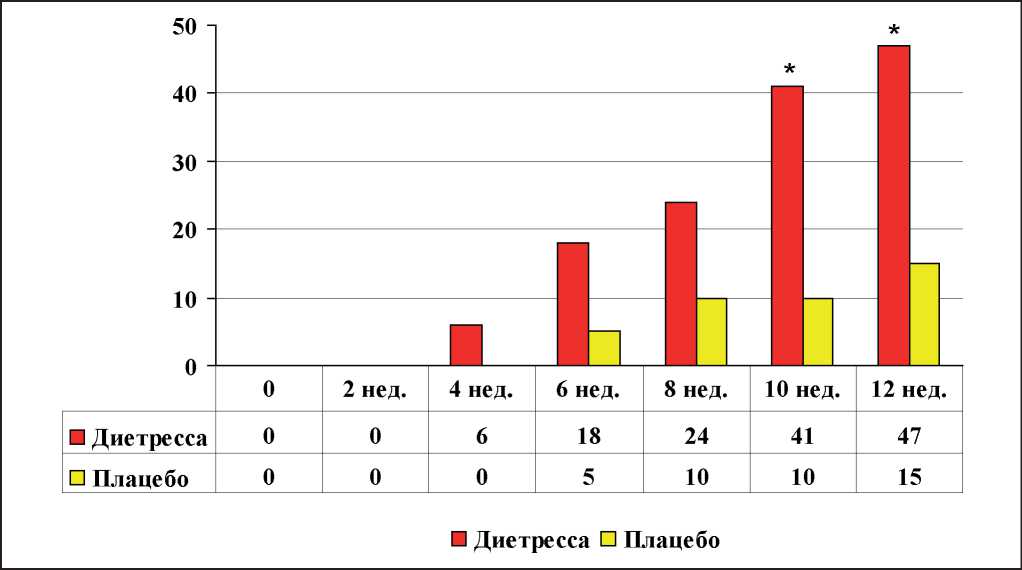
Рис. 2. Доли пациентов с ожирением I степени с потерей веса на 5 процентов и более.
Примечание. * — p <0,05. Сравнение долей пациентов в двух подгруппах производилось с помощью одностороннего точного критерия Фишера по каждому из визитов.
Среди пациентов с диагностированным ожирением II степени также наблюдали быстрое снижение веса. Достоверное, по сравнению с исходными значениями, снижение массы тела в этой группе наблюдали уже на 4 неделе, затем на протяжении следующих 8 недель терапии эффект увеличивался. Однако достоверных различий в доле пациентов, похудевших на 5% и более, и в среднем изменении массы тела между группой диетрессы и группой плацебо обнаружено не было. Вероятно, для данной категории пациентов продолжительность терапии и доза препарата оказались недостаточными, так как пациенты с диагностированным ожирением II степени нуждаются в более длительном лечении (до 1 года), прежде чем можно будет говорить об эффективности данной терапии.
Диетресса эффективно снижала чувство голода у пациентов и помогала им легче переносить назначаемую врачом диету. Данный эффект препарата наблюдали уже в течение первых 4-х недель лечения, и несмотря на различия в выраженности эффекта в разное время суток и у пациентов с разными степенями ожирения, снижение чувства голода сохранялось на протяжении всего периода терапии.
В ходе мониторинга безопасности было выявлено также благоприятное влияние диетрессы на липидный профиль крови пациентов, в частности на уровень триглицеридов.
Таким образом, в доклинических исследованиях показана эффективность препарата на основе антител к каннабиноидному рецептору 1 типа (диетресса) в снижении массы тела мышей, находящихся на высококалорийной диете, не уступающая по выраженности препарату сравнения сибутрамину. В полном токсикологическом исследовании и при изучении возможного наркогенного потенциала была выявлена безопасность диетрессы. Эффективность и безопасность применения препарата была подтверждена в рандомизированных клинических исследованиях у пациентов с избыточным весом и ожирением I и II степени. Прием препарата в течение 1 или 3 месяцев приводил к достоверному снижению массы тела у пациентов, причем наиболее значимый эффект препарата был отмечен в группе пациентов с ожирением I степени. В настоящее время в Российской Федерации проходят два рандомизированных клинических исследования эффективности и безопасности приема диетрессы в течение 6 месяцев для лечения пациентов с I и II степенями ожирения, которые позволят более точно определить место препарата в фармакотерапии избыточного веса и ожирения.
Список литературы Перспективы применения диетрессы, нового препарата на основе антител к каннабиноидному рецептору 1 типа, в лечении ожирения
- Мкртумян А. М. Эндоканнабиноидная система как терапевтическая ми шень Диетрессы -нового препарата для лечения ожирения.//Эффектив ная фармакотерапия эндокринология. № 5. 2011. 2-10.
- Романцова Т. И., Гиляревский С. Р. Кардиометаболический риск и совре менные подходы к его коррекции//РМЖ. Кардиология. 2008. Т. 16, № 11. 1576-1578.
- Хейфец И. А., Бугаева Л. И., Воробьева Т. М. и др. Экспериментальное иссле дование эффектов «Диетрессы» -нового препарата для лечения ожире ния.//Бюллетень экспериментальной биологии и медицины. 2011. Т.152, № 9. 290-293.
- Bures J., Buresova O., Huston J. P. Techniques and Basic Experiments for the Study of Brain and Behavior//Amsterdam -N.Y.: Elsevier Sci. Publ. 1983.
- Carr T. P., Jesch E. D., Brown A. W.//Nut. Res. 2008. V.28. No.10. P.641-650.
- Cota D.//Front. Horm. Res. 2008. No.36. P.135-145.
- Hu F. B., Manson J. E., Stampfer M. J. et al.//N. Engl. J. Med. 2001. No.345. P.790-797.
- Lee H. K., Choi E. B., Pak C. S. The current status and future perspectives of studies of cannabinoid receptor 1 antagonists as anti obesity agents.//Curr. Top. Med. Chem., 2009, 9 (6): 482-503
- Lean M. E., Han T. S., Seidell J. C.//Lancet. 1998. No.351. P.853-856.
- Magni P., Dozio E., Ruscica M. et al.//Ann. NY Acad. Sci. 2009. No.1163. P.221-232.
- Matias I., Cristino L., Di Marzo V. Endocannabinoids: some like it fat (and sweet too)//J. Neuroendocrinol. 2008. V.20. Suppl 1. P.100-109.
- «Public statement on Acomplia: Withdrawal of the marketing authorisa tion in the European Union», European Medicines Agency, 2009. http://www.ema.europa.eu/docs/en_GB/document_library/Public_state ment/2009/11/WC500012189.pdf
- Vorob'eva T. M.//Neuroscience translations published by the Federation of American Societies for experimental biology for the National Institute of Mental Health. 1969. No.12. P.95-10.


